Нормальная физиология [Николай Александрович Агаджанян] (fb2) читать онлайн
[Настройки текста] [Cбросить фильтры]
[Оглавление]
Николай Александрович Агаджанян Нормальная физиология
Сокращения в тексте
АД – артериальное давление АДГ – антидиуретический гормон АДФ – аденозиндифосфорная кислота АКТГ – адренокортикотропный гормон APUD – система – Amine Precursors Uptake and Decarboxylating system АТФ – адепозинтрифосфориая кислота ВВП – вторичный вызванный потенциал ВИП – вазоактивный интестинальиый пептид ВНС – вегетативная нервная система ВП – вызванный потенциал ВПСП – возбуждающий постсипаптический потенциал ГАМК – гамма-аминомасляпаи кислота ГДФ – гуапозиндифосфаг ГИП – гастроинтестипальный пеп тид ГОМК – гамма-оксимасляная кислота ГТФ – гуапозинтрифосфат ГЭБ – гематоэицефалический барьер ДК – дыхательный коэффициент ДНК – дезоксирибонуклеиновая кислота ДО – дыхательный объем ЖЕЛ – жизненная емкость легких ЖИП – желудочный иигибирующий пептид ИЛ – интерлейкины ИБС – ишемическая болезнь сердца КОЕ-Э – колопиеобразующая единица эритроцитов КОМТ – катехоло-метилтрансфераза КОС – кислотно-основное состояние КСФ-Г – грапулоцитарный колопиестимулирующий фактор КСФ-М – мопоцитарный колопиестимулирующий фактор ЛГ – лютеипизирующий гормон МАО – мопоаминоксидаза МВЛ – максимальная вентиляция легких МДД – медлеичая диастолическая деполяризация МОК – минутный объем крови МП – мембранный потенциал МПК – максимальное потребление кислорода НЬО., – оксигомоглобип ОЕЛ – остаточная емкость легких ОО – основной обмен ОЦК – объем циркулирующей крови ПАГ – параамипогиппуровая кислота ПД – потенциал действия ПО – первичный ответ ПП – панкреатический пептид П'ГГ – наратиреотропный гормон PACK – рефляция агрегатного состояния крови РНК – рибонуклеиновая кислота РФ – ретикулярная формация СРПВ – скорость распространения пульсовой волны СТГ – соматотропный гормон ТПСГТ – тормозной постсинаптический потенциал ТТГ – тиреотропный гормон ФНО – фактор некроза опухолей ФОЕ – функциональная остаточная емкость ФСГ – фолликулостимулирующий гормон цАМФ – циклический аденозинмонофосфат ЦВД – центральное венозное давление ЦСЖ – цереброспинальная жидкость цГМФ – циклический 3,5-гуанозинмонофосфат ЦНС – центральная нервная система ЧСС – число сердечных сокращений ЭКоГ – электрокортикограмма ЭЭГ – электроэнцефалограмма ЭКГ – электрокардиограмма ЮГА – юкстагломерулярный аппаратГлава 1. История физиологии. Методы физиологических исследований
Физиология – важная область человеческого знания, наука о жизнедеятельности целостного организма, физиологических систем, органов, клеток и отдельных клеточных структур. Как важнейшая синтетическая отрасль знаний физиология стремится вскрыть механизмы регуляции и закономерности жизнедеятельности организма и взаимодействия его с окружающей средой. Физиология является базисом, теоретической основой – философией медицины, объединяющей разрозненные знания и факты в одно целое. Врач оценивает состояние человека, уровень его дееспособности по степени функциональных нарушений, т. е. по характеру и величине отклонения от нормы важнейших физиологических функций. Для того чтобы вернуть эти отклонения к норме, необходимо учитывать индивидуальные возрастные, этнические особенности организма, а также экологические и социальные условия среды обитания. При фармакологической коррекции нарушенных в неадекватных условиях функций организма следует обращать внимание не только на особенности влияния природно-климатических и производственных условий среды обитания, но и на характер антропогенного загрязнения – количество и качество вредных высокотоксичных веществ в атмосфере, воде, продуктах питания. Структура и функция тесно связаны между собой и взаимо-обусловлены. Для интегративной оценки жизнедеятельности целостного организма физиология синтезирует конкретные комплексные сведения, полученные такими науками, как анатомия, цитология, гистология, молекулярная биология, биохимия, экология, биофизика и смежными с ними. Для оценки всего многообразия сложных физиологических процессов, которые протекают в организме в ходе адаптации, необходим системный подход и глубокое философское осмысление и обобщение. Физиологические знания были добыты в результате накопленных учеными разных стран оригинальных экспериментальных материалов. Главный объект медицинского исследования – человек, но основные физиологические закономерности по известной причине установлены в экспериментах на различных видах животных как в лабораторных, так и естественных условиях. Чем выше организация животного, чем ближе изучаемый объект подходит к человеку, тем ценнее полученные результаты. Однако результаты экспериментальных исследований на животных в области сравнительной и экологической физиологии могут быть перенесены на человека только после тщательного анализа и обязательного критического сопоставления полученных материалов с клиническими данными. При возникновении у обследуемого признаков функциональных нарушений, например, при адаптации в неадекватных условиях, экстремальных воздействиях или при приеме фармакологических препаратов физиолог должен осмыслить, объяснить, чем детерминированы эти нарушения, и дать эколого-физиологическое обоснование. Одним из основных жизненных свойств является способность организма к компенсации, т. е. к выравниванию отклонений от нормы, восстановлению тем или иным путем нарушенной функции. Физиология изучает новое качество живого – его функцию или проявления жизнедеятельности организма и его частей, направленные на достижение полезного результата и обладающие приспособительными свойствами. В основе жизнедеятельности любой функции лежит обмен веществ, энергии и информацией. Условия существования человека определяются специфическими физическими и химическими особенностями внутренней и внешней среды, природно-климатическими факторами, а также социально-культурными традициями и качеством жизни населения. Феногенотипическую особенность каждого индивидуума надо учитывать при использовании фармакологических препаратов. В основе формирования сложной физиологической системы каждого организма лежит индивидуальная временная шкала. Методологические принципы биоритмологии – хронофизиологии, хронофармакологии в настоящее время уверенно проникают в исследования всех уровней организации живого – от молекулярного до целостного организма. Ритмичность как одна из фундаментальных особенностей функционирования организма непосредственно связана с механизмами обратной связи, саморегуляции и адаптации. При проведении хронофизиологических и хронофармакологических исследований необходимо учитывать данные о сезоне года, времени суток, возрасте, типологических и конституциональных особенностях организма и экологических условиях среды обитания. Основная суть жизни проявляется в осуществлении двух принципиально важных процессов – рождения и выживания. Потребность сохранения жизни человека была на всех этапах его развития, и уже в древности формировались элементарные представления о деятельности организма человека. Отец медицины Гиппократ (460 – 377 гг. до н.э.) заложил основы для понимания роли отдельных систем и функций организма как целого. Подобных воззрений придерживался и другой знаменитый врач древности – римский анатом Гален (201 – 131гг. до н.э.). Гуморальные гипотезы и теории в течение целых тысячелетий оставались господствующими и среди врачей древнего Китая, Индии, Ближнего Востока и Европы. На важность временных факторов и циклических изменений окружающей среды впервые указывал еще Аристотель (384 – 322 гг. до н. э.). Он писал: «Продолжительность всех этих явлений: и беременности, и развития, и жизни – совершенно естественно измерять периодами. Я называю периодами день и ночь, месяц, год и времена, измеряемые ими; кроме того, лунные периоды…». Все эти оригинальные идеи на какое-то время были забыты. Их основательное изучение началось на базе научного наблюдения и опыта лишь в эпоху Возрождения. Крупнейший врач этой эпохи Т. Парацельс (1493 – 1541 гг.) подчеркивал в своих трудах, что теория врача – это опыт, никто не может стать врачом без науки и опыта. Дальнейшему развитию физиологии предшествовали успехи анатомии. Работа профессора Падуанского университета – анатома и физиолога А. Везалия «О строении человеческого тела» подготовила почву для открытий в области физиологии. Углубление знаний о строении тканей животных побуждает к изучению функционального назначения разнообразных структур. Рене Декарт (1596–1650 гг.) сформулировал рефлекторный принцип организации движений – принцип отражения в ответ на побуждающий их стимул. Декарт пытался законами механики объяснить как ход небесных светил, так и поведение животных. В этот же период, в 1628 г. Вильям Гарвей (1578–1657 гг.) опубликовал свою работу «Анатомические исследования о движении сердца и крови у животных». Открытие Гарвеем кровообращения считается датой основания физиологии. Он ввел в практику научных исследований прием, получивший название вивисекции, или живосечения. М. Мальпиги (1628- 1694 гг.), используя микроскоп, в 1661 г. показал, что артерии и вены соединяются между собой мельчайшими сосудами – капиллярами, благодаря которым в организме образуется замкнутая сеть кровеносных сосудов. В 1822 г. Ф. Мажанди (1785–1855 гг.) доказал раздельное существование чувствительных – афферентных (центростремительных) и двигательных – эфферентных (центробежных) нервных волокон. Это явилось важным шагом в установлении связей между функциями нервной системы и ее структурой. В 1842 г. ученик Н. И. Пирогова А. П. Вальтер (1817–1889 гг.) установил влияние нервной системы на «внутренние» процессы в организме. В том же году В. А. Басов (1812–1879 гг.) разработал оригинальную методику доступа в желудок совершенно здорового животного путем наложения желудочной фистулы. Этими ис-следованиями впервые в физиологии была доказана возможность проведения хронического эксперимента для длительного наблюдения и изучения функций организма. Основоположником отечественной экспериментальной физиологии является профессор Московского университета А. М. Филомафитский (1802–1849 гг.), изучавший вопросы, связанные с физиологией дыхания, переливанием крови, применением наркоза. Он написал первый учебник по физиологии. Три великих открытия естествознания – закон сохранения энергии, клеточная теория и эволюционное учение – явились основой развития многих естественно-научных дисциплин. На базе физико-химических знаний во второй половине XIX столетия стала интенсивно развиваться физиология. Возникли физиологические школы, привлекающие молодых ученых из разных стран (К. Людвиг, Р. Гейденгайн и других). В этот период были достигнуты определяющие успехи в углубленном изучении деятельности органов и систем, развивалась физиология нервов и мышц как возбудимых тканей (Дюбуа Реймон, Г. Гельмгольц, Э. Пфлюгер). Большой вклад в разработку физиологических проблем внес Клод Бернар, который изучал роль нервной системы в регуляции тонуса кровеносных сосудов и углеводного обмена, а также создал представление о внутренней среде организма как основе «свободной» жизни. Новый этап русской и мировой физиологии начинается работами И. М. Сеченова (1829- 1905 гг.). Его по праву называют «отцом русской физиологии». Первые его работы были посвящены вопросам переноса газов кровью, разработке проблем гипоксических состояний. И. М. Сеченов и Поль Бер независимо друг от друга объяснили причину гибели французских аэронавтов, поднявшихся на аэростате «Зенит» на высоту более 8000 м, где имел место острый недостаток кислорода в разреженной атмосфере вдыхаемого воздуха. И. М. Сеченов показал, что гемоглобин эритроцитов переносит не только кислород, по и углекислоту. Его научная деятельность многогранна. Он разрабатывал вопросы физиологии труда. Изучая процесс утомления, впервые научно обосновал и установил значение активного отдыха. Всеобщее признание получило открытие И. М. Сеченовым явления центрального торможения. В 1863 г. вышла в свет его знаменитая книга «Рефлексы головного мозга», в которой сформулировано материалистическое положение о рефлекторной деятельности головного мозга, о том, что все бесконечное разнообразие внешних проявлений мозговой деятельности сводится в конечном итоге к одному лишь явлению – к мышечному движению. И. М. Сеченов вошел в историю науки как великий ученый-мыслитель, дерзнувший подвергнуть анализу естествоиспытателя самую сложную область природы – явления сознания высших отделов головного мозга. Обогатив науку величайшими открытиями, он выдвинул наиболее правильные представления по важнейшим принципиальным вопросам физиологии, создал первую в России физиологическую школу. Его учениками были Н. Е. Введенский, В. Ф. Вериго, А. Ф. Самойлов. Идеи, разработанные И. М. Сеченовым, были развиты в трудах И. П. Павлова (1849- 1936 гг.) и его многочисленных учеников. И. П. Павлов вывел рефлекторную деятельность мозга на качественно новый уровень, создав учение о высшей нервной деятельности (поведении) человека и животных, ее проявлениях в норме и при патологии. Научная деятельность И. П. Павлова развивалась в трех основных направлениях: изучение важнейших проблем физиологии кровообращения (1874–1889 гг.), физиологии пищеварения (1889- 1901 гг.), высшей нервной деятельности (1901 – 1936 гг.). В 1904 г. И. П. Павлов получил крупнейшую международную награду – Нобелевскую премию. В 1935 г., незадолго до смерти И. П. Павлова, Международный физиологический конгресс присвоил ему звание «старейшины физиологов мира». Учениками и последователями И. П. Павлова были Л. А. Орбели, П. К. Анохин, Э. А. Асратян, К. М. Быков и многие другие, которые своими фундаментальными трудами способствовали дальнейшему развитию основных положений учения о высшей нервной деятельности. Распространение естественно-научного исследования на высшие формы нервной деятельности основывалось на принципах детерминизма (причинности), структурности. Исследование высшей нервной деятельности на основе дальнейшего развития рефлекторной теории, выявление объективных законов этой деятельности составляет ярчайшую страницу современного естествознания. Вклад отечественных ученых в мировую науку о мозге общепризнан, многое сделано и в изучении локализации функций в мозге (В. М. Бехтерев, Н. А. Миславский и др.) Физиология мозга и других важнейших систем организма успешно развивается в странах Европы и в США. Основные принципы координационной деятельности мозга были разработаны и сформулированы Ч. С. Шеррингтоном (1856–1952 гг.). Его работы вместе с результатами исследований электрофизиолога Э. Д. Эдриана (1889–1977 гг.) были в 1932 г. удостоены Нобелевской премии. За исследования капиллярного кровообращения Нобелевскую премию получил А. Крог. Большой научный вклад в физиологию сердечно-сосудистой системы внесли отечественные ученые В. В. Парин, В. Н. Черниговский и др. За работы в области физиологии дыхания и в частности – выяснения механизмов регуляции этой важнейшей функции Нобелевской премии был удостоен К. Гейманс, а за открытие ферментативного механизма клеточного дыхания – О. Г. Варбург. Велик вклад ученых в физиологию дыхательного центра и его роли в регуляции дыхания (Н. А. Миславский, Д. С. Холдейн, М. В. Сергиевский). Большое значение имели работы Ф. В. Овсянникова, описавшего сосудодвигательный центр. В области физиологии пищеварения, продолжая славные традиции первооткрывателей, огромный вклад внесли И. П. Разенков, Г. В. Фольборт, Б. П. Бабкин и др. Особенно следует отметить заслуги A. M. Уголева, которому принадлежит честь открытия мембранного кишечного пищеварения, а также вклад в разработку современной концепции эндокринной деятельности желудочно-кишечного тракта. Наше столетие богато открытиями в области изучения желез внутренней секреции. Целой плеяде замечательных ученых присуждены Нобелевские премии за работы по инсулину, дважды за открытия в области физиологии гипофиза, за исследование функции надпочечников, за регуляцию и гормональное воздействие на обмен веществ. В разработке медико-биологических проблем наибольшие успехи в этом столетии достигнуты иммунологами. За открытия в этой области учеными разных стран получено наибольшее число Нобелевских премий – одиннадцать! Среди них и выдающиеся физиологи, биохимики, клиницисты и представители других смежных наук. Если XIX век характеризуется как период расцвета аналитической физиологии, когда были сделаны выдающиеся открытия по всем важнейшим физиологическим системам, то XX век – период интеграции и специализации наук.Именно в двадцатом столетии выделились два основных направления развития физиологической науки: 1. Глубокое изучение физико-химических процессов в клетках, мембранах, преобразований на молекулярном уровне. Делаются принципиальные открытия в области цитофизиологии и цитохимии, утверждается мембранная теория биоэлектрических потенциалов. За создание этой теории и установление ионных механизмов возбуждения нейронов в 1963 г. были удостоены Нобелевской премии Д. Экклс, Э. Хаксли, А. Ходжкин. 2. Формирование представлений о единстве организма, гомеостазе (К. Бернар, У. Кеннон) и взаимосвязи организма с окружающей внешней средой (И. М. Сеченов, И. П. Павлов).
На основе всего этого в настоящее время успешно развиваются адаптология, биоритмология, а также междисциплинарная область знаний – экология человека. В условиях резкого изменения и антропогенного загрязнения среды обитания человека, необычайной миграционной подвижности, урбанизации, сложных демографических процессов в масштабах планеты становятся приоритетными такие медико-биологические направления как разработка физиологически обоснованных средств охраны здоровья населения и экологической безопасности биосферы. Отрицательные факторы антропогенного воздействия способствуют снижению резервов здоровья, нарастанию степени психофизиологического напряжения, появлению новых форм экологических болезней. Деятельность человека как существа биосоциального изучают гуманитарные науки, а как эта деятельность реализуется в его живом теле исследуют физиология и экология человека. Со временем физиология может дать конкретные рекомендации для сохранения здоровья биосферы и совершенствования общества и самого человека. В новых природных и производственных условиях человек нередко испытывает влияние весьма необычных, чрезмерных и жестких факторов среды, неадекватных его природе. Речь идет о специфической и весьма сложной социально-биологической адаптации в зонах экологического бедствия, в огромных городахгигантах, в условиях аридной зоны, Арктики, Антарктики и Заполярья, в подводных сооружениях и пещерах, в обитаемых космических летательных аппаратах. В исследовании физиологических механизмов адаптации человека в экстремальных природных и производственных условиях, разработке объективных критериев и путей оптимизации адаптации, а также создании таких важнейших новых направлений, как космическая, экологическая, социальная физиология, хронофизиология, высокогорная и спортивная физиология, несомненно, приоритет принадлежит отечественным ученым. Внедрение в науку современных электронно-вычислительных машин и механизмов позволило физиологам использовать в своих исследованиях современную аппаратуру и дало возможность при анализе качественно и количественно оценить полученные результаты. Знание важнейших физиологических закономерностей позволило в современных условиях создать их математические модели, с помощью которых жизненные процессы воспроизводят на компьютерах, исследуя различные варианты реакции при воздействии на организм лекарственных веществ, а также неблагоприятных экологических факторов. Союз физиологии и современных компьютеров, несомненно, оказывается полезным, особенно в чрезвычайных условиях при дефиците времени и проведении сложных исследований мозговой деятельности, хирургических операций, при реанимации, тяжелых отравлениях, но во всем нужна мера. Чрезмерное увлечение компьютерами, сложными приборами и механизмами деформирует мышление врача. Используя для физиологических исследований самую совершенную машину, надо помнить, что компьютер и любой механизм лишен абстрактного мышления, а главное – духовности. Знание физиологических закономерностей потребовалось не только для научной организации и повышения производительности труда. Использование действующих в организме принципов высочайшего совершенства в конструкции и управлении функциями живых организмов открывает новые перспективы для научно-технического прогресса, создания новейших машин и механизмов. На стыке физиологии и других естественных и технических наук рождаются новые науки и научные направления, в частности, бионика, иммунология, нейрокибернетика, биотехнология, биоэнергетика и другие. Физиология и экология человека синтезируют все естествознание в единую фундаментальную и всеобъемлющую науку о ЧЕЛОВЕКЕ.
Глава 2. Физиология возбудимых тканей
Способность адаптироваться к постоянно изменяющимся условиям внешней среды является одним из основных признаков живых систем. В основе приспособительных реакций организма лежит раздражимость – способность реагировать на действие различных факторов изменением структуры и функций. Раздражимостью обладают все ткани животных и растительных организмов. В процессе эволюции происходила постепенная дифференциация тканей, участвующих в приспособительной деятельности организма. Раздражимость этих тканей достигла наивысшего развития и трансформировалась в новое свойство – возбудимость. Под этим термином понимают способность ряда тканей (нервной, мышечной, железистой) отвечать на раздражение генерацией процесса возбуждения. Возбуждение – это сложный физиологический процесс временной деполяризации мембраны клеток, который проявляется специализированной реакцией ткани (проведение нервного импульса, сокращение мышцы, отделение секрета железой и т. д.). Возбудимостью обладают нервная, мышечная и секреторная ткани, которые называют возбудимыми тканями. Возбудимость различных тканей неодинакова. Ее величину оценивают по порогу раздражения – минимальной силе раздражителя, которая способна вызвать возбуждение. Менее сильные раздражители называются подпороговыми, а более сильные – сверхпороговыми. Раздражителями, вызывающими возбуждение, могут быть любые внешние (действующие из окружающей среды) или внутренние (возникающие в самом организме) воздействия. Все раздражители по их природе можно разделить на три группы: физические (механические, электрические, температурные, звуковые, световые), химические (щелочи, кислоты и другие химические вещества, в том числе и лекарственные) и биологические (вирусы, бактерии, насекомые и другие живые существа). По степени приспособленности биологических структур к их восприятию раздражители можно разделить на адекватные и не-адекватные. Адекватными называются раздражители, к восприятию которых биологическая структура специально приспособлена в процессе эволюции. Например, адекватным раздражителем для фоторецепторов является свет, для барорецепторов – изменение давления, для мышц – нервный импульс. Неадекватными называются такие раздражители, которые действуют на структуру, специально не приспособленную для их восприятия. Например, мышца может сокращаться под влиянием механического, теплового, электрического раздражений, хотя адекватным раздражителем для нее является нервный импульс. Пороговая сила неадекватных раздражителей во много раз превышает пороговую силу адекватных.Биоэлектрические явления в возбудимых тканях. Природа возбуждения
Возбуждение представляет собой сложную совокупность физических, химических и физико-химических процессов, в результате которых происходит быстрое и кратковременное изменение электрического потенциала мембраны. Первые исследования электрической активности живых тканей были проведены Л. Гальвани. Он обратил внимание на ссн сращение мышц препарата задних лапок лягушки, подвешенной на медном крючке, при соприкосновении с железными перилами балкона (первый опыт Гальвани). На основании этих наблюдений им был сделал вывод, что сокращение лапок вызвано «животным электричеством», которое возникает в спинном мозге и передается по металлическим проводникам (крючку и перилам) к мышцам. Физик А. Вольта, повторив этот опыт, пришел к другому заключению. Источником тока, по его мнению, является не спинной мозг и «животное электричество», а разность потенциалов, образующаяся в месте контакта разнородных металлов – меди и железа, а нервно-мышечный препарат лягушки является лишь проводником электричества. В ответ на эти возражения Л. Гальвани усовершенствовал опыт, исключив из него металлы. Он препарировал седалищный нерв вдоль бедра лапки лягушки, затем набрасывал нерв на мышцы голени, что вызывало сокращение мышцы (второй опыт Гальвани), тем самым доказав существование «животного электричества». Позднее Дюбуа-Реймоном было установлено, что поврежденный участок мышцы имеет отрицательный заряд, а неповрежденный участок – положительный. При набрасывании нерва между поврежденным и неповрежденным участками мышцы возникает ток, который раздражает нерв и вызывает сокращение мышцы. Этот ток был назван током покоя, или током повреждения. Так было показано, что наружная поверхность мышечных клеток заряжена положительно по отношению к внутреннему содержимому.Мембранный потенциал
В состоянии покоя между наружной и внутренней поверхностями мембраны клетки существует разность потенциалов, которая называется мембранным потенциалом [МП), или, если это клетка возбудимой ткани, – потенциалом покоя. Так как внутренняя сторона мембраны заряжена отрицательно по отношению к наружной, то, принимая потенциал наружного раствора за нуль, МП записывают со знаком «минус». Его величина у разных клеток колеблется от минус 30 до минус 100 мВ. Первая теория возникновения и поддержания мембранного потенциала была разработана Ю. Бернштейном (1902). Исходя из того, что мембрана клеток обладает высокой проницаемостью для ионов калия и малой проницаемостью для других ионов, он показал, что величину мембранного потенциала можно определить, используя формулу Нернста.Изменения мембранного потенциала. Пороговые и подпороговые раздражители
Если раздражать нейрон через электрод, находящийся в цитоплазме, кратковременными импульсами деполяризующего электрического тока различной величины, то, регистрируя через другой электрод изменения мембранного потенциала, можно наблюдать следующие биоэлектрические реакции: электротонический потенциал, локальный ответ и потенциал действия (рис.1). Если наносятся раздражения, величина которых не превышает 0,5 величины порогового раздражения, то деполяризация мембраны наблюдается только во время действия раздражителя. Это пассивная электротоническая деполяризация (электротонический потенциал). Развитие и исчезновение электротонического потенциала происходит по экспоненте и определяется параметрами раздражающего тока, а также свойствами мембраны (ее сопротивлением и емкостью). Во время развития электротонического потенциала проницаемость мембраны для ионов практически не изменяется.
Локальный ответ.
При увеличении амплитуды подпороговых раздражений от 0,5 до 0,9 пороговой величины развитие деполяризации мембраны происходит не прямолинейно, а по S-образной кривой. Деполяризация продолжает нарастать и после прекращения раздражения, а затем сравнительно медленно исчезает. Этот процесс получил название локального ответа.
Локальный ответ имеет следующие свойства: 1. возникает при действии подпороговых раздражителей; 2. находится в градуальной зависимости от силы стимула (не подчиняется закону «все или ничего»); локализуется в месте действия раздражителя и не способен к распространению на большие расстояния; 3. может распространяться лишь локально, при этом его амплитуда быстро уменьшается; 4. локальные ответы способны суммироваться, что приводит к увеличению деполяризации мембраны. В период развития локального ответа возрастает поток ионов натрия в клетку, что повышает ее возбудимость. Локальный ответ является экспериментальным феноменом, однако по перечисленным выше свойствам он близок к таким явлениям, как процесс местного нераспространяющегося возбуждения и возбуждающего постсинаптического потенциала (ВПСП), который возникает под влиянием деполяризующего действия возбуждающих медиаторов.
Потенциал действия
Потенциал действия (ПД) возникает на мембранах возбудимых клеток под влиянием раздражителя пороговой или сверхпороговой величины, который увеличивает проницаемость мембраны для ионов натрия. Ионы натрия начинают входить внутрь клетки, что приводит к уменьшению величины мембранного потенциала – деполяризации мембраны. При уменьшении МП до критического уровня деполяризации открываются потенциалозависимые каналы для натрия и проницаемость мембраны для этих ионов увеличивается в 500 раз (превышая проницаемость для ионов калия в 20 раз). В результате проникновения ионов натрия в цитоплазму и их взаимодействия с анионами разность потенциалов на мембране исчезает, а затем происходит перезарядка клеточной мембраны (инверсия заряда, овершут) – внутренняя поверхность мембраны заряжается положительно по отношению к наружной (на 30 – 50 мВ), после чего закрываются натриевые каналы и открываются потенциалозависимые калиевые каналы. В результате выхода калия из клетки начинается процесс восстановления исходного уровня мембранного потенциала покоя – реполяризация мембраны. Если такое повышение проводимости для калия предотвратить введением тетраэтиламмония, который избирательно блокирует калиевые каналы, мембрана реполяризуется гораздо медленнее. Натриевые каналы можно блокировать тетродотоксином и разблокировать последующим введением фермента проназы, который расщепляет белки. Таким образом, в основе возбуждения (генерации ПД) лежит повышение проводимости мембраны для натрия, вызываемое ее деполяризацией до порогового (критического) уровня.В потенциале действия различают следующие фазы: 1. Предспайк – процесс медленной деполяризации мембраны до критического уровня деполяризации (местное возбуждение, локальный ответ). 2. Пиковый потенциал, или спайк, состоящий из восходящей части (деполяризация мембраны) и нисходящей части (реполяризация мембраны). 3. Отрицательный следовой потенциал – от критического уровня деполяризации до исходного уровня поляризации мембраны (следовая деполяризация). 4. Положительный следовой потенциал – увеличение мембранного потенциала и постепенное возвращение его к исходной величине (следовая гиперполяризация).
Изменения возбудимости при возбуждении
При развитии потенциала действия происходят фазные изменения возбудимости ткани (рис. 2). Состоянию исходной поляризации мембраны (мембранный потенциал покоя) соответствует нормальный уровень возбудимости. В период предспайка возбудимость ткани повышена. Эта фаза возбудимости получила название повышенной возбудимости (первичной экзальтации). В это время мембранный потенциал приближается к критическому уровню деполяризации, поэтому дополнительный стимул, даже если он меньше порогового, может довести мембрану до критического уровня деполяризации. В период развития спайка (пикового потенциала) идет лавинообразное поступление ионов натрия внутрь клетки, в результате чего происходит перезарядка мембраны и она утрачивает способность отвечать возбуждением на раздражители даже сверхпороговой силы. Эта фаза возбудимости получила название абсолютной рефрактерности (абсолютной невозбудимости). Она длится до конца перезарядки мембраны и возникает в связи с тем, что натриевые каналы инактивируются. После окончания фазы перезарядки мембраны возбудимость ее постепенно восстанавливается до исходного уровня – фаза относительной рефрактерности. Она продолжается до восстановления заряда мембраны, достигая величины критического уровня деполяризации. Так как в этот период мембранный потенциал покоя еще не восстановлен, то возбудимость ткани понижена и новое возбуждение может возникнуть только при действии сверхпорогового раздражителя. Снижение возбудимости в фазу относительной рефрактерности связано с частичной инактивацией натриевых каналов и активацией калиевых. Периоду отрицательного следового потенциала соответствует повышенный уровень возбудимости (фаза вторичной экзальтации). Так как мембранный потенциал в эту фазу ближе к критическому уровню деполяризации по сравнению с состоянием покоя (исходной поляризацией), то порог раздражения снижен и новое возбуждение может возникнуть при действии раздражителей подпороговой силы. В период развития положительного следового потенциала возбудимость ткани понижена – фаза субнормальной возбудимости (вторичной рефрактерности). В эту фазу мембранный потенциал увеличивается (состояние гиперполяризации мембраны), удаляясь от критического уровня деполяризации, порог раздражения повышается и новое возбуждение может возникнуть только при действии раздражителей сверхпороговой величины. Рефрактерность мембраны является следствием того, что натриевый канал состоит из собственно канала (транспортной части) и воротного механизма, который управляется электрическим полем мембраны. В канале предполагают наличие двух типов «ворот» – быстрых активационных (ш) и медленных инактивационных (Л). «Ворота» могут быть полностью открыты или закрыты, например, в натриевом канале в состоянии покоя «ворота» т закрыты, а «ворота» h – открыты. При уменьшении заряда мембраны (деполяризации) в начальный момент «ворота» т и h открыты – канал способен проводить ионы. Через открытые каналы ионы движутся по концентрационному и электрохимическому градиенту. Затем инактивационные «ворота» закрываются, т. е. канал инактивируется. По мере восстановления МП инактивационные «ворота» медленно открываются, а активационные быстро закрываются и канал возвращается в исходное состояние. Следовая гиперполяризация мембраны может возникать вследствие трех причин: во-первых, продолжающимся выходом ионов калия; во-вторых, открытием каналов для хлора и поступлением этих ионов в клетку; в-третьих, усиленной работой натрий-калиевого насоса.Законы раздражения возбудимых тканей
Эти законы отражают определенную зависимость между действием раздражителя и ответной реакцией возбудимой ткани. К законам раздражения относятся: закон силы, закон «все или ничего», закон раздражения Дюбуа-Реймона (аккомодации), закон силы-времени (силы-длительности), закон полярного действия постоянного тока, закон физиологического электротона.Закон силы: чем больше сила раздражителя, тем больше величина ответной реакции. В соответствии с этим законом функционирует скелетная мышца. Амплитуда ее сокращений постепенно увеличивается с увеличением силы раздражителя вплоть до достижения максимальных значений. Это обусловлено тем, что скелетная мышца состоит из множества мышечных волокон, имеющих различную возбудимость. На пороговые раздражители отвечают только волокна, имеющие самую высокую возбудимость, амплитуда мышечного сокращения при этом минимальна. Увеличение силы раздражителя приводит к постепенному вовлечению волокон, имеющих меньшую возбудимость, поэтому амплитуда сокращения мышцы усиливается. Когда в реакции участвуют все мышечные волокна данной мышцы, дальнейшее повышение силы раздражителя не приводит к увеличению амплитуды сокращения.
Закон «все или ничего»: подпороговые раздражители не вызывают ответной реакции («ничего»), на пороговые раздражители возникает максимальная ответная реакция («все»). По закону «все или ничего» сокращаются сердечная мышца и одиночное мышечное волокно. Закон «все или ничего» не абсолютен. Вопервых, на раздражители подпороговой силы не возникает видимой ответной реакции, но в ткани происходят изменения мембранного потенциала покоя в виде возникновения местного возбуждения (локального ответа). Во-вторых, сердечная мышца, растянутая кровью, реагирует по закону «все или ничего», но амплитуда ее сокращения будет больше по сравнению с таковой при сокращении нерастянутой сердечной мышцы.
Закон раздражения Дюбуа-Реймона (аккомодации): стимулирующее действие постоянного тока зависит не только от абсолютной величины силы тока, но и от скорости нарастания тока во времени. При действии медленно нарастающего тока возбуждение не возникает, так как происходит приспособление возбудимой ткани к действию этого раздражителя, что получило название аккомодации. Аккомодация обусловлена тем, что при действии медленно нарастающего раздражителя в мембране происходит повышение критического уровня деполяризации. При снижении скорости нарастания силы раздражителя до некоторого минимального значения ПД не возникает, так как деполяризация мембраны является пусковым стимулом к началу двух процессов: быстрого, ведущего к повышению натриевой проницаемости и тем самым обусловливающего возникновение потенциала действия, и медленного, приводящего к инактивации натриевой проницаемости и как следствие этого – к окончанию потенциала действия. При быстром нарастании стимула повышение натриевой проницаемости успевает достичь значительной величины прежде, чем наступит инактивация натриевой проницаемости. При медленном нарастании тока на первый план выступают процессы инактивации, приводящие к повышению порога генерации ПД. Способность к аккомодации различных структур неодинакова. Наиболее высокая она у двигательных нервных волокон, а наиболее низкая у сердечной мышцы, гладких мышц кишечника, желудка. Исследования зависимости силы-длительности показали, что она имеет гиперболический характер. Ток меньше некоторой минимальной величины не вызывает возбуждение, как бы длительно он не действовал, и чем короче импульсы тока, тем меньшую раздражающую способность они имеют. Причиной такой зависимости является мембранная емкость. Очень «короткие» токи не успевают разрядить эту емкость до критического уровня деполяризации. Минимальная величина тока, способная вызвать возбуждение при неограниченно длительном его действии, называется реобазой. Время, в течение которого ток, равный реобазе, вызывает возбуждение, называется полезным временем.
Закон силы-времени: раздражающее действие постоянного тока зависит не только от еговеличины, но и от времени, в течение которого он действует. Чем больше ток, тем меньше времени он должен действовать на возбудимые ткани, чтобы вызвать возбуждение (рис.3).
 Закон полярного действия постоянного тока: при замыкании тока возбуждение возникает под катодом, а при размыкании – под анодом. Прохождение постоянного электрического тока через нервное или мышечное волокно вызывает изменение мембранного потенциала. Так, в области приложения катода положительный потенциал на наружной стороне мембраны уменьшается, возникает деполяризация, которая быстро достигает критического уровня и вызывает возбуждение. В области же приложения анода положительный потенциал на наружной стороне мембраны возрастает, происходит гиперполяризация мембраны и возбуждение не возникает. Но при этом под анодом критический уровень деполяризации смещается к уровню потенциала покоя. Поэтому при размыкании цепи тока гиперполяризация на мембране исчезает, и потенциал покоя, возвращаясь к исходной величине, достигает смещенного критического уровня и возникает возбуждение.
Закон полярного действия постоянного тока: при замыкании тока возбуждение возникает под катодом, а при размыкании – под анодом. Прохождение постоянного электрического тока через нервное или мышечное волокно вызывает изменение мембранного потенциала. Так, в области приложения катода положительный потенциал на наружной стороне мембраны уменьшается, возникает деполяризация, которая быстро достигает критического уровня и вызывает возбуждение. В области же приложения анода положительный потенциал на наружной стороне мембраны возрастает, происходит гиперполяризация мембраны и возбуждение не возникает. Но при этом под анодом критический уровень деполяризации смещается к уровню потенциала покоя. Поэтому при размыкании цепи тока гиперполяризация на мембране исчезает, и потенциал покоя, возвращаясь к исходной величине, достигает смещенного критического уровня и возникает возбуждение.
Закон физиологического электротона: действие постоянного тока на ткань сопровождается изменением ее возбудимости. При прохождении постоянного тока через нерв или мышцу порог раздражения под катодом и в соседних с ним участках понижается вследствие деполяризации мембраны (возбудимость повышается). В области приложения анода происходит повышение порога раздражения, т. е. снижение возбудимости вследствие гипериоляризации мембраны. Эти изменения возбудимости под катодом и анодом получили название электротона (электротоническое изменение возбудимости). Повышение возбудимости под катодам называется катэлектротоном, а снижение возбудимости иод анодом – анэлектротоном. При дальнейшем действии постоянного тока первоначальное повышение возбудимости под катодом сменяется ее понижением, развивается так называемая католическая депрессия. Первоначальное же снижение возбудимости под анодом сменяется ее повышением – анодная экзальтация. При этом в области приложения катода – инактивация натриевых каналов, а в области действия анода происходит снижение калиевой проницаемости и ослабление исходной инактивации натриевой проницаемости.
Физиология нервов и нервных волокон
Нервные волокна выполняют специализированную функцию – проведение нервных импульсов. По морфологическому признаку волокна делятся на миелиновые (покрытые миелиновой оболочкой) и безмиелиновые. Нерв состоит из большого числа нервных волокон (миелиновых и безмиелиновых), заключенных в общую оболочку. Нервное волокно обладает следующими свойствами: возбудимостью, проводимостью и лабильностью. Распространение возбуждения по нервным волокнам осуществляется на основе ионных механизмов генерации потенциала действия. При распространении возбуждения по безмиелиновому нервному волокну местные электрические токи, которые возникают между его возбужденным участком, заряженным отрицательно, и невозбужденными, Заряженными положительно, деполяризуют мембрану до критического уровня, что приводит к генерации ПД в соседних невозбужденных участках, которые становятся возбужденными, и т. д. Этот процесс происходит в каждой точке мембраны на всем протяжении волокна. Такое проведение возбуждения называется непрерывным. Возбуждение по нервному волокну может распространяться в обе стороны от места его возникновения. Если на нервное волокно наложить регистрирующие электроды на некотором расстоянии друг от друга, а между ними нанести раздражение, то возбуждение зафиксируют электроды по обе стороны от места раздражения. Наличие у миелиновых волокон оболочки, обладающей высоким электрическим сопротивлением, а также участков волокна, лишенных оболочки (перехватов Ранвье), приводит к тому, что местные электрические токи не могут проходить через миелин, они возникают только между соседними перехватами Ранвье, где деполяризуют мембрану невозбужденного перехвата и генерируют ПД (рис.4). Возбуждение как бы «перепрыгивает» через участки нервного волокна, покрытые миелином. Такой механизм распространения возбуждения называется сальтаторным, или скачкообразным, он позволяет более быстро и экономично передавать информацию по сравнению с непрерывным проведением, поскольку в него вовлекается не вся мембрана, а только ее небольшие участки. Амплитуда ПД в 5 6 раз превышает пороговую величину, не-обходимую для возбуждения соседнего перехвата, поэтому ПД может «перепрыгивать» не только через один, но и через несколько перехватов. Это явление может наблюдаться при снижении возбудимости соседнего перехвата под действием какого-либо фармакологического вещества, например, новокаина, кокаина и др.
Проведение возбуждения по нервному волокну возможно лишь в том случае, если сохранена его анатомическая и физиологическая целостность. Различные факторы, изменяющие свойства волокон (наркотические вещества, охлаждение, перевязка и т. д.), приводят к нарушению передачи возбуждения.
Возбуждение по нервному волокну, входящему в состав нерва, распространяется изолированно, т. е. не переходя с одного волокна на другое. Это обусловлено тем, что сопротивление жидкости, заполняющей межклеточные пространства, значительно ниже сопротивления мембраны нервных волокон, и основная часть тока, возникающего между возбужденным и невозбужденным участками, проходит по межклеточной жидкости, не действуя на другие волокна. Если бы возбуждение передавалось с одного нервного волокна на другое, то нормальное функционирование организма было бы невозможно, так как нервы содержат большое количество чувствительных, двигательных, вегетативных волокон, которые несут информацию как от различных рецепторов к ЦНС, так и от ЦНС к эффекторным органам.
Нервные волокна по скорости проведения возбуждения делятся на три типа: А, В, С. Волокна типа А, в свою очередь, делятся на подтипы: А-а, А-р, А-у, А-5 (рис. 5).
Амплитуда ПД в 5 6 раз превышает пороговую величину, не-обходимую для возбуждения соседнего перехвата, поэтому ПД может «перепрыгивать» не только через один, но и через несколько перехватов. Это явление может наблюдаться при снижении возбудимости соседнего перехвата под действием какого-либо фармакологического вещества, например, новокаина, кокаина и др.
Проведение возбуждения по нервному волокну возможно лишь в том случае, если сохранена его анатомическая и физиологическая целостность. Различные факторы, изменяющие свойства волокон (наркотические вещества, охлаждение, перевязка и т. д.), приводят к нарушению передачи возбуждения.
Возбуждение по нервному волокну, входящему в состав нерва, распространяется изолированно, т. е. не переходя с одного волокна на другое. Это обусловлено тем, что сопротивление жидкости, заполняющей межклеточные пространства, значительно ниже сопротивления мембраны нервных волокон, и основная часть тока, возникающего между возбужденным и невозбужденным участками, проходит по межклеточной жидкости, не действуя на другие волокна. Если бы возбуждение передавалось с одного нервного волокна на другое, то нормальное функционирование организма было бы невозможно, так как нервы содержат большое количество чувствительных, двигательных, вегетативных волокон, которые несут информацию как от различных рецепторов к ЦНС, так и от ЦНС к эффекторным органам.
Нервные волокна по скорости проведения возбуждения делятся на три типа: А, В, С. Волокна типа А, в свою очередь, делятся на подтипы: А-а, А-р, А-у, А-5 (рис. 5).
 Волокна типа А покрыты миелиновой оболочкой. Наиболее толстые из них А-а имеют диаметр 12 – 22 мкм и скорость проведения возбуждения 70–120 м/с. Эти волокна проводят возбуждение от моторных нервных центров спинного мозга к скелетным мышцам (двигательные волокна) и от рецепторов мышц к соответствующим нервным центрам.
Три другие группы волокон типа А (р, у, 5) имеют меньший диаметр – от 8 до 1 мкм и меньшую скорость проведения возбуждения – от 5 до 70 м/с. Волокна этих групп преимущественно проводят возбуждение от различных рецепторов (тактильных, температурных, болевых, рецепторов внутренних органов) в ЦНС, за исключением у-волокон, значительная часть которых проводит возбуждение от спинного мозга к интрафузальным мышечным волокнам.
К волокнам типа В относятся миелинизироваыные преганглионарные волокна вегетативной нервной системы. Их диаметр – 1 – 3,5 мкм, а скорость проведения возбуждения – 3–18 м/с.
К волокнам типа С относятся безмиелиповые нервные волокна малого диаметра – 0,5 – 2 мкм. Скорость проведения возбуждения в этих волокнах не более 3 м/с (0,5 – 3 м/с). Большинство волокон типа С – это постганглионарные волокна симпатического отдела вегетативной нервной системы, а также нервные волокна, которые проводят возбуждение от болевых рецепторов, некоторых терморецепторов и рецепторов давления.
Нервные волокна обладают лабильностью (функциональной подвижностью) – способностью воспроизводить определенное количество циклов возбуждения в единицу времени в соответствии с ритмом действующих раздражителей. Мерой лабильности является максимальное количество циклов возбуждения, которое способно воспроизвести нервное волокно в соответствии с ритмом раздражения без искажений. Лабильность определяется длительностью потенциала действия (длительностью фазы абсолютной рефрактерности), у нервных волокон лабильность очень высокая (до 1000 Гц).
Н. Е. Введенский (1891 г.) обнаружил, что если участок нерва подвергнуть воздействию повреждающего агента (химического вещества, нагревания или охлаждения, постоянного тока), то лабильность такого участка резко снижается. Восстановление исходного состояния нервного волокна после каждого потенциала действия в поврежденном участке происходит медленно. При действии на этот участок частых раздражителей он не может воспроизвести ритм раздражения – проведение импульсов нарушается. Такое состояние было названо парабиозом. В развитии парабиоза различают три последовательно сменяющие друг друга фазы: уравнительную, парадоксальную, тормозную.
В уравнительную фазу ответные реакции на частые и редкие раздражители становятся одинаковыми. В нормальных условиях величина ответной реакции иннервируемых нервом мышечных волокон зависит от частоты раздражения: на редкие раздражители ответная реакция меньше, а на частые – больше. В начальную стадию парабиоза при редком ритме раздражений (25 Гц) все импульсы проводятся через поврежденный участок, так как возбудимость после предыдущего импульса успевает восстановиться. При высоком ритме раздражений (100 Гц) последующие импульсы могут поступать в период рефрактерности, поэтому часть импульсов не проводится. Например, если проводится только каждое четвертое возбуждение (т. е. 25 импульсов из 100), то амплитуда ответной реакции становится такой же, как на редкие раздражители (25 Гц) – происходит уравнивание ответной реакции.
В парадоксальную фазу происходит дальнейшее снижение лабильности. Ответная реакция возникает и на редкие, и на частые раздражители, но на частые она меньше, так как они еще больше снижают лабильность, удлиняя фазу абсолютной рефрактерности. В результате ответная реакция на редкие раздражители будет больше, чем на частые.
В тормозную фазу и редкие, и частые раздражители не вызывают ответной реакции. При этом мембрана нервного волокна де-поляризована и не способна генерировать ПД, т. е. нерв утрачивает способность к проведению возбуждений.
Явление парабиоза лежит в основе локального обезболивания. Влияние анестезирующих веществ связано с нарушением механизма проведения возбуждения по нервным волокнам и снижением лабильности. Парабиоз – явление обратимое. Если парабнотическое вещество действует недолго, то после прекращения его действия нерв выходит из состояния парабиоза через те же фазы, по в обратной последовательности.
Возникновение парабиотического состояния связано с тем, что при действии на нервное волокно парабиотического фактора нарушается способность мембраны увеличивать натриевую проницаемость (инактивация натриевых каналов) в ответ на раздражение, и проведение следующего импульса блокируемся.
Волокна типа А покрыты миелиновой оболочкой. Наиболее толстые из них А-а имеют диаметр 12 – 22 мкм и скорость проведения возбуждения 70–120 м/с. Эти волокна проводят возбуждение от моторных нервных центров спинного мозга к скелетным мышцам (двигательные волокна) и от рецепторов мышц к соответствующим нервным центрам.
Три другие группы волокон типа А (р, у, 5) имеют меньший диаметр – от 8 до 1 мкм и меньшую скорость проведения возбуждения – от 5 до 70 м/с. Волокна этих групп преимущественно проводят возбуждение от различных рецепторов (тактильных, температурных, болевых, рецепторов внутренних органов) в ЦНС, за исключением у-волокон, значительная часть которых проводит возбуждение от спинного мозга к интрафузальным мышечным волокнам.
К волокнам типа В относятся миелинизироваыные преганглионарные волокна вегетативной нервной системы. Их диаметр – 1 – 3,5 мкм, а скорость проведения возбуждения – 3–18 м/с.
К волокнам типа С относятся безмиелиповые нервные волокна малого диаметра – 0,5 – 2 мкм. Скорость проведения возбуждения в этих волокнах не более 3 м/с (0,5 – 3 м/с). Большинство волокон типа С – это постганглионарные волокна симпатического отдела вегетативной нервной системы, а также нервные волокна, которые проводят возбуждение от болевых рецепторов, некоторых терморецепторов и рецепторов давления.
Нервные волокна обладают лабильностью (функциональной подвижностью) – способностью воспроизводить определенное количество циклов возбуждения в единицу времени в соответствии с ритмом действующих раздражителей. Мерой лабильности является максимальное количество циклов возбуждения, которое способно воспроизвести нервное волокно в соответствии с ритмом раздражения без искажений. Лабильность определяется длительностью потенциала действия (длительностью фазы абсолютной рефрактерности), у нервных волокон лабильность очень высокая (до 1000 Гц).
Н. Е. Введенский (1891 г.) обнаружил, что если участок нерва подвергнуть воздействию повреждающего агента (химического вещества, нагревания или охлаждения, постоянного тока), то лабильность такого участка резко снижается. Восстановление исходного состояния нервного волокна после каждого потенциала действия в поврежденном участке происходит медленно. При действии на этот участок частых раздражителей он не может воспроизвести ритм раздражения – проведение импульсов нарушается. Такое состояние было названо парабиозом. В развитии парабиоза различают три последовательно сменяющие друг друга фазы: уравнительную, парадоксальную, тормозную.
В уравнительную фазу ответные реакции на частые и редкие раздражители становятся одинаковыми. В нормальных условиях величина ответной реакции иннервируемых нервом мышечных волокон зависит от частоты раздражения: на редкие раздражители ответная реакция меньше, а на частые – больше. В начальную стадию парабиоза при редком ритме раздражений (25 Гц) все импульсы проводятся через поврежденный участок, так как возбудимость после предыдущего импульса успевает восстановиться. При высоком ритме раздражений (100 Гц) последующие импульсы могут поступать в период рефрактерности, поэтому часть импульсов не проводится. Например, если проводится только каждое четвертое возбуждение (т. е. 25 импульсов из 100), то амплитуда ответной реакции становится такой же, как на редкие раздражители (25 Гц) – происходит уравнивание ответной реакции.
В парадоксальную фазу происходит дальнейшее снижение лабильности. Ответная реакция возникает и на редкие, и на частые раздражители, но на частые она меньше, так как они еще больше снижают лабильность, удлиняя фазу абсолютной рефрактерности. В результате ответная реакция на редкие раздражители будет больше, чем на частые.
В тормозную фазу и редкие, и частые раздражители не вызывают ответной реакции. При этом мембрана нервного волокна де-поляризована и не способна генерировать ПД, т. е. нерв утрачивает способность к проведению возбуждений.
Явление парабиоза лежит в основе локального обезболивания. Влияние анестезирующих веществ связано с нарушением механизма проведения возбуждения по нервным волокнам и снижением лабильности. Парабиоз – явление обратимое. Если парабнотическое вещество действует недолго, то после прекращения его действия нерв выходит из состояния парабиоза через те же фазы, по в обратной последовательности.
Возникновение парабиотического состояния связано с тем, что при действии на нервное волокно парабиотического фактора нарушается способность мембраны увеличивать натриевую проницаемость (инактивация натриевых каналов) в ответ на раздражение, и проведение следующего импульса блокируемся.
Физиология мышц
Существует три типа мышц: поперечно-полосатые скелетные мышцы, поперечно-полосатая сердечная мышца и гладкие мышцы.Мышцы обладают следующими физиологическими свойствами: 1. возбудимостью, т. е. способностью возбуждаться при действии раздражителей; 2. проводимостью – способностью проводить возбуждение; 3. сократимостью – способностью изменять свою длину или напряжение при возбуждении; 4. растяжимостью – способностью изменять свою длину под действием растягивающей силы; 5. эластичностью – способностью восстанавливать свою первоначальную длину после прекращения растяжения.
Сила мышцы определяется максимальным грузом, который мышца может поднять. Мышцы способны совершать работу. Работа мышц определяется произведением величины поднятого груза на высоту подъема. Максимальная работа производится при средних величинах нагрузок. Лабильность мышцы равна 200–300 Гц. При непосредственном раздражении мышцы (прямое раздражение) или опосредованно через иннервирующий ее двигательный нерв (непрямое раздражение) одиночным стимулом возникает одиночное мышечное сокращение, в котором выделяют три фазы: латентный период. – время от начала действия раздражителя до начала ответной реакции; фазу сокращения (фаза укорочения) и фазу расслабления. В естественных условиях к скелетной мышце из ЦНС поступают не одиночные импульсы, а серия импульсов, на которые мышца отвечает длительным сокращением. Длительное сокращение мышцы, возникающее в ответ на ритмическое раздражение, называется тетаническим сокращением, или тетанусом (рис.6). Различают два вида тетануса: зубчатый и гладкий.
 Если каждый последующий стимул поступает к мышце в тот период, когда она находится в фазе укорочения, то возникает гладкий тетанус, а если в фазу расслабления – зубчатый тетанус.
Амплитуда тетанического сокращения превышает амплитуду одиночного мышечного сокращения. Н. Е. Введенский объяснил это явление фазными изменениями возбудимости мышцы, введя понятие об оптимуме и пессимуме частоты раздражения. Оптимум – такая частота раздражения, при которой каждое последующее раздражение наносится в фазу повышенной возбудимости. Тетанус при этом будет максимальным по амплитуде. Пессимум – такая частота раздражения, при которой каждое последующее раздражение наносится в фазу пониженной возбудимости. Амплитуда тетануса при этом будет минимальной.
Различают несколько видов мышечных сокращений: изотонический, изометрический и смешанный. При изотоническом сокращении мышцы происходит изменение ее длины, а напряжение остается постоянным. Такое сокращение происходит в том случае, если отсутствует сопротивление изменению ее длины. К изотоническому типу сокращений относятся сокращения мышц языка. При изометрическом сокращении длина мышечных волокон остается постоянной, а их напряжение возрастает. Такое сокращение мышцы возникает при попытке поднять чрезмерно большой груз. В естественных условиях сокращения мышц никогда не бывают чисто изотоническими или изометрическими, они имеют смешанный характер, т. е. происходит изменение и длины, и напряжения мышцы.
Если каждый последующий стимул поступает к мышце в тот период, когда она находится в фазе укорочения, то возникает гладкий тетанус, а если в фазу расслабления – зубчатый тетанус.
Амплитуда тетанического сокращения превышает амплитуду одиночного мышечного сокращения. Н. Е. Введенский объяснил это явление фазными изменениями возбудимости мышцы, введя понятие об оптимуме и пессимуме частоты раздражения. Оптимум – такая частота раздражения, при которой каждое последующее раздражение наносится в фазу повышенной возбудимости. Тетанус при этом будет максимальным по амплитуде. Пессимум – такая частота раздражения, при которой каждое последующее раздражение наносится в фазу пониженной возбудимости. Амплитуда тетануса при этом будет минимальной.
Различают несколько видов мышечных сокращений: изотонический, изометрический и смешанный. При изотоническом сокращении мышцы происходит изменение ее длины, а напряжение остается постоянным. Такое сокращение происходит в том случае, если отсутствует сопротивление изменению ее длины. К изотоническому типу сокращений относятся сокращения мышц языка. При изометрическом сокращении длина мышечных волокон остается постоянной, а их напряжение возрастает. Такое сокращение мышцы возникает при попытке поднять чрезмерно большой груз. В естественных условиях сокращения мышц никогда не бывают чисто изотоническими или изометрическими, они имеют смешанный характер, т. е. происходит изменение и длины, и напряжения мышцы.
Механизм мышечного сокращения
Мышцы состоят из мышечных волокон, а те – из множества тонких нитей – миофибрилл, расположенных продольно. Каждая миофибрилла состоит из нитей сократительных белков актина и миозина. Перегородки, называемые Z-пластинами, разделяют миофибриллы на участки – саркомеры. В саркомере чередуются поперечные светлые и темные полосы. Поперечная исчерченность миофибрилл обусловлена определенным расположением нитей актина и миозина. В центральной части каждого саркомера расположены толстые нити миозина. На обоих концах саркомера находятся тонкие нити актина, прикрепленные к Z-пластинам. Нити миозина выглядят в световом микроскопе как светлая полоска (Н-зона) в темном диске, который содержит нити миозина и актина и называется анизотропным, или А-диском. По обе стороны от А-диска находятся участки, которые содержат только тонкие нити актина и кажутся светлыми, они называются изотропными, или I-дисками. По их середине проходит темная линия – Z-мембрана. Благодаря такому периодическому чередованию светлых и темных дисков сердечная и скелетная мышцы выглядят поперечно-полосатыми (рис.7). В состоянии покоя концы толстых и тонких нитей лишь незначительно перекрываются на уровне А-диска. При сокращении тонкие актиновые нити скользят вдоль толстых миозиновых нитей, двигаясь между ними к середине саркомера. Сами актиновые и миозиновые нити своей длины не изменяют. Миозиновые нити имеют поперечные мостики (выступы) с головками, которые отходят от нити биполярно. Актиновая нить состоит из двух закрученных одна вокруг другой цепочек молекул актина. На нитях актина расположены молекулы тропонина, а в желобках между двумя актина лежат нити тропомиозина. Молекулы тропомиозина в покое располагаются так, что предотвращают прикрепление поперечных мостиков миозина к актиновым нитям. Во многих местах участки поверхностной мембраны мышечной клетки углубляются в виде трубочек внутрь волокна, перпендикулярно его продольной оси, образуя систему поперечных трубочек (Т-систему). Параллельно миофибриллам и перпендикулярно поперечным трубочкам расположена система продольных трубочек (альфа-система). Пузырьки на концах этих трубочек, в которых сосредоточено основное количество внутриклеточного кальция, подходят очень близко к поперечным трубочкам, образуя совместно с ними так называемые триады. В состоянии покоя миозиновый мостик заряжен энергией (миозин фосфорилирован), но он не может соединиться с нитью актина, так как между ними находится система из нитей тропомиозина и молекул тропонина. При возбуждении ПД распространяется по мембранам Тсистемы внутрь клетки и вызывает высвобождение ионов кальция из альфа-системы. С появлением ионов кальция в присутствии АТФ происходит изменение пространственного положения тропонина – нить тропомиозина сдвигается и открываются участки актина, присоединяющие миозиновые головки. Соединение головки фосфорилированного миозина с актином приводит к изменению положения мостика (его «сгибанию»), в результате нити актина перемещаются на 1 мм к середине саркомера. Затем происходит отсоединение мостика от актина. Ритмические прикрепления и отсоединения головок миозина тянут актиновую нить к середине саркомера.
При отсутствии повторного возбуждения ионы кальция закачиваются кальциевым насосом из межфибриллярного пространства в систему саркоплазматического ретикулума. Это приводит к снижению концентрации ионов кальция и отсоединению его от тропонина. Вследствие чего тропомиозин возвращается на прежнее место и снова блокирует активные центры актина. Затем происходит фосфорилирование миозина за счет АТФ, что также способствует временному разобщению нитей. Расслабление мышцы после ее сокращения происходит пассивно – актиновые и миозиновые нити легко скользят в обратном направлении под влиянием сил упругости мышечных волокон, а также сокращения мышц-антагонистов.
Во многих местах участки поверхностной мембраны мышечной клетки углубляются в виде трубочек внутрь волокна, перпендикулярно его продольной оси, образуя систему поперечных трубочек (Т-систему). Параллельно миофибриллам и перпендикулярно поперечным трубочкам расположена система продольных трубочек (альфа-система). Пузырьки на концах этих трубочек, в которых сосредоточено основное количество внутриклеточного кальция, подходят очень близко к поперечным трубочкам, образуя совместно с ними так называемые триады. В состоянии покоя миозиновый мостик заряжен энергией (миозин фосфорилирован), но он не может соединиться с нитью актина, так как между ними находится система из нитей тропомиозина и молекул тропонина. При возбуждении ПД распространяется по мембранам Тсистемы внутрь клетки и вызывает высвобождение ионов кальция из альфа-системы. С появлением ионов кальция в присутствии АТФ происходит изменение пространственного положения тропонина – нить тропомиозина сдвигается и открываются участки актина, присоединяющие миозиновые головки. Соединение головки фосфорилированного миозина с актином приводит к изменению положения мостика (его «сгибанию»), в результате нити актина перемещаются на 1 мм к середине саркомера. Затем происходит отсоединение мостика от актина. Ритмические прикрепления и отсоединения головок миозина тянут актиновую нить к середине саркомера.
При отсутствии повторного возбуждения ионы кальция закачиваются кальциевым насосом из межфибриллярного пространства в систему саркоплазматического ретикулума. Это приводит к снижению концентрации ионов кальция и отсоединению его от тропонина. Вследствие чего тропомиозин возвращается на прежнее место и снова блокирует активные центры актина. Затем происходит фосфорилирование миозина за счет АТФ, что также способствует временному разобщению нитей. Расслабление мышцы после ее сокращения происходит пассивно – актиновые и миозиновые нити легко скользят в обратном направлении под влиянием сил упругости мышечных волокон, а также сокращения мышц-антагонистов.
Гладкие мышцы
Эти мышцы образуют мышечные слои стенок желудка, кишечника, мочеточников, бронхов, кровеносных сосудов и других внутренних органов. Они построены из веретенообразных одноядерных мышечных клеток. Гладкие мышцы разделяются на две основные группы: мультиунитарные и унитарные. Мультиунитарные мышцы функционируют независимо друг от друга, и каждое волокно может иннервироваться отдельным нервным окончанием. Такие волокна обнаружены в ресничной мышце глаза, мигательной перепонке и мышечных слоях некоторых крупных сосудов, к ним относятся мышцы, поднимающие волосы. У унитарных мышц волокна настолько тесно переплетены, что их мембраны могуг сливаться, образуя электрические контакты (нексусы). При раздражении одного волокна за счет этих контактов ПД быстро распространяются на соседние волокна. Поэтому, несмотря на то, что двигательные нервные окончания расположены на небольшом числе мышечных волокон, в реакцию вовлекается вся мышца. Такие мышцы имеются в большинстве органов: пищеварительном тракте, матке, в мочеточниках. Особенностью гладких мышц является их способность осуществлять медленные и длительные тонические сокращения. Медленные, ритмические сокращения гладких мышц желудка, кишечника, мочеточников и других органов обеспечивают перемещение содержимого этих органов. Длительные тонические сокращения гладких мышц обеспечивают функционирование сфинктеров полых органов, которые препятствуют выходу их содержимого. Гладкие мышцы стенок кровеносных сосудов, особенно артерий и артериол, также находятся в состоянии постоянного тонического сокращения. Изменение тонуса мышц стенок артериальных сосудов влияет на величину их просвета и, следовательно, на уровень кровяного давления и кровоснабжения органов. Важным свойством гладких мышц является их пластичность, т. е. способность сохранять приданную им при растяжении длину. Скелетная мышца в норме почти не обладает пластичностью. При удалении растягивающего груза скелетная мышца быстро укорачивается, а гладкая остается растянутой. Высокая пластичность гладких мышц имеет большое значение для нормального функционирования полых органов. Например, пластичность мышц мочевого пузыря по мере его наполнения предотвращает избыточное повышение давления. Сильное и резкое растяжение гладких мышц вызывает их сокращение, что обусловлено нарастающей при растяжении деполяризацией клеток, которая обеспечивает автоматию гладкой мышцы. Такое сокращение играет важную роль в авторегуляции тонуса кровеносных сосудов, а также способствует непроизвольному опорожнению переполненного мочевого пузыря в тех случаях, когда нервная регуляция отсутствует в результате повреждения спинного мозга. В гладких мышцах тетаническое сокращение возникает при низкой частоте стимуляции. В отличие от скелетных, гладкие мышцы способны развивать спонтанные тетанообразные сокращения в условиях денервации и даже после блокады интрамуральных ганглиев. Такие сокращения возникают вследствие активности клеток, обладающих автоматией (пейсмекерных клеток), которые отличаются по электрофизиологическим свойствам от других мышечных клеток. В них появляются пейсмекерные потенциалы, деполяризующие мембрану до критического уровня, что вызывает возникновение потенциала действия. Особенностью гладких мышц является их высокая чувствительность к медиаторам, которые оказывают на спонтанную активность пейсмекеров модулирующие влияния. При нанесении ацетилхолина на препарат мышцы толстой кишки частота ПД возрастает. Вызываемые ими сокращения сливаются, образуется почти гладкий тетанус. Чем выше частота ПД, тем сильнее сокращение. Норадреналин, напротив, гиперполяризует мембрану, снижая частоту ПД и величину тетануса. Возбуждение гладкомышечных клеток вызывает повышение концентрации кальция в саркоплазме, что активирует сократительные структуры. Так же как сердечная и скелетная мышцы, гладкая мышца расслабляется при снижении концентрации ионов кальция. Расслабление гладких мышц происходит медленнее, так как удаление ионов кальция замедлено.Физиология синапсов
Термин «синапс» был введен Ч. Шеррингтоном. Синапсом называется функциональное соединение между нервной клеткой и другими клетками. Синапсы – это те участки, где нервные импульсы могут влиять на деятельность постсинаптической клетки, возбуждая или тормозя ее. Существуют две разновидности синапсов: электрические и химические. В химическом синапсе выделяется медиатор, генерирующий потенциалы на постсинаптической мембране, а в электрическом от пресинаптического нейрона к постсинаптическому идет электрический ток.Электрические синапсы.
Этим синапсам свойственны очень узкая синаптическая щель и очень низкое удельное сопротивление пре- и постсинаптических мембран, что обеспечивает прохождение локальных электрических токов. Низкое сопротивление связано с наличием каналов, пересекающих обе мембраны, т. е. идущих из клетки в клетку (щелевой контакт). Каналы образуются белковыми молекулами контактирующих мембран, которые соединяются комплементарно. Ток, вызванный пресинаптическим потенциалом действия, раздражает постсинаптическую мембрану, где возникает ВПСП, а затем и потенциал действия. Электрические синапсы формируются, как правило, между клетками одного типа (например, между клетками сердечной мышцы).Химические синапсы
Химические синапсы можно классифицировать по их местоположению и принадлежности соответствующим структурам: периферические (нервно-мышечные, нейросекреторные, рецепторно-нейрональные); центральные (аксосоматические, аксодендритные, аксоаксональные, соматодендритные, соматосоматические); по знаку их действия – возбуждающие и тормозящие; по медиатору, который осуществляет передачу, – холинергические, адренергические, серотонинергические, глицинергические и т. д. Синапс состоит из трех основных элементов: пресинаптической мембраны, постсинаптической мембраны и синаптической щели. Особенностью постсинаптической мембраны является наличие в ней специальных рецепторов, чувствительных к определенному медиатору, и наличие хемозависимых ионных каналов. Возбуждение передается с помощью медиаторов (посредников). Медиаторы – это химические вещества, которые в зависимости от их природы делятся на следующие группы: моноамины (ацетилхолин, дофамин, норадреналин, серотонин), аминокислоты (гамма-аминомасляная кислота – ГАМК, глутаминовая кислота, глицин и др.) и нейропептиды (вещество Р, эндорфины, нейротензин, ангиотензин, вазопрессин, соматостатин и др.). Медиатор находится в пузырьках пресинаптического утолщения, куда он может поступать либо из центральной области нейрона с по-мощью аксонального транспорта, либо за счет обратного захвата медиатора из синаптической щели. Он может также синтезироваться в синаптических терминалях из продуктов его расщепления. Когда к окончанию аксона приходит ПД и пресинаптическая мембрана деполяризуется, ионы кальция начинают поступать из внеклеточной жидкости внутрь нервного окончания (рис. 8). Кальций активирует перемещение синаптических пузырьков к пресинаптической мембране, где они разрушаются с выходом медиатора в синаптическую щель. В возбуждающих синапсах медиатор диффундирует в щели и связывается с рецепторами постсинаптической мембраны, что приводит к открытию каналов для ионов натрия, а следовательно, к ее деполяризации – возникновению возбуждающего постсинаптического потенциала (ВПСП). Между деполяризованной мембраной и соседними с ней участками возникают местные токи. Если они деполяризуют мембрану до критического уровня, то в ней возникает потенциал действия. В тормозных синапсах медиатор (например, глицин) аналогичным образом взаимодействует с рецепторами постсинаптической мембраны, но открывает в ней калиевые и/или хлорные каналы, что вызывает переход ионов по концентрационному градиенту: калия из клетки, а хлора – внутрь клетки. Это приводит к гиперполяризации постсинаптической мембраны – возникновению тормозного постсинаптического потенциала (ТПСП). Один и тот же медиатор может связываться не с одним, а с несколькими различными рецепторами. Так, ацетилхолин в нервно-мышечных синапсах скелетных мышц взаимодействует с Н-холинорецепторами, которые открывают каналы для натрия, что вызывает ВПСП, а в вагосердечных синапсах он действует на М-холинорецепторы, открывающие каналы для ионов калия (ге-нерируется ТПСП). Следовательно, возбуждающий или тормозной характер действия медиатора определяется свойствами постсинаптической мембраны (видом рецептора), а не самого медиатора.
Кроме нейромедиаторов, пресинаптические окончания выделяют вещества, которые не участвуют непосредственно в передаче сигнала и играют роль нейромодуляторов эффектов сигнала. Модуляция осуществляется влиянием либо на выделение медиатора, либо на его связывание рецепторами постсинаптического нейрона, а также на реакцию этого нейрона на медиаторы. Функцию классических медиаторов выполняют амины и аминокислоты, функцию нейромодуляторов – нейропептиды. Медиаторы синтезируются в основном в терминалях аксона, нейропептиды образуются в теле нейрона путем синтеза белков, от которых они отщепляются под влиянием протеаз.
Синапсы с химической передачей возбуждения обладают рядом общих свойств: возбуждение через синапсы проводится только в одном направлении, что обусловлено строением синапса (медиатор выделяется только из пресинаптической мембраны и взаимодействует с рецепторами постсинаптической мембраны); передача возбуждения через синапсы осуществляется медленнее, чем по нервному волокну (синаптическая задержка); синапсы обладают низкой лабильностью и высокой утомляемостью, а также высокой чувствительностью к химическим (в том числе и к фармакологическим) веществам; в синапсах происходит трансформация ритма возбуждения.
Один и тот же медиатор может связываться не с одним, а с несколькими различными рецепторами. Так, ацетилхолин в нервно-мышечных синапсах скелетных мышц взаимодействует с Н-холинорецепторами, которые открывают каналы для натрия, что вызывает ВПСП, а в вагосердечных синапсах он действует на М-холинорецепторы, открывающие каналы для ионов калия (ге-нерируется ТПСП). Следовательно, возбуждающий или тормозной характер действия медиатора определяется свойствами постсинаптической мембраны (видом рецептора), а не самого медиатора.
Кроме нейромедиаторов, пресинаптические окончания выделяют вещества, которые не участвуют непосредственно в передаче сигнала и играют роль нейромодуляторов эффектов сигнала. Модуляция осуществляется влиянием либо на выделение медиатора, либо на его связывание рецепторами постсинаптического нейрона, а также на реакцию этого нейрона на медиаторы. Функцию классических медиаторов выполняют амины и аминокислоты, функцию нейромодуляторов – нейропептиды. Медиаторы синтезируются в основном в терминалях аксона, нейропептиды образуются в теле нейрона путем синтеза белков, от которых они отщепляются под влиянием протеаз.
Синапсы с химической передачей возбуждения обладают рядом общих свойств: возбуждение через синапсы проводится только в одном направлении, что обусловлено строением синапса (медиатор выделяется только из пресинаптической мембраны и взаимодействует с рецепторами постсинаптической мембраны); передача возбуждения через синапсы осуществляется медленнее, чем по нервному волокну (синаптическая задержка); синапсы обладают низкой лабильностью и высокой утомляемостью, а также высокой чувствительностью к химическим (в том числе и к фармакологическим) веществам; в синапсах происходит трансформация ритма возбуждения.
Фармакологические влияния на возбудимые ткани
Существует большое число препаратов, способных влиять на передачу возбуждения и торможения в химических синапсах. В зависимости от вида синапсов и характера действия их делят на несколько групп. Холинотропные средства влияют на передачу нервного импульса в холинергических синапсах. Эти вещества по строению близки к молекуле ацетилхолина и могут взаимодействовать либо с холинорецепторами, либо с инактивирующими ферментами (ацетилхолинэстераза, бутирилхолинэстераза). Холинотропные средства делят на стимулирующие холинорецепторы – холиномиметики и блокирующие эти рецепторы – холинолитики. Холиномиметики – вещества, имитирующие эффекты ацетилхолина. К М-холиномиметикам относятся пилокарпин, ацеклидин, карбахолин. Н-холиномиметическими средствами являются лобелин, цитизин, анабазин, карбахолин. Непрямые холиномиметические средства (физостигмина салицилат, галантамина гидробромид, прозерин, оксазил) сами не влияют на холинорецепторы, а усиливают действие медиатора, предупреждая его разрушение (угнетая обе холинэстеразы). Холиноблокирующие (холинолитические) средства делятся на М- и Н-холинолитики. К М-холинолитическим препаратам относятся атропин, скополамин, платифиллин, метацин. Н-холинолитики можно разделить на ганглиоблокаторы и миорелаксанты. Ганглиоблокаторы (пахикарпин, пирилен, бензогексоний, пентамин и др.) нарушают проведение импульсов через вегетативные ганглии. Миорелаксанты вызывают расслабление скелетных мышц. Различают антидеполяризующие (d-тубокурарин, ардуан) и деполяризующие (дитилин и др.) миорелаксанты. Деполяризующие миорелаксанты сначала кратковременно активируют Н-холинорецепторы, в результате возникает деполяризация (длящаяся несколько секунд) мембраны рецептора, сопровождающаяся фибрилляцией скелетных мышц. Деполяризация сменяется потерей чувствительности к ацетилхолину – десентизацией, которая длится несколько минут. Она возникает как следствие изменения конформации рецептора и тормозящего влияния ионов кальция (в избытке попавших внутрь мышечного волокна в момент длительной деполяризации) на Na+,К+-АТФазу, что задерживает реполяризацию постсинаптической мембраны и восстановление ее реакции на поступающую импульсацию. Препараты, взаимодействующие с адренорецепторами, делят на подгруппы в зависимости от типа рецепторов, на которые они влияют: α1, α2, β1, β2. К α1-адреномиметикам относится норадреналин, α2-адреномиметиком является клофелин. Добутамин относится к β1-адреномиметикам, он преимущественно влияет на миокард, увеличивая силу, но не частоту сокращений. Средствами с преимущественным воздействием на β2-адренорецепторы являются орципреналин, салбутамол, фенотерол, их применяют для купирования бронхоспазма. β2-Адреномиметики способны ослабить сокращения беременной матки, их используют для сохранения беременности. Дофамин – медиатор нервного импульса и предшественник норадреналина и адреналина. В физиологических концентрациях он влияет на дофаминорецепторы (D-рецепторы), при увеличении концентрации в крови способен стимулировать β-адренорецепторы, а в еще больших дозах – α-адренорецепторы. Стимуляция D1-рецепторов вызывает расслабление гладкой мускулатуры сосудов, сфинктеров пищевода, желудка, кишечника; увеличение силы сердечных сокращений. Стимуляция D2-рецепторов сопровождается ограничением освобождения катехоламинов из окончаний симпатических волокон, ацетилхолина – из преганглиопарных волокон симпатических нервов, уменьшением секреции пролактина гипофизом, слюны подчелюстной железой. Леводопа – предшественник дофамина, норадреналина и ад-реналина, не инактивируется МАО (моноаминоксидаза) и КОМТ (катехол-о-метилтрансфераза), проникает во все ткани, включая ЦНС. Нормализуя содержание дофамина в подкорковых структурах, леводопа восстанавливает нормальные сокращения скелетных мышцу больных, страдающих дистонией и паркинсонизмом. К непрямым адреномиметическим средствам относятся эфедрин и фенамин, которые похожи по структуре на катехоламин, поэтому их активно транспортируют специальные механизмы из синаптической щели в пресинаптическое окончание, где они депонируются в везикулах. Эти препараты вытесняют из везикул содержащиеся в них катехоламины, увеличивая их освобождение как спонтанное, так и во время нервного импульса. Кроме того, эти вещества блокируют возврат катехоламинов из синаптической щели в пресинаптическое окончание, увеличивая этим их концентрацию в области адренорецепторов и приводя их к возбуждению, помимо этого они сенсибилизируют адренорецепторы к катехоламинам. Эфедрин преимущественно повышает активность норадреналина, а фенамин – дофамина, особенно в ЦНС. Адренонегативные средства – это вещества, нарушающие передачу возбуждения в адренергических синапсах. Различают аи p-адреноблокаторы (их называют также аи β-адренолитиками). К α-адреноблокаторам относятся празозин (α1-адреноблокатор), фентоламин (неселективный α-адреноблокатор), пирроксан и др. Средства из группы β-адреноблокаторов отличаются друг от друга не только способностью блокировать β1 и β2-адренорецепторы, но и наличием или отсутствием мембраностабилизирующей и симпатомиметической активности. Мембраностабилизирующей активностью обладают анаприлин, окспренолол, пиндолол, алпренолол, это действие, заключающееся в уменьшении проницаемости мембраны для ионов натрия и калия, не связано с блокированием p-адренорецепторов. Симпатомиметической активностью обладают пиндолол, окспренолол, алпренолол. Эти вещества, взаимодействуя с адренорецепторами, активируют их, вызывая небольшой миметический эффект, но одновременно предотвращают реакцию этих же рецепторов на медиатор, выделяющийся при прохождении нервного импульса. Средства, блокирующие дофаминовые рецепторы. Способностью блокировать D-рецепторы обладают аминазин (и другие производные фенотиазина), галоперидол, дроперидол (и другие производные бутирофенонов), метоклопрамид (церукал) и пр. Все они характеризуются широким спектром нейротропного действия. Симпатолитики – вещества, нарушающие освобождение медиатора из окончаний симпатических волокон. К этой группе относятся резерпин, октадин (изобарин) и орнид. Местноанестезирующими средствами называются вещества, которые при соприкосновении с чувствительными нервными окончаниями или с нервными волокнами вызывают обратимое угнетение их возбудимости и проводимости. Большинство местных анестетиков являются аминами, у которых аминогруппа (с помощью эфирной или амидной связи) соединена с ароматическим радикалом. По химическому строению их делят на две группы: сложные эфиры ароматических кислот (новокаин, дикаин, анестезин) и замещенные амиды кислот (лидокаин, тримекаин, пиромекаин). Катионы ряда анестетиков ведут себя как антагонисты ионов кальция. Они взаимодействуют с белковыми молекулами «медленных» кальциевых каналов, препятствуя проникновению Са++ внутрь клетки (не только нервного волокна, но и гладких мышц, миокарда, водителей ритма в сердце и др.). В результате происходит «стабилизация» мембраны, не раскрываются натриевые каналы в момент прихода возбуждения, Na+ не проникает внутрь клетки. Многие анестетики прямо влияют на натриевые каналы, способствуя их инактивации. Отсутствие потенциала действия и является причиной понижения возбудимости препаратами данной группы, в том числе антиаритмического и противосудорожного действия. Местные анестетики способны блокировать проведение возбуждения по всем нервным волокнам (чувствительным, двигательным, вегетативным), однако в различных концентрациях и с неодинаковой скоростью, что зависит от наличия или отсутствия миелиновой оболочки. Наиболее чувствительны к анестетикам тонкие безмякотные волокна, поэтому в первую очередь исчезает тактильная, болевая и температурная чувствительность, возникает блокада симпатических волокон, что приводит к расширению сосудов. Другие виды чувствительности угнетаются медленнее, в последнюю очередь блокируется проведение по двигательным нервам. Местные анестетики не проникают через шванновскую оболочку, поэтому проведение блокируется только в перехватах Ранвье. Восстановление проводимости по нервам происходит в обратном порядке: позже всего этот процесс происходит в безмякотных волокнах. Анестезия развивается только при непосредственном контакте препаратов данной группы с нервной тканью. При резорбтивном действии анестетики оказывают угнетающее влияние на ЦНС, которая чувствительна к значительно меньшим их концентрациям, чем периферический отдел нервной системы. Местные анестетики тормозят передачу нервных импульсов в центральных синапсах, в вегетативных ганглиях. Они тормозят освобождение ацетилхолина, норадреналина из пресинаптических окончаний (тоже результат «стабилизации» их мембран). Различают несколько видов местной анестезии. Терминальная (концевая, поверхностная) анестезия развивается при воздействии препаратов на чувствительные нервные окончания, находящиеся в слизистых оболочках или на раневых поверхностях. Этот метод используют для анестезии роговицы глаза, носовых ходов при интраназальной интубации пищевода вследствие зондирования желудка, уретры при цистоскопии, поверхности ожогов при их лечении и т. д. Для данного вида обезболивания применяют дикаин или докаин, которые легко проникают в поверхностные слои слизистых оболочек и достигают чувствительных нервных окончаний. Для терминальной анестезии применяют также анестезин, однако он плохо проникает через неповрежденные слизистые оболочки и кожу. Проводниковая (регионарная) анестезия наступает в результате блокады анестетиком нервного ствола. Нарушается проведение нервных импульсов от рецепторов к центральной нервной системе и утрачивается в результате этого чувствительность в той области, которая иннервируется нервным проводником. Для данного вида обезболивания применяют новокаин, тримекаин, лидокаин. Спинномозговая (корешковая) анестезия – один из вариантов проводниковой анестезии. Осуществляется путем введения растворов анестезирующих веществ в субарахноидальное пространство между остистыми отростками поясничных позвонков для воздействия на задние (чувствительные) корешки спинного мозга. С этой целью наиболее широко используют тримекаин, несколько реже – лидокаин и совкаин. Инфильтрационная анестезия достигается послойным пропитыванием тканей раствором анестетика, начиная с кожи. При этом препарат действует и на нервные волокна, и на их окончания. Для данного вида обезболивания используют новокаин, тримекаин, лидокаин. Чтобы замедлить всасывание анестетиков из ме т введения и удлинить эффект, к их растворам (особенно к новокаину) добавляют раствор адреналина гидрохлорида. Местные анестетики, особенно новокаин, лидокаин и тримекаин, используют и для резорбтивных целей. Новокаин применяют для блокирования вегетативных ганглиев, лидокаин и тримекаин – в качестве антиаритмических средств, для дополнения и потенцирования наркоза, так как они вызывают небольшой анальгетический эффект.Глава 3. Физиология центральной нервной системы
Особое место в живом организме занимает нервная система, функционально объединяющая клетки, ткани, отдельные органы и системы органов в одно целое. Она осуществляет регуляцию всех процессов жизнедеятельности, обеспечивает связь организма с окружающей средой и приспособление к ее постоянным изменениям. С функциями ЦНС связаны процессы, лежащие в основе поведения и психической деятельности человека. ЦНС – это сложно организованная высокоспецифичная система быстрой передачи информации, ее обработки и управления, которая содержит около 50 миллиардов нервных клеток. Различные нейроны представляют собой единую структуру, которая приобретает новые функции. Активность нервных клеток выражается в генерации и передаче нервных импульсов, которые служат общим механизмом взаимодействия различных отделов ЦНС. Нервная система воспринимает огромное число импульсов от различных сенсорных систем, интегрирует всю эту информацию, анализирует ее и дает команду исполнительным органам, обеспечивая адекватную ответную реакцию. В мозге находятся чувствительные центры, анализирующие изменения, которые происходят как во внешней, так и внутренней среде.Нейрон
Нервная клетка (нейрон) – это функциональная единица нервной системы, строение и функции которой приспособлены к передаче и обработке информации. В каждом нейроне различают четыре различные области: тело, дендриты, аксон и аксонные окончания (терминали). Все эти области выполняют строго определенные функции. Центр процессов синтеза в нервной клетке – ее тело (сома), которое содержит ядро, рибосомы, эндоплазматический ретикулум и другие органеллы, здесь синтезируются медиаторы и клеточные белки. При разрушении сомы дегенерирует вся клетка, включая аксон и дендриты. Главная функция аксона состоит в проведении нервных импульсов к другим клеткам – нервным, мышечным или секреторным. Большинство аксонов представляет собой длинные нитевидные отростки (длиной от нескольких миллиметров до нескольких метров). Аксоны чувствительных (сенсорных) нейронов передают информацию от расположенных на периферии рецепторов к ЦНС. Аксоны двигатель-ных (моторных) нейронов проводят нервные импульсы от ЦНС к скелетным мышцам. Другие аксоны соединяют ЦНС с рецепторами, мышечными и секреторными клетками внутренних органов. Специфической функцией аксона является проведение нервных импульсов, которые возникают в результате небольших изменений проницаемости мембраны аксона и проходят по всей длине аксона. Ближе к окончанию аксон ветвится и образует кисточку из конечных ветвей (терминалей). На конце каждая терминаль образует специализированный контакт (синапс) с нервной, мышечной или железистой клеткой. Функция синапса заключается водносторонней передаче информации от клетки к клетке. Когда к окончанию аксона приходит нервный импульс, в нем секретируется небольшое количество нейромедиатора, который высвобождается из окончания и связывается с рецепторами мембраны постсинаптического нейрона, изменяя ее проницаемость. Возникающий в результате этого синаптический потенциал может быть возбуждающим или тормозным. В первом случае он может вызвать генерацию нервного импульса в постсинаптическом нейроне; тормозный потенциал, напротив, этому препятствует. Дендриты образуются в результате древовидного разветвления отростков нервной клетки, отходящих от ее тела, их функция заключается в восприятии синаптических влияний. На дендритах и соме нервной клетки оканчиваются терминали аксонов сотен или тысяч нейронов, которые покрывают всю поверхность нейрона. В активном состоянии каждая терминаль высвобождает медиатор, вызывающий местное изменение проницаемости мембраны дендрита, т. е. изменение ее электрического потенциала. Эти возбуждающие и тормозные потенциалы передаются к начальному сегменту аксона (аксонному холмику), который является зоной генерации ПД. Этот участок обладает более низким пороговым уровнем возбуждения, чем тело и дендриты, здесь наиболее высока плотность натриевых каналов. Если мембрана аксонного холмика деполяризуется до критического уровня, то здесь возникают импульсы, частота которых возрастает пропорционально степени деполяризации.Все нейроны можно разделить на 3 класса: 1. чувствительные (сенсорные) 2. вставочные 3. эффекторные.
Чувствительные нейроны представляют собой афферентные пути, по которым импульсы передаются от рецепторов в ЦНС, а эфферентные нейроны проводят импульсы от ЦНС к эффекторам (мышцам и железам). К эффекторным нейронам относятся двигательные (моторные) нейроны, иннервирующие скелетные мышцы, и нейроны вегетативной нервной системы, осуществляющие центральную регуляцию гладких мышц и желез. Отростки вставочных нейронов не выходят за пределы ЦНС. Почти все нейроны ЦНС, за исключением сенсорных и зффекторных, являются вставочными. В ЦНС вставочные нейроны образуют цепи, осуществляющие анализ входной сенсорной информации, хранение опыта в виде памяти и формирование соответствующих команд.
Глиальные клетки
Хотя именно нервные клетки являются функциональными единицами ЦНС, но на их долю приходится лишь 10% общего числа клеток в нервной системе. Большинство же составляют глиальные клетки, заполняющие все пространство между нейронами. Существуют четыре основные разновидности глиальных клеток: астроциты, олигодендроциты и микроглия, находящиеся в головном и спинном мозге, и шванновские клетки, расположенные в периферических нервах. Многие клетки глии – олигодендроциты в ЦНС и шванновские клетки периферических нервов – тесно связаны с нервными путями, образованными пучками аксонов. Многие крупные аксоны заключены в футляр из мембранных выростов глиальных клеток, образующих миелиновую оболочку, которая изолирует мембрану аксона, что способствует повышению скорости проведения нервного импульса. Другие глиальные клетки – астроциты расположены между кровеносными сосудами и телами нейронов, их отростки контактируют со стенкой капилляров и служат компонентом гематоэнцефалического барьера. Клетки глии регулируют транспорт питательных веществ от капилляров к нейронам. Между клетками глии и связанными с ними нейронами осуществляется обмен белками, нуклеиновыми кислотами и другими веществами. Активность нейронов способна влиять на мембранный потенциал глиальных клеток путем увеличения концентрации К+ во внеклеточном пространстве. Клетки микроглии являются фагоцитами мозга и входят в состав ретикулоэндотелиальной системы. Они редки в неповрежденном мозге, в области же повреждений ткани мозга их всегда много.Организация нервной системы
Нервная система подразделяется на две части: центральную и периферическую. ЦНС состоит из нейронов, их отростков и глии, расположенных в головном и спинном мозге. Периферическая нервная система образована нейронами, их отростками и глией, находящимися за пределами ЦНС. К ней относятся все нервные отростки, идущие в составе периферических нервов (черепномозговых, спинномозговых и вегетативных), а также расположенные на периферии скопления нервных клеток – чувствительные и вегетативные ганглии. ЦНС организована таким образом, что вставочные нейроны, выполняющие одинаковые функции (с одинаковыми входами и выходами), сгруппированы в виде ядер. В мозге имеются сотни различных ядер, каждое из которых содержит тысячи нейронов, участвующих в интеграции связанных между собой функций. Наиболее сложна нервная организация коры. Все ее отделы состоят из нескольких слоев нейронов и их отростков. В большинстве областей кора образована чередующимися ядерными (содержащими тела клеток) и плексиформными (содержащими дендриты и синаптические окончания) слоями. Разные слои коры состоят из разных нейронов. Центростремительные пути к коре обычно оканчиваются в одном или двух плексиформных слоях; аксоны же, передающие сигналы из коры к другим отделам ЦНС, как правило, отходят от основания одного из ядерных слоев.Общие закономерности деятельности центральной нервной системы
Рефлекторный принцип регуляции
Основной формой деятельности ЦНС является рефлекс. Рефлекс – это ответная реакция организма на раздражение рецепторов, осуществляемая при участии ЦНС. Впервые понятие о рефлексе как ответной реакции (отражении) на раздражения органов чувств было сформулировано французским ученым Рене Декартом (XVII в.). Это представление было развито чешским физиологом И. Прохаской (XVIII в.) и другими исследователями. Дальнейшее углубление учения о рефлекторной деятельности ЦНС связано с именами отечественных физиологов И. М. Сеченова и И. П. Павлова. В книге «Рефлексы головного мозга» (1863) И. М. Сеченов показал, что рефлексы являются не только реакциями отдельных органов, а представляют собой целостные акты, определяющие поведение. И. М. Сеченов выдвинул идею о рефлекторной природе всех процессов (сознательных и бессознательных), происходящих в головном мозге, включая психические. Но в то время не существовало методов объективной оценки деятельности мозга, которые могли бы подтвердить это предположение. Такой метод был разработан И. П. Павловым – метод условных рефлексов, с помощью которого он расширил рефлекторную теорию, показав, что наиболее сложные и совершенные формы поведения осуществляются на основе условнорефлекторной деятельности. Рефлексы можно классифицировать по различным показателям. По биологическому значению рефлексы подразделяются на ориентировочные, оборонительные, пищевые и половые. По расположению рецепторов они делятся на зкстерорецептивные – вызываемые раздражением рецепторов, расположенных на внешней поверхности тела; интерорецептивные – вызываемые раздражением рецепторов внутренних органов и сосудов; проприорецептивные – возникающие при раздражении рецепторов, находящихся в мышцах, сухожилиях и связках. В зависимости от органов, которые участвуют в формировании ответной реакции, рефлексы могут быть двигательными (локомоторными), секреторными, сосудистыми и др. В зависимости от того, какие отделы мозга необходимы для осуществления данного рефлекса, различают: спинальные рефлексы, для которых достаточно нейронов спинного мозга; бульбарные (возникающие при участии продолговатого мозга); мезэнцефальные (участвуют нейроны среднего мозга); диэнцефальные (нейроны – промежуточного мозга); кортикальные (для которых необходимы нейроны коры головного мозга). Следует отметить, что в большинстве рефлекторных актов участвуют как высший отдел ЦНС – кора головного мозга, так и низшие отделы одновременно. Рефлексы можно также разделить на безусловные (врожденные) и условные (приобретенные в процессе индивидуальной жизни). Структурной основой рефлекса, его материальным субстратом является рефлекторная дуга – нейронная цепь, по которой проходит нервный импульс от рецептора к исполнительному органу (мышце, железе).В состав рефлекторной дуги входят: 1. воспринимающий раздражение рецептор; 2. чувствительное (афферентное) волокно (аксон чувствительного нейрона), по которому возбуждение передается в ЦНС; 3. нервный центр, в который входят один или несколько вставочных нейронов; 4. эфферентное нервное волокно (аксон эфферентного нейрона), по которому возбуждение направляется к органу.
В рефлекторной реакции всегда участвуют афферентные нейроны, передающие импульсы от рецепторов (например, проприорецепторов) исполнительного органа в ЦНС. С помощью обратной афферентации происходит коррекция ответной реакции нервными центрами, регулирующими данную функцию. Поэтому понятие «рефлекторная дуга» заменяется в настоящее время представлением о рефлекторном кольце, поскольку в функциональном отношении дуга замкнута и на периферии, и в центре беспрерывно циркулирующими во время работы органа нервными сигналами. Простейшая рефлекторная дуга (моносинаптическая) состоит из двух нейронов: чувствительного и двигательного. Примером такого рефлекса является коленный рефлекс. Большинство рефлексов включают один или несколько последовательно связанных вставочных нейронов и называются полисинаптическими. Наиболее элементарной полисинаптической дугой является трехнейронная рефлекторная дуга, состоящая из чувствительного, вставочного и эфферентного нейронов. В осуществлении пищевых, дыхательных, сосудодвигательных рефлексов участвуют нейроны, расположенные на разных уровнях – в спинном, продолговатом, среднем и промежуточном мозге, в коре головного мозга. Рефлексы возникают под влиянием специфических для них раздражителей, действующих на их рецептивное поле. Рецептивным полем рефлекса называется участок тела, содержащий рецепторы, раздражение которых всегда вызывает данную рефлекторную реакцию. Так, рефлекс сужения зрачка возникает при освещении сетчатки глаза, разгибание голени наступает при нанесении легкого удара по сухожилию ниже колена и т. д.
Нервные центры
Нервным центром называется функциональное объединение нейронов, обеспечивающее осуществление какого-либо рефлекса или регуляцию какой-либо определенной функции. Нейроны, входящие в нервный центр, обычно находятся в одном отделе ЦНС, но могут располагаться и в нескольких. Центр дыхания располагается в средней трети продолговатого мозга, центр мочеиспускания – в крестцовом, центр коленного рефлекса – в поясничном отделе спинного мозга. В осуществлении сложных рефлексов целостного организма принимают участие, как правило, не один, а многие центры, расположенные в разных отделах мозга, включая его высшие отделы. Например, в акте дыхания участвует не только центр дыхания в продолговатом мозге, но и нервные клетки варолиева моста, коры головного мозга и мотонейроны спинного мозга.Особенности распространения возбуждения в ЦНС в основном определяются свойствами нервных центров: 1. Одностороннее проведение возбуждения. В ЦНС возбуждение может распространяться только в одном направлении: от рецепторного нейрона через вставочный к эфферентному нейрону, что обусловлено наличием синапсов. 2. Более медленное проведение возбуждения по сравнению с нервными волокнами. Промежуток времени от момента нанесения раздражения на рецептор до ответной реакции исполнительного органа называется временем рефлекса. Большая его часть тратится на проведение возбуждения в нервных центрах, где возбуждение проходит через синапсы. На выделение и диффузию медиатора в синапсе требуется промежуток времени в 1,5–2 мс (синоптическая задержка). Чем больше нейронов в рефлекторной дуге, тем продолжительнее время рефлекса. 3. Суммация возбуждений (или торможения). Нервные центры могут суммировать афферентные импульсы, что проявляется в усилении рефлекса при увеличении частоты раздражений или числа раздражаемых рецепторов. Различают два вида суммации: временная суммация – если импульсы приходят к нейрону по одному и тому же пути через один синапс с коротким интервалом, то происходит суммирование ВПСП на постсииаптической мембране и она деполяризуется до уровня, достаточного для генерации ПД; пространственная суммация связана с суммированием ВПСП, возникающих одновременно в разных синапсах одного нейрона. Оба вида суммации происходят в области аксонного холмика, где и генерируется ПД. 4. Конвергенция. В нервном центре несколько клеток могут передавать импульсы к одному нейрону, т. е. возбуждения конвергируют на нем. Конвергенция может быть результатом прихода возбуждающих или тормозных входных сигналов от различных источников. Так, моторные нейроны спинного мозга могут получать импульсы: от периферических нервных волокон, входящих в спинной мозг; волокон, соединяющих сегменты спинного мозга; кортикоспинальных волокон от коры мозга; тормозных путей от ретикулярной формации. В результате конвергенции происходит суммация импульсов от этих источников и возникает ответ, являющийся суммарным эффектом разнородной информации. 5. Дивергенция и иррадиация. Возбуждение даже единственного нервного волокна, по которому импульсы поступают в нервный центр, может послужить причиной возбуждения множества выходящих из центра нервных волокон. Морфологическим субстратом широкого распространения импульсов (иррадиации) возбуждения является ветвление аксонов и наличие большого числа вставочных нейронов в пределах центра. 6. Облегчение и окклюзия. На нейронах нервных центров оканчиваются не только волокна их собственных афферентных входов. Каждый из них получает веточки от афферентов соседнего центра, что может обусловливать развитие окклюзии (закупорки) или, наоборот, облегчения. Феномен окклюзии состоит в том, что количество возбужденных нейронов при одновременном раздражении афферентных входов обоих нервных центров оказывается меньше, чем арифметическая сумма возбужденных нейронов при раздельном раздражении каждого афферентного входа в отдельности. Явление окклюзии приводит к снижению силы суммарной ответной реакции. Феномен центрального облегчения характеризуется противоположным эффектом. На облегчении основано проторение пути – распространение возбуждения не по той цепи нейронов, по которой информация не поступала ранее, а через нейроны, уже облегченные первым раздражением. 7. Трансформация ритма возбуждений. Если сопоставить частоту импульсов в задних (чувствительных) и передних (двигательных) корешках спинного мозга при раздражении рецепторов, то обычно их ритм не совпадает. Центры способны как снижать, так и повышать ритмы возбуждений, поступающих от рецепторов. 8. Рефлекторное последействие. Продолжительность рефлекса всегда больше, чем время раздражения, так как возбуждение в нервных центрах сохраняется в течение некоторого времени после прекращения действия раздражителя. Это объясняется тем, что вставочные нейроны в центре образуют замкнутые цепи («нейронные ловушки»), по которым ПД могут длительно циркулировать. 9. Высокая чувствительность к недостатку кислорода. Уменьшение доставки к клеткам мозга кислорода быстро ведет к тяжелым расстройствам деятельности ЦНС и гибели нейронов. Кратковременное нарушение кровоснабжения мозга вследствие временного спазма его сосудов или падения давления крови приводит к потере сознания – обмороку. Своевременно принятые меры по восстановлению кровоснабжения мозга (нашатырный спирт, кофеин, горизонтальное положение тела и др.) выводят больного из обморока. 10. Высокая чувствительность к химическим веществам объясняется большим числом синапсов. На одном нейроне могут рас-полагаться синапсы, обладающие чувствительностью к различным химическим веществам. Подбирая фармакологические препараты, которые избирательно блокируют одни синапсы, оставляя другие в рабочем состоянии, можно корректировать реакции организма. 11. Низкая функциональная подвижность (лабильность) и высокая утомляемость. Нервные центры, как и синапсы, обладают низкой функциональной подвижностью и быстрой утомляемостью в отличие от нервных волокон, которые считаются практически неутомляемыми и имеют высокую лабильность. 12. Посттетаническая потенциация – явление усиления рефлекторного ответа после длительного ритмического раздражения нервного центра. Это связано с сохранением ВПСП на нейронах центра в течение некоторого времени, что облегчает проведение последующих возбуждений через синапсы. 13. Тонус нервных центров. Регистрация биоэлектрической активности ЦНС даже при отсутствии раздражений показывает, что многие нервные центры (составляющие их нейроны) постоянно генерируют импульсы. Эта импульсация поступает к рабочим органам и свидетельствует о существовании некоторого постоянного тонического возбуждения нервных центров. 14. Пластичность. Нервные центры обладают способностью изменять собственное функциональное назначение и расширять свои функциональные возможности, т. е. существенно модифицировать картину осуществляемых рефлекторных реакций. Пластичность нервных центров тесно связана с изменением эффективности или направленности связей между нейронами.
Торможение в центральной нервной системе и его виды
Нормальная деятельность отдельных нервных центров и ЦНС в целом может осуществляться лишь при обязательном участии тормозных процессов. Торможение в ЦНС – это активный процесс, проявляющийся в подавлении или ослаблении возбуждения. Явление торможения в центральной нервной системе было открыто И. М. Сеченовым в 1862 г. в эксперименте на лягушке, у которой перерезали мозг на уровне зрительных бугров и удалили полушария головного мозга. После этого измеряли время рефлекса отдергивания задних лапок при погружении их в раствор серной кислоты. Этот рефлекс осуществляется спинномозговыми нейронами и его время служит показателем возбудимости нервных центров. Если на область зрительных бугров наложить кристалл хлорида натрия, то время рефлекса увеличивается, т. е. в области зрительных бугров имеются центры, оказывающие тормозящее влияние на спинномозговые рефлексы. Торможение может наступить не только в результате непосредственного воздействия на нервные центры, но и на рецепторы. Гольц показал, что рефлекс отдергивания одной лапки может быть заторможен более сильным раздражителем – сдавливанием другой лапки лягушки пинцетом. В данном случае торможение развивается в результате встречи двух возбуждений в ЦНС, т. е. если в ЦНС поступают импульсы из разных рецептивных полей, то более сильные раздражения угнетают слабые и рефлекс на последние тормозится. Таким образом, процесс торможения тесно связан с процессом возбуждения.Классификация видов торможения
Торможение в ЦНС можно классифицировать по различным признакам (рис.9): электрическому состоянию мембраны (гипер-поляризационное и деполяризационное); отношению к синапсу (постсинаптическое и пресинаптическое); нейрональной организации (поступательное, возвратное, латеральное). Торможение мембраны обычно является гиперполяризационным, тормозной медиатор увеличивает проницаемость мембраны для ионов калия или хлора (возникает ТПСП) и мембрану труднее довести до критического уровня деполяризации (при котором нейрон генерирует ПД). В нейронных сетях коры тормозная функция принадлежит в основном ГАМК-эргическим вставочным нейронам. Эти тормозные нейроны имеют относительно короткие проекции, поэтому их влияние ограничено локальными областями коры. Ингибирующее действие ГАМК осуществляется через ГАМКрецепторы А-типа, которые изменяют проницаемость мембраны для ионов хлора, что приводит к гиперполяризации мембраны. Есть данные, что ТПСП могут возникать и за счет взаимодействия ГАМК с рецепторами В-типа, которые связаны с калиевыми каналами. Деполяризация мембраны тоже может привести к торможению, если она становится чрезмерно длительной (застойной), такая деполяризация сопровождается инактивацией натриевых каналов, т.е мембрана теряет свою возбудимость и не в состоянии ответить на приход новых возбуждений генерацией ПД.Постсинаптическое торможение
Это основной вид торможения, заключается в том, что в нервных окончаниях тормозящих нейронов под влиянием приходящего по аксону импульса выделяется медиатор, который гиперполяризует постсинаптическую мембрану другого возбуждающего нейрона. В мембране последнего деполяризация не может достигнуть критического уровня, и поэтому возбуждение по нейрону не распространяется.
Пресинаптическое торможение
Локализуется в пресинаптических окончаниях, т. е. в разветвлениях (терминалях) возбуждающего нейрона. На этих терминалях располагаются окончания аксона тормозящего нейрона. При его возбуждении тормозной медиатор частично или полностью блокирует проведение возбуждения возбуждающего нейрона, и его влияние не передается на другой нейрон. Поступательное торможение обусловлено тем, что на пути следования возбуждения встречается тормозной нейрон.Возвратное торможение
Осуществляется вставочными тормозными клетками (клетками Реншоу). Аксоны мотонейронов часто дают коллатерали (ответвления), оканчивающиеся на клетках Реншоу. Аксоны клеток Реншоу оканчиваются на теле или дендритах этого мотонейрона, образуя тормозные синапсы. Возбуждение, возникающее в мотонейроне, распространяется по прямому пути к скелетной мускулатуре, а также по коллатералям к тормозящему нейрону, который посылает импульсы к мотонейронам и тормозит их. Чем сильнее возбуждение мотонейрона, тем сильнее возбуждаются клетки Реншоу и тем более интенсивно они оказывают свое тормозящее действие, что предохраняет нервные клетки от перевозбуждения.Латеральное торможение
Является разновидностью возвратного торможения. Вставочные клетки могут формировать тормозные синапсы на соседних нейронах, блокируя боковые пути распространения возбуждения. В таких случаях возбуждение направляется по строго определенному пути. Этот вид торможения обеспечивает направленную иррадиацию возбуждения в ЦНС.Пессимальное торможение
Для ЦНС свойственно пессимальное торможение, близкое по своему происхождению пессимуму Введенского в нервно-мышечных соединениях. Пессимальное торможение развивается в синапсах при разражениях высокой частоты и зависит от низкой лабильности синапсов. Данное явление связано с появлением при частых импульсах стойкой деполяризации постсинаптической мембраны, что нарушает распространение возбуждения и рефлекс тормозится. К пессимальному торможению особенно склонны вставочные нейроны спинного мозга и клетки ретикулярной формации. Пессимальное торможение предохраняет нервную клетку от перевозбуждения. В нервной клетке может развиваться торможение после прекращения ее возбуждения – так называемое торможение вслед за возбуждением, возникающее в том случае, если после окончания возбуждения в клетке развивается сильная следовая гиперполяризация мембраны. Если в этот момент к клетке приходит новый импульс, то возникший посгсипаптический потенциал оказывается недостаточным для критической деполяризации мембраны.Реципрокное (сопряженное) торможение.
Это явление, открытое Ч. Шеррингтоном, обеспечивает согласованную работу мышц-антагонистов, например, сгибателей и разгибателей конечностей, т. е. движение конечностей. При сгибании ног в коленном суставе развивается возбуждение в спинномозговом центре мышц-сгибателей и одновременно развивается торможение в нервном центре мышц-разгибателей. Наоборот, при разгибании, в нервном центре мышц-разгибателей наступает возбуждение, а в центре мышц-сгибателей – торможение. Такие взаимодействия названы реципрокным торможением. Реципрокное взаимодействие возникает и при более сложных двигательных актах, например при ходьбе. В этом случае происходит сгибание то одной, то другой ноги. Если в данный момент правое колено согнуто, то в центре сгибателей правой ноги развивается возбуждение, а в центре ее разгибателей – торможение. На левой стороне имеются противоположные взаимоотношения – центры разгибателей левой ноги возбуждены, а центры сгибателей заторможены. Во время следующего шага соотношения возбуждения и торможения в нейронах меняются в противоположном направлении. Чем сложнее двигательный акт, тем большее количество нейронов, регулирующих отдельные мышцы или их группы, находится в сопряженных соотношениях. Реципрокное торможение осуществляется при участии тормозящих вставочных нейронов спинного мозга. Реципрокные соотношения между отдельными центрами не постоянны и в типичной форме они выявляются лишь у спинальных животных. Реципрокное торможение может изменяться под влиянием нейронов, расположенных выше спинальных центров (особенно центров коры головного мозга). Например, обе ноги можно согнуть одновременно вопреки описанному выше сопряженному торможению центров сгибателей и разгибателей. Изменчивость взаимодействия между двигательными центрами обеспечивает сложнейшие движения человека во время разнообразной трудовой деятельности, сложных спортивных движений, танцев, игры на музыкальных инструментах и др.Принципы координационной деятельности центральной нервной системы
Для осуществления сложных реакций необходима интеграция работы отдельных нервных центров. Большинство рефлексов являются сложными, последовательно и одновременно совершающимися реакциями. Рефлексы при нормальном состоянии организма строго упорядочены, так как имеются общие механизмы их координации. Возбуждения, возникающие в ЦНС, иррадиируют по ее центрам. Координация обеспечивается избирательным возбуждением одних центров и торможением других. Координация – это объединение рефлекторной деятельности ЦНС в единое целое, что обеспечивает реализацию всех функций организма.Выделяют следующие основные принципы координации: 1. Принцип иррадиации возбуждений. Нейроны разных центров связаны между собой вставочными нейронами, поэтому импульсы, поступающие при сильном и длительном раздражении рецепторов, могут вызвать возбуждение не только нейронов центра данного рефлекса, но и других нейронов. Например, если раздражать у спинальной лягушки одну из задних лапок, слабо сдавливая ее пинцетом, то она сокращается (оборонительный рефлекс), если раздражение усилить, то происходит сокращение обеих задних лапок и даже передних. Иррадиация возбуждения обеспечивает при сильных и биологически значимых раздражениях включение в ответную реакцию большего количества мотонейронов. 2. Принцип общего конечного пути. Импульсы, приходящие в ЦНС по разным афферентным волокнам, могут сходиться (конвергировать) к одним и тем же вставочным, или эфферентным, нейронам. Шеррингтон назвал это явление «принципом общего конечного пути». Один и тот же мотонейрон может возбуждаться импульсами, приходящими от различных рецепторов (зрительных, слуховых, тактильных), т. е. участвовать во многих рефлекторных реакциях (включаться в различные рефлекторные дуги). Так, например, мотонейроны, иннервирующие дыхательную мускулатуру, помимо обеспечения вдоха участвуют в таких рефлекторных реакциях, как чихание, кашель и др. На мотонейронах, как правило, конвергируют импульсы от коры больших полушарий и от многих подкорковых центров (через вставочные нейро-ны или за счет прямых нервных связей). На мотонейронах передних рогов спинного мозга, иннервирующих мускулатуру конечности, оканчиваются волокна пирамидного тракта, экстрапирамидных путей, от мозжечка, ретикулярной формации и других структур. Мотонейрон, обеспечивающий различные рефлекторные реакции, рассматривается как их общий конечный путь. В какой конкретный рефлекторный акт будут вовлечены мотонейроны, зависит от характера раздражений и от функционального состояния организма. 3. Принцип доминанты. Был открыт А. А. Ухтомским, который обнаружил, что раздражение афферентного нерва (или коркового центра), обычно ведущего к сокращению мышц конечностей при переполнении у животного кишечника, вызывает акт дефекации. В данной ситуации рефлекторное возбуждение центра дефекации" подавляет, тормозит двигательные центры, а центр дефекации начинает реагировать на посторонние для него сигналы. А. А. Ухтомский считал, что в каждый данный момент жизни возникает определяющий (доминантный) очаг возбуждения, подчиняющий себе деятельность всей нервной системы и определяющий характер приспособительной реакции. К доминантному очагу конвергируют возбуждения из различных областей ЦНС, а способность других центров реагировать на сигналы, приходящие к ним, затормаживается. Благодаря этому создаются условия для формирования определенной реакции организма на раздражитель, имеющий наибольшее биологическое значение, т. е. удовлетворяющий жизненно важную потребность. В естественных условиях существования доминирующее возбуждение может охватывать целые системы рефлексов, в результате возникает пищевая, оборонительная, половая и другие формы деятельности.
Доминантный центр возбуждения обладает рядом свойств: 1. для его нейронов характерна высокая возбудимость, что способствует конвергенции к ним возбуждений из других центров; 2. его нейроны способны суммировать приходящие возбуждения; 3. возбуждение характеризуется стойкостью и инертностью, т. е. способностью сохраняться даже тогда, когда стимул, вызвавший образование доминанты, прекратил действие.
Несмотря на относительную стойкость и инертность возбуждения в доминантном очаге, деятельность ЦНС в нормальных условиях существования весьма динамична и изменчива. ЦНС обладает способностью к перестройке доминантных отношений в соответствии с изменяющимися потребностями организма. Учение о доминанте нашло широкое применение в психологии, педагогике, физиологии умственного и физического труда, спорте.
Принципы: 1. Принцип обратной связи. Процессы, происходящие в ЦНС, невозможно координировать, если отсутствует обратная связь, т. е. данные о результатах управления функциями. Обратная связь позволяет соотнести выраженность изменений параметров системы с ее работой. Связь выхода системы с ее входом с положительным коэффициентом усиления называется положительной обратной связью, а с отрицательным коэффициентом – отрицательной обратной связью. Положительная обратная связь в основном характерна для патологических ситуаций. Отрицательная обратная связь обеспечивает устойчивость системы (ее способность возвращаться к исходному состоянию после прекращения влияния возмущающих факторов). Различают быстрые (нервные) и медленные (гуморальные) обратные связи. Механизмы обратной связи обеспечивают поддержание всех констант гомеостаза. Например, сохранение нормального уровня кровяного давления осуществляется за счет изменения импульсной активности барорецепторов сосудистых рефлексогенных зон, которые изменяют тонус вагуса и вазомоторных симпатических нервов. 2. Принцип реципрокности. Он отражает характер отношений между центрами, ответственными за осуществление противоположных функций (вдоха и выдоха, сгибание и разгибание конечностей), и заключается в том, что нейроны одного центра, возбуждаясь, тормозят нейроны другого и наоборот. 3. Принцип субординации (соподчинения). Основная тенденция в эволюции нервной системы проявляется в сосредоточении функций регуляции и координации в высших отделах ЦНС – цефализация функций нервной системы. В ЦНС имеются иерархические взаимоотношения – высшим центром регуляции является кора больших полушарий, базальные ганглии, средний, продолговатый и спинной мозг подчиняются ее командам. 4. Принцип компенсации функций. ЦНС обладает огромной компенсаторной способностью, т. е. может восстанавливать некоторые функции даже после разрушения значительной части нейронов, образующих нервный центр (см. пластичность нервных центров). При повреждении отдельных центров их функции могут перейти к другим структурам мозга, что осуществляется при обязательном участии коры больших полушарий. У животных, которым после восстановления утраченных функций удаляли кору, вновь происходила их утрата.
При локальной недостаточности тормозных механизмов или при чрезмерном усилении процессов возбуждения в том или ином нервном центре определенная совокупность нейронов начинает автономно генерировать патологически усиленное возбуждение – формируется генератор патологически усиленного возбуждения. При высокой мощности генератора возникает целая система функционирующих в едином режиме нейрональных образований, что отражает качественно новый этап в развитии заболевания; жесткие связи между отдельными составными элементами такой патологической системы лежат в основе ее устойчивости к различным лечебным воздействиям. Изучение природы этих связей позволило Г. Н. Крыжановскому обнаружить новую форму внутрицентральных отношений и интегративной деятельности ЦНС – принцип детерминанты. Его суть состоит в том, что структура ЦНС, формирующая функциональную посылку, подчиняет себе те отделы ЦНС, к которым она адресована и образует вместе с ними патологическую систему, определяя характер ее деятельности. Для такой системы характерно отсутствие постоянства и неадекватности функциональных посылок, т. е. такая система является биологически отрицательной. Если в силу тех или иных причин патологическая система исчезает, то образование ЦНС, игравшее главную роль, теряет свое детерминантное значение.
Частная физиология центральной нервной системы
Спинной мозг
Спинной мозг располагается в спинномозговом канале. Основная особенность строения спинного мозга – это его сегментарность. Спинной мозг человека имеет 31–33 сегмента и по функциональному принципу делится на 8 шейных (С1-С8), 12 грудных (Т1–Т12), 5 поясничных (L1-L5), 5 крестцовых (S1–S5) и 1–3 копчиковых (С1-С3). Один сегмент иннервирует 3 метамера тела – свой и два других прилежащих к нему соседних метамера. Поэтому поражение или перерезка корешков одного сегмента спинного мозга не приводит к полной потере чувствительности и движения в соответствующем метамере тела, а лишь к ослаблению этих функций. Каждый сегмент имеет афферентные входы в виде задних корешков, клеточную массу нервных клеток (серое вещество) и эфферентные выходы в составе передних корешков. В задних корешках проходят чувствительные центростремительные нервные волокна от рецепторов кожи (болевые, температурные, тактильные и давления) – это кожная рецептирующая система; от рецепторов мышц, сухожилий, суставов – это проприоцептивная система, наконец, от рецепторов внутренних органов – это висцероцептивная система. Передние корешки являются двигательными цетробежными (закон Белла -Мажанди). Если в опыте на лягушке в области пояснично-крестцовых сегментов справа перерезать все задние корешки, а слева – все передние, то правая конечность теряет чувствительность, но способна к движению, а левая, наоборот, сохраняет чувствительность, но не сможет совершать движения. Серое вещество спинного мозга, состоящее из нейронов, образует два передних и два задних рога и на поперечном разрезе имеет вид буквы Н. Задние рога выполняют сенсорные функции, передние – двигательные. В грудных и верхних поясничных сегментах помимо задних и передних рогов есть еще и боковые, в которых располагаются нейроны симпатического, а в крестцовых – парасимпатического отделов вегетативной нервной системы. При поражении боковых рогов спинного мозга возникает целый ряд вегетативных расстройств: нарушаются кожные сосудистые рефлексы, усиливается потоотделение, наблюдаются трофические изменения кожи и ногтей.Нейроны спинного мозга
Существует функциональное деление нейронов на 4 группы. В первую группу входят мотонейроны, или двигательные нейроны, расположенные в передних рогах, а их аксоны образуют передние корешки. Вторую группу составляют интернейроны – промежуточные нейроны, расположенные в задних рогах и получающие информацию от чувствительных ганглиев. Они реагируют на болевые, температурные, тактильные и проприоцептивные раздражители. Интернейроны отвечают за висцеромоторные рефлексы. Кроме того, они обеспечивают восходящие и нисходящие тормозные и возбуждающие влияния на клетки выше- и нижележащих структур спинного мозга. Интернейроны участвуют в реципрокном торможении. Третья группа нейронов – это симпатические и парасимпатические нейроны, расположенные в боковых рогах. Аксоны этих клеток выходят из спинного мозга в составе передних корешков. Разряды симпатических нейронов синхронизируются с колебаниями артериального давления. К четвертой группе относят ассоциативные нейроны, обеспечивающие внутрии межсегментарные связи. В средней части спинного мозга находится промежуточное ядро, содержащее нейроны, аксоны которых образуют сеть – студенистое вещество (желатинозную субстанцию Роланда), или ретикулярную формацию спинного мозга. Мотонейроны спинного мозга делят на альфа и гамма-нейроны. Альфа-мотонейроны иннервируют экстрафузальные мышечные волокна, обеспечивая мышечное сокращение. На дендритах этих клеток располагается около 20 тысяч синапсов. Альфа-мотонейроны обладают низкой частотой импульсации (10 -20 в сек). Гамма-мотонейроны иннервируют интрафузальные мышечные волокна мышечного веретена. Они обладают высокой частотой импульсации (до 200 в сек). Главная функция гамма-мотонейрс нов состоит в предотвращении во время сокращения экстрафу зальных волокон расслабления мышечных веретен. Возбуждс ние гамма-мотонейронов способствует развитию начавшегося движения и используется для выполнения особенно тонких " мелких движений. Это сервомеханизм для оптимизации движений.Собственные функции спинного мозга
Эти функции осуществляются за счет сегментарных рефлек торных дуг (монои полисинаптических). Шейные сегменты спинного мозга С3-С5 иннервируют диафрагму, Т1–12 – наружные и внутренние межреберные мышцы. С5-С8 и Т1-Т2 – центры движения верхних конечностей, L2–L4 и S1–S2 – центры движения задних или нижних конечностей. альфа- и гамма-мотонейроны поддерживают тонус тела и обеспечивают рефлексы сгибания и разгибания – миостатические рефлексы: коленный, ахиллов, подошвенный, сгибательный и разгибательный рефлексы предплечья, брюшной рефлекс. Рефлексы с рецепторов кожи выражаются в усилении сокращения мышц-сгибателей. Висцеромоторные рефлексы возникают при стимуляции афферентных нервов внутренних органов и проявляются в виде двигательных реакций мышц грудной клетки, брюшной стенки и разгибателя спины. Вегетативные рефлексы – это ответная реакция внутренних органов на раздражение висцеральных и соматических рецепторов. Вегетативные центры спинного мозга, расположенные в боковых рогах, участвуют в регуляции кровяного давления, деятельности сердца, секреции и моторики пищеварительного тракта и функции мочеполовой системы. В пояснично-крестцовом отделе спинного мозга находится центр дефекации, из которого по парасимпатическим волокнам в составе тазового нерва поступают импульсы, усиливающие моторику прямой кишки и обеспечивающие непроизвольный акт дефекации. Произвольный акт дефекации совершается за счет нисходящих влияний головного мозга на спинальный центр. Во II – IV крестцовых сегментах спинного мозга находится рефлекторный центр мочеиспускания, обеспечивающий непроизвольное отделение мочи. Головной мозг осуществляет произвольное мочеиспускание.Проводниковая функция спинного мозга
В состав белого вещества спинного мозга входят миелиновые нервные волокна, собранные в пучки и образующие проводящие пути спинного мозга. Короткие ассоциативные волокна обеспечивают межсегментарные связи или соединяют нейроны противоположной стороны спинного мозга. Длинные проекционные волокна делят на восходящие, идущие к различным отделам головного мозга, и нисходящие – от головного мозга к спинному. Восходящие проводящие пути проходят в белом веществе задних канатиков, расположенных между задними рогами серого вещества. К ним относится тонкий пучок Голля (fasciculus gracilis), отвечает за проведение проприоцептивной, тактильной и висцеральной чувствительности от нижней части туловища и нижних конечностей. Клиновидный пучок Бурдаха (fasciculus cuneatus) проводит проприоцептивную, тактильную и висцеральную чувствительность от верхней половины туловища и верхних конечностей. Оба пучка перекрещиваются на уровне продолговатого мозга, где находятся соответствующие ядра (n.gracilis и п.cuneatus) и синаптическое переключение на второй нейрон. После перекреста аксоны нейронов в составе медиального лемнискового пути направляются к специфическим ядрам вентробазального комплекса таламуса, где они вновь переключаются на третий нейрон. Аксоны нейронов специфических таламических ядер заканчиваются в IV слое соматосенсорной коры больших полушарий. Оба пучка передают информацию о локализации, форме и контурах периферического раздражителя с большой точностью от небольшого количества рецепторов в высшие отделы головного мозга. При поражении тонкого и клиновидного пучков наблюдаются потеря тактильной чувствительности и нарушение координации движений. В боковых канатиках проходит восходящийдорсальный спиномозжечковый тракт (пучок Флексига), который, не перекрещиваясь, восходит до коры мозжечка и передает в мозжечок информацию от рецепторов мышц, связок и кожи конечностей, а также восходящий вентральный спиномозжечковый тракт (пучок Говерса). Он вступает в мозжечок после перекреста. Передает в мозжечок информацию от сухожилий, кожи и висцерорецепторов. Участвует в поддержании тонуса мышц при движении и сохранении позы тела. К восходящим путям относится спиноталамический тракт. Информация от рецепторов кожи поступает в спинальный ганглий, затем через задние корешки – к заднему рогу спинного мозга (первое переключение). Аксоны чувствительных нейронов переходят на противоположную сторону в каждом сегменте спинного мозга и поднимаются по боковому канатику к таламусу, а затем в сенсорную кору. Боковой спиноталамический тракт проводит болевую и температурную чувствительность. Часть волокон спиноталамического тракта идет к таламусу по переднему канатику, который делает перекрест на противоположную сторону через несколько вышележащих сегментов. Передний спиноталамический тракт передает в зрительный бугор тактильную чувствительность. Нисходящие проводящие пути спинного мозга включают несколько трактов, заканчивающихся на мотонейронах передних рогов. К ним относится пирамидный, или кортикоспинальный, тракт, который делится на латеральный и передний пучки. Латеральный пучок начинается от нейронов коры больших полушарий и делает перекрест на уровне продолговатого мозга, спускаясь на противоположную сторону спинного мозга. Передний пучок делает перекрест на уровне сегмента, в котором он заканчивается. Пирамидный тракт обеспечивает связь нейронов двигательной зоны коры больших полушарий с мотонейронами передних рогов спинного мозга и отвечает за произвольные движения. Руброспинальный (красноядерно-спиномозжечковый) тракт (Монакова) относится к экстрапирамидной системе, делает перекрест после выхода из красного ядра, связывает нейроны красного ядра среднего мозга с мозжечком, продолговатым мозгом и спинным, заканчивается на интернейронах соответствующего сегмента спинного мозга, управляет тонусом мышц и непроизвольной координацией движений. Вестибулоспинальный (преддверно-спинномозговой) тракт от-носится к экстрапирамидной системе, отвечает за связь между ядром Дейтерса варолиева мосга, мозжечком и мотонейронами передних рогов спинного мозга. Регулирует тонус мускулатуры, координацию движений, равновесие и ориентацию в пространстве. Ретикулоспинальный (ретикулярно-спинномозговой) тракт также относится к экстрапирамидной системе. Начинается на ретикулярных нейронах различных уровней моста и продолговатого мозга и заканчивается на мотонейронах спинного мозга. Оказывает тормозные и облегчающие влияния на рефлексы спинного мозга. Отвечает за осуществление фазных двигательных реакций и поддержание позы тела. При одностороннем поражении спинного мозга (при травме, опухоли) развевается сложный симптомокомплекс (синдром Броун-Секара). На стороне поражения (ниже места поражения) нарушаются двигательные функции вследствие повреждения пирамидного тракта. На противоположной стороне движения сохраняются, но отсутствует болевая и температурная чувствительность (повреждение перекрещенного спиноталамического тракта), и с обеих сторон частично нарушена тактильная чувствительность. Полное пересечение спинного мозга приводит к возникновению спинального шока (шок-удар). В результате ниже перерезки исчезают все виды рефлекторной деятельности: нарушается двигательная активность, все виды чувствительности, вегетативные функции (мочеиспускание и отделение кала становятся непроизвольными). Причина спинального шока – это потеря связей с вышележащими отделами центральной нервной системы и особенно с корой больших полушарий. Это доказано повторной перерезкой спинного мозга ниже места перерезки. При этом спинальный шок вновь не возникает. Арефлексия у разных животных длится определенное время: у лягушки – несколько минут, у хищных млекопитающих – часы, у обезьян – недели или месяцы, у человека – несколько месяцев. Восстанавливаются лишь простые спинальные рефлексы: сгибание-разгибание, рефлекторное опорожнение мочевого пузыря и сосудистые рефлексы. Не восстанавливаются все виды чувствительности и произвольные двигательные акты.Ствол мозга
В состав ствола мозга входят: продолговатый мозг, варолиев мост, средний мозг и мозжечок.Ствол мозга выполняет ряд сложных и многообразных функций: 1. Осуществляет рефлекторные соматические рефлексы, направленные на поддержание позы тела в пространстве. 2. Обеспечивает различные вегетативные рефлексы, некоторые из них (дыхательные, сердечно-сосудистые) имеют жизненно важное значение. 3. Проводниковые функции: через ствол проходят многочисленные восходящие и нисходящите пути, связывающие кору больших полушарий со спинным мозгом. 4. Ассоциативные функции: первичный анализ силы и качества сенсорного раздражителя, а также взаимодействие структур, входящих в состав ствола мозга.
Продолговатый мозг
Продолговатый мозг является продолжением спинного мозга, имеет длину около 25 мм, в нем отсутствует сегментарное строение, серое вещество образует отдельные скопления нейронов – ядра. Он выполняет собственные, вегетативные и проводниковые функции.Собственные функции продолговатого мозга
В продолговатом мозге расположены ядра VIII, IX, X, XI и XII пар черепно-мозговых нервов. VIII пара – преддверно-улитковый нерв (n.vestibulocochlearis). Находится на границе между продолговатым мозгом и варолиевым мостом. Волокна улитки или собственно слухового нерва являются началом слуховых путей, идущих от спирального ганглия улитки (слуховые функции). IX пара – языкоглоточный нерв (n.glossopharyngeus). Содержит двигательные (иннервация мышц глотки и полости рта), чувствительные (от рецепторов вкуса задней трети языка) и вегетативные волокна (иннервация слюнных желез). X пара – блуждающий нерв (n.vagus) имеет три ядра. Вегетативное ядро отвечает за парасимпатическую иннервацию гортани, пищевода, сердца, желудка, тонкой кишки, пищеварительных желез. Нервные волокна чуствительного ядра образуют солитарный тракт в продолговатом мозге. Ядро получает информацию от рецепторов альвеол легких и других внутренних органов. Двигательное ядро отвечает за сокращение мышц глотки и гортани при глотании и дыхании. XI пара – добавочный нерв (n.accessorius) – двигательный нерв, иннервирующий грудино-ключично-сосцевидную и трапециевидную мышцу своей стороны. При поражении нерва снижается тонус иннервируемых мышц и плечо на стороне поражения опускается, а поворот головы в сторону, противоположную поражению, затруднен. XII пара – подъязычный нерв (n.hypoglossus) иннервирует мышцы языка своей стороны. Одностороннее поражение нерва сопровождается нарушением функций мышц языка.Вегетативные функции продолговатого мозга
Продолговатый мозг содержит дыхательный центр (центр вдоха – инспираторный и центр выдоха – экспираторный), сосудодвигательный центр – регулирует тонус сосудов и уровень кровяного давления, главный центр сердечной деятельности – группа нейронов ядра блуждающего нерва (тормозящая) и группа нейронов, связанная со спинальными центрами (стимулирующая). Блуждающий нерв регулирует (усиливает) моторику желудочно-кишечного тракта и его секреторную деятельность. В продолговатом мозге находится центр слюноотделения, парасимпатическая часть которого обеспечивает выделение большого количества жидкой слюны, богатой неорганическими веществами, а симпатическая – небольшого количества густого белкового секрета. Продолговатый мозг отвечает за некоторые защитные рефлексы: рвоты, кашля, чихания, слезоотделения, смыкания век, а также рефлексы пищевого поведения (сосания, жевания, глотания). Продолговатый мозг реализует соматические рефлексы: рефлексы поддержания позы тела за счет статических рефлексов, регулирующих тонус мышц, удерживающих положение тела в пространстве, а также статокинетических, обеспечивающих перераспределение тонуса мышц туловища для организации позы в момент прямолинейного и вращательного движения. На дне IV желудочка продолговатого мозга находятся нейроны «голубого пятна», которые выделяют медиатор норадреналин. Через ретикулоспинальный тракт эти нейроны тормозят спинальные рефлексы и снижают мышечный тонус в фазу «быстрого сна». Продолговатый мозг регулирует некоторые анализаторные функции, осуществляя первичный анализ сенсорных раздражителей (кожного, вкусового, слухового, вестибулярного).Проводниковые функции продолговатого мозга
В продолговатом мозге начинаются нисходящие пути: вестибулоспинальный, оливоспинальный и ретикулоспинальный, обеспечивающие связь между вестибулярными ядрами, оливой, ретикулярной формацией продолговатого мозга и мотонейронами спинного мозга, отвечающими за тонус и координацию мышечных реакций. Раздражение ретикулярной формации продолговатого мозга оказывает нисходящие влияния на моторную активность скелетных мышц, а также восходящие, активирующие влияния на кору больших полушарий, вызывая десинхронизацию электроэнцефалограммы. Через продолговатый мозг проходят все восходящие и нисходящие пути спинного мозга: спиноталамический, кортикоспинальный, руброспинальный. В нем заканчиваются пути из коры больших полушарий – корковоретикулярный, а также восходящие пути проприоцептивной чувствительности – тонкий пучок Голля и клиновидный пучок Бурдаха. Поэтому при повреждении одной из половин продолговатого мозга выше перекреста восходящих путей проприоцептивной чувствительности происходит нарушение чувствительности и работы мышц лица и головы на стороне повреждения, в то время как на неповрежденной стороне возникают нарушения кожной чувствительности и двигательные параличи туловища и конечностей. Это связано с тем, что все восходящие и нисходящие пути перекрещиваются.Варолиев мост
Мост (pons Varolii) располагается выше продолговатого мозга и выполняет двигательные, сенсорные, интегративные и проводниковые функции.Собственные функции варолиева моста
В состав моста входят ядра VIII пары черепно-мозговых нервов, вестибулярное ядро (латеральное – Дейтерса и верхнее – Бехтерева), отвечает за первичный анализ вестибулярных раздражителей. VII пара – лицевой нерв (п.facialis), иннервирует мимические мышцы лица, подъязычную и подчелюстную слюнные железы, передает информацию от вкусовых рецепторов передней части языка. VI пара – отводящий нерв (n.abducens), иннервирует прямую наружную мышцу, отводящую глазное яблоко кнаружи. V пара – тройничный нерв (п.trigeminus). Двигательное ядро нерва иннервирует жевательные мышцы, мышцы нёбной занавески и мышцы, напрягающие барабанную перепонку. Чувствительное ядро получает афферентные аксоны от рецепторов кожи лица, слизистой оболочки носа, зубов, надкостницы костей черепа, конъюнктивы глазного яблока. В мосте располагается пневмотаксический центр, запускающий центр выдоха продолговатого мозга, а также группа нейронов, активирующих центр вдоха. Ретикулярная формация моста является продолжением ретикулярной формации продолговатого мозга. Она влияет на кору больших полушарий, активируя ее и вызывая пробуждение. Аксоны ретикулярной формации моста идут в мозжечок и спинной мозг.Проводниковая функция варолиева моста
Через мост проходят все восходящие и нисходящие пути, связывающие мост с мозжечком и спинным мозгом, корой больших полушарий и другими структурами центральной нервной системы.Средний мозг
Основными структурными образованиями среднего мозга являются: ядро блокового нерва – IV пара черепно-мозговых нервов (n.trochlearis), ядро глазодвигательного нерва (n.oculomotorius) – III пара черепно-мозговых нервов, красное ядро (n.ruber), черное вещество (substantia nigra), четверохолмие, ножки мозга и ядра ретикулярной формации. Блоковой нерв иннервирует верхнюю косую мышцу глаза, обеспечивает поворот глаза вверх-наружу. Глазодвигательный нерв отвечает за поднятие верхнего века, регуляцию движений глаза вверх, вниз, к носу и вниз к углу носа. Нейроны добавочного ядра глазодвигательного нерва (ядро Якубовича) регулируют просвет зрачка и кривизну хрусталика, обеспечивая процесс аккомодации. Красные ядра имеют связи с корой больших полушарий, подкорковыми ядрами, мозжечком, спинным мозгом. Они регулируют тонус мускулатуры. Стимуляция красных ядер приводит к увеличению тонуса мышц-сгибателей. Эти ядра оказывают тормозное влияние на латеральное вестибулярное ядро (Дейтерса) продолговатого мозга, которое активирует тонус мышц-разгибателей. Перерезка между средним и продолговатым мозгом приводит к децеребрационной ригидности, характеризующейся резким повышением тонуса мышц-разгибателей конечностей, шеи и спины. Это связано с активацией ядра Дейтерса, не получающего тормозные влияния со стороны красного ядра. Ригидность исчезает, если разрушить ядро Дейтерса или произвести перерезку ниже ромбовидной ямки продолговатого мозга. Черное вещество располагается в ножках мозга, участвует в регуляции актов жевания, глотания и их последовательности, а также в координации мелких и точных движений пальцев рук, например, при письме, игре на скрипке, на рояле. Нейроны этого ядра синтезируют дофамин, поставляемый к базальным ядрам головного мозга. Последний играет важную роль в контроле сложных двигательных актов. Поражение черного вещества приводит к дегенерации дофаминергических волокон, проецирующихся в полосатое тело, нарушению тонких движений пальцев рук, развитию мышечной ригидности и тремору (болезнь Паркинсона). Ретикулярная формация среднего мозга принимает участие в регуляции сна и бодрствования. Проводниковая функция среднего мозга Эта функция определяется наличием в нем как восходящих путей к таламусу (спиноталамический тракт, медиальная петля), к коре больших полушарий и мозжечку, так и нисходящих – к продолговатому и спинному мозгу (пирамидный тракт, корково-мостовой и рубро-ретикулоспинальный пуги). Рефлекторная функция среднего мозга Верхние бугры четверохолмия – это первичный зрительный подкорковый центр, обеспечивающий зрительный ориентировочный рефлекс – поворот головы и глаз в сторону светового раздражителя, фиксацию взора и слежение за движущимися объектами. При повреждении или раздражении верхних бугров наблюдается нистагм глаз. Нижние бугры четверохолмия – это первичный слуховой подкорковый центр, участвующий в ориентировочном слуховом рефлексе – повороте головы в сторону источника звука. Двустороннее повреждение нижних бугров сопровождается потерей способности локализовать источник звука в пространстве. У человека рефлекс четверохолмия называется сторожевым, обеспечивает старт-реакцию на внезапные звуковые или зрительные раздражители. Связь среднего мозга с гипоталамусом создает вегетативное обеспечение подготовки к избеганию, оборонительной и двигательной реакции (вскакивание на ноги, вздрагивание, бегство от раздражителя). Средний мозг участвует в реализации статических рефлексов при относительном покое тела, т. е. при стоянии, лежании в различных положениях, и статокинетических, связанных с изменением положения тела в пространстве. Статические рефлексы делят на позно-тонические и установочные, или выпрямительные. Они обеспечивают удержание частей тела (например, головы) на месте, а также корректируют ориентацию конечностей при смене их положения. Так, в опытах на кошках с удаленным вестибулярным аппаратом показано, что пассивное поднимание головы приводит к снижению тонуса разгибателей задних конечностей и повышению тонуса разгибателей передних конечностей. При пассивном опускании головы наблюдаются противоположные явления. Статокинетические рефлексы проявляются при вращении, пе-ремещении тела в горизонтальной и вертикальной плоскостях. При вращательном движении наблюдается нистагм головы и глаз, который выражается в медленном движении головы и глаз в сторону, противоположную направлению вращения, и быстром возвращении в исходное состояние. При быстром подъеме или опускании туловища в самолете или лифте наблюдается рефлекс лифта. Опускание приводит к разгибанию конечностей, а подъем – к сгибанию.Мозжечок
Мозжечок расположен позади больших полушарий мозга над продолговатым мозгом и мостом мозга и представляет собой очень древнюю структуру, выполняющую функцию координации и регуляции произвольных и непроизвольных движений, их коррекции и программирования. Мозжечок принимает участие в двигательной адаптации и двигательном научении, в осуществлении вегетативных функций и некоторых поведенческих актов. Анатомически мозжечок состоит из средней части – червя, расположенных по обе стороны от него полушарий и боковых флоккулонодулярных долей. Кроме того, мозжечок делят на архицеребеллум (древний мозжечок), к нему относится флоккуломедулярная доля, связанная с вестибулярной системой, и палеоцеребеллум (старый мозжечок), в него входят участки червя мозжечка, пирамида, язык, парафлоккулярный отдел. Он получает информацию в основном от проприоцептивных систем мышц, сухожилий, надкостницы, оболочек суставов. Неоцеребеллум (новый мозжечок) состоит из коры полушарий, мозжечка и участков червя, получает информацию от коры, зрительных и слуховых сенсорных систем. Кора мозжечка состоит из трех слоев. Верхний слой – молекулярный, в него входят дендритные разветвления грушевидных клеток (клеток Пуркинье), параллельные волокна – аксоны вставочных нейронов. В нижней части молекулярного слоя находятся тела корзинчатых клеток, аксоны которых контактируют с помощью синапсов с телами клеток Пуркинье. Там же находятся и звездчатые клетки. Второй слой – ганглиозный – содержит тела клеток Пуркинье, имеющих самую мощную дендритную систему с большим количеством синапсов (до 60 тысяч). Третий, гранулярный слой состоит из тел вставочных нейронов (гранулярных клеток или клеток-зерен). Аксоны этих клеток образуют в молекулярном слое Т-образные разветвления. В гранулярном слое находятся также клетки Гольджи, аксоны которых направляются в молекулярный слой. Аксоны клеток Пуркинье передают информацию в подкорковые структуры мозга и ядра мозжечка: ядра шатра, пробковидное, шаровидное и зубчатое ядра. В кору мозжечка поступают два типа афферентных волокон – лазающие и мшистые (ИЛИ моховидные). Лазающие волокна – это аксоны нейронов нижних олив продолговатого мозга, через которые проходят спиномозжечковые тракты (дорсальный и вентральный), передающие информацию от рецепторов кожи, мышц, суставов. Лазающие волокна контактируют с дендритами клеток Пуркинье. Мшистые волокна – это афферентные пути от ядер моста в мозжечок, они заканчиваются на клетках-зернах коры мозжечка. С помощью афферентных адренергических волокон мозжечок связан с голубым пятном среднего мозга. В окончаниях этих волокон выделяется норадреналин, который, попадая в кору мозжечка, изменяет возбудимость его клеток. Аксоны гранулярных клеток тормозят клетки Пуркинье и клетки-зерна своего же слоя. Клетки Пуркинье являются только тормозными. Они тормозят клетки ядер мозжечка, регулирующих тонус двигательных центров промежуточного, среднего, продолговатого и спинного мозга. Ядра мозжечка имеют морфофункциональные связи с различными структурами мозга. Медиальные части коры мозжечка проецируются к ядрам шатра и являются вестибулярными регуляторами. Последние имеют связи с ядром Дейтерса и ретикулярной формацией продолговатого и среднего мозга и через ретикулоспинальный тракт – с мотонейронами спинного мозга. Промежуточные части коры мозжечка отвечают за координацию позы, целенаправленное движение и коррекцию выполнения медленных движений на основе механизма обратной связи с пробковидным и шаровидным ядрами. Последние влияют на деятельность красного ядра и ретикулярной формации, проецируясь на таламус и двигательную кору. От нейронов латеральной части коры мозжечка информация поступает в зубчатое ядро, затем через таламус в двигательную кору, а оттуда – к мотонейронам спинного мозга. Латеральные части коры мозжечка отвечают за программирование сложных движений без использования механизмов обратной связи. Из мозжечка информация поступает по трем парам ножек. Через верхние – к таламусу, варолиеву мосту, к красному ядру, ядру ствола мозга, в ретикулярную формацию среднего мозга. Через нижние ножки мозжечка сигналы идут к вестибулярным ядрам продолговатого мозга, оливам. Средние ножки связывают неоцеребеллум с лобными долями коры больших полушарий.Функции мозжечка
Мозжечок регулирует силу и точность мышечных сокращений и их тонус как в покое, так и при движениях, а также синергию сокращений разных мышц при сложных движениях. При поражении мозжечка возникает целый ряд как двигательных расстройств, так и нарушений со стороны вегетативной нервной системы. К ним относятся астения – быстрая утомляемость, снижение силы мышечных сокращений, астазия – утрата способности к длительному сокращению мышц, поэтому больной не может долго стоять или сидеть, неточность движений; атаксия – нарушение координации движений, неуверенная походка; абазия – невозможность сохранить центр тяжести тела; атония или дистония – понижение или повышение тонуса мышц; тремор – дрожание пальцев рук, кистей и головы в покое, но его усиление при движении; дизартрия – нарушение кординации мышц лица, необходимое для четкого произнесения слов. Речь становится монотонной, медленной и невыразительной. Дисметрия – расстройство равномерности движения (гиперметрия или гипометрия). Страдает кожная и проприоцептивная чувствительность нижних (пучок Флексига) и верхних конечностей (пучок Говерса). При поражении мозжечка тормозится процесс обучения, так как многие движения человек заучивает во время жизни (письмо, ходьба). Нарушение функций мозжечка приводит к неточности движений, их разбросанности, негармоничности, а это говорит об участии мозжечка в деятельности коры больших полушарий, ответственной за организацию процессов высшей нервной деятельности. Мозжечок влияет на возбудимость сенсомоторной коры больших полушарий и контролирует тем самым уровень тактильной, температурной и зрительной чувствительности. Мозжечок играет адаптационно-трофическую роль в регуляции не только мышечной деятельнсти, но и ее вегетативного обеспечения. Удаление мозжечка приводит к нарушению целого ряда вегетативных функций (Л. А. Орбели). Мозжечок оказывает как угнетающее, так и стимулирующее влияние на работу сердечно-сосудистой системы. При раздражении последнего высокое артериальное давление снижается, а исходное низкое – повышается. Снижается частота дыхания, повышается тонус гладких мышц кишечника. При повреждении мозжечка нарушается углеводный, белковый и минеральный обмен, а также процессы энергообразования, терморегуляции и кроветворения. Стимуляция мозжечка приводит к нарушению репродуктивной функции, к сокращению матки у беременных кошек. Удаление мозжечка провоцирует рождение нежизнеспособного потомства или препятствует зачатию.Промежуточный мозг
В состав промежуточного мозга входят: 1. таламус (область зрительного бугра) 2. гипоталамус (подталамическая область) 3. третий желудочек.Область зрительного бугра, в свою очередь, слагается: 1. из зрительного бугра (таламус оптикус) 2. надталамической области (эпиталамус – эпифиз, шишковидная железа) 3. заталамической области (метаталамус – медиальное и латеральное коленчатые тела).
Таламус
Зрительный бугор является местом переключения всех чувствительных проводников, идущих от экстеро-, проприои интерорецепторов, поднимающихся в кору головного мозга. В нем происходит обработка всей информации, поступающей в кору из спинного мозга и подкорковых структур. По мнению А. Уолкера, выдающегося исследователя зрительного бугра, «таламус является посредником, в котором сходятся все раздражения от внешнего мира и, видоизменяясь здесь, направляются к подкорковым и корковым центрам таким образом, чтобы организм смог адекватно приспособиться к постоянно меняющейся среде. Таламус, как видно, таит в себе тайну многого из того, что происходит в коре больших полушарий». О полифункциональности таламуса говорит наличие в нем около 120 ядер, которые топографически можно разделить на три основные группы: переднюю, имеет проекции в поясную кору, медиальную – в лобную, латеральную – в теменную, височную, затылочную. По функциональным признакам ядра зрительного бугра делят на три группы: специфические, образующие с соответствующими областями коры специфическую таламокортикальную систему, неспецифические, составляющие диффузную, неспецифическую таламокортикальную систему, и ассоциативные. В состав группы специфических ядер входят переднее вентральное, медиальное, вентролатеральное, постмедиальное, постлатеральное, а также медиальные и латеральные коленчатые тела. Специфические ядра содержат так называемые «релейные» (передаточные) нейроны, имеющие мало дендритов и длинный аксон, заканчивающийся в III -IV слоях коры больших полушарий (соматосенсорная зона). Если раздражать какое-либо из специфических ядер электрическими импульсами, то в соответствующих проекционных областях коры с коротким латентным периодом возникает реакция, названная первичным ответом. Каждое из специфических ядер отвечает за свой вид чувствительности, так как они, так же как и кора больших полушарий, имеют соматотопическую локализацию, т. е. к ним поступают сигналы от тактильных, болевых, температурных, мышечных рецепторов, а также от интерорецепторов зон проекции блуждающего и чревного нервов. Латеральное, или наружное, коленчатое тело – это подкорковый центр зрения, таламическое реле для зрительных импульсов. Оно имеет афферентные связи с сетчаткой глаза и буграми четверохолмия и эфферентные – с затылочной долей коры больших полушарий. Медиальное коленчатое тело – подкорковый, таламический центр слуха, получает афферентные импульсы из латеральной петли и нижних бугров четверохолмия и посылает информацию в височную долю коры больших полушарий. К неспецифическим ядрам таламуса относятся: срединный центр, парацентральное ядро, центральное медиальное и латеральное, субмедиальное, вентральное переднее, парафасцикулярпое, ретикулярное ядро, перивентрикулярное и центральная серая масса. Нейроны неспецифических ядер являются клетками ретикулярной формации, аксоны которых контактируют со всеми слоями коры больших полушарий, образуя диффузные связи. В свою очередь, к неспецифическим ядрам поступает информация от ретикулярной формации ствола мозга, лимбической системы, базальных ганглиев и специфических ядер таламуса. Раздражение неспецифических ядер электрическим током вызывает возникновение в коре больших полушарий не локально, а диффузно специфической электрической активности, имеющей длинный латентный период и вид веретена, названной сонными веретенами, или реакцией вовлечения. Основная функция неспецифических ядер состоит в облегчении или торможении специфических ответов коры, т. е. в изменении их возбудимости. Ассоциативные ядра таламуса включают в себя медиодорсальное, латеральное дорсальное ядро и подушку. Нейроны этих ядер имеют разную форму и количество отростков, что позволяет им выполнять разнообразные функции, связанные с переработкой информации различных модальностей, после чего она поступает в 1-е и 2-е слои ассоциативной зоны коры, частично – в проекционные зоны коры (4-е и 5-е слои). При поражении таламических ядер, отвечающих за переработку всей сенсорной информации, в том числе и болевой, могут возникать сильнейшие боли. С наличием застойного очага возбуждения в таламусе и коре больших полушарий связаны «фантомные боли» (в ампутированной конечности). Таламус обеспечивает двигательные и вегетативные реакции, связанные с сосанием, жеванием, глотанием и смехом.Гипоталамус
Гипоталамус является частью промежуточного мозга и входит в состав лимбической системы. Это сложноорганизованный отдел мозга, выполняющий целый ряд вегетативных функций, отвечает за гуморальное и нейросекреторное обеспечение организма, эмоциональные поведенческие реакции и другие функции.Морфологически в гипоталамусе выделяют около 50 пар ядер, разделенных топографически на 5 больших групп: 1. преоптическая группа или область, в которую входят: перивентрикулярное, преоптическое ядро, медиальное и латеральное преоптическое ядра 2. передняя группа: супраоптическое, паравентрикулярное и супрахиазматическое ядра 3. средняя группа: вентромедиальное и дорсомедиальное ядра 4. наружная группа: латеральное гипоталамическое ядро, ядро серого бугра 5. задняя группа: заднее гипоталамическое ядро, перифорникальное ядро, медиальные и латеральные ядра сосцевидных (мамиллярных) тел.
Нейроны гипоталамуса имеют особую чувствительность к составу омывающей их крови: изменениям рН, рСО2, рО2, содержанию катехоламинов, ионов калия и натрия. В супраоптическом ядре имеются осморецепторы. Гипоталамус – единственная структура мозга, в которой отсутствует гематоэнцефалический барьер. Нейроны гипоталамуса способны к нейросекреции пептидов, гормонов, медиаторов. В заднем и латеральном гипоталамусе выявлены нейроны, чувствительные к адреналину. Адренорецептивные нейроны могут находится в одном и том же ядре гипоталамуса вместе с холинорецептивными и серотонинорецептивными. Введение адреналина или норадреналина в латеральный гипоталамус вызывает реакцию еды, а введение ацетилхолина или карбохолина – питьевую реакцию. Нейроны вентромедиального и латерального ядер гипоталамуса проявляют высокую чувствительность к глюкозе за счет наличия в них «глюкорецепторов».
Проводниковая функция гипоталамуса
Гипоталамус имеет афферентные связи с обонятельным мозгом, базальными ганглиями, таламусом, гиппокампом, орбитальной, височной и теменной корой. Эфферентные пути представлены: мамилло-таламическим, гипоталамо-таламическим, гипоталамо-гипофизарным, мамиллотегментальным, гипоталамо-гиппокампальным трактами. Кроме того, гипоталамус посылает импульсы к вегетативным центрам ствола мозга и спинного мозга. Гипоталамус имеет тесные связи с ретикулярной формацией ствола мозга, определяющей протекание вегетативных реакций организма, его пищевое и эмоциональное поведение.Собственные функции гипоталамуса
Гипоталамус является главным подкорковым центром, регулирующим вегетативные функции. Раздражение передней группы ядер имитирует эффекты парасимпатической нервной системы, ее трофотропное влияние на организм: сужение зрачка, брадикардию, снижение артериального давления, усиление секреции и моторики желудочно-кишечного тракта. Супраоптическое и паравентрикулярное ядра участвуют в регуляции водного и солевого обмена за счет выработки антидиуретического гормона. Стимуляция задней группы ядер оказывает эрготропные влияния, активирует симпатические эффекты: расширение зрачка, тахикардию, повышение кровяного давления, торможение моторики и секреции желудочно-кишечного тракта. Гипоталамус обеспечивает механизмы терморегуляции. Так, ядра передней группы ядер содержат нейроны, отвечающие за теплоотдачу, а задней группы – за процесс теплопродукции. Ядра средней группы участвуют в регуляции метаболизма и пищевого поведения. В вентромедиальных ядрах находится центр насыщения, а в латеральных – центр голода. Разрушение вентромедиального ядра приводит к гиперфагии – повышенному потреблению пищи и ожирению, а разрушение латеральных ядер – к полному отказу от пищи. В этом же ядре находится центр жажды. В гипоталамусе располагаются центры белкового, углеводного и жирового обмена, центры регуляции мочеотделения и полового поведения (супрахиазматическое ядро), страха, ярости, цикла «сон-бодрствование». Регуляция многих функций организма гипоталамусом осуществляется за счет продукции гормонов гипофиза и пептидных гормонов: либеринов, стимулирующих высвобождение гормонов передней доли гипофиза, и статинов – гормонов, которые тормозят их выделение. Эти пептидные гормоны (тиролиберин, кортиколиберин, соматостатин и др.) через портальную сосудистую систему гипофиза достигают его передней доли и вызывают изменение продукции соответствующего гормона аденогипофиза. Супраоптическое и паравентрикулярное ядра помимо их участия в водно-солевом обмене, лактации, сокращении матки продуцируют гормоны полипептидной природы – окситоцин и антидиуретический гормон (вазопрессин), которые с помощью аксонального транспорта достигают нейрогипофиза и, кумулируясь в нем, оказывают соответствующее действие на реабсорбцию воды в почечных канальцах, на тонус сосудов, на сокращение беременной матки. Супрахиазматическое ядро имеет отношение к регуляции полового поведения, а патологические процессы в области этого ядра приводят к ускорению полового созревания и нарушениям менструального цикла. Это же ядро является центральным водителем циркадианных (околосуточных) ритмов многих функций в организме. Гипоталамус имеет непосредственное отношение, как уже отмечалось выше, к регуляции цикла «сон-бодрствование». При этом задний гипоталамус стимулирует бодрствование, передний – сон, а повреждение заднего гипоталамуса может вызвать патологический летаргический сон. В гипоталамусе и гипофизе вырабатываются нейропептиды, относящиеся к антинотицептивной (обезболивающей) системе, или опиаты: энкефалины и эндорфины. Гипоталамус является частью лимбической системы, принимающей участие в реализации эмоционального поведения. Д. Олдс, вживляя электроды в некоторые ядра гипоталамуса крысы, наблюдал, что при стимуляции одних ядер происходила негативная реакция, других – положительная: крыса не отходила от педали, замыкающей стимулирующий ток, и нажимала ее до изнеможения (опыт с самораздражением). Можно предположить, что она раздражала «центры удовольствия». Раздражение переднего гипоталамуса провоцировало картину ярости, страха, пассивно-оборонительную реакцию, а заднего – активную агрессию, реакцию нападения.Лимбическая система
Лимбическая система – это функционально единый комплекс нервных структур, ответственных за эмоциональное поведение, побуждения к действию (мотивации), процессы научения и запоминания, инстинкты (пищевые, оборонительные, половые) и регуляцию цикла «сон-бодрствование». В связи с тем, что лимбическая система воспринимает большое количество информации от внутренних органов, она получила второе название – «висцеральный мозг». В состав лимбической системы входят три структурных комплекса: древняя кора (палеокортекс), старая кора (архикортекс), срединная кора (мезокортекс). Древняя кора (палеокортекс) включает в себя препериформную, периамигдалярную, диагональную кору, обонятельные луковицы, обонятельный бугорок, прозрачную перегородку. Второй комплекс – старая кора (архикортекс) состоит из гиппокампа, зубчатой фасции, поясной извилины. Структурами третьего комплекса (мезокортекса) являются островковая кора и парагиппокампальная извилина. Лимбическая система включает в себя такие подкорковые образования, как миндалины мозга, ядра перегородки, переднее таламическое ядро, мамиллярные тела, гипоталамус. Основное отличие лимбической системы от других отделов центральной нервной системы – это наличие двусторонних реципрокных связей между ее структурами, образующими замкнутые круги, по которым циркулируют импульсы, обеспечивающие функциональное взаимодействие между различными частями лимбической системы. В так называемый «круг Пейпеса» входят: гиппокамп – мамиллярные тела – передние ядра таламуса – кора поясной извилины – парагиппокампальная извилина – гиппокамп. Этот круг отвечает за эмоции, формирование памяти и обучения. Другой круг: амигдала – гипоталамус – мезенцефальные структуры – амигдала регулирует агрессивно-оборонительные, пищевые и сексуальные формы поведения. Лимбическая система образует связи с новой корой посредством лобных и височных долей. Последние передают информацию от зрительной, слуховой и соматосенсорной коры к миндалине и гиппокампу. Считают, что лобные области мозга являются основным корковым регулятором деятельности лимбической системы.Функции лимбической системы
Многочисленные связи лимбической системы с подкорковыми структурами мозга, корой больших полушарий и внутренними органами позволяют ей принимать участие в реализации различных функций, как соматических, так и вегетативных. Она контролирует эмоциональное поведение и совершенствует приспособительные механизмы организма в новых условиях существоваания. При поражении лимбической системы или экспериментальном воздействии на нее нарушается пищевое, половое и социальное поведение. Лимбическая система, ее древняя и старая кора отвечают за обонятельные функции, а обонятельный анализатор является самым древним. Он запускает все виды деятельности коры больших полушарий. В состав лимбической системы входит высший вегетативный центр – гипоталамус, создающий вегетативное обеспечение любого поведенческого акта. Более всего изучены такие структуры лимбической системы, как миндалина, гиппокамп и гипоталамус. Последний описан ранее (см. с. 72). Миндалина (амигдала, миндалевидное тело) располагается в глубине височной доли мозга. Нейроны миндалины полисенсорны и обеспечивают ее участие в оборонительном поведении, соматических, вегетативных, гомеостатических и эмоциональных реакциях и в мотивации условно-рефлекторного поведения. Раздражение миндалины приводит к изменениям в сердечно-сосудистой системе: колебаниям частоты сердечных сокращений, появлению аритмий и экстрасистол, понижению артериального давления, а также реакциям со стороны желудочно-кишечного тракта: жеванию, глотанию, саливации, изменениям моторики кишечника. После двустороннего удаления миндалин у обезьян утрачивается способность к социальному внутригрупповому поведению, они избегают остальных членов группы, ведут себя отчужденно, кажутся встревоженными и неуверенными в себе животными. Они не отличают съедобные предметы от несъедобных (психическая слепота), у них становится выраженным оральный рефлекс (берут в рот все предметы) и возникает гиперсексуальность. Полагают, что подобные расстройства у амигдалаэктомированных животных связаны с нарушением двусторонних связей между височными долями и гипоталамусом, которые отвечают за приобретенное мотивационное поведение и эмоции. Эти структуры мозга сопоставляют вновь поступившую информацию с уже накопившимся жизненным опытом, т. е. с памятью. В настоящее время довольно распространенным эмоциональным нарушением, связанным с патологическими функциональными изменениями в структурах лимбической системы, является состояние тревоги, которое проявляется в двигательных и вегетативных нарушениях, возникновение чувства страха перед реальной или вымышленной опасностью. Гиппокамп – одна из основных структур лимбической системы – расположен в глубине височных долей мозга. Он образует комплекс стереотипно повторяющихся взаимосвязанных микросетей или модулей, позволяющих циркулировать информации в данной структуре при обучении, т. е. гиппокамп имеет прямое отношение к памяти. Повреждение гиппокампа приводит к ретроантероградной амнезии или нарушению памяти на события, близкие к моменту повреждения, снижению эмоциональности, инициативности. Гиппокамп участвует в ориентировочном рефлексе, реакции настороженности, повышении внимания. Он отвечает за эмоциональное сопровождение страха, агрессии, голода, жажды. В общей регуляции поведения человека и животного большое значение имеет связь между лимбической и моноаминергической системами мозга. К последним относятся дофаминергические, норадренергические и серотонинергические системы. Они начинаются в стволе и иннервируют различные отделы мозга, в том числе и некоторые структуры лимбической системы. Так, норадренергические нейроны посылают свои аксоны из голубого пятна, где они находятся в большом количестве, в миндалину, гиппокамп, поясную извилину, энторинальную кору. Дофаминергические нейроны помимо черной субстанции и базальных ядер иннервируют миндалину, перегородку и обонятельный бугорок, лобные доли, поясную извилину и энторинальную область коры. Серотонинергические нейроны располагаются в основном в срединных и околосрединных ядрах (ядра срединного шва) продолговатого мозга и в составе медиального пучка переднего мозга иннервируют почти все отделы промежуточного и переднего мозга. Опыты с самораздражением с помощью вживленных электродов или на человеке во время нейрохирургических операций показали, что стимуляция зон иннервации катехоламинергическими нейронами, расположенными в области лимбической системы, приводит к возникновению приятных ощущений. Эти зоны получили название «центры удовольствия». Рядом с ними находятся скопления нейронов, раздражение которых вызывает реакцию избегания, их назвали «центрами неудовольствия». Многиепсихические расстройства связывают с моноаминергическими системами. За последние десятилетия для лечения нарушений деятельности лимбической системы разработаны психотропные препараты, влияющие на моноаминергические системы и опосредованно – на функции лимбической системы. К ним относятся транквилизаторы бензодиазепинового ряда (седуксен, элениум и др.), снимающие состояние тревоги, антидепрессанты (имизин), нейролептики (аминозин, галоперидол и др.).Базальные ганглии
Базальные ганглии, или подкорковые ядра, относятся к структурам переднего мозга и включают в себя полосатое тело, или неостриатум (хвостатое ядро и скорлупа), палеостриатум (бледный шар) и ограду. Эта структура мозга играет главную роль в процессе перехода от замысла (фазы подготовки) движения к выбранной программе действия (фазе выполнения движения). Базальные ганглии образуют многочисленные связи как между структурами, входящими в их состав, так и другими отделами мозга. Эти связи представлены в виде параллельных функциональных петель, связывающих кору больших полушарий (двигательную, соматосенсорную и лобную) с таламусом. Информация поступает из вышеперечисленных зон коры, проходит через базальные ядра (хвостатое ядро и скорлупу) и черное вещество в двигательные ядра таламуса, оттуда снова возвращается в эти же зоны коры – это скелетомоторная петля. Одна из таких петель управляет движениями лица и рта, контролирует такие параметры движения, как сила, амплитуда и направление. Другая петля – глазодвигательная (окуломоторная) специализируется на регуляции движения глаз. Предполагается, что медиатором, возбуждающим кортикостриарные нейроны, является аминокислота – глутамат, а между базальными ганглиями и таламусом существуют в основном тормозные пути и их медиатором является ГАМК. Так, между хвостатым ядром и бледным шаром имеются тормозные взаимовлияния. Хвостатое ядро и скорлупа связаны также со структурами, не входящими в эти петли: черной субстанцией, красным ядром, мозжечком, мотонейронами спинного мозга. Некоторые из этих структур, например черная субстанция, оказывают модулирующее влияние на функцию хвостатого ядра. В черной субстанции продуцируется дофамин, который транспортируется к нейронам хвостатого ядра и там накапливается. Высвобождаясь в хвостатом ядре, дофамин модулирует глютаматергическую кортикостриарную передачу информации, вызывая или ее облегчение, или торможение. Полосатое тело (хвостатое ядро и скорлупа) принимают участие в организации и регуляции движений и обеспечении перехода одного вида движения в другое. Раздражение хвостатого ядра, с одной стороны, тормозит активность коры, подкорки, безусловные рефлексы (пищевой, оборонительный и др.) и выработку условных рефлексов. При поражении полосатого тела наблюдается ретроантероградная амнезия – выпадение памяти на события, предшествующие травме. Стимуляция хвостатого ядра тормозит восприятие зрительной, слуховой и других видов сенсорной информации. С другой стороны, хвостатое ядро оказывает возбуждающее действие. Так, при его поражении наблюдается ригидность мышц (повышение мышечного тонуса). Двустороннее повреждение полосатого тела побуждает к стремлению движения вперед, одностороннее – приводит к манежным движениям. Скорлупа выполняет специфическую функцию: она отвечает за организацию пищевого поведения. При ее поражении наблюдаются трофические нарушения кожи, а ее раздражение вызывает слюноотделение и изменение дыхания. Функции бледного шара заключаются в провоцировании ориентировочной реакции, движения конечностей, пищевого поведения (жевание, глотание). После разрушения бледного шара возникают гипомимия (маскообразное лицо), гиподинамия, эмоциональная тупость, тремор головы, конечностей при движении, монотонная речь. При повреждениях бледного шара могут появиться подергивания отдельных мышц лица и туловища, нарушается синергизм движения конечностей при ходьбе. Функции ограды мало изучены. Она имеет двусторонние связи с лобной, затылочной, височной корой, обонятельной луковицей, таламусом и другими базальными ядрами. Ограда оказывает облегчающее влияние на зрительные, слуховые и соматические раздражения. Атрофия ограды приводит к полной потере способности больного говорить, а ее раздражение вызывает моторные реакции со стороны пищеварительного тракта (жевание, глотание, рвотные движения), ориентировочную реакцию. Таким образом, симптомы, связанные с нарушением двигательных функций при поражении базальных ганглиев, можно разделить на гипофункциональные, или недостаточность, и гиперфункциональные, или избыточность. К первым относят акинезию (отсутствие движений), ко вторым – ригидность (повышение мышечного тонуса), баллизм (крупноразмашистый гиперкинез конечностей), атетоз («червеобразные»движения), хорею (быстрые подергивания), тремор (дрожание). Поражение базальных ганглиев приводит к возникновению болезни Паркинсона, имеющей целый ряд симптомов, из которых главными являются ригидность, тремор и акинезия. Усилены тонические рефлексы растяжения, наблюдается восковая ригидность, сильное дрожание пальцев, губ и других частей тела. Больному трудно начать и закончить движения, лицо его маскообразно, нарушена координация движений верхних и нижних конечностей во время ходьбы, он идет мелкими шажками, согнувшись вперед. При болезни Паркинсона нарушается планирование движений. Это заболевание связано с дегенерацией дофаминергических нейронов черного вещества, в результате в стриатуме резко падает содержание дофамина и происходит растормаживание холинергических нейронов. Поэтому лечение этого заболевания оказалось эффективным благодаря введению предшественника дофамина – L-дофа, так как сам дофамин не проходит через гематоэнцефалический барьер.Хорея – наследственное дегенеративное заболевание базальных ганглиев, сопровождающееся уменьшением количества нейронов стриатума и прежде всего синтезирующих ГАМК – стриопаллидарных и стрионигральных нейронов, а также холинергических клеток базальных ганглиев. Отсутствие стрионигрального торможения приводит к гиперактивности дофаминергических клеток и возникновению характерных для хореи непроизвольных судорожных подергиваний.
Ретикулярная формация
Термин «ретикулярная формация» (англ. ret – сеть) был введен впервые Дейтерсом более 100 лет назад. Ретикулярная формация (РФ) располагается в центральной части мозгового ствола, заходя ростральным концом в таламус, а каудальным – в спинной мозг. Благодаря наличию сетевых связей почти со всеми структурами центральной нервной системы она получила название ретикулярной, или сетевой, формации. Различные по форме и величине нейроны РФ имеют длинные дендриты и короткий аксон, хотя встречаются гигантские нейроны с длинными аксонами, образующими, например, руброспинальный и ретикулоспинальный тракты. На одной нервной клетке может заканчиваться до 40 000 синапсов, что указывает на широкие межнейрональные связи в пределах РФ. В ней был выделен целый ряд ядер и ядерных групп, отличающихся как в структурном отношении, так и выполняемыми ими функциями. Ретикулярная формация образует многочисленные как афферентные пути: спиноретикулярный, церебеллоретикулярный, корково-подкорково-ретикулярный (от коры, базальных ганглиев, гипоталамуса), от структур каждого уровня ствола мозга (от среднего мозга, варолиева моста, продолговатого мозга), так и эфферентные: нисходящие ретикулоспинальные, ретикулокорково-подкорковые, ретикуломозжечковые, а также пути к другим структурам ствола мозга. Ретикулярная формация оказывает генерализованное, тонизирующее, активирующее влияние на передние отделы головного мозга и кору больших полушарий (восходящая активирующая система РФ) и нисходящее, контролирующее деятельность спинного.мозга (нисходящая ретикулоспинальная система), которое может быть как облегчающим на многие функции организма, так и тормозным. Одним из видов тормозного влияния РФ на рефлекторную деятельность спинного мозга является сеченовское торможение, заключающееся в угнетении спинальных рефлексов при раздражении таламической ретикулярной формации кристалликом соли. Г. Мэгун показал, что локальное электрическое раздражение гигантоклеточного ядра РФ продолговатого мозга вызывает торможение сгибательного и разгибательного рефлексов спинного мозга, а на мотонейроне возникает длительный ТПСП и постсинаптическое торможение по типу гиперполяризации. Тормозные влияния на сгибательные рефлексы оказывает преимущественно медиальная ретикулярная формация продолговатого мозга, а облегчающие – латеральные зоны РФ моста. Ретикулярная формация принимает участие в реализации многих функций организма. Так, РФ контролирует двигательную активность, постуральный тонус и фазные движения. В 1944 г. в США во время эпидемии полиомиелита – заболевания, нарушающего двигательную активность, основные структурные изменения были обнаружены в ретикулярной формации. Это навело американского ученого Г. Мэгуна на мысль об участии РФ в моторной активности. Основными ее структурами, отвечающими за этот вид деятельности, являются ядро Дейтерса продолговатого мозга и красное ядро среднего мозга. Ядро Дейтерса поддерживает тонус альфа- и гамма-мотонейронов спинного мозга, иннервирующих мышцы-разгибатели, и тормозит альфа- и гамма-мотонейроны мышц-сгибателей. Красное ядро, напротив, тонизирует альфа- и гамма-мотонейроны мышц-сгибателей и тормозит альфа- и гаммамотонейроны мышц-разгибателей. Красное ядро оказывает тормозное влияние на ядро Дейтерса, поддерживая равномерный тонус мышц-разгибателей. Повреждения или перерезка мозга между средним и продолговатым приводит к снятию тормозных влияний со стороны красного ядра на ядро Дейтерса, а значит, и на тонус мышц-разгибателей, который начинает преобладать над тонусом мышц-сгибателей и возникает децеребрационная ригидность или повышенный тонус мышц, проявляющийся в сильном сопротивлении растяжению. Такое животное имеет характерную позу тела: запрокинута голова, вытянуты передние и задние конечности. Поставленное на ноги, оно при малейшем толчке падает, так как отсутствует тонкая регуляция позы тела. Раздражение ретикулярной формации вызывает тремор, спастический тонус. РФ среднего мозга играет роль в координации сокращений глазных мышц. Получив информацию от верхних бугров четверохолмия, мозжечка, вестибулярных ядер, зрительных областей коры головного мозга, РФ ее интегрирует, что приводит к рефлекторным изменениям работы глазодвигательного аппарата, особенно при внезапном появлении движущихся объектов, изменении положения головы и глаз. Ретикулярная формация регулирует вегетативные функции, в реализации которых принимают участие так называемые стартовые нейроны РФ, запускающие процесс возбуждения внутри определенной группы нейронов, отвечающих за дыхательные и сосудодвигательные функции. В РФ продолговатого мозга расположены два ядра, одно из них отвечает за вдох, другое – за выдох. Их деятельность контролируется пневмотаксическим центром РФ варолиева моста. Раздражением этих участков РФ можно воспроизвести различные дыхательные акты. Сосудодвигательный центр расположен в ромбовидной ямке дна четвертого желудочка, входящего в состав РФ. При электрораздражении определенных точек варолиева моста и продолговатого мозга возникают сосудодвигательные реакции. Ретикулярная формация связана со всеми отделами коры мозга с помощью диффузной неспецифической проекционной афферентной системы, которая, в отличие от специфической, проводит возникшее на периферии возбуждение к коре больших полушарий медленно через последовательно связанные многонейронные системы. РФ оказывает активирующее восходящее влияние на кору больших полушарий. Раздражение РФ вызывает «реакцию пробуждения», а на электроэнцефалограмме – десинхронизацию альфа-ритма и ориентировочный рефлекс. Перерезка головного мозга ниже РФ вызывает картину бодрствования, выше – сна. РФ регулирует цикл «сон-бодрствование». Ретикулярная формация оказывает влияние на сенсорные системы мозга: на остроту слуха, зрения, обонятельные ощущения. Так, повреждение РФ и барбитуровый наркоз приводят к усилению сенсорных импульсов, которые в норме находятся под тормозным, регулирующим влиянием РФ. Восприятие различных ощущений при сосредоточении внимания на каком-либо другом ощущении, привыкание к повторяющимся раздражителям также объясняется ретикулярными влияниями. В ретикулярной формации продолговатого, среднего мозга и таламуса имеются нейроны, реагирующие на болевые раздражения от мышц и внутренних органов, при этом создается ощущение тупой боли.Кора больших полушарий
Кора больших полушарий – наиболее молодой в филогенетическом отношении отдел мозга, по своим структурным и функциональным особенностям отличается от других частей центральной нервной системы. Являясь ее высшим отделом на основе безусловных и условных рефлексов, кора отвечает за совершенную организацию поведения животного и человека. Она представляет собой слой серого вещества толщиной 1,3 – 4,5 мм. Благодаря складкам, образующим извилины и борозды мозга, поверхность коры составляет 2200 см2. В ее состав входит более 10 млрд нейронов и еще больше глиальных клеток. Филогенетически кору больших полушарий делят на древнюю (архикортекс), старую (палеокортекс) и новую (неокортекс). К архикортексу относят обонятельные луковицы, обонятельные тракты, расположенные на нижней поверхности лобной доли, обонятельные бугорки с обонятельными центрами. Палеокортекс включает поясную извилину, гиппокамп и миндалину. Все остальные области относят к неокортексу, который особенно хорошо развит у млекопитающих и человека. В коре различают три основных типа нейронов: пирамидные, звездчатые, веретенообразные. Пирамидные клетки, имеющие длинные аксоны, заходящие в другие отделы мозга и дендриты, покрытые большим количеством шипиков – синаптических структур, благодаря которым нервная клетка контактирует с другими нервными элементами. Шипики крайне чувствительны к различным факторам: гипоксии, асфиксии, влиянию токсических веществ, под действием которых они атрофируются, и при этом нарушаются функциональные связи. Звездчатые клетки имеют короткие дендриты и аксон, их функция сводится к обеспечению связей между нейронами самой коры. Веретенообразные клетки образуют вертикальные или горизонтальные связи нейронов разных слоев коры. Неокортекс имеет шестислойное строение. Первый слой – молекулярный, ИЛИ плексиформный, содержит мало клеток, а в основном нервные волокна, образованные восходящими дендритами пирамидных нейронов и волокнами неспецифических ядер зрительного бугра, регулирующих уровень возбудимости коры больших полушарий. Второй слой – наружный зернистый, ИЛИ наружный гранулярный, состоит из звездчатых клеток, ответственных за циркуляцию возбуждения в коре, т. е. кратковременную память. Третий слой – наружный пирамидный состоит из малых пирамидных клеток и совместно со вторым слоем обеспечивает «меж-корковую» передачу информации. Четвертый слой – внутренний зернистый содержит звездчатые клетки, на которых заканчиваются специфические таламокортикальные афферентные пути от анализаторов. Пятый слой – внутренний слой крупных пирамидных клеток, аксоны которых спускаются в продолговатый и спинной мозг. В моторной коре в этом слое находятся гигантские пирамидные клетки Беца, апикальные дендриты которых достигают поверхностных слоев, а самые длинные аксоны образуют пирамидный тракт, достигающий спинного мозга. Шестой слой – полиморфные клетки веретенообразной и треугольной формы, образующие кортикоталамические пути. Распределение нейронов различается в определенных областях коры. Это позволило Бродману выделить 53 цитоархитектонических поля. Кроме того, по функциональным признакам нейроны коры объединяются в специальные модули, «колонки», расположенные вертикально. Каждая колонка отвечает за определенный вид информации. Она связана с соседними колонками реципрокными отношениями – возбуждение одной приводит к торможению соседних. Так, например, каждая колонка связана с определенным суставом и от нее идет команда к мышцам. Возбуждающим медиатором пирамидных клеток может быть или глутамат или аспартат, тормозным – ГАМК. Часть нейронов выделяет моноамины: норадреналин и дофамин, другая – ацетилхолин.Локализация функций в коре больших полушарий
В настоящее время принято делить кору на сенсорные, двигательные, или моторные, и ассоциативные зоны. Такое деление было получено благодаря экспериментам на животных с удалениями различных участков коры, наблюдениями за больными, имеющими патологический очаг в мозге, а также с помощью прямого электрического раздражения коры и периферических структур с регистрацией электрической активности в коре. В сенсорных зонах представлены корковые концы всех анализаторов. Для зрительного он располагается в затылочной доле мозга (поля 17, 18, 19). В поле 17 заканчивается центральный зрительный путь, информирующий о наличии и интенсивности зрительного сигнала. Поля 18 и 19 анализируют цвет, форму, размеры и качество предмета. При поражении поля 18 больной видит, но не узнает предмета и не различает его цвета (зрительная агнозия). Корковый конец слухового анализатора локализуется в височной доле коры (извилина Гешля), поля 41,42,22. Они участвуют в восприятии и анализе слуховых раздражений, организации слухового контроля речи. Больной, имеющий повреждение поля 22, теряет способность понимать значение произносимых слов. В височной доле располагается также корковый конец вестибулярного анализатора. Кожный анализатор, а также болевая и температурная чувствительность проецируются на заднюю центральную извилину, в верхней части которой представлены нижние конечности, в средней – туловище, в нижней – руки и голова. В коре теменной доли заканчиваются пути соматической чувствительности, относящиеся к речевой функции, связанной с оценкой воздействия на рецепторы кожи, веса и свойств поверхности, формы и размера предмета. Корковый конец обонятельного и вкусового анализаторов расположен в гиппокампальной извилине. При раздражении этой области возникают обонятельные галлюцинации, а ее повреждение приводит к аносмии (потере способности ощущать запахи). Моторные зоны находятся в лобных долях в области передней центральной извилины мозга, раздражение которой вызывает двигательную реакцию. Кора прецентральной извилины (поле 4) представляет первичную двигательную зону. В пятом слое этого поля находятся очень крупные пирамидные клетки (гигантские клетки Беца). Лицо проецируется на нижнюю треть прецентральной извилины, рука занимает ее среднюю треть, туловище и таз – верхнюю треть извилины. Двигательная зона коры для нижних конечностей находится на медиальной поверхности полушария в области передней части парацентральной дольки. Премоторная область коры (поле 6) располагается кпереди от первичной двигательной зоны. Поле б называют вторичной моторной областью. Ее раздражение вызывает вращение туловища п глаз с подниманием контралатеральной руки. Аналогичные движения наблюдаются у больных во время приступа эпилепсии, если эпилептический очаг локализуется в этой области. Недавно доказана ведущая роль поля б в реализации двигательных функций. Поражение поля б у человека вызывает резкое ограничение двигательной активности, с трудом выполняются сложные комплексы движений, страдает спонтанная речь. К полю б примыкает поле 8 (лобное глазодвигательное), раздражение которого сопровождается поворотом головы и глаз в сторону, противоположную раздражаемой. Стимуляция различных участков двигательной коры вызывает сокращение соответствующих мышц на противоположной стороне. Передние отделы лобной коры связывают с «творческим» мышлением. С клинической и функциональной точек зрения интересной областью является нижняя лобная извилина (поле 44). В левом полушарии она связана с организацией двигательных механизмов речи. Раздражение этой области может вызвать вокализацию, но не членораздельную речь, а также прекращение речи, если человек говорил. Поражение этой области приводит к моторной афазии – больной понимает речь, но сам говорить не может. К ассоциативной коре относят теменно-височно-затылочную, префронтальную и лимбическую области. Она занимает около 80% всей поверхности коры больших полушарий. Ее нейроны обладают мультисенсорными функциями. В ассоциативной коре происходит интеграция различной сенсорной информации и формируется программа целенаправленного поведения, ассоциативная кора окружает каждую проекционную зону, обеспечивая взаимосвязь, например, между сенсорными и моторными областями коры. Нейроны, расположенные в этих областях, обладают полисенсорностью, т. е. способностью отвечать как на сенсорную, так и моторную информацию. Теменная ассоциативная область коры больших полушарий участвует в формировании субъективного представления об окружающем пространстве, о нашем теле. Височная область коры участвует в речевой функции посредством слухового контроля речи. При поражении слухового центра речи больной может говорить, правильно излагать свои мысли, но не понимает чужой речи (сенсорная слуховая афазия). Эта область коры играет определенную роль в оценке пространства. Поражение зрительного центра речи приводит к потере способности читать и писать. С височной корой связывают функцию памяти и сновидений. Лобные ассоциативные поля имеют прямое отношение к лимбическим отделам мозга, они принимают участие в формировании программы сложных поведенческих актов в ответ на воздействие внешней среды на основе сенсорных сигналов всех модальностей. Особенностью ассоциативной коры является пластичность нейронов, способных к перестройкам в зависимости от поступающей информации. После операции удаления какой-либо области коры в раннем детстве утраченные функции этой области полностью восстанавливаются. Кора больших полушарий способна, в отличие от нижележащих структур мозга, длительно, в течение всей жизни сохранять следы поступившей информации, т. е. участвовать в механизмах долговременной памяти. Кора больших полушарий – регулятор вегетативных функций организма («кортиколизация функций»). В ней представлены все безусловные рефлексы, а также внутренние органы. Без коры невозможно выработать условные рефлексы на внутренние органы. При раздражении интерорецепторов методом вызванных потенциалов, электростимуляции и разрушения определенных участков коры доказано ее влияние на деятельность различных органов. Так, разрушение поясной извилины изменяет акт дыхания, функции сердечно-сосудистой системы, желудочно-кишечного тракта. Кора тормозит эмоции – «умейте властвовать собой».Электрическая активность коры головного мозга
Мембранный потенциал пирамидных клеток составляет от 50 до 80 мкВ, потенциал – действия 60–100 мкВ. Частота ПД – около 100 Гц. Он возникает в аксонном холмике нейронов коры, регистрируется с помощью микроэлектродной техники. При помещении электрода на поверхность нейрона можно записать его спонтанную, ритмическую активность. С поверхности обнаженной коры между двумя электродами регистрируется суммарная электрическая активность коры и под-корковых структур, которая называется электрокортикограммой (ЭКоГ). Эту активность можно записать и с интактной кожи головы – это электроэнцефалограмма (ЭЭГ). При этом можно использовать или два активных электрода, помещенных на коже головы (биполярное отведение), или один активный, другой – индифферентный (на мочке уха) (монополярное отведение).Ритмы электроэнцефалограммы
При закрытых глазах, но не во время сна регистрируется аль-фа-ритм, особенно четко в затылочной области, его частота 8 -13 Гц, амплитуда около 50 мкВ. Действие раздражителя (например, звука), переход к какой-либо деятельности при открытых глазах приводит к переходу альфа-ритма к бета-ритму с большей частотой (14 – 30 Гц) и амплитудой 25 мкВ. Это называется реакцией десинхронизации ЭЭГ. Переход от бодрствования ко сну сопровождается возникновением тета-ритма (частота 4 – 7 Гц). При глубоком сне регистрируется дельта-ритм с частотой 0,5 – 3,5 Гц. Амплитуда этих медленных волн составляет 100 – 300 мкВ. Метод ЭЭГ широко используется в клинике и психофизиологии для изучения механизмов обработки информации и управления поведением человека, для выявления первых признаков эпилепсии, диффузных поражений головного мозга, скрытых травм и эндогенной интоксикации, опухолей мозга. Психотропные препараты также влияют на ЭЭГ. Метод электроэнцефалографии используют для констатации «клинической» смерти («изоэлектрическая» или «плоская» ЭЭГ), а также для определения «предела реанимации» при ишемии мозга, который для коры составляет всего 3 – 8 мин. ЭКоГ и ЭЭГ отражают постсинаптическую активность нейронов коры, но не их ПД, и активность глиальных клеток. Колебания потенциала, возникающие в коре и подкорковых структурах в ответ на раздражение рецепторов, периферических нервов, сенсорных трактов и ядер, называются вызванными потенциалами (ВП). Они могут иметь короткий латентный период (6 – 8 мс), первое положительное отклонение и возникать в ограниченном участке коры (фокусе максимальной активности – ФМА). Эти потенциалы называются первичными ответами (ПО). Второй вид потенциала – вторичный вызванный потенциал (ВВП) имеет более длительный латентный период и может начинаться с отрицательного отклонения, охватывает обширную область коры. Регистрация ВП может служить для клинической диагностики сохранности периферических сенсорных и подкорковых путей (например, слуховых, зрительных).Гематоэнцефалический барьер
Термин «гематоэнцефалический барьер» (от гр. haima – кровь, encephalon – мозг) был предложен Л. С. Штерн и Р. Готье в 1921 г. Гематоэнцефалический барьер (ГЭБ) принадлежит к числу внутренних, или гистогематических, барьеров (гематоофтальмического, легочного, перикардиального, перитонеального и других), которые отгораживают непосредственную питательную среду отдельных органов от универсальной внутренней среды – крови. Было показано, что если ввести витальную краску – трипановый синий в кровеносное русло, то при интенсивном окрашивании всех органов не окрашенной остается только центральная нервная система. Краска была обнаружена только в эпителиальных клетках сосудистых сплетений. Вещества оказываются эффективными лишь при введении их непосредственно в цереброспинальную жидкость. Гематоэнцефалический барьер – это комплексный физиоло-гический механизм, находящийся в центральной нервной системе на границе между кровью и нервной тканью и регулирующий поступление из крови в цереброспинальную жидкость и нервную ткань циркулирующих в крови веществ.Функции гематоэнцефалического барьера
Гематоэнцефалический барьер выполняет ряд функций. Защитная заключается в задержке доступа из крови в нервную ткань различных веществ, могущих оказать повреждающее действие на мозг. Регуляторная функция заключается в поддержании состава и постоянства цереброспинальной жидкости. Даже при изменении состава крови константы цереброспинальной жидкости не изменяются. ГЭБ работает как селективный фильтр, пропускающий в цереброспинальную жидкость одни вещества и не пропускающий другие, которые могут циркулировать в крови, но чужды мозговой ткани. Так, не проходят через ГЭБ адреналин, норадреналин, ацетилхолин, дофамин, серотонин, гамма-аминомасляная кислота (ГАМК), пенициллин, стрептомицин. Билирубин всегда находится в крови, но никогда, даже при желтухе, он не проходит в мозг, оставляя неокрашенной лишь нервную ткань. Поэтому трудно получить эффективную концентрацию какого-либо лекарственного препарата, чтобы оно достигло паренхимы мозга. Проходят через ГЭБ морфий, атропин, бром, стрихнин, кофеин, эфир, уретан, алкоголь и гамма-оксимасляная кислота (ГОМК). При лечении, например, туберкулезного менингита стрептомицин вводят непосредственно в цереброспинальную жидкость, минуя барьер с помощью люмбальной пункции. Необходимо учесть необычность действия многих веществ, введенных непосредственно в цереброспинальную жидкость. Трипановый синий при введении в цереброспинальную жидкость вызывает судороги и смерть, аналогичное действие оказывает желчь. Ацетилхолин, введенный непосредственно в мозг, действует как адреномиметик, а адреналин, наоборот, – как холиномиметик: артериальное давление понижается, возникает брадикардия, температура тела вначале снижается, а потом повышается. Он вызывает наркотический сон, заторможенность и аналгезию. Ионы К+ выступают в качестве симпатомиметика, а Са2+ – парасимпатомиметика. Лобелии – рефлекторный стимулятор дыхания, проникая через ГЭБ, вызывает ряд побочных реакций (головокружение, рвоту, судороги). Инсулин при внутримышечных инъекциях снижает содержание сахара крови, а при непосредственном введении в цереброспинальную жидкость – повышает. Защитная функция ГЭБ менее развита к моменту рождения и в раннем возрасте, формируясь в постнатальном периоде. Поэтому у ребенка при различных заболеваниях часто появляются судороги и значительно повышается температура тела, что указывает на легкое проникновение в цереброспинальную жидкость токсических веществ, у взрослого человека такие явления не наблюдаются.Факторы, повышающие проницаемость гематоэнцефалического барьера
Повысить проницаемость гематоэнцефалического барьера могут следующие факторы: 1. Нарушение анатомической структуры мозга. 2. Введение некоторых лекарственных препаратов (например, антибиотиков) вместе с гиалуронидазой или гистамином. 3. Для ускорения проникновения через ГЭБ антибиотиков можно использовать их аэрозольную ингаляцию, а не внутримышечные инъекции. 4. Длительная бессонница и голодание, усиленная мышечная работа (переутомление). 5. Низкая (34°С) или высокая температура тела (42 -43° С). 6. Алкалоз (рН до 7,7) и ацидоз (рН до 6,6). 7. Введение гипери гипотонических растворов в кровь. 8. Наркоз (эфир, уретан, хлоралгидрат) нарушает проницаемость ГЭБ для сахара, поэтому после наркоза его много в цереброспинальной жидкости.Особенности морфологического строения гематоэнцефалического барьера
Капилляры мозга отличаются тем, что эндотелиальные клетки не обладают ни порами, ни фенестрами. Соседние клетки черепицеобразно накладываются одна на другую. В области стыков клеток находятся замыкательные пластинки. Базальная мембрана имеет трехслойное строение и содержит мало перицитов. Главное отличие этой структуры – наличие глиальных элементов, расположенных между кровеносным сосудом и нейроном. Отростки астроцитов формируют своеобразный футляр вокруг капилляра, это исключает проникновение веществ в мозговую ткань, минуя глиальные элементы. Имеются перинейрональные глиоциты, находящиеся в тесном контакте с нейронами. В состав ГЭБ входит внеклеточное пространство, заполненное основным аморфным веществом углеводно-белковой природы (мукополисахариды и мукопротеины).Цереброспинальная жидкость
Цереброспинальная жидкость (ЦСЖ) образуется сосудистым сплетением, элементами мягкой мозговой оболочки, эпендимой желудочков, клетками паренхимы мозга, в ее продукции принимают участие нейроны и глия. Ток ЦСЖ происходит следующим образом: из желудочков мозга (боковые желудочки, III желудочек) жидкость через отверстие Мажанди и Лушка поступает в IV желудочек и в подмозжечковые цистерны, затем в цистерны основания мозга на его выпуклую поверхность, подпаутинное пространство и в центральный канал спинного мозга, после чего через венозный синус она оттекает в кровь. Количество ЦСЖ составляет от 100 до 150 мл, суточное количество может достигать 600 мл, при травмах черепа – до 1000 мл. Состав ЦСЖ обновляется до 5 – 10 раз в сутки. Давление ЦСЖ в горизонтальном положении – 100 – 200 мм вод. ст. Оно может увеличиваться при нарушении ГЭБ, при опухолях, отеке мозга и заболеваниях сердечно-сосудистой системы. Удельный вес ЦСЖ составляет от 1001 до 1012, рН – 7,35 – 7,8. Количество воды – 90%, сухой остаток – 10%. Из органических веществ большое значение имеет белок – 15–30 мг%. В клинике используется коэффициент Кафки – отношение между глобулинами и альбуминами. В норме он равен 0,2 – 0,3, но может изменяться при менингитах, прогрессивном параличе и других заболеваниях мозга, остаточный азот составляет 12–18 мг%, глюкоза – 38–70 мг%, холестерин – 0,1–0,4мг%. Кроме того, в ЦСЖ содержатся аминокислоты, мочевина, мочевая кислота. Из неорганических веществ диагностическое значение в клинике имеют хлориды (норма 720 -740 мг%), их количество снижается при менингитах (до 600 мг%) и при алкалозе (до 240 мг%). В ЦСЖ содержатся железо, калий, кальций, магний и др. В ЦСЖ могут находиться некоторые гормоны: АКТГ, гонадотропин, меланофорный гормон, окситоцин, вазопрессин и медиатор ацетилхолин. Нормальное содержание форменных элементов (в основном лимфоциты) вликворе составляет от 0 до 5 в 1 мм3, свыше 10 является патологией.Фармакологические препараты, регулирующие функцию центральной нервной системы
Фармакологические средства позволяют вносить коррекцию в возбудительный и тормозной процессы, происходящие в центральной нервной системе, влияя на деятельность как всего мозга и его частей, так и отдельной нервной клетки. К препаратам общего угнетающего действия относятся средства для наркоза: ингаляционного (эфир, закись азота и др.), неингаляционного (гексенал, тиопентал-натрий и др.), этиловый спирт, а также снотворные средства (барбамил, этаминал-натрий и др.). В настоящее время в качестве снотворных средств используют производные бензодиазепина (неозепам, флунитразепам и др.), которые связываются со специфическими бензодиазепиновыми рецепторами (Бз-1 и Бз-2) и, активируя ГАМК-рецепторы, подавляют функциональную активность центральной нервной системы и особенно клеток ретикулярной формации. Механизм действия общих анестетиков и наркотических средств основан на блокаде межнейронной синаптической передачи возбуждения во всех звеньях рефлекторной дуги. Подавление синаптической передачи сопровождается выключением сознания, потерей всех видов чувствительности, в том числе и болевой, торможением всей рефлекторной деятельности и снижением тонуса скелетной мускулатуры. К средствам, подавляющим возбудимость центральной нервной системы, относятся также противоэпилептические, противосудорожные препараты (гексамедин, дифенин, клоназепам и др.). Стимулирующее действие на центральную нервную систему оказывают препараты, влияющие преимущественно на спинной мозг (стрихнин, секуринин). Они блокируют тормозной медиатор (глицин) вставочных нейронов (клеток Реншоу) спинного мозга, облегчая проведение нервных импульсов, усиливают возбудительный процесс. Кроме того, имеется другая группа препаратов – аналептики, избирательно возбуждающие сосудодвигательный (камфора, коразол, кордиамин) и дыхательный (цититон, лобелии) центры продолговатого мозга.Глава 4. Вегетативная (автономная) нервная система
Еще в начале XIX века французский физиолог М. Биша разделил функции животного организма на животные (анимальные, соматические) и вегетативные (растительные). В соответствии с этим и нервная система была разделена на соматическую и вегетативную (от лат. vegetativus – растительный). Согласно международной анатомической номенклатуре вегетативная (висцеральная, растительная) нервная система называется автономной нервной системой. Вегетативная и соматическая нервные системы действуют в организме содружественно. Их нервные центры тесно связаны друг с другом. В то же время между этими двумя системами существует много различий, особенно это касается их периферических отделов.Различия между вегетативной и соматической нервными системами
Вегетативная нервная система (автономная) – непроизвольная, т. е. не контролируется сознанием. Соматическая же нервная система является произвольной. Вегетативная нервная система иннервирует внутренние органы, железы внешней и внутренней секреции, кровеносные и лимфатические сосуды, гладкую и скелетную мускулатуру, а также центральную нервную систему, поддерживает постоянство внутренней среды организма. Соматическая нервная система иннервирует поперечно-полосатую мускулатуру. Рефлекторная дуга как соматического, так и вегетативного рефлекса состоит из трех звеньев: афферентного (сенсорного, чувствительного), вставочного (ассоциативного) и эффекторного (исполнительного). Афферентное звено может быть общим для соматической и вегетативной рефлекторных дуг. Однако в вегетативной нервной системе эффекторный нейрон располагается за пределами спинного или головного мозга и находится в ганглиях (рис.10). Ганглии могут располагаться около позвоночника (паравертебральные), в нервных сплетениях вблизи внутренних органов (превертебральные) или в стенках внутренних органов (интрамуральные). В соматической нервной системе эффекторные нейроны находятся в ЦНС (серое вещество спинного мозга). Перерезка передних корешков спинного мозга приводит к полному перерождению всех эфферентных соматических волокон и не влияет на вегетативные, так как их эффекторный нейрон находится в периферических ганглиях. В этом и состоит автономия данного отдела ЦНС.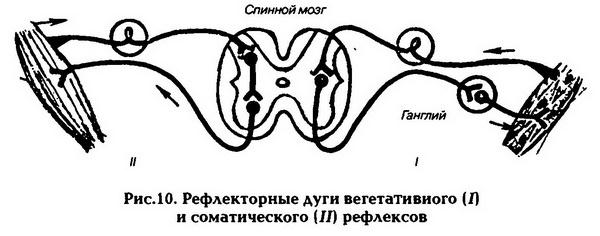 Волокна вегетативной нервной системы выходят из ЦНС только на определенных участках головного мозга, грудопоясничного и крестцового отделов спинного мозга. Во внутриорганном отделе рефлекторные дуги полностью находятся в органе и не имеют выходов из ЦНС. Волокна соматической нервной системы выходят из спинного мозга сегментарно на всем протяжении и перекрывают иннервацией не менее 3 смежных сегментов.
Вегетативные нервные волокна имеют меньший диаметр, чем соматические. Волокна типа В покрыты тонкой миелиновой оболочкой, типа С – лишены ее. Соматические нервные волокна миелинизированы (относятся к типу А). Отсюда и различная скорость проведения нервных импульсов. Если в вегетативных нервах возбуждение распространяется со скоростью от 1–3 до 18–20 м/с, то в соматических нервах – 70–120 м/с. Вегетативные нервные волокна менее возбудимы, чем соматические, и обладают более длительным рефрактерным периодом, большей хронаксией и меньшей лабильностью. Поэтому для их возбуждения необходимо более сильное раздражение, чем для соматических волокон. Аксоны соматических нейронов длинные, на своем протяжении не прерываются. Вегетативные нервные волокна прерываются в ганглиях.
Медиатором соматической нервной системы является только ацетилхолин. В вегетативной нервной системе медиаторную функцию выполняют несколько веществ, главными из которых являются: ацетилхолин, норадреналин, АТФ, аденозгистамин, серотонин.
Волокна вегетативной нервной системы выходят из ЦНС только на определенных участках головного мозга, грудопоясничного и крестцового отделов спинного мозга. Во внутриорганном отделе рефлекторные дуги полностью находятся в органе и не имеют выходов из ЦНС. Волокна соматической нервной системы выходят из спинного мозга сегментарно на всем протяжении и перекрывают иннервацией не менее 3 смежных сегментов.
Вегетативные нервные волокна имеют меньший диаметр, чем соматические. Волокна типа В покрыты тонкой миелиновой оболочкой, типа С – лишены ее. Соматические нервные волокна миелинизированы (относятся к типу А). Отсюда и различная скорость проведения нервных импульсов. Если в вегетативных нервах возбуждение распространяется со скоростью от 1–3 до 18–20 м/с, то в соматических нервах – 70–120 м/с. Вегетативные нервные волокна менее возбудимы, чем соматические, и обладают более длительным рефрактерным периодом, большей хронаксией и меньшей лабильностью. Поэтому для их возбуждения необходимо более сильное раздражение, чем для соматических волокон. Аксоны соматических нейронов длинные, на своем протяжении не прерываются. Вегетативные нервные волокна прерываются в ганглиях.
Медиатором соматической нервной системы является только ацетилхолин. В вегетативной нервной системе медиаторную функцию выполняют несколько веществ, главными из которых являются: ацетилхолин, норадреналин, АТФ, аденозгистамин, серотонин.
Структура и функции вегетативной нервной системы
В вегетативной нервной системе выделяют симпатический и парасимпатический отделы. Эти отделы имеют центральную и периферические части. Центральные структуры расположены в среднем, продолговатом и спинном мозге; периферические представлены ганглиями и нервными волокнами. Многие внутренние органы получают как симпатическую, так и парасимпатическую иннервацию. Влияние этих двух отделов носит антагонистический характер, но этот антагонизм относителен. Имеется много примеров, когда симпатический и парасимпатический отделы действуют синергично (например, и тот и другой увеличивают слюноотделение). Обычно повышение тонуса одного отдела вегетативной нервной системы вызывает усиление активности другого. Многие внутренние органы наряду с симпатической и пара-симпатической иннервациями имеют собственный местный нервный механизм регуляции функций, в значительной степени автономный. Наличие общих черт в структурной и функциональной организации, а также данные онто- и филогенеза позволили выделить в составе вегетативной нервной системы (в периферическом ее отделе) еще и третий отдел – внутриорганный. Ранее к этому отделу относили только интрамуральную систему кишечника, поэтому его называли энтеральным. В настоящее время показано, что подобной автономией обладают и интрамуральные системы других органов. Поэтому был предложен термин «метасимпатический отдел» (А. Д. Ноздрачев), который в последнее время используется в отечественной литературе.Симпатический отдел вегетативной нервной системы
Центры симпатической нервной системы представлены ядрами, расположенными в боковых рогах серого вещества грудного и поясничного отделов спинного мозга (от I грудного до Н-ГУ поясничных сегментов). Аксоны нейронов, составляющих эти ядра, выходят из спинного мозга в составе его передних корешков и в виде белых соединительных ветвей вступают в узлы пограничного симпатического ствола. Эти волокна называются преганглионарными. Здесь большинство волокон переключаются на эффекторный ганглионарный нейрон. Отростки ганглиозных клеток образуют постганглионарные волокна, которые по серой соединительной ветви вновь возвращаются в спинномозговой нерв и достигают иннервируемого органа. Часть преганглионарных волокон, выходящих из ядер спинного мозга, проходит через вертебральные ганглии, не прерываясь, и переключаются на эффекторные нейроны в превертебральных ганглиях. Превертебральные ганглии представлены чревным, верхним и нижним брыжеечными узлами. Два первых узла вместе сотходящими от них ветвями образуют солнечное сплетение. Преганглионарные волокна относятся к типу В (тонкие миелиновые), постганглионарные – к типу С (безмиелиновые). Окончания преганглионарных волокон вырабатывают ацетилхолин, постганглионарных – в основном норадреналин. Исключение составляют постганглионарные волокна, иннервирующие потовые железы, и симпатические нервы, расширяющие сосуды скелетных мышц, в окончаниях которых вырабатывается ацетилхолин, взаимодействующий с М-холинорецепторами. Эти волокна называются симпатическими холинергическими. Надпочечники иннервируются симпатическими нервами, которые не прерываются в ганглиях, т. е. преганглионарными волокнами, в окончаниях которых выделяется ацетилхолин, взаимодействующий с Н-холинорецепторами. Симпатическая нервная система иннервирует все органы и ткани организма, в том числе скелетные мышцы и центральную нервную систему. При возбуждении симпатических нервов усиливается работа сердца (положительные ино-, хроно-, тоно-, дромои батмотропное действия), расслабляется мускулатура бронхов и увеличивается их просвет, снижается моторная и секреторная деятельность желудочно-кишечного тракта, происходит сокращение сфинктеров мочевого и желчного пузыря и расслабление их тел, что приводит к прекращению выделения мочи и желчи, расширяется зрачок. Симпатическая нервная система не только регулирует работу внутренних органов, но и оказывает влияние на обменные процессы, протекающие в скелетных мышцах и в нервной системе. И. П. Павлов первым показал трофическое действие симпатической нервной системы на усиливающем нерве сердца. В лаборатории А. А. Орбели был проведен эксперимент на нервно-мышечном препарате лягушки. Путем раздражения двигательного нерва вызывали сокращения мышцы и доводили ее до степени утомления. Раздражение симпатического нерва восстанавливало работоспособность скелетной мышцы. Повышение работоспособности было результатом увеличения обменных процессов под влиянием симпатических возбуждений. Этот опыт вошел в историю как феномен Орбели – Гинецинского. На основании данного и многих других наблюдений было сформулировано понятие об адаптационно-трофической функции симпатической нервной системы, которая заключается в ее влиянии на интенсивность обменных процессов и приспособление их уровня к условиям существования организма. Симпатическая нервная система отвечает на любой стресс. Ее возбуждение приводит к увеличению активности мозгового вещества надпочечников и выделению адреналина, что вместе образует симпатоадреналовую систему. Симпатический отдел автономной нервной системы – это система тревоги, мобилизации защитных сил и ресурсов организма. Возбуждение симпатической нервной системы приводит к повышению кровяного давления, выходу крови из депо, поступлению в кровь глюкозы, ферментов, повышению метаболизма тканей. Все эти процессы связаны с расходом энергии в организме, т. е. симпатическая нервная система выполняет эрготрофную функцию.Парасимпатический отдел вегетативной нервной системы
Центрами парасимпатического отдела автономной нервной системы являются ядра, находящиеся в среднем мозге (III пара че-репно-мозговых нервов), продолговатом мозге (VII, IX и X пары черепно-мозговых нервов) и крестцовом отделе спинного мозга (ядра тазовых внутренних нервов). От среднего мозга отходят преганглионарные волокна парасимпатических нервов, которые входят в состав глазодвигательного нерва. Из продолговатого мозга выходят преганглионарные волокна, идущие в составе лицевого, языкоглоточного и блуждающих нервов. От крестцового отдела спинного мозга отходят преганглионарные парасимпатические волокна, которые входят в состав тазового нерва. Ганглии пара-симпатической нервной системы располагаются вблизи иннервируемых органов или внутри них. Поэтому преганглионарные волокна парасимпатического отдела длинные, а постганглионарные волокна короткие по сравнению с волокнами симпатического отдела. В окончаниях как преганглионарных, так и большинства постганглионарных волокон вырабатывается ацетилхолин. Пара-симпатические волокна иннервируют, как правило, только определенные части тела, которые имеют также симпатическую, а иногда и внутриорганную иннервацию. Парасимпатическая нервная система не иннервирует скелетные мышцы, головной мозг, гладкие мышцы кровеносных сосудов, за исключением сосудов языка, слюнных желез, половых желез и коронарных артерий, органы чувств и мозговое вещество надпочечников. Постганглионарные парасимпатические волокна иннервируют глазные мышцы, слезные и слюнные железы, мускулатуру и железы пищеварительного тракта, трахею, гортань, легкие, предсердия, выделительные и половые органы. При возбуждении парасимпатических нервов тормозится работа сердца (отрицательные хроно-, ино-, дромои батмотропное действия), повышается тонус гладкой мускулатуры бронхов, в результате чего уменьшается их просвет, сужается зрачок, стимулируются процессы пищеварения (моторика и секреция), обеспечивая тем самым восстановление уровня питательных веществ в организме, происходит опорожнение желчного пузыря, мочевого пузыря, прямой кишки. Действие парасимпатической нервной системы направлено на восстановление и поддержание постоянства состава внутренней среды организма, нарушенного в результате возбуждения симпатической нервной системы. Парасимпатическая нервная система выполняет в организме трофотропную функцию.Внутриорганный отдел (энтеральный, метасимпатический)
К этому отделу относятся интрамуральные системы всех полых висцеральных органов, обладающих собственной автоматической двигательной активностью: сердце, бронхи, мочевой пузырь, пищеварительный тракт, матка, желчный пузырь и желчные пути. Внутриорганный отдел имеет все звенья рефлекторной дуги: афферентный, вставочный и эфферентный нейроны, которые полностью находятся в органе и нервных сплетениях внутренних органов (например, ауэрбаховском и мейснеровском). Этот отдел отличается более строгой автономностью, т. е. независимостью от ЦНС, так как не имеет прямых синаптических контактов с эфферентным звеном соматической рефлекторной дуги. Вставочные и эфферентные нейроны внутриорганной нервной системы имеют контакты с симпатическими и парасимпатическими нервами, а некоторые эфферентные нейроны могут быть общими с постганглионарными нейронами парасимпатической нервной системы. Все это обеспечивает надежность в деятельности органов. Внутриорганный отдел характеризуется наличием собственных сенсорного и медиаторного звеньев. Преганглионарные волокна выделяют ацетилхолин и норадреналин, постганглионарные – АТФ и аденозин, ацетилхолин, норадреналин, серотонин, дофамин, адреналин, гистамин и т. д. Главная роль принадлежит АТФ и аденозину. В сфере управления этого отдела находятся гладкие мышцы, всасывающий и секретирующий эпителий, локальный кровоток, местные эндокринные и иммунные механизмы. Если с помощью ганглиоблокаторов выключить внутриорганную иннервацию, то орган теряет способность к осуществлению координированной ритмической моторной функции. Основная функциональная роль внутриорганного отдела – это осуществление механизмов, обеспечивающих относительное динамическое постоянство внутренней среды и устойчивость основных физиологических функций.Синаптическая передача
В вегетативной нервной системе существует три вида синаптической передачи: химическая, электрическая и смешанная. Основным способом передачи возбуждения является химический посредством медиатора. Нервные клетки вегетативной нервной системы секретируют разные медиаторы: ацетилхолин, норадреналин, дофамин, серотонин и другие биогенные амины, АТФ и аминокислоты и др. В зависимости от того, какой медиатор образуется и выделяется в окончаниях нервных волокон, принято делить их на холинергические, адренергические, пуринергические, серотонинергические и т. д. Под влиянием нервных импульсов и ионов кальция происходит высвобождение медиатора в синаптическую щель и взаимодействие с белками-рецепторами постсинаптической мембраны. Взаимодействие медиатора с белком-рецептором приводит к повышению проницаемости постсинаптической мембраны для определенных ионов. Повышение проницаемости для ионов натрия вызывает деполяризацию постсинаптической мембраны и возбуждение постсинаптической структуры. Увеличение проницаемости для ионов калия и хлора приводит к гиперполяризации постсинаптической мембраны и тормозному эффекту. После того как медиатор выполнил свою функцию, он подвергается обязательной инактивации: разрушается специфическим ферментом, подвергается нейрональному и экстранейрональному захвату. Существует и другой механизм действия медиаторов. В результате взаимодействия со специфическими рецепторами постсинаптической мембраны происходит активация систем вторичных посредников, например, циклического аденозинмонофосфата (цАМФ), что, в конечном итоге, изменяет функциональную активность эффекторной клетки. Кроме постсинаптических рецепторов выделяют пре- и внесинаптические рецепторы. Пресинаптические рецепторы непосредственно на функции органов и тканей не влияют. Они распо-лагаются на пресинаптической мембране и по принципу обратной связи (положительной или отрицательной) регулируют выброс медиатора в синаптическую щель. Внесинаптические рецепторы располагаются вне синаптической зоны и взаимодействуют с биологически активными соединениями межклеточной среды, в том числе и с некоторыми медиаторами (катехоламинами). Название рецепторов зависит от того, с каким медиатором они взаимодействуют: холинорецепторы, адренорецепторы, серотонинорецепторы, пуринорецепторы. Имеются также рецепторы дофамина, пептидов, простагландинов. Локализация и количество любых рецепторов на мембране клетки детерминировано генетическим аппаратом. Однако это количество может меняться в течение жизни. При денервации органов происходит резкое повышение чувствительности к медиаторам. Считают, что это может быть связано с увеличением числа соответствующих рецепторов во внесинаптических областях, а также с уменьшением количества или активности ферментов, расщепляющих данный медиатор. Как правило, каждый медиатор выделяется и осуществляет свою функцию в определенных звеньях рефлекторной дуги.Медиаторы вегетативной нервной системы
Ацетилхолин является первым биологически активным веществом, которое было идентифицировано как нейромедиатор. Он высвобождается в окончаниях холинергических парасимпатических и симпатических волокон. Процесс освобождения медиатора является кальцийзависимым. Инактивация медиатора происходит с помощью фермента ацетилхолинэстеразы. Ацетилхолин оказывает свое воздействие на органы и ткани посредством специфических холинорецепторов. Действие ацетилхолина на постсинаптическую мембрану постганглионарных нейронов может быть воспроизведено никотином, а действие ацетилхолина на исполнительные органы – мускарином (токсин гриба мухомора). На этом основании холинорецепторы разделили на Н-холинорецепторы (никотиновые) и М-холинорецепторы (мускариновые). Однако и эти виды холинорецепторов не однородны. Н-холинорецепторы в периферических отделах вегетативной нервной системы расположены в ганглионарных синапсах симпатического и парасимпатического отделов, в каротидных клубочках и хромаффинных клетках мозгового слоя надпочечников. Возбуждение этих холинорецепторов сопровождается соответственно облегчением проведения возбуждения через ганглии, что ведет к повышению тонуса симпатического и парасимпатического отделов вегетативной нервной системы; повышением рефлекторного возбуждения дыхательного центра, в результате чего углубляется дыхание; повышением секреции адреналина. Вышеперечисленные Н-холинорецепторы блокируются веществами типа бензогексония (ганглиоблокаторами), но не реагируют на курареподобные вещества (d-тубокурарин), которые блокируют Н-холинорецепторы, локализованные на клетках скелетных мышц (в нервно-мышечном синапсе). В свою очередь, Н-холинорецепторы скелетных мышц не чувствительны к ганглиоблокаторам. В связи с этим Н-холинорецепторы подразделили на Н-холинорецепгоры ганглионарного типа (Нп-холинорецепторы) и мышечного типа (Нм-холинорецепторы). М-холинорецепторы также подразделяются на несколько типов: М1-, М2- и М3-холинорецепторы. Но все они блокируются атропином. М-холинорецепторы находятся на обкладочпых клетках желудочных желез и их возбуждение приводит к усилению секреции соляной кислоты. М2-холинорецепторы располагаются в проводящей системе сердца. Возбуждение этих рецепторов приводит к понижению концентрации цАМФ, открытию калиевых каналов и увеличению тока К+, что приводит к гиперполяризации и тормозным эффектам: брадикардии, замедлению атриовентрикулярной проводимости, ослаблению сокращений сердца, понижению потребности сердечной мышцы в кислороде. М3-холинорецепторы локализованы в основном в гладких мышцах некоторых внутренних органов и экзокринных железах. Взаимодействие ацетилхолина с этими рецепторами приводит к активации натриевых каналов, деполяризации, формированию ВПСП, вследствие чего клетки возбуждаются и происходит сокращение гладких мышц и выделение соответствующих секретов. Возбуждение этих рецепторов в гладких мышцах бронхов, кишечника, мочевого пузыря, матки, круговой и цилиарной мышцах глаза приводит соответственно к бронхоспазму, усилению перистальтики кишечника, желудка при расслаблении сфинктеров, сокращению мочевого пузыря, матки, сужению зрачка и спазму аккомодации. Возбуждение М3-холинорецепторов экзокринных желез вызывает слезотечение, усиление потоотделения, выделение обильной бедной белком слюны, бронхорею, выделение желудочного сока. Имеются также внесинаптические М3-холинорецепторы, которые располагаются в эндотелии сосудов, где они ассоциированы с сосудорасширяющим фактором – окисью азота. Их возбуждение приводит к расширению сосудов и понижению артериального давления. Норадреналин обеспечивает химическую передачу нервного импульса в норадренергических синапсах вегетативной нервной системы. Норадреналин относится к катехоламинам. Он синтезируется из аминокислоты тирозина в области пресинаптической мембраны адренергического синапса. В хромаффинных клетках надпочечников этот процесс продолжается, в результате чего образуется адреналин (тирозин-ДОФА-дофамин-норадреналин-адреналин). Инактивация норадреналина происходит с помощью ферментов катехол-о-метилтрасферазы (КОМТ) и моноаминоксидазы (МАО), а также путем обратного захвата нервными окончаниями с последующим повторным использованием. Частично норадреналин диффундирует в кровеносные сосуды. Действие норадреналина на клетку опосредуется адренорецепторами. По современным представлениям, норадреналин воз-действует на норадреналин-чувствительную аденилатциклазу клеточной мембраны адренорецептора, что приводит к усилению образования внугриклеточного 3–5-циклического аденозинмонофосфата (цАМФ), играющего роль «вторичного передатчика», к активации биосинтеза макроергических соединений и к осуществлению адренергических физиологических эффектов. Адренорецепторы находятся в различных тканях организма и воспринимают действие норадреналина и адреналина. Адренорецепторы делят на α-адренорецепторы и β-адренорецепторы, а в пределах этих классов выделяют α1, α2, β1, β2 и β3-адренорецепторы. На одной и той же клетке могут располагаться различные адренорецепторы. Конечный эффект возбуждения симпатических волокон зависит от того, какие адренорецепторы преобладают в органе. α-адренорецепторы (постсинаптические) в основном локализованы в гладких мышцах сосудов кожи, слизистых и органов брюшной полости, а также в радиальной мышце глаза, гладких мышцах кишечника, матки, семявыносящих протоков, семенных пузырьках, капсуле селезенки, сфинктерах пищеварительного тракта и мочевого пузыря, пиломоторах. Возбуждение а,-адренорецепторов приводит к сужению радиальной мышцы глаза и расширению зрачка (мидриаз), сужению соответствующих сосудов и повышению АД, сокращению капсулы селезенки и выбросу депонированной крови, сокращению сфинктеров пищеварительного тракта и мочевого пузыря, расслаблению гладких мышц кишечника и снижению его перистальтики и т. д. Среди α2-адренорецепторов выделяют пре-, пост- и внесинаптические. Возбуждение пресинаптических α2-адренорецепторов по механизму отрицательной обратной связи уменьшает выделение норадреналина при его избытке в синаптической щели. Постсинаптические α2-адренорецепторы находятся в бета-клетках поджелудочной железы. Их возбуждение вызывает угнетение выброса инсулина в кровь. Внесинаптические α2-адренорецепторы обнаружены преимущественно на мембране тромбоцитов, эндотелии некоторых сосудов, в жировых клетках. Возбуждение этих рецепторов вызывает сужение сосудов, агрегацию тромбоцитов, угнетение липолиза. β-адренорецепторы (постсинаптические) выявлены в основном в проводящей системе сердца и гладкой мышце кишечника. Их возбуждение приводит к увеличению частоты сердечных сокращений, повышению проводимости и сократимости сердечной мышцы, увеличению потребности сердца в кислороде, понижению тонуса и моторной активности кишечника. Стимуляция пресинаптических β2-адренорецепторов по механизму положительной обратной связи вызывает выделение норадреналина при его недостатке в синаптической щели. Постсинаптические β2-адренорецепторы расположены в основном в эндотелии сосудов скелетных мышц, головного мозга, легких, коронаров, а также в гладкой мускулатуре бронхов, матки и на гепатоцитах. Их возбуждение вызывает расширение соответствующих сосудов и понижение АД, расслабление бронхов и матки, усиление в печени гликогенолиза за счет активации цАМФ-зависимой фосфорилазы и повышение в крови сахара. β3-адренорецепторы находятся в жировых клетках. Их стимуляция приводит к активации липолиза. В гладкой мышце артерий скелетных мышц содержатся α,β-адренорецепторы. Возбуждение α-адренорецепторов приводит к сужению артериол, а возбуждение β2-адренорецепторов – к их расширению. В гладких мышцах кишечника находятся α- и β-адренорецепторы, возбуждение и тех и других приводит к расслаблению мышц. Эффекты норадреналина реализуются через аи p-адренорецепторы, однако норадреналин обладает большим сродством к α-адренорецепторам. Адреналин выполняет гормональную функцию в организме, его эффекты реализуются через кровь посредством возбуждения внесинаптических аи радренорецепторов, но большим сродством он обладает к β-адренорецепторам. Реакция органа на норадреналин и адреналин зависит от преобладания α- или β-адренергического действия. Дофамин осуществляет химическую передачу нервных импульсов не только в дофаминергических синапсах ЦНС, но и во вставочных нейронах симпатических ганглиев и во внутриорганном отделе вегетативной нервной системы. В дофаминергических нейронах биосинтез катехоламинов заканчивается на дофамине. Инактивация дофамина осуществляется ферментами КОМТ и МАО, а также путем обратного нейронального захвата. Периферические дофаминовые рецепторы (Д-рецепторы) изучены недостаточно. Д-рецепторы выявлены на гладкомышечных клетках кишечника, сосудов почек, аорты, паращитовидных железах, канальцах почек. Возбуждение этих рецепторов приводит к расслаблению гладких мышц, понижению тонуса кишечника, расширению соответствующих сосудов, повышению высвобождения паратгормона, усилению выделения натрия и воды. Дофаминовые рецепторы выявлены также в надпочечниках и поджелудочной железе, но пока не идентифицированы. Эти рецепторы регулируют секрецию панкреатического полипептида, бикарбонатов и альдостерона. АТФ может играть роль не только макроергического соединения, но и медиатора. Местом его локализации является пресинаптические терминали эффекторных нейронов внутриорганного отдела вегетативной нервной системы. Эта передача получила название пуринергической, так как при стимуляции этих окончаний выделяются пуриновые продукты распада – аденозин и инозин. Действие АТФ проявляется в основном в расслаблении гладкой мускулатуры. Пуринергические нейроны являются, по-видимому, главной антагонистической тормозной системой по отношению к холинергической возбуждающей системе. Пуринорецспторы представлены двумя группами: и В2. В1-рецепторы более чувствительны к продукту распада АТФ – аденозину, В2-рецепторы – к самому АТФ. В1-рецепторы преобладают в сердечнососудистой системе, трахее, мозге. Специфичными антагонистами Р2-рецепторов являются метилксантины, например, алкалоиды кофе и чая – кофеин и теофиллин. В2-рецепторы располагаются в основном в органах желудочно-кишечного тракта и мочеполовой системы. Специфическим блокатором В2-рецепторов служит хинидин. Одним из медиаторов внутриорганного отдела вегетативной нервной системы является серотонин, или 5-окситриптамин, который выполняет также медиаторную функцию в центральных образованиях. Серотонин оказывает свое воздействие путем взаимодействия со специфическими серотониновыми рецепторами. Периферические рецепторы (или 5-НТ,) в основном обнаружены в гладких мышцах желудочно-кишечного тракта, сосудах скелетных мышц и сердца, проводящей системе сердца. Их возбуждение сопровождается спазмом гладких мышц кишечника, вазодилатацией, тахикардией. 52-рецепторы (5-НТ2) находятся в гладких мышцах стенок сосудов, бронхов, на тромбоцитах. При их стимуляции возникает спазм сосудов, за исключением сосудов скелетных мышц и сердца, и повышается АД, увеличивается агрегация тромбоцитов. Рецепторы (5-НТ3) локализуются в гладких мышцах, вегетативных ганглиях. Посредством взаимодействия с этими рецепторами серотонин осуществляет регуляцию сократительной способности гладких мышц и усиление освобождения ацетилхолина в терминалях вегетативных нервов. Роль медиатора в вегетативной нервной системе может играть гистамин. Наибольшее количество его находится в постганглионарных симпатических волокнах. Инактивация гистамина осуществляется ферментом диаминоксидазой. Периферические гистаминовые рецепторы встречаются во всех органах и тканях организма. Известно два класса гистаминовых рецепторов: Н1 и Н2. Н1-рецепторы локализуются в гладкой мускулатуре бронхов, желудочно-кишечного тракта, сосудов, в сердце (атриовентрикулярный узел). Возбуждение Н1-рецепторов сопровождается спазмом бронхов, повышением тонуса и перистальтики кишечника, сужением крупных сосудов, но расширением артериол, венул и развитием, в общем итоге, гипотензии, повышением сосудистой проницаемости, уменьшением времени проведения по атриовентрикулярному узлу, тахикардией, увеличением образования простагландинов. Н2-рецепторы обнаружены преимущественно в слизистой желудка и 12-перстной кишки, слизистой бронхов, на базофилах, на Т-супрессорах. Возбуждение Н2-рецепторов приводит к повышению секреции кислоты в желудке и секреции бронхиальных желез, уменьшению высвобождения гистамина базофилами, стимуляции Т-супрессоров. Функцию медиаторов синаптической передачи во внутриорганном отделе вегетативной нервной системы выполняют и некоторые аминокислоты, регуляторные нейропептиды, простагландины и другие биологические активные вещества. Аспарагиновая и глутаминовая кислоты являются медиаторами возбуждающего типа, гамма-аминомасляная кислота (ГАМК) – медиатором тормозного типа. В результате взаимодействия ГАМК с ГАМК-рецепторами происходит открытие каналов для ионов хлора, что обусловливает гиперполяризующее действие ГАМК. Периферическое действие ГАМК практически не исследовано, хотя имеются сведения о способности ГАМК изменять состояние внутренних органов. Например, ГАМК-рецепторы обнаружены в кишечнике. Различают ГАМК-а и ГАМК-в-рецепторы. Возбуждение ГАМК-арецепторов приводит к сокращению гладких мышц кишечника, возбуждение ГАМК-в, наоборот, – расслаблению. ГАМК-в-рецепторы выявлены также в предсердиях и сосудах. Их возбуждение приводит к снижению сократительной активности предсердий и тонуса сосудов. ГАМК способна влиять на освобождение других медиаторов из пресинаптических окончаний: ацетилхолина, дофамина, серотонина. Представителем регуляторных нейропептидов является субстанция Р. Периферические рецепторы к субстанции Р обнаружены на гладкомышечных клетках кишки (SP-P-рецепторы) и на клетках мочевого пузыря, семявыносящих протоков (SP-E-рецепторы). В волокнах блуждающего нерва содержится большое количество простагландинов.Вегетативные (автономные) рефлексы
Процессы в вегетативной и соматической нервных системах тесно связаны. Различают висцеро-висцеральные, висцеросоматические, вьсцеросенсорные рефлексы. Классическим примером висцеро-висцерального рефлекса является рефлекс Гольца, показывающий, что механическое раздражение брыжейки вызывает замедление частоты сердечных сокращений. Разновидностью висцеро-висцерального рефлекса является аксон-рефлекс, например, возникновение сосудистой реакции при раздражении кожных болевых рецепторов. К висцеросоматическим рефлексам относятся торможение общей двигательной активности организма при раздражении хемо- и механорецепторов каротидной зоны, а также сокращение мышц брюшного пресса или подергивание конечностей при раздражении рецепторов пищеварительного тракта. При висцеросенсорных рефлексах в ответ на раздражение вегетативных чувствительных волокон возникают не только реакции во внутренних органах, но и изменяется соматическая чувствительность. Для их вызова необходимо продолжительное и сильное воздействие. Зона повышенного восприятия обычно ограничивается участком кожи, иннервируемым сегментом, к которому поступают импульсы от раздражаемого висцерального органа. В клинике имеют определенное значение висцеродермальные рефлексы. Вследствие сегментарной организации вегетативной и соматической иннервации при заболеваниях внутренних органов на ограниченных участках кожи возникает повышение тактильной и болевой чувствительности. Эти боли называются отраженными, а области, в которых они появляются, – зонами Захарьина-Геда. При раздражении некоторых областей поверхности тела возникают сосудистые реакции и изменения функций определенных висцеральных органов. Это дермовисцеральный рефлекс, который является разновидностью соматовисцерального рефлекса. На этом основана рефлексотерапия.Центры регуляции вегетативных функций
Центры регуляции вегетативных функций разделяются на спинальные, стволовые (бульбарные, мезэнцефалические), гипоталамические, мозжечковые, центры ретикулярной формации, лимбической системы, корковые. В основе их взаимодействия лежит принцип иерархии. Каждый более высокий уровень регуляции обеспечивает и более высокую степень интеграции вегетативных функций.Спинальные центры.
На уровне спинного мозга происходит регуляция просвета зрачка, величины глазной щели, сосудистого тонуса, потоотделения. Стимуляция этих центров приводит к усилению и учащению сердечной деятельности, расширению бронхов. Здесь расположены также центры дефекации, мочеиспускания, половых рефлексов (эрекции и эякуляции).Стволовые центры.
Эти центры находятся в продолговатом мозге, мосту, среднем мозге. За счет ядер блуждающих нервов происходит торможение деятельности сердца, возбуждение слезоотделения, усиление секреции слюнных, желудочных желез, поджелудочной железы, желчевыделения, усиление сокращений желудка и тонкой кишки. Сосудодвигательный центр отвечает за рефлекторное сужение и расширение сосудов и регуляцию кровяного давления. Дыхательный центр регулирует смену вдоха и выдоха. В продолговатом мозге находятся центры, с помощью которых осуществляются такие сложные рефлексы, как сосание, жевание, глотание, чихание, кашель, рвота. В передних буграх четверохолмия в среднем мозге располагаются центры, регулирующие зрачковый рефлекс и аккомодацию глаза.Гипоталамические центры.
Гипоталамус является главным подкорковым центром интеграции висцеральных процессов, что обеспечивается вегетативными, соматическими и эндокринными механизмами. Стимуляция ядер задней группы гипоталамуса сопровождается реакциями, аналогичными раздражению симпатической нервной системы: расширение зрачков и глазных щелей, учащение сердечных сокращений, сужение сосудов и повышение АД, торможение моторной активности желудка и кишечника, увеличение содержания в крови адреналина и норадреналина, концентрации глюкозы. Задняя область гипоталамуса отвечает за регуляцию теплопродукции и оказывает тормозящее влияние на половое развитие. Стимуляция передних ядер гипоталамуса приводит к эффектам, подобным раздражению парасимпатической нервной системы: сужение зрачков и глазных щелей, замедление частоты сердечных сокращений, снижение артериального давления, усиление моторной активности желудка и кишечника, увеличение секреции желудочных желез, стимуляция секреции инсулина и снижение уровня глюкозы в крови. Передние ядра регулируют теплоотдачу и оказывают стимулирующее влияние на половое развитие. Средняя группа ядер гипоталамуса обеспечивает регуляцию метаболизма и водного баланса. Вентромедиальные ядра отвечают за насыщение, латеральные ядра – за голод (центры голода и насыщения). Паравентрикулярное ядро – центр жажды. Гипоталамус отвечает за эмоциональное поведение, формирование половых и агрессивно-оборонительных реакций. С помощью нейротропных средств можно избирательно воздействовать на гипоталамические структуры и регулировать состояние голода, жажды, аппетита, страха, половые реакции.Центры лимбической системы.
Эти центры отвечают за формирование вегетативного компонента эмоциональных реакций, пищевое, сексуальное, оборонительное поведение, регуляцию систем, обеспечивающих сон и бодрствование, внимание.Мозжечковые центры.
Благодаря наличию активирующего и тормозного механизмов мозжечок может оказывать стабилизирующее влияние на деятельность висцеральных органов посредством корригирования висцеральных рефлексов.Центры ретикулярной формации.
Ретикулярная формация осуществляет тонизирование и повышение активности других вегетативных нервных центров.Центры коры больших полушарий.
Кора больших полушарий осуществляет высший интегративный контроль вегетативных функций посредством нисходящих тормозных и активирующих влияний на ретикулярную формацию и другие подкорковые вегетативные центры. Координирует вегетативные и соматические функции в системе поведенческого акта.Средства, влияющие на синаптическую передачу
Понимание тонких физиологических механизмов синаптической передачи в вегетативной нервной системе позволило создать новые лекарственные средства, применяемые в клинической и экспериментальной медицине для воздействия на функции различных внутренних органов и висцеральных систем. В настоящее время большинство эндогенных медиаторов выделено из организма в чистом виде, установлена их химическая структура и осуществлен синтез. Получен также целый ряд современных синтетических лекарственных препаратов, имеющих структурное сходство с эндогенными нейромедиаторами. Одни из них, связываясь с соответствующими рецепторами, оказывают эффекты, подобные эндогенным медиаторам, т. е. действуют как агонисты. Другие, блокируя рецепторы, препятствуют действию эндогенных медиаторов, т. е. являются их антагонистами. Открытие субпопуляций рецепторов (α1, α2, β1, β2-адренорецепторы; М1, М2, М3-холинорецепторы и др.) привело к созданию новых лекарственных средств, действующих преимущественно на различные подгруппы рецепторов, что позволяет избирательно регулировать различные процессы в определенных органах и тканях и получать специфические эффекты. Так, существуют фармакологические препараты, которые могут вызывать такой же эффект, как и ацетилхолин. Такие вещества называются холиномиметиками. Одни из них, как и сам медиатор, прямо воздействуют на рецепторы, имитируя действие ацетилхолина (карбахолин). Другие, ингибируя фермент ацетилхолинэстеразу, инактивирующую ацетилхолин, продлевают и усиливают действие эндогенного ацетилхолина (прозерин). Синтезированы и избирательные холиномиметики, воздействующие только на определенные виды холинорецепторов. Например, к веществам, избирательно стимулирующим Н-холинорецепторы, относятся дыхательные аналептики лобелин и цитизин. К М-холиномиметикам относится алкалоид пилокарпин, который преимущественно возбуждает М3-холинорецепторы экзокринных желез (используется в офтальмологической практике для понижения внутриглазного давления при глаукоме). Лекарственные препараты, устраняющие или ослабляющие влияние ацетилхолина, носят название холинолитиков. Вещества, блокирующие М-холинорецепторы исполнительных органов и устраняющие мускариноподобный эффект ацетилхолина, называются М-холинолитиками. К ним относится атропин. Избирательным антагонистом М-холинорецепторов является гастроцепин (применяется для лечения язвенной болезни желудка и 12-перстной кишки). Холинолитики, устраняющие никотиноподобное действие ацетилхолина путем блокады Н-холинорецепторов на постганглионарных нейронах вегетативных ганглиев, мозгового слоя надпочечников и каротидного синуса (Нн-холинорецепторы), называют ганглиоблокаторами (бензогексоний, пирилен). С помощью ганглиоблокаторов можно выключить синаптическую передачу только в вегетативных ганглиях, не изменяя тонуса скелетных мышц. Лекарственные вещества, оказывающие действие, аналогичное возбуждению постганглионарных симпатических волокон, получили название адреномиметиков. Некоторые из них преимущественно возбуждают α-адренорецепторы (мезатон), другие вещества действуют на p-адренорецепторы (изадрин). Получены и фармакологические препараты, избирательно стимулирующие отдельные подгруппы адренорецепторов. Так, широкое применение в медицине в качестве бронхорасширяющих средств нашли препараты, оказывающие сильное избирательное действие на β2-адренорецепторы (алупент, беротек). Эффекты, аналогичные действию медиатора, можно получить, подавив активность ферментов, инактивирующих норадреналин и адреналин: МАО (ниаламид) или КОМТ (пирогалол). Такой же эффект может быть получен в результате угнетения обратного захвата медиатора пресинаптическими окончаниями (имизин). Известны вещества, действующие на пресинаптические адренергические окончания и способствующие выделению норадреналина – симпатомиметики непрямого действия (например, эфедрин). В экспериментальной физиологии и медицине широко используются вещества, блокирующие адренорецепторы и препятствующие их взаимодействию с медиатором. Фармакологические препараты, блокирующие α-адренорецепторы, называются α-адреноблокаторами (фентоламин, дигидроэрготоксин); блокирующие β-адренорецепторы – β-адреноблокаторами (анаприлин). Синтезированы и избирательные адреноблокаторы, например избирательно блокирующие β1-адренорецепторы сердца (атенолол). Если нарушить передачу адренергического возбуждения на пресинаптическом уровне, можно вызвать эффекты, аналогичные снижению тонуса симпатической нервной системы. Так действуют лекарственные средства группы симпатолитиков. Можно вызвать истощение запасов норадреналина в пресинаптической мембране (октадин) или блокировать выделение норадреналина из пресинаптической мембраны (орнид). Длительное введение агонистов или антагонистов адренорецепторов вызывает соответственно понижение или повышение чувствительности адренорецепторов, что необходимо помнить при применении этих фармакологических препаратов. Синтезировано также большое количество лекарственных веществ, являющихся агонистами и антагонистами и других эндогенных медиаторов. Так, широкое применение в медицине нашли блокаторы Н1-гистаминовых рецепторов (димедрол, тавегил), используемые главным образом для лечения и предупреждения аллергических заболеваний. Блокаторы Н2-гистаминовых рецепторов (циметидин) используются для лечения язвенной болезни желудка и 12-перстной кишки. Антагонист Б2-серотониновых рецепторов кетансерин является антигипертензивным препаратом.Глава 5. Железы внутренней секреции
Интеграция клеток, тканей и органов в единый человеческий организм, приспособление его к различным изменениям внешней среды или потребностям самого организма осуществляется за счет нервной и гуморальной регуляции. Система нейрогуморальной регуляции представляет собой единый, тесно связанный механизм. Связь нервной и гуморальной систем регуляции хорошо видна на следующих примерах. Во-первых, природа биоэлектрических процессов является физико-химической, т. е. заключается в трансмембранных перемещениях ионов. Во-вторых, передача возбуждения с одной нервной клетки на другую или исполнительный орган происходит посредством медиатора. И наконец, наиболее тесная связь между этими механизмами прослеживается на уровне гипоталамо-гипофизарной системы. Гуморальная регуляция в филогенезе возникла раньше. В дальнейшем в процессе эволюции она дополнилась высокоспециализированной нервной системой. Нервная система осуществляет свои регуляторные влияния на органы и ткани с помощью нервных проводников, передающих нервные импульсы. Для передачи нервного сигнала требуются доли секунды. Поэтому нервная система осуществляет запуск быстрых приспособительных реакций при изменениях внешней или внутренней среды. Гуморальная регуляция – это регуляция процессов жизнедеятельности с помощью веществ, по-ступающих во внутреннюю среду организма (кровь, лимфу, ликвор). Гуморальная регуляция обеспечивает более длительные адаптивные реакции. К факторам гуморальной регуляции относятся гормоны, электролиты, медиаторы, кинины, простагландины, различные метаболиты и т. д.Общая физиология желез внутренней секреции
Высшей формой гуморальной регуляции является гормональная. Термин «гормон» был впервые применен в 1902 г. Стерлингом и Бейлиссом в отношении открытого ими вещества, продуцирующегося в двенадцатиперстной кишке, – секретина. Термин «гормон» в переводе с греческого означает «побуждающий к действию», хотя не все гормоны обладают стимулирующим эффектом. Гормоны – это биологически высокоактивные вещества, синтезирующиеся и выделяющиеся во внутреннюю среду организма эндокринными железами, или железами внутренней секреции, и оказывающие регулирующее влияние на функции удаленных от места их секреции органов и систем организма. Эндокринная железа – это анатомическое образование, лишенное выводных протоков, единственной или основной функцией которого является внутренняя секреция гормонов. К эндокринным железам относятся гипофиз, эпифиз, щитовидная железа, надпочечники (мозговое и корковое вещество), паращитовидные железы. В отличие от внутренней секреции, внешняя секреция осуществляется экзокринными железами через выводные протоки во внешнюю среду. В некоторых органах одновременно присутствуют оба типа секреции. Инкреторная функция осуществляется эндокринной тканью, т. е. скоплением клеток с инкреторной функцией в органе, обладающем функциями, не связанными с продукцией гормонов. К органам со смешанным типом секреции относятся поджелудочная железа и половые железы. Одна и та же железа внутренней секреции может продуцировать неодинаковые по своему действию гормоны. Так, например, щитовидная железа продуцирует тироксин и тирокальцитонин. В то же время продукция одних и тех же гормонов может осуществляться разными эндокринными железами. Например, половые гормоны продуцируются и половыми железами, и надпочечниками. Продукция биологически активных веществ – это функция не только желез внутренней секреции, но и других традиционно неэндокринных органов: почек, желудочно-кишечного тракта, сердца. Не все вещества, образующиеся специфическими клетками этих органов, удовлетворяют классическим критериям понятия «гормоны». Поэтому наряду с термином «гормон» в последнее время используются также понятия гормоноподобные и биологически активные вещества (БАВ), гормоны местного действия. Так, например, некоторые из них синтезируются так близко к своим органам-мишеням, что могут достигать их диффузией, не попадая в кровоток. Клетки, вырабатывающие такие вещества, называют паракринными. Трудность точного определения термина «гормон» особенно хорошо видна на примере катехоламинов – адреналина и норадреналина. Когда рассматривается их выработка в мозговом веществе надпочечников, их обычно называют гормонами, если речь идет об их образовании и выделении симпатическими окончаниями, их называют медиаторами. Регуляторные гипоталамические гормоны – группа нейропептидов, включая недавно открытые энкефалины и эндорфины, действуют не только как гормоны, но и выполняют своеобразную медиаторную функцию. Некоторые из регуляторных гипоталамических пептидов обнаружены не только в нейронах головного мозга, но и в особых клетках других органов, например кишечника: это вещество Р, нейротензин, соматостатин, холецистокинин и др. Клетки, вырабатывающие эти пептиды, образуют согласно современным представлениям диффузную нейроэндокринную систему, состоящую из разбросанных по разным органам и тканям клеток. Клетки этой системы характеризуются высоким содержанием аминов, способностью к захвату предшественников аминов и наличием декарбоксилазы аминов. Отсюда названиесистемы по первым буквам английских слов Amine Precursors Uptake arid Decarboxylating system – APUD-система – система захвата предшественников аминов и их декарбоксилирования. Поэтому правомерно говорить не только об эндокринных железах, но и об эндокринной системе, которая объединяет все железы, ткани и клетки организма, выделяющие во внутреннюю среду специфические регуляторные вещества. Химическая природа гормонов и биологически активных веществ различна. От сложности строения гормона зависит продолжительность его биологического действия, например, от долей секунды у медиаторов и пептидов до часов и сугок у стероидных гормонов и йодтиронипов. Анализ химической структуры и физико-химических свойств гормонов помогает понять механизмы их действия, разрабатывать методы их определения в биологических жидкостях и осуществлять их синтез.Классификация гормонов и БАВ по химической структуре: 1. Производные аминокислот: • производные тирозина: тироксин, трийодтиронин, дофамин, адреналин, норадреналин; • производные триптофана: мелатонин, серотонин; • производные гистидина: гистамин. 2. Белково-пептидные гормоны: • полипептиды: глюкагон, кортикотропин, меланотропин, вазопрессин, окситоцин, пептидные гормоны желудка и кишечника; • простые белки (протеины): инсулин, соматотропин, пролактин, паратгормон, кальцитонин; • сложные белки (гликопротеиды): тиреотропин, фоллитропин, лютропин. 3. Стероидные гормоны: • кортикостероиды (альдостерон, кортизол, кортикостерон); • половые гормоны: андрогены (тестостерон), эстрогены и прогестерон. 4. Производные жирных кислот: • арахидоновая кислота и ее производные: простагландинм: простациклины, тромбоксаны, лейкотриены.
Несмотря на то, что гормоны имеют разное химическое строение, для них характерны некоторые общие биологические свойства.
Общие свойства гормонов: 1. Строгая специфичность (тропность) физиологического действия. 2. Высокая биологическая активность: гормоны оказывают свое физиологическое действие в чрезвычайно малых дозах. 3. Дистантный характер действия: клетки-мишени располагаются обычно далеко от места образования гормона. 4. Многие гормоны (стероидные и производные аминокислот) не имеют видовой специфичности. 5. Генерализованность действия. 6. Пролонгированность действия.
Установлены четыре основных типа физиологического действия на организм: кинетическое, или пусковое, вызывающее определенную деятельность исполнительных органов; метаболическое (изменения обмена веществ); морфогенетическое (дифференциация тканей и органов, действие на рост, стимуляция формообразовательного процесса); корригирующее (изменение интенсивности функций органов и тканей). Гормональный эффект опосредован следующими основными этапами: синтезом и поступлением в кровь, формами транспорта, клеточными механизмами действия гормонов. От места секреции гормоны доставляются к органам-мишеням циркулирующими жидкостями: кровью, лимфой.
В крови гормоны циркулируют в нескольких формах: 1. в свободном состоянии; 2. в комплексе со специфическими белками плазмы крови; 3. в форме неспецифического комплекса с плазменными белками; 4. в адсорбированном состоянии на форменных элементах крови.
В состоянии покоя 80% приходится на комплекс со специфическими белками. Биологическая активность определяется содержанием свободных форм гормонов. Связанные формы гормонов являются как бы депо, физиологическим резервом, из которого гормоны переходят в активную свободную форму по мере необходимости. Обязательным условием для проявления эффектов гормона является его взаимодействие с рецепторами.
Гормональные рецепторы представляют собой особые белки клетки, для которых характерны: 1. высокое сродство к гормону; 2. высокая избирательность; 3. ограниченная связывающая емкость; 4. специфичность локализации рецепторов в тканях.
На одной и той же мембране клетки могут располагаться десятки разных типов рецепторов. Количество функционально активных рецепторов может изменяться при различных состояниях и в патологии. Так, например, при беременности в миометрии исчезают М-холинорецепторы, но возрастает количество окситоциновых рецепторов. При некоторых формах сахарного диабета имеет место функциональная недостаточность инсулярного аппарата, т. е. уровень инсулина в крови высокий, но часть инсулиновых рецепторов оккупирована аутоантителами к этим рецепторам. В 50% случаев рецепторы локализуются на мембранах клетки-мишени; 50% – внутри клетки.
Механизмы действия гормонов.
Существуют два основных механизма действия гормонов на уровне клетки: реализация эффекта с наружной поверхности клеточной мембраны и реализация эффекта после проникновения гормона внутрь клетки. В первом случае рецепторы расположены на мембране клетки. В результате взаимодействия гормона с рецептором активируется мембранный фермент – аденилатциклаза. Этот фермент способствует образованию из аденозинтрифосфорной кислоты (АТФ) важнейшего внутриклеточного посредника реализации гормональных эффектов – циклического 3,5-аденозинмонофосфата (цАМФ). цАМФ активирует клеточный фермент протеинкиназу, реализующую действие гормона. Установлено, что гормонозависимая аденилатциклаза – это общий фермент, на который действуют различные гормоны, в то время как рецепторы гормонов множественны и специфичны для каждого гормона. Вторичными посредниками кроме цАМФ могут быть циклический 3,5-гуанозинмонофосфат (цГМФ), ионы кальция, инозитол-трифосфат. Так действуют пептидные, белковые гормоны, производные тирозина – катехоламины. Характерной особенностью действия этих гормонов является относительная быстрота возникновения ответной реакции, что обусловлено активацией предшествующих уже синтезированных ферментов и других белков. Во втором случае рецепторы для гормона находятся в цитоплазме клетки. Гормоны этого механизма действия в силу своей липофильности легко проникают через мембрану внутрь клеткимишени и связываются в ее цитоплазме специфическими белка-ми-рецепторами. Гормон-рецепторный комплекс входит в клеточное ядро. В ядре комплекс распадается, и гормон взаимодействует с определенными участками ядерной ДНК, следствием чего является образование особой матричной РНК. Матричная РНК выходит из ядра и способствует синтезу на рибосомах белка или белка-фермента. Так действуют стероидные гормоны и производные тирозина – гормоны щитовидной железы. Для их действия характерна глубокая и длительная перестройка клеточного метаболизма. Инактивация гормонов происходит в эффекторных органах, в основном в печени, где гормоны претерпевают различные химические изменения путем связывания с глюкуроновой или серной кислотой либо в результате воздействия ферментов. Частично гормоны выделяются с мочой в неизмененном виде. Действие некоторых гормонов может блокироваться благодаря секреции гормонов, обладающих антагонистическим эффектом.Гормоны выполняют в организме следующие важные функции: 1. Регуляция роста, развития и дифференцировки тканей и органов, что определяет физическое, половое и умственное развитие. 2. Обеспечение адаптации организма к меняющимся условиям существования. 3. Обеспечение поддержания гомеостаза.
Функциональная классификация гормонов: 1. Эффекторные гормоны – гормоны, которые оказывают влияние непосредственно на орган-мишень. 2. Тропные гормоны – гормоны, основной функцией которых является регуляция синтеза и выделения эффекторных гормонов. Выделяются аденогипофизом. 3. Рилизинг-гормоны – гормоны, регулирующие синтез и вы-деление гормонов аденогипофиза, преимущественно тропных. Выделяются нервными клетками гипоталамуса.
Виды взаимодействия гормонов. Каждый гормон не работает в одиночку. Поэтому необходимо учитывать возможные результаты их взаимодействия. Синергизм – однонаправленное действие двух или нескольких гормонов. Например, адреналин и глюкагон активируют распад гликогена печени до глюкозы и вызывают увеличение уровня сахара в крови. Антагонизм всегда относителен. Например, инсулин и адреналин оказывают противоположные действия на уровень глюкозы в крови. Инсулин вызывает гипогликемию, адреналин – гипергликемию. Биологическое же значение этих эффектов сводится к одному – улучшению углеводного питания тканей. Пермиссивное действие гормонов заключается в том, что гормон, сам не вызывая физиологического эффекта, создает условия для ответной реакции клетки или органа на действие другого гормона. Например, глюкокортикоиды, не влияя на тонус мускулатуры сосудов и распад гликогена печени, создают условия, при которых даже небольшие концентрации адреналина увеличивают артериальное давление и вызывают гипергликемию в результате гликогенолиза в печени.
Регуляция функций желез внутренней секреции
Регуляция деятельности желез внутренней секреции осуществляется нервными и гуморальными факторами. Нейроэндокринные зоны гипоталамуса, эпифиз, мозговое вещество надпочечников и другие участки хромаффинной ткани регулируются непосредственно нервными механизмами. В большинстве случаев нервные волокна, подходящие к железам внутренней секреции, регулируют не секреторные клетки, а тонус кровеносных сосудов, от которых зависит кровоснабжение и функциональная активность желез. Основную роль в физиологических механизмах регуляции играют нейрогормональные и гормональные механизмы, а также прямые влияния на эндокринные железы тех веществ, концентрацию которых регулирует данный гормон. Регулирующее влияние ЦНС на деятельность эндокринных желез осуществляется через гипоталамус. Гипоталамус получает по афферентным путям мозга сигналы из внешней и внутренней среды. Нейросекреторные клетки гипоталамуса трансформируют афферентные нервные стимулы в гуморальные факторы, продуцируя рилизинг-гормоны. Рилизинг-гормоны избирательно регулируют функции клеток аденогипофиза. Среди рилизинг-гормонов различают либерины – стимуляторы синтеза и выделения гормонов аденогипофиза и статины – ингибиторы секреции. Они носят название соответствующих тропных гормонов: тиреолиберин, кортиколиберин, соматолиберин и т. д. В свою очередь, тропные гормоны аденогипофиза регулируют активность ряда других периферических желез внутренней секреции (кора надпочечников, щитовидная железа, гонады). Это так называемые прямые нисходящие регулирующие связи. Кроме них внутри указанных систем существуют и обратные восходящие саморегулирующие связи. Обратные связи могут исходить как от периферической железы, так и от гипофиза. По направленности физиологического действия обратные связи могут быть отрицательными и положительными. Отрицательные связи самоограничивают работу системы. Положительные связи само-запускают ее. Так, низкие концентрации тироксина через кровь усиливают выработку тиреотропного гормона гипофизом и тиреолиберина – гипоталамусом. Гипоталамус значительно более чувствителен, чем гипофиз к гормональным сигналам, поступающим от периферических эндокринных желез. Благодаря механизму обратной связи устанавливается равновесие в синтезе гормонов, реагирующее на снижение или повышение концентрации гормонов желез внутренней секреции. Некоторые железы внутренней секреции, такие как поджелудочная железа, околощитовидные железы, не находятся под влиянием гормонов гипофиза. Деятельность этих желез зависит от концентрации тех веществ, уровень которых регулируется этими гормонами. Так, уровень паратгормона околощитовидных желез и кальцитонина щитовидной железы определяется концентрацией ионов кальция в крови. Глюкоза регулирует продукцию инсулина и глюкагона поджелудочной железой. Кроме того, функционирование этих желез осуществляется за счет влияния уровня гормонов-антагонистов.Частная физиология желез внутренней секреции
Гипофиз
Гипофизу принадлежит особая роль в системе желез внутренней секреции. С помощью своих гормонов он регулирует деятельность других эндокринных желез. Гипофиз состоит из передней (аденогипофиз), промежуточной и задней (нейрогипофиз) долей. Промежуточная доля у человека практически отсутствует.Гормоны передней доли гипофиза
В аденогипофизе образуются следующие гормоны: адренокортикотропный (АКТГ). или кортикотропин; тиреотропный (ТТГ), или тиреотропин, гонадотропные: фолликулостимулирующий (ФСГ), или фоллитропин, и лютеинизирующий (ЛГ), или лютропин, соматотропный (СТГ), или гормон роста, или соматотропин, пролактин. Первые 4 гормона регулируют функции так называемых периферических желез внутренней секреции. Соматотропин и пролактин сами действуют на ткани-мишени. Адренокортикотропный гормон (АКТГ), или кортикотропин, оказывает стимулирующее действие на кору надпочечников. В большей степени его влияние выражено на пучковую зону, что приводит к увеличению образования глюкокортикоидов, в меньшей – на клубочковую и сетчатую зоны, поэтому на продукцию минералокортикоидов и половых гормонов он не оказывает зна-чительного воздействия. За счет повышения синтеза белка (цАМФ-зависимая активация) происходит гиперплазия коркового вещества надпочечников. АКТГ усиливает синтез холестерина и скорость образования прегненолона из холестерина. Вненадпочечниковые эффекты АКТГ заключаются в стимуляции липолиза (мобилизует жиры из жировых депо и способствует окислению жиров), увеличении секреции инсулина и соматотропина, накоплении гликогена в клетках мышечной ткани, гипогликемии, что связано с повышенной секрецией инсулина, усилении пигментации за счет действия на пигментные клетки меланофоры. Продукция АКТГ подвержена суточной периодичности, что связано с ритмичностью выделения кортиколиберина. Максимальные концентрации АКТГ отмечаются утром в 6–8 часов, минимальные – с 18 до 23 часов. Образование АКТГ регулируется кортиколиберином гипоталамуса. Секреция АКТГ усиливается при стрессе, а также под влиянием факторов, вызывающих стрессогенные состояния: холод, боль, физические нагрузки, эмоции. Гипогликемия способствует увеличению продукции АКТГ. Торможение продукции АКТГ происходит под влиянием самих глюкокортикоидов по механизму обратной связи. Избыток АКТГ приводит к гиперкортицизму, т. е. увеличенной продукции кортикостероидов, преимущественно глюкокортикоидов. Это заболевание развивается при аденоме гипофиза и носит название болезни Иценко-Кушинга. Основные проявления ее: гипертония, ожирение, имеющее локальный характер (лицо и туловище), гипергликемия, снижение иммунной защиты организма. Недостаток гормона ведет к уменьшению продукции глюкокортикоидов, что проявляется нарушением метаболизма и снижением устойчивости организма к различным влияниям среды. Тиреотропный гормон (ТТГ), или тиреотропин, активирует функцию щитовидной железы, вызывает гиперплазию ее железистой ткани, стимулирует выработку тироксина и трийодтиронина. Образование тиреотропина стимулируется тиреолиберином гипоталамуса, а угнетается соматостатином. Секреция тиреолиберина и тиреотропина регулируется йодсодержащими гормонами щитовидной железы по механизму обратной связи. Секреция тиреотропина усиливается также при охлаждении организма, что приводит к повышению выработки гормонов щитовидной железы и повышению тепла. Глюкокортикоиды тормозят продукцию тиреотропина. Секреция тиреотропина угнетается также при травме, боли, наркозе. Избыток тиреотропина проявляется гиперфункцией щитовидной железы, клинической картиной тиреотоксикоза. Фолликулостимулирующий гормон (ФСГ), или фоллитропин, вызывает рост и созревание фолликулов яичников и их подготовку к овуляции. У мужчин под влиянием ФСГ происходит образование сперматозоидов. Лютеинизирующий гормон (ЛГ), или лютропин, способствует разрыву оболочки созревшего фолликула, т. е. овуляции и образованию желтого тела. ЛГ стимулирует образование женских половых гормонов – эстрогенов. У мужчин этот гормон способствует образованию мужских половых гормонов – андрогенов. Секреция ФСГ и ЛС регулируется гонадолиберином гипоталамуса. Образование гонадолиберина, ФСГ и ЛГ зависит от уровня эстрогенов и андрогенов и регулируется по механизму обратной связи. Гормон аденогипофиза пролактин угнетает продукцию гонадотропных гормонов. Тормозное действие на выделение ЛГ оказывают глюкокортикоиды. Соматотропный гормон (СТГ), или соматотропин, или гормон роста, принимает участие в регуляции процессов роста и физического развития. Стимуляция процессов роста обусловлена способностью соматотропина усиливать образование белка в организме, повышать синтез РНК, усиливать транспорт аминокислот из крови в клетки. Наиболее ярко влияние гормона выражено на костную и хрящевую ткани. Действие соматотропина происходит посредством «соматомединов», которые образуются в печени под влиянием соматотропина. Обнаружено, что у пигмеев на фоне нормального содержания соматотропина не образуется соматомедин С, что, по мнению исследователей, служит причиной их маленького роста. Соматотропин влияет на углеводный обмен, оказывая инсулиноподобное действие. Гормон усиливает мобилизацию жира из депо и использование его в энергетическом обмене. Продукция соматотропина регулируется соматолиберином и соматостатином гипоталамуса. Снижение содержания глюкозы и жирных кислот, избыток аминокислот в плазме крови также приводят к увеличению секреции соматотропина. Вазопрессин, эндорфин стимулируют продукцию соматотропина. Если гиперфункция передней доли гипофиза проявляется в детском возрасте, то это приводит к усиленному пропорциональному росту в длину – гигантизму. Если гиперфункция возникает у взрослого человека, когда рост тела в целом уже завершен, наблюдается увеличение лишь тех частей тела, которые еще способны расти. Это пальцы рук и ног, кисти и стопы, нос и нижняя челюсть, язык, органы грудной и брюшной полостей. Это заболевание называется акромегалией. Причиной являются доброкачественные опухоли гипофиза. Гипофункция передней доли гипофиза в детстве выражается в задержке роста – карликовости («гипофизарный нанизм»). Умственное развитие не нарушено. Соматотропин обладает видовой специфичностью. Пролактин стимулирует рост молочных желез и способствует образованию молока. Гормон стимулирует синтез белка – лактальбумина, жиров и углеводов молока. Пролактин стимулирует также образование желтого тела и выработку им прогестерона. Влияет на водно-солевой обмен организма, задерживая воду и натрий в организме, усиливает эффекты альдосторона и вазопрессина, повышает образование жира из углеводов. Образование пролактина регулируется пролактолиберином и пролактостатином гипоталамуса. Установлено также, что стимуляцию секреции пролактина вызывают и другие пептиды, выделяющиеся гипоталамусом: тиреолиберин, вазоактивный интестинальный полипептид (ВИП), ангиотензин II, вероятно, эндогенный опиоидный пептид В-эндорфин. Секреция пролактина усиливается после родов и рефлекторно стимулируется при кормлении грудью. Эстрогены стимулируют синтез и секрецию пролактина. Угнетает продукцию пролактина дофамин гипоталамуса, который, вероятно, также тормозит клетки гипоталамуса, секретирующие гонадолиберин, что приводит к нарушению менструального цикла – лактогенной аменорее. Избыток пролактина наблюдается при доброкачественной аденоме гипофиза (гиперпролактинемическая аменорея), при менингитах, энцефалитах, травмах мозга, избытке эстрогенов, при применении некоторых противозачаточных средств. К его проявлениям относятся выделение молока у некормящих женщин (галакторея) и аменорея. Лекарственные вещества, блокирующие рецепторы дофамина (особенно часто психотропного действия), также приводят к повышению секреции пролактина, следствием чего могут быть галакторея и аменорея.Гормоны задней доли гипофиза
Эти гормоны образуются в гипоталамусе. В нейрогипофизе происходит их накопление. В клетках супраоптического и паравентрикулярного ядер гипоталамуса осуществляется синтез окситоцина и антидиуретического гормона. Синтезированные гормоны путем аксонального транспорта с помощью белка – переносчика нейрофизина по гипоталамо-гипофизарному тракту – транспортируются в заднюю долю гипофиза. Здесь происходит депонирование гормонов и в дальнейшем выделение в кровь. Антидиуретический гормон (АДГ), или вазопрессин, осуществляет в организме 2 основные функции. Первая функция заключается в его антидиуретическом действии, которое выражается в стимуляции реабсорбции воды в дистальном отделе нефрона. Это действие осуществляется благодаря взаимодействию гормона с вазопрессиновыми рецепторами типа V-2, что приводит к повышению проницаемости стенки канальцев и собирательных трубочек для воды, ее реабсорбции и концентрированию мочи. В клетках канальцев происходит также активация гиалуронидазы, что приводит к усилению деполимеризации гиалуроновой кислоты, в результате чего повышается реабсорбция воды и увеличивается объем циркулирующей жидкости. В больших дозах (фармакологических) АДГ суживает артериолы, в результате чего повышается артериальное давление. Поэтому его также называют вазопрессином. В обычных условиях при его физиологических концентрациях в крови это действие не имеет существенного значения. Однако при кровопотере, болевом шоке происходит увеличение выброса АДГ. Сужение сосудов в этих случаях может иметь адаптивное значение. Образование АДГ усиливается при повышении осмотического давления крови, уменьшении объема внеклеточной и внутриклеточной жидкости, снижении артериального давления, при активации ренин-ангиотензиновой системы и симпатической нервной системы. При недостаточности образования АДГ развивается несахарный диабет, или несахарное мочеизнурение, который проявляется выделением больших количеств мочи (до 25 л в сутки) низкой плотности, повышенной жаждой. Причинами несахарного диабета могут быть острые и хронические инфекции, при которых поражается гипоталамус (грипп, корь, малярия), черепно-мозговые травмы, опухоль гипоталамуса. Избыточная секреция АДГ ведет, напротив, к задержке воды в организме. Окситоцин избирательно действует на гладкую мускулатуру матки, вызывая ее сокращения при родах. На поверхностной мембране клеток существуют специальные окситоциновые рецепторы. Во время беременности окситоцин не повышает сократительную активность матки, но перед родами под влиянием высоких концентраций эстрогенов резко возрастает чувствительность матки к окситоцину. Окситоцин участвует в процессе лактации. Усиливая сокращения миоэпителиальных клеток в молочных железах, он способствует выделению молока. Увеличение секреции окситоцина происходит под влиянием импульсов от рецепторов шейки матки, а также механорецепторов сосков грудной железы при кормлении грудью. Эстрогены усиливают секрецию окситоцина. Функции окситоцина в мужском организме изучены не достаточно. Считают, что он является антагонистом АДГ. Недостаток продукции окситоцина вызывает слабость родовой деятельности.Щитовидная железа
Щитовидная железа состоит из двух долей, соединенных перешейком и расположенных на шее по обеим сторонам трахеи ниже щитовидного хряща. Она имеет дольчатое строение. Ткань железы состоит из фолликулов, заполненных коллоидом, в котором имеются йодсодержащие гормоны тироксин (тетрайодтиронин) и трийодтиронин в связанном состоянии с белком тиреоглобулином. В межфолликулярном пространстве расположены парафолликулярные клетки, которые вырабатывают гормон тиреокальцитонин. Содержание тироксина в крови больше, чем трийодтиронина. Однако активность трийодтиронина выше, чем тироксина. Эти гормоны образуются из аминокислоты тирозина путем ее йодирования. Инактивация происходит в печени посредством образования парных соединений с глюкуроновой кислотой.Йодсодержащие гормоны выполняют в организме следующие функции: 1. усиление всех видов обмена (белкового, липидного, углеводного), повышение основного обмена и усиление энергооб-разования в организме; 2. влияние на процессы роста, физическое и умственное развитие; 3. увеличение частоты сердечных сокращений; 4. стимуляция деятельности пищеварительного тракта: повышение аппетита, усиление перистальтики кишечника, увеличение секреции пищеварительных соков; 5. повышение температуры тела за счет усиления теплопродукции; 6. повышение возбудимости симпатической нервной системы.
Секреция гормонов щитовидной железы регулируется тиреотропным гормоном аденогипофиза, тиреолиберином гипоталамуса, содержанием йода в крови. При недостатке йода в крови, а также йодсодержащих гормонов по механизму положительной обратной связи усиливается выработка тиреолиберина, который стимулирует синтез тиреотропного гормона, что, в свою очередь, приводит к увеличению продукции гормонов щитовидной железы. При избыточном количестве йода в крови и гормонов щитовидной железы работает механизм отрицательной обратной связи. Возбуждение симпатического отдела вегетативной нервной системы стимулирует гормонообразовательную функцию щитовидной железы, возбуждение парасимпатического отдела – тормозит ее. Нарушения функции щитовидной железы проявляются ее гипофункцией и гиперфункцией. Если недостаточность функции развивается в детском возрасте, то это приводит к задержке роста, нарушению пропорций тела, полового и умственного развития. Такое патологическое состояние называется кретинизмом. У взрослых гипофункция щитовидной железы приводит к развитию патологического состояния – микседемы. При этом заболевании наблюдается торможение нервно-психической активности, что проявляется в вялости, сонливости, апатии, снижении интеллекта, уменьшении возбудимости симпатического отдела вегетативной нервной системы, нарушении половых функций, угнетении всех видов обмена веществ и снижении основного обмена. У таких больных увеличена масса тела за счет повышения количества тканевой жидкости и отмечается одутловатость лица. Отсюда и название этого заболевания: микседема – слизистый отек. Гипофункция щитовидной железы может развиться у людей, проживающих в местностях, где в воде и почве отмечается недостаток йода. Это так называемый эндемический зоб. Щитовидная железа при этом заболевании увеличена (зоб), возрастает количество фолликулов, однако из-за недостатка йода гормонов образуется мало, что приводит к соответствующим нарушениям в организме, проявляющимся в виде гипотиреоза. При гиперфункции щитовидной железы развивается заболевание тиреотоксикоз (диффузный токсический зоб, Базедова болезнь, болезнь Грейвса). Характерными признаками этого заболевания являются увеличение щитовидной железы (зоб), экзофтальм, тахикардия, повышение обмена веществ, особенно основного, потеря массы тела, увеличение аппетита, нарушение теплового баланса организма, повышение возбудимости и раздражительности. Кальцитонин, или тиреокальцитонин, вместе с паратгормоном околощитовидных желез участвует в регуляции кальциевого обмена. Под его влиянием снижается уровень кальция в крови (гипокальциемия). Это происходит в результате действия гормона на костную ткань, где он активирует функцию остеобластов и усиливает процессы минерализации. Функция остеокластов, разрушающих костную ткань, напротив, угнетается. В почках и кишечнике кальцитонин угнетает реабсорбцию кальция и усиливает обратное всасывание фосфатов. Продукция тиреокальцитонина регулируется уровнем кальция в плазме крови по типу обратной связи. При снижении содержания кальция тормозится выработка тиреокальцитонина, и наоборот.
Околощитовидные (паращитовидные) железы
Человек имеет 2 пары околощитовидных желез, расположенных на задней поверхности или погруженных внутри щитовидной железы. Главные, или оксифильные, клетки этих желез вырабатывают паратгормон, или паратирин, или паратиреоидный гормон (ПТГ). Паратгормон регулирует обмен кальция в организме и поддерживает его уровень в крови. В костной ткани паратгормон усиливает функцию остеокластов, что приводит к деминерализации кости и повышению содержания кальция в плазме крови (гиперкальциемия). В почках паратгормон усиливает реабсорбцию кальция. В кишечнике повышение реабсорбции кальция происходит благодаря стимулирующему действию паратгормона на синтез кальцитриола – активного метаболита витамина D3. Витамин D3 образуется в неактивном состоянии в коже под воздействием ультрафиолетового излучения. Под влиянием паратгормона происходит его активация в печени и почках. Кальцитриол повышает образование кальцийсвязывающего белка в стенке кишечника, что способствует обратному всасыванию кальция. Влияя на обмен кальция, паратгормон одновременно воздействует и на обмен фосфора в организме: он угнетает обратное всасывание фосфатов и усиливает их выведение с мочой (фосфатурия). Активность околощитовидных желез определяется содержанием кальция в плазме крови. Если в крови концентрация кальция возрастает, то это приводит к снижению секреции паратгормона. Уменьшение уровня кальция в крови вызывает усиление выработки паратгормона. Удаление околощитовидных желез у животных или их гипофункция у человека приводит к усилению нервно-мышечной возбудимости, что проявляется фибриллярными подергиваниями одиночных мышц, переходящих в спастические сокращения групп мышц, премущественно конечностей, лица и затылка. Животное погибает от тетанических судорог. Гиперфункция околощитовидных желез приводит к деминерализации костной ткани и развитию остеопороза. Гиперкальциемия усиливает склонность к камнеобразованию в почках, способствует развитию нарушений электрической активности сердца, возникновению язв в желудочно-кишечном тракте в результате повышенных количеств гастрина и НСl в желудке, образование которых стимулируют ионы кальция.Надпочечники
Надпочечники являются парными железами. Это эндокринный орган, который имеет жизненно важное значение. В надпочечниках выделяют два слоя – корковый и мозговой. Корковый слой имеет мезодермальное происхождение, мозговой слой развивается из зачатка симпатического ганглия.Гормоны коры надпочечников
В коре надпочечников выделяют 3 зоны: наружную – клубочковую, среднюю – пучковую и внутреннюю – сетчатую. В клубочковой зоне продуцируются в основном минералокортикоиды, в пучковой – глюкокортикоиды, в сетчатой – половые гормоны преимущественно андрогены). По химическому строению гормоны коры надпочечников являются стероидами. Механизм действия всех стероидных гормонов заключается в прямом влиянии на генетический аппарат ядра клеток, стимуляции синтеза соответствующих РНК, активации синтеза транспортирующих катионы белков и ферментов, а также повышении проницаемости мембран для аминокислот.Минералокортикоиды.
К этой группе относятся альдостерон, дезоксикортикостерон, 18-оксикортикостерон, 18-оксидезоксикортикостерон. Эти гормоны участвуют в регуляции минерального обмена. Основным представителем минералокортикоидов является альдостерон. Альдостерон усиливает реабсорбцию ионов натрия и хлора в дистальных почечных канальцах и уменьшает обратное всасывание ионов калия. В результате этого уменьшается выделение натрия с мочой и увеличивается выведение калия. В процессе реабсорбции натрия пассивно возрастает и реабсорбция воды. За счет задержки воды в организме увеличивается объем циркулирующей крови, повышается уровень артериального давления, уменьшается диурез. Аналогичное влияние на обмен натрия и калия альдостерон оказывает в слюнных и потовых железах. Альдостерон способствует развитию воспалительной реакции. Его провоспалительное действие связано с усилением экссудации жидкости из просвета сосудов в ткани и отечности тканей. При повышенной продукции альдостерона усиливается также секреция водородных ионов и аммония в почечных канальцах, что может привести к изменению кислотно-основного состояния – алкалозу. В регуляции уровня альдостерона в крови имеют место несколько механизмов, основной из них – это ренин-ангиотензин-альдостероновая система. В небольшой степени продукцию аль-достерона стимулирует АКТГ аденогипофиза. Гипонатриемия или гиперкалиемия по механизму обратной связи стимулирует выработку альдостерона. Антагонистом альдостерона является натрийуретический гормон предсердий.Глюкокортикоиды.
К глюкокортикоидным гормонам относятся кортизол, кортизон, кортикостерон, 11-дезоксикортизол, 11-дегидрокортикостерон. У человека наиболее важным глюкокортикоидом является кортизол.Эти гормоны оказывают влияние на обмен углеводов, белков и жиров: 1. Глюкокортикоиды вызывают повышение содержания глюкозы в плазме крови (гипергликемия). Этот эффект обусловлен стимулированием процессов глюконеогенеза в печени, т. е. образования глюкозы из аминокислот и жирных кислот. Глюкокортикоиды угнетают активность фермента гексокиназы, что ведет к уменьшению утилизации глюкозы тканями. Глюкокортикоиды являются антагонистами инсулина в регуляции углеводного обмена. 2. Глюкокортикоиды оказывают катаболическое влияние на белковый обмен. Вместе с тем они обладают и выраженным анти-анаболическим действием, что проявляется снижением синтеза особенно мышечных белков, так как глюкокортикоиды угнетают транспорт аминокислот из плазмы крови в мышечные клетки. В результате снижается мышечная масса, может развиться остеопороз, уменьшается скорость заживления ран. 3. Действие глюкокортикоидов на жировой обмен заключается в активации липолиза, что приводит к увеличению концентрации жирных кислот в плазме крови. 4. Глюкокортикоиды угнетают все компоненты воспалительной реакции: уменьшают проницаемость капилляров, тормозят экссудацию и снижают отечность тканей, стабилизируют мембраны лизосом, что предотвращает выброс протеолитических ферментов, способствующих развитию воспалительной реакции, угнетают фагоцитоз в очаге воспаления. Глюкокортикоиды уменьшают лихорадку. Это действие связано с уменьшением выброса интерлейкина-1 из лейкоцитов, который стимулирует центр теплопродукции в гипоталамусе. 5. Глюкокортикоиды оказывают противоаллергическое действие. Это действие обусловлено эффектами, лежащими в основе противовоспалительного действия: угнетение образования факторов, усиливающих аллергическую реакцию, снижение экссудации, стабилизация лизосом. Повышение содержания глюкокортикоидов в крови приводит к уменьшению числа эозинофилов, концентрация которых обычно увеличена при аллергических реакциях. 6. Глюкокортикоиды угнетают как клеточный, так и гуморальный иммунитет. Они снижают продукцию Ти В-лимфоцитов, уменьшают образование антител, снижают иммунологический надзор. При длительном приеме глюкокортикоидов может возникнуть инволюция тимуса и лимфоидной ткани. Ослабление защитных иммунных реакций организма является серьезным побочным эффектом при длительном лечении глюкокортикоидами, так как возрастает вероятность присоединения вторичной инфекции. Кроме того, усиливается и опасность развития опухолевого процесса из-за депрессии иммунологического надзора. С другой стороны, эти эффекты глюкокортикоидов позволяют рассматривать их как активных иммунодепрессантов. 7. Глюкокортикоиды повышают чувствительность гладких мышц сосудов к катехоламинам, что может привести к возрастанию артериального давления. Этому способствует и их небольшое минералокортикоидное действие: задержка натрия и воды в организме. 8. Глюкокортикоиды стимулируют секрецию соляной кислоты.
Образование глюкокортикоидов корой надпочечников стимулируется АКТГ аденогипофиза. Избыточное содержание глюкокортикоидов в крови приводит к торможению синтеза АКТГ и кортиколиберина гипоталамусом. Таким образом, гипоталамус, аденогипофиз и кора надпочечников объединены функционально и поэтому выделяют единую гипоталамо-гипофизарно-надпочечниковую систему. При острых стрессовых ситуациях быстро повышается уровень глюкокортикоидов в крови. В связи с метаболическими эффектами они быстро обеспечивают организм энергетическим материалом. Содержание глюкокортикоидов в крови самое высокое в 6–8 часов утра. Гипофункция коры надпочечников проявляется снижением содержания кортикоидных гормонов и носит название Аддисоновой (бронзовой) болезни. Главными симптомами этого заболевания являются: адинамия, снижение объема циркулирующей крови, артериальная гипотония, гипогликемия, усиленная пигментация кожи, головокружение, неопределенные боли в области живота, поносы. При опухолях надпочечников может развиться гиперфункция коры надпочечников с избыточным образованием глюкокортикоидов. Это так называемый первичный гиперкортицизм, или синдром Иценко – Кушинга. Клинические проявления этого синдрома такие же, как и при болезни Иценко – Кушинга.
Половые гормоны
Половые гормоны играют определенную роль только в детском возрасте, когда внутрисекреторная функция половых желез еще слабо развита. Половые гормоны коры надпочечников способствуют развитию вторичных половых признаков. Они также стимулируют синтез белка в организме. АКТГ стимулирует синтез и секрецию андрогенов. При избыточной выработке половых гормонов корой надпочечников развивается адреногенитальный синдром. Если происходит избыточное образование гормонов одноименного пола, то ускоряется процесс полового развития, если противоположного пола – то появляются вторичные половые признаки, присущие другому полу.Гормоны мозгового слоя надпочечников
Мозговой слой надпочечников вырабатывает катехоламины: адреналин и норадреналин. На долю адреналина приходится около 80%, на долю норадреналина – около 20% гормональной секреции. Секреция адреналина и норадреналина осуществляется хромаффинными клетками из аминокислоты тирозина (тирозинДОФА-дофамин-норадреналин-адреналин). Инактивация осуществляется моноаминоксидазой и катехол-о-метилтрансферазой. Физиологические эффекты адреналина и норадреналина аналогичны активации симпатической нервной системы, но гормональный эффект является более длительным. В то же время продукция этих гормонов усиливается при возбуждении симпатического отдела вегетативной нервной системы. Адреналин стимулирует деятельность сердца, суживает сосуды, кроме коронарных, сосудов легких, головного мозга, работающих мышц, на которые он оказывает сосудорасширяющее действие. Адреналин расслабляет мышцы бронхов, тормозит перистальтику и секрецию кишечника и повышает тонус сфинктеров, расширяет зрачок, уменьшает потоотделение, усиливает процессы катаболизма и образования энергии. Адреналин выраженно влияет на углеводный обмен, усиливая расщепление гликогена в печени и мышцах, в результате чего повышается содержание глюкозы в плазме крови. Адреналин активирует липолиз. Катехоламины участвуют в активации термогенеза. Действия адреналина и норадреналина опосредованы их взаимодействием с аи p-адренорецепторами, которые, в свою очередь, фармакологически подразделены на α1, α2, β1, β2-рецепторы (см. главу 4). Адреналин имеет большее сродство к (β-адренорецепторам, норадреналин – к α-адренорецепторам. В клинической практике широко используются вещества, избирательно возбуждающие или блокирующие эти рецепторы. Избыточная секреция катехоламинов отмечается при опухоли хромаффинного вещества надпочечников – феохромоцитоме. К основным ее проявлениям относятся: пароксизмальные повышения артериального давления, приступы тахикардии, одышка. При воздействии на организм различных по своей природе чрезвычайных или патологических факторов (травма, гипоксия, охлаждение, бактериальная интоксикация и т. д.) наступают однотипные неспецифические изменения в организме, направленные на повышение его неспецифической резистентности, названные общим адаптационным синдромом (Г. Селье). В развитии адаптационного синдрома основную роль играет гипофизарно-надпочечниковая система.Поджелудочная железа
Поджелудочная железа относится к железам со смешанной функцией. Эндокринная функция осуществляется за счет продукции гормонов панкреатическими островками (островками Лангерганса). Островки расположены преимущественно в хвостовой части железы, и небольшое их количество находится в головном отделе. В островках имеется несколько типов клеток: α, β, d, G и ПП. α-клетки вырабатывают глюкагон, β-клетки продуцируют инсулин, d-клетки синтезируют соматостатин, который угнетает секрецию инсулина и глюкагона. G-клетки вырабатывают гастрин, в ПП-клетках происходит выработка небольшого количества панкреатического полипептида, являющегося антагонистом холецистокинина. Основную массу составляют р-клетки, вырабатывающие инсулин. Инсулин влияет на все виды обмена веществ, но прежде всего на углеводный. Под воздействием инсулина происходит уменьшение концентрации глюкозы в плазме крови (гипогликемия). Это связано с тем, что инсулин способствует превращению глюкозы в гликоген в печени и мышцах (гликогенез). Он активирует ферменты, участвующие в превращении глюкозы в гликоген печени, и ингибирует ферменты, расщепляющие гликоген. Инсулин также повышает проницаемость клеточной мембраны для глюкозы, что усиливает ее утилизацию. Кроме того, инсулин угнетает активность ферментов, обеспечивающих глюконеогенез, за счетчего тормозится образование глюкозы из аминокислот. Инсулин стимулирует синтез белка из аминокислот и уменьшает катаболизм белка. Инсулин регулирует жировой обмен, усиливая процессы липогенеза: способствует образованию жирных кислот из продуктов углеводного обмена, тормозит мобилизацию жира из жировой ткани и способствует отложению жира в жировых депо. Образование иисулина регулируется уровнем глюкозы в плазме крови. Гипергликемия способствует увеличению выработки инсулина, гипогликемия уменьшает образование и поступление гормона в кровь. Некоторые гормоны желудочно-кишечного тракта, такие как желудочный ингибирующий пептид, холецистокинин, секретин, увеличивают выход инсулина. Блуждающий нерв и ацетилхолин усиливают продукцию инсулина, симпатические нервы и норадреналин подавляют секрецию инсулина. Антагонистами инсулина по характеру действия на углеводный обмен являются глюкагон, АКТГ, соматотропин, глюкокортикоиды, адреналин, тироксин. Введение этих гормонов вызывает гипергликемию. Недостаточная секреция инсулина приводит к заболеванию, которое получило название сахарного диабета. Основными симптомами этого заболевания являются гипергликемия, глюкозурия, полиурия, полидипсия. У больных сахарным диабетом нарушается не только углеводный, но и белковый и жировой обмен. Усиливается липолиз с образованием большого количества несвязанных жирных кислот, происходит синтез кетоновых тел. Катаболизм белка приводит к снижению массы тела. Интенсивное образование кислых продуктов расщепления жиров и дезаминирования аминокислот в печени могут вызвать сдвиг реакции крови в сторону ацидоза и развитие гипергликемической диабетической комы, которая проявляется потерей сознания, нарушениями дыхания и кровообращения. Избыточное содержание инсулина в крови (например, при опухоли островковых клеток или при передозировке экзогенного инсулина) вызывает гипогликемию и может привести к нарушению энергетического обеспечения мозга и потере сознания (гипогликемической коме). α-клетки островков Лангерганса синтезируют глюкагон, который является антагонистом инсулина. Под влиянием глюкагона происходит распад гликогена в печени до глюкозы. В результате этого повышается содержание глюкозы в крови. Глюкагон способствует мобилизации жира из жировых депо. Секреция глюкагона также зависит от концентрации глюкозы в крови. Гипергликемия тормозит образование глюкагона, гипогликемия, напротив, увеличивает.Половые железы
Половые железы, или гонады – семенники (яички) у мужчин и яичники у женщин относятся к числу желез со смешанной секрецией. Внешняя секреция связана с образованием мужских и женских половых клеток – сперматозоидов и яйцеклеток. Внутрисекреторная функция заключается в секреции мужских и женских половых гормонов и их выделении в кровь. Как семенники, так и яичники синтезируют и мужские и женские половые гормоны, но у мужчин значительно преобладают андрогены, а у женщин – эстрогены. Половые гормоны способствуют эмбриональной дифференцировке, в последующем развитию половых органов и появлению вторичных половых признаков, определяют половое созревание и поведение человека. В женском организме половые гормоны регулируют овариально-менструальный цикл, а также обеспечивают нормальное протекание беременности и подготовку молочных желез к секреции молока.Мужские половые гормоны (андрогены)
Интерстициальные клетки яичек (клетки Лейдига) вырабатывают мужские половые гормоны. В небольшом количестве они также вырабатываются в сетчатой зоне коры надпочечников у мужчин и женщин и в наружном слое яичников у женщин. Все половые гормоны являются стероидами и синтезируются из одного предшественника – холестерина. Наиболее важным из андрогенов является тестостерон. Тестостерон разрушается в печени, а его метаболиты экскретируются с мочой в виде 17-кетостероидов. Концентрация тестостерона в плазме крови имеет суточные колебания. Максимальный уровень отмечается в 7 – 9 часов утра, минимальный – с 24 до 3 часов. Тестостерон участвует в половой дифференцировке гонады и обеспечивает развитие первичных (рост полового члена и яичек) и вторичных (мужской тип оволосения, низкий голос, характерное строение тела, особенности психики и поведения) половых признаков, появление половых рефлексов. Гормон участвует и в созревании мужских половых клеток – сперматозоидов, которые образуются в сперматогенных эпителиальных клетках семенных канальцев. Тестостерон обладает выраженным анаболическим действием, т. е. увеличивает синтез белка, особенно в мышцах, что приводит к увеличению мышечной массы, к ускорению процессов роста и физического развития. За счет ускорения образования белковой матрицы кости, а также отложения в ней солей кальция гормон обеспечивает рост, толщину и прочность кости. Способствуя окостенению эпифизарных хрящей, половые гормоны практически останавливают рост костей. Тестостерон уменьшает содержание жира в организме. Гормон стимулирует эритропоэз, чем объясняется большее количество эритроцитов у мужчин, чем у женщин. Тестостерон оказывает влияние на деятельность центральной нервной системы, определяя половое поведение и типичные психофизиологические черты мужчин. Продукция тестостерона регулируется лютеинизирующим гормоном аденогипофиза по механизму обратной связи. Повышенное содержание в крови тестостерона тормозит выработку лютропина, сниженное – ускоряет. Созревание сперматозоидов происходит под влиянием ФСГ. Клетки Сертоли, наряду с участием в сперматогенезе, синтезируют и секретируют в просвет семенных канальцев гормон ингибин, который тормозит продукцию ФСГ. Недостаточность продукции мужских половых гормонов может быть связана с развитием патологического процесса в паренхиме яичек (первичный гипогонадизм) и вследствие гипоталамогигюфизарной недостаточности (вторичный гипогонадизм). Различают врожденный и приобретенный первичный гипогонадизм. Причинами врожденного являются дисгенезии семенных канальцев, дисгенезия или аплазия яичек. Приобретенные нарушения функции яичек возникают вследствие хирургической кастрации, травм, туберкулеза, сифилиса, гонореи, осложнений орхита, например при эпидемическом паротите. Проявления заболевания зависят от возраста, когда произошло повреждение яичек. При врожденном недоразвитии яичек или при повреждении их до полового созревания возникает евнухоидизм. Основные симптомы этого заболевания: недоразвитие внутренних и наружных половых органов, а также вторичных половых признаков. У таких мужчин отмечаются небольшие размеры туловища и длинные конечности, увеличение отложения жира на груди, бедрах и нижней части живота, слабое развитие мускулатуры, высокий тембр голоса, увеличение молочных желез (гинекомастия), отсутствие либидо, бесплодие. При заболевании, развившемся в постпубертатном возрасте, недоразвитие половых органов менее выражено. Либидо часто сохранено. Диспропорций скелета нет. Наблюдаются симптомы демаскулинизации: уменьшение оволосения, снижение мышечной силы, ожирение по женскому типу, ослабление потенции вплоть до импотенции, бесплодие. Усиленная продукция мужских половых гормонов в детском возрасте приводит к преждевременному половому созреванию. Избыток тестостерона в постпубертатном возрасте вызывает гиперсексуальность и усиленный рост волос.Женские половые гормоны
Эти гормоны вырабатываются в женских половых железах – яичниках, во время беременности – в плаценте, а также в небольших количествах клетками Сертоли семенников у мужчин. В фолликулах яичников осуществляется синтез эстрогенов, желтое тело яичника продуцирует прогестерон. К эстрогенам относятся эстрон, эстрадиол и эстриол. Наибольшей физиологической активностью обладает эстрадиол. Эстрогены стимулируют развитие первичных и вторичных женских половых признаков. Под их влиянием происходит рост яичников, матки, маточных труб, влагалища и наружных половых органов, усиливаются процессы пролиферации в эндометрии. Эстрогены стимулируют развитие и рост молочных желез. Кроме этого эстрогены влияют на развитие костного скелета, ускоряя его созревание. За счет действия на эпифизарные хрящи они тормозят рост костей в длину. Эстрогены оказывают выраженный анаболический эффект, усиливают образование жира и его распределение, типичное для женской фигуры, а также способствуют оволосению по женскому типу. Эстрогены задерживают азот, воду, соли. Под влиянием этих гормонов изменяется эмоциональное и психическое состояние женщин. Во время беременности эстрогены способствуют росту мышечной ткани матки, эффективному маточно-плацентарному кровообращению, вместе с прогестероном и пролактином – развитию молочных желез. При овуляции в желтом теле яичника, которое развивается на месте лопнувшего фолликула, вырабатывается гормон – прогестерон. Главная функция прогестерона – подготовка эндометрия к имплантации оплодотворенной яйцеклетки и обеспечение нормального протекания беременности. Если оплодотворение не наступает, желтое тело дегенерирует. Во время беременности прогестерон вместе с эстрогенами обусловливает морфологические перестройки в матке и молочных железах, усиливая процессы пролиферации и секреторной активности. В результате этого в секрете желез эндометрия возрастают концентрации липидов и гликогена, необходимых для развития эмбриона. Гормон угнетает процесс овуляции. У небеременных женщин прогестерон участвует в регуляции менструального цикла. Прогестерон усиливает основной обмен и повышает базальную температуру тела, что используется в практике для определения времени наступления овуляции. Прогестерон обладает антиальдостероновым эффектом. Концентрации тех или иных женских половых гормонов в плазме крови зависят от фазы менструального цикла.Овариально-менструальный (менструальный) цикл
Менструальный цикл обеспечивает интеграцию во времени различных процессов, необходимых для репродуктивной функции: созревание яйцеклетки и овуляцию, периодическую подготовку эндометрия к имплантации оплодотворенной яйцеклетки и др. Различают яичниковый цикл и маточный цикл. В среднем весь менструальный цикл у женщин продолжается 28 дней. Возможны колебания от 21 до 32 дней. Яичниковый цикл состоит из трех фаз: фолликулярной (с 1-го по 14-й день цикла), овуляторной (13-й день цикла) и лютеиновой (с 15-го по 28-й день цикла). Количество эс-трогенов преобладает в фолликулярной фазе, достигая максимума за сутки до овуляции. В лютеиновую фазу преобладает прогестерон. Маточный цикл состоит из 4 фаз: десквамации (продолжительность 3 – 5 дней), регенерации (до 5 -6-го дня цикла), пролиферации (до 14-го дня) и секреции (от 15 до 28-го дня). Эстрогены обусловливают пролиферативную фазу, во время которой происходит утолщение слизистой оболочки эндометрия и развитие его желез. Прогестерон способствует секреторной фазе. Продукция эстрогенов и прогестерона регулируется гонадотропными гормонами аденогипофиза, выработка которых увеличивается у девочек в возрасте 9–10 лет. При высоком содержании в крови эстрогенов угнетается секреция ФСГ и ЛГ аденогипофизом, а также гонадолиберина гипоталамусом. Прогестерон тормозит продукцию ФСГ. В первые дни менструального цикла под влиянием ФСГ происходит созревание фолликула. В это время увеличивается и концентрация эстрогенов, которая зависит не только от ФСГ, но и ЛГ. В середине цикла резко возрастает секреция ЛГ, что приводит к овуляции. После овуляции резко повышается концентрация прогестерона. По обратным отрицательным связям подавляется секреция ФСГ и ЛГ, что препятствует созреванию нового фолликула. Происходит дегенерация желтого тела. Падает уровень прогестерона и эстрогенов. Центральная нервная система участвует в регуляции нормального менструального цикла. При изменении функционального состояния ЦНС под влиянием различных экзогенных и психологических факторов (стресс) менструальный цикл может нарушаться вплоть до прекращения менструации. Недостаточная продукция женских половых гормонов может возникнуть при непосредственном воздействии патологического процесса на яичники. Это так называемый первичный гипогонадизм. Вторичный гипогонадизм встречается при снижении продукции гонадотропинов аденогипофизом, в результате чего наступает резкое уменьшение секреции эстрогенов яичниками. Первичная недостаточнось яичников может быть врожденной вследствие нарушений половой дифференцировки, а также приобретенной в результате хирургического удаления яичников или повреждения инфекционным процессом (сифилис, туберкулез). При повреждении яичников в детском возрасте отмечается недоразвитие матки, влагалища, первичная аменорея (отсутствие менструаций), недоразвитие молочных желез, отсутствие или скудное оволосение на лобке и под мышками, евнухоидные пропорции: узкий таз, плоские ягодицы. При развитии заболевания у взрослых недоразвитие половых органов менее выражено. Возникает вторичная аменорея, отмечаются различные проявления вегетоневроза.Плацента
Плацента человека вырабатывает прогестерон, предшественники эстрогенов, хорионический гонадотропин, хориальный соматотропин, хориональный тиреотропин, АКТГ, окситоцин, релаксин. Гормоны плаценты обеспечивают нормальное протекание беременности. Наиболее изучен хорионический гонадотропин. По своим физиологическим свойствам он близок к гонадотропинам гипофиза. Гормон оказывает эффект на процессы дифференцировки и развитие плода, а также на метаболизм матери: задерживает воду и соли, стимулирует секрецию антидиуретического гормона и сам обладает антидиуретическим действием, стимулирует механизмы иммунитета. Из-за тесной функциональной связи плаценты с плодом принято говорить о «фетоплацентарном комплексе» или «фетоплацентарной системе». Например, синтез эстриола в плаценте идет из предшественника дегидроэпиандростерона, который образуется в надпочечниках плода.Эпифиз
Эпифиз (верхний мозговой придаток, пинеальная железа, шишковидная железа) является железой нейроглиального происхождения. Вырабатывает в первую очередь серотонин и мелатонин, а также норадреналин, гистамин. В эпифизе обнаружены пептидные гормоны и биогенные амины, что позволяет отнести его клетки (пинеалоциты) к клеткам АПУД-системы. Так, например, в нем вырабатываются аргинин-вазотоцин (стимулирует секрецию пролактина); эпифиз-гормон, или фактор «Милку»; эпиталамин – суммарный пептидный комплекс и др. Основной функцией эпифиза является регуляция циркадных (суточных) биологических ритмов, эндокринных функций и метаболизма и приспособление организма к меняющимся условиям освещенности. Избыток света тормозит превращение серотонина в мелатонин и другие метоксииндолы и способствует накоплению серотонина и его метаболитов. В темноте, напротив, усиливается синтез мелатонина. Этот процесс идет под влиянием ферментов, активность которых также зависит от освещенности. Учитывая, что эпифиз регулирует целый ряд важных реакций организма, а в связи со сменой освещенности эта регуляция циклична, можно считать его регулятором «биологических часов» в организме. Влияние эпифиза на эндокринную систему носит в основном ингибиторный характер. Доказано действие его гормонов на систему гипоталамус-гипофиз-гонады. Мелатонин угнетает секрецию гонадотропинов как на уровне секреции либеринов гипоталамуса, так и на уровне аденогипофиза. Мелатонин определяет ритмичность гонадотропных эффектов, в том числе продолжительность менструального цикла у женщин. Гормоны гипофиза угнетают биоэлектрическую активность мозга и нервно-психическую деятельность, оказывая снотворный, анальгезирующий и седативный эффект. В эксперименте экстракты эпифиза вызывают инсулиноподобный (гипогликемический), паратиреоподобный (гиперкальциемический) и диуретический эффекты.Тимус
Тимус, или вилочковая железа – парный орган, расположенный в верхнем средостении. После 30 лет подвергается возрастной инволюции. В вилочковой железе наряду с образованием из стволовых клеток костного мозга Т-лимфоцитов продуцируются гормональные факторы – тимозин и тимопоэтин. Гормоны обеспечивают дифференцировку Т-лимфоцитов и играют определенную роль в клеточных иммунных реакциях. Имеются также сведения, что гормоны обеспечивают синтез клеточных рецепторов к медиаторам и гормонам, например, рецепторов ацетилхолина на постсинаптических мембранах нервно-мышечных синапсов. Эндокринной активностью обладают также и другие органы. Почки синтезируют и секретируют в кровь ренин, эритропоэтин. В предсердиях продуцируется натрийуретический гормон, или атриопептид. Клетки слизистой оболочки желудка и двенадцатиперстной кишки секретируют большое количество пептидных соединений, значительная часть которых выявляется также в мозге: секретин, гастрин, холецистокинин-панкреозимин, гастроингибирующий пептид, бомбезин, мотилин, соматостатин, нейротензин, панкреатический полипептид и др. Более подробно об этих веществах изложено в соответствующих разделах учебника.Гормональные средства, используемые в фармакологические целях
Многие гормоны применяются в медицинской практике в качестве средств заместительной терапии при гипофункции соответствующих желез внутренней секреции, а также при лечении некоторых патологических процессов. Гормоны, не имеющие видовой специфичности, используются в виде экстрактов, выделенных из организма животных. Установление химической структуры эндогенных гормонов позволило осуществлять направленный синтез как самих гормонов, так и их активных аналогов и антигормонов. Гормоны, полученные синтетическим путем, а также их аналоги обладают более избирательным действием, оказывают свои влияния в меньших дозах, а значит, вызывают меньше побочных, нежелательных эффектов. Так, например, из задней доли гипофиза крупного рогатого скота и свиней получают гормональный препарат питуитрин, обладающий окситоциновой (маточной), вазопрессорной и антидиуретической активностью. Полученный синтетическим путем окситоцин обладает более избирательным действием на матку и применяется для вызывания и стимуляции родовой деятельности. Препарат задней доли гипофиза адиурекрин, основным действующим веществом которого является вазопрессин, используют для лечения несахарного диабета. Из передней доли гипофиза получают кортикотропин. (назначают при гипофунции коры надпочечников), лактин, обладающий активностью пролактина (стимулирует лактацию в послеродовом периоде). Для ускорения роста используют фармакологические препараты соматотропин и соматолиберин человека, так как эти гормоны обладают видовой специфичностью. В качестве лекарственных средств, обладающих активностью ФСГ, применяют гонадотропин менопаузный, получаемый из мочи женщин, находящихся в менопаузе, а с активностью ЛГ – гонадотропин хорионический, выделяемый из мочи беременных женщин. При гипотиреозе применяют гормональный препарат из щитовидных желез убойного скота тиреоидин (тироксин и трийодтиронин) и синтетический препарат трийодтиронин. Для лечения сахарного диабета используют инсулин из поджелудочной железы свиней и человека. При недостаточной функции яичников применяют эстрон (фолликулин), выделенный из мочи беременных женщин и животных. Синтетический гормон прогестерон назначают при бесплодии и невынашивании беременности. Способность прогестинов блокировать высвобождение рилизинг-факторов гипоталамуса, угнетать секрецию гипофизом гонадотропных гормонов и тормозить овуляцию явилась основанием для использования прогестинов в качестве контрацептивных средств. Контрацептивное действие усиливается при сочетанном применении прогестинов с эстрогенами. При нарушении половой функции у мужчин применяют синтетический гормон тестостерон или синтетический аналог метилтестостерон. Наиболее широкое применение в медицинской практике имеют гормоны коры надпочечников – кортикостероиды, получаемые в настоящее время синтетическим путем: минералокортикоид – дезоксикортикостерона ацетат и глюкокортикоиды – кортизон, гидрокортизон. Более активными, чем природные глюкокортикоиды, являются их синтетические аналоги (преднизон, преднизолон, дексаметазон). Они используются не только при гипофункции коры надпочечников, но и как противовоспалительные, противоаллергические средства, в качестве иммунодепрессантов при трансплантации органов и тканей для торможения реакции отторжения. Введение этих веществ в большом количестве может вызвать описанные выше эффекты глюкокортикоидов, но в более выраженной форме, и явиться побочным действием этих веществ. Так, надо учитывать, что, подавляя воспалительные процессы, глюкокортикоиды одновременно ослабляют защитные иммунные реакции организма. Нежелательным побочным действием является также торможение образования рубца при заживлении язвы желудка или других внутренних повреждений тканей. Так как глюкокортикоиды стимулируют секрецию соляной кислоты, их не следует назначать больным с язвой желудка. Разрушение белкового матрикса костей может привести к патологическому состоянию – остеопорозу. При длительном лечении глкжокортикоидами может развиться преддиабетическое состояние вплоть до сахарного диабета (стероидный диабет), так как эти вещества являются антагонистами инсулина. Знание биоритмов выделения гормонов необходимо учитывать в клинической практике при распределении суточной дозы гормонов. Кроме того, при длительном лечении кортикоидными гормонами необходимо помнить, что эти лекарства нельзя резко отменять, так как при длительном лечении экзогенными кортикоидами тормозится выработка АКТГ аденогипофизом по механизму отрицательной обратной связи. В этих условиях ослабляется или даже полностью прекращается выработка корой надпочечников собственных эндогенных кортикоидов. Если резко прекратить введение экзогенных кортикоидов, развивается острая надпочечниковая недостаточноть, которая может привести к летальному исходу. Это патологическое состояние получило название «синдром отмены». Для предотвращения атрофии надпочечников надо одновременно назначать кортикотропин.Глава 6. Физиология крови
Кровь, лимфа, тканевая, спинномозговая, плевральная, суставная и другие жидкости образуют внутреннюю среду организма. Внутренняя среда отличается относительным постоянством своего состава и физико-химических свойств, что создает оптимальные условия для нормальной жизнедеятельности клеток организма. Впервые положение о постоянстве внутренней среды организма сформулировал более 100 лет тому назад физиолог Ююд Бернар. Он пришел к заключению, что «постоянство внутренней среды организма есть условие независимого существования», т. е. жизни, свободной от резких колебаний внешней среды. В 1929 г. Уолтер Кэннон ввел термин гомеостаз. В настоящее время под гомеостазом понимают как динамическое постоянство внутренней среды организма, так и регулирующие механизмы, которые обеспечивают это состояние. Главная роль в поддержании гомеостаза принадлежит крови. В 1939 г. Г. Ф. Ланг создал представление о системе крови, в которую он включил периферическую кровь, циркулирующую по сосудам, органы кроветворения и кроверазрушения, а также регулирующий нейрогуморальный аппарат.Основные функции крови
Кровь, циркулирующая в сосудах, выполняет перечисленные ниже функции. Транспортная – перенос различных веществ: кислорода, углекислого газа, питательных веществ, гормонов, медиаторов, электролитов, ферментов и др. Дыхательная (разновидность транспортной функции) – перенос кислорода от легких к тканям организма, углекислого газа – от клеток к легким. Трофическая (разновидность транспортной функции) – перенос основных питательных веществ от органов пищеварения к тканям организма. Экскреторная (разновидность транспортной функции) – транспорт конечных продуктов обмена веществ (мочевины, мочевой кислоты и др.), избытка воды, органических и минеральных веществ к органам их выделения (почки, потовые железы, легкие, кишечник). Терморегуляторная – перенос тепла от более нагретых органов к менее нагретым. Защитная – осуществление неспецифического и специфического иммунитета; свертывание крови предохраняет от кровопотери при травмах. Регуляторная (гуморальная) – доставка гормонов, пептидов, ионов и других физиологически активных веществ от мест их синтеза к клеткам организма, что позволяет осуществлять регуляцию многих физиологических функций. Гомеостатическая – поддержание постоянства внутренней среды организма (кислотно-основного равновесия, водно-электролитного баланса и др.).Объем и физико-химические свойства крови
Объем крови – общее количество крови в организме взрослого человека составляет в среднем 6 – 8% от массы тела, что соответствует 5–6 л. Повышение общего объема крови называют гиперволемией, уменьшение – гиповолемией. Относительная плотность крови – 1.050-1.060 зависит в основном от количества эритроцитов. Относительная плотность плазмы крови – 1.025-1.034, определяется концентрацией белков. Вязкость крови – 5 усл.ед., плазмы – 1,7 – 2,2 усл.ед., если вязкость воды принять за 1. Обусловлена наличием в крови эритроцитов и в меньшей степени белков плазмы. Осмотическое давление крови – сила, с которой растворитель переходит через полунепроницаемую мембрану из менее в более концентрированный раствор. Осмотическое давление крови вычисляют криоскопическим методом путем определения точки замерзания крови (депрессии), которая для нее равна 0,56 – 0,58°С. Осмотическое давление крови в среднем составляет 7,6 атм. Оно обусловлено растворенными в ней осмотически активными веществами, главным образом неорганическими электролитами, в значительно меньшей степени – белками. Около 60% осмотического давления создается солями натрия (NaCl). Осмотическое давление определяет распределение воды между тканями и клетками. Функции клеток организма могут осуществляться лишь при относительной стабильности осмотического давления. Если эритроциты поместить в солевой раствор, имеющий осмотическое давление, одинаковое с кровью, они не изменяют свой объем. Такой раствор называют изотоническим, или физиологическим. Это может быть 0,85% раствор хлористого натрия. В растворе, осмотическое давление которого выше осмотического давления крови, эритроциты сморщиваются, так как вода выходит из них в раствор. В растворе с более низким осмотическим давлением, чем давление крови, эритроциты набухают в результате перехода воды из раствора в клетку. Растворы с более высоким осмотическим давлением, чем давление крови, называются гипертоническими, а имеющие более низкое давление – гипотоническими. Онкотическое давление крови – часть осмотического давления, создаваемого белками плазмы. Оно равно 0,03 – 0,04 атм, или 25 – 30 мм рт.ст. Онкотическое давление в основном обусловлено альбуминами. Вследствие малых размеров и высокой гидрофильное™ они обладают выраженной способностью притягивать к себе воду, за счет чего она удерживается в сосудистом русле. При снижении онкотического давления крови происходит выход воды из сосудов в интерстициальное пространство, что приводит к отеку тканей.Кислотно-основное состояние крови (КОС).
Активная реакция крови обусловлена соотношением водородных и гидроксильных ионов. Д/iH определения активной реакции крови используют водородный показатель рН – концентрацию водородных ионов, которая выражается отрицательным десятичным логарифмом молярной концентрации ионов водорода. В норме рН – 7,36 (реакция слабоосновная); артериальной крови – 7,4; венозной – 7,35. При различных физиологических состояниях рН крови может изменяться от 7,3 до 7,5. Активная реакция крови является жесткой константой, обеспечивающей ферментативную деятельность. Крайние пределы рН крови, совместимые с жизнью, равны 7,0 – 7,8. Сдвиг реакции в кислую сторону называется ацидозом, который обусловливается увеличением в крови водородных ионов. Сдвиг реакции крови в щелочную сторону называется алкалозом. Это связано с увеличением концентрации гидроксильных ионов ОН и уменьшением концентрации водородных ионов. В организме человека всегда имеются условия для сдвига активной реакции крови в сторону ацидоза или алкалоза, которые могут привести к изменению рН крови. В клетках тканей постоянно образуются кислые продукты. Накоплению кислых соединений способствует потребление белковой пищи. Напротив, при усиленном потреблении растительной пищи в кровь поступают основания. Поддержание постоянства рН крови является важной физиологической задачей и обеспечивается буферными системами крови. К буферным системам крови относятся гемоглобиновая, карбонатная, фосфатная и белковая. Буферные системы нейтрализуют значительную часть по-ступающих в кровь кислот и щелочей, тем самым препятствуя сдвигу активной реакции крови. В организме в процессе метаболизма в большей степени образуется кислых продуктов. Поэтому запасы щелочных веществ в крови во много раз превышают запасы кислых. Их рассматривают как щелочной резерв крови. Гемоглобиновая буферная система на 75% обеспечивает буферную емкость крови. Оксигемоглобин является более сильной кислотой, чем восстановленный гемоглобин. Оксигемоглобин обычно бывает в виде калиевой соли. В капиллярах тканей в кровь поступает большое количество кислых продуктов распада. Одновременно в тканевых капиллярах при диссоциации оксигемоглобина происходит отдача кислорода и появление большого количества щелочно реагирующих солей гемоглобина. Последние взаимодействуют с кислыми продуктами распада, например угольной кислотой. В результате образуются бикарбонаты и восстановленный гемоглобин. В легочных капиллярах гемоглобин, отдавая ионы водорода, присоединяет кислород и становится сильной кислотой, которая связывает ионы калия. Ионы водорода используются для образования угольной кислоты, в дальнейшем выделяющейся из легких в виде Н2О и СО2. Карбонатная буферная система по своей мощности занимает второе место. Она представлена угольной кислотой (Н2СО3) и бикарбонатом натрия или калия (NaHCО3, КНСО3) в пропорции 1/20. Если в кровь поступает кислота, более сильная, чем угольная, то в реакцию вступает, например, бикарбонат натрия. Образуются нейтральная соль и слабодиссоциированная угольная кислота. Угольная кислота под действием карбоангидразы эритроцитов распадается на Н2О и СО2, последний выделяется легкими в окружающую среду. Если в кровь поступает основание, то в реакцию вступает угольная кислота, образуя гидрокарбонат натрия и воду. Избыток бикарбоната натрия удаляется через почки. Бикарбонатный буфер широко используется для коррекции нарушений кислотно-основного состояния организма. Фосфатная буферная система состоит из натрия дигидрофосфата (NaH2PО4) и натрия гидрофосфата (Na2HPО4). Первое соединение обладает свойствами слабой кислоты и взаимодействует с поступившими в кровь щелочными продуктами. Второе соединение имеет свойства слабой щелочи и вступает в реакцию с более сильными кислотами. Белковая буферная система осуществляет роль нейтрализации кислот и щелочей благодаря амфотерным свойствам: в кислой среде белки плазмы ведут себя как основания, в основной – как кислоты. Буферные системы имеются и в тканях, что способствует поддержанию рН тканей на относительно постоянном уровне. Главными буферами тканей являются белки и фосфаты. Поддержание рН осуществляется также с помощью легких и почек. Через легкие удаляется избыток углекислоты. Почки при ацидозе выделяют больше кислого одноосновного фосфата натрия, а при алкалозе – больше щелочных солей: двухосновного фосфата натрия и бикарбоната натрия.Состав крови
Кровь состоит из жидкой части плазмы и взвешенных в ней форменных элементов: эритроцитов, лейкоцитов и тромбоцитов. На долю форменных элементов приходится 40–45%, на долю плазмы – 55–60% от объема крови. Это соотношение получило название гематокритного соотношения, или гематокритного числа. Часто под гематокритным числом понимают только объем крови, приходящийся на долю форменных элементов.Плазма крови
В состав плазмы крови входят вода (90–92%) и сухой остаток (8–10%). Сухой остаток состоит из органических и неорганических веществ. К органическим веществам плазмы крови относятся белки, которые составляют 7 – 8%. Белки представлены альбуминами (4,5%), глобулинами (2–3,5%) и фибриногеном (0,2–0,4%).Белки плазмы крови выполняют разнообразные функции: 1. коллоидно-осмотический и водный гомеостаз; 2. обеспечение агрегатного состояния крови; 3. кислотно-основной гомеостаз; 4. иммунный гомеостаз; 5. транспортная функция; 6. питательная функция; 7. участие в свертывании крови.
Альбумины составляют около 60% всех белков плазмы. Благодаря относительно небольшой молекулярной массе (70 000) и высокой концентрации альбумины создают 80% онкотического давления. Альбумины осуществляют питательную функцию, являются резервом аминокислот для синтеза белков. Их транспортная функция заключается в переносе холестерина, жирных кислот, билирубина, солей желчных кислот, солей тяжелых металлов, лекарственных препаратов (антибиотиков, сульфаниламидов). Альбумины синтезируются в печени. Глобулины подразделяются на несколько фракций: а-, В- и у-глобулины. α-глобулины включают гликопротеины, т. е. белки, простетической группой которых являются углеводы. Около 60% всей глюкозы плазмы циркулирует в составе гликопротеинов. Эта группа белков транспортирует гормоны, витамины, микроэлементы, липиды. К а-глобулинам относятся эритропоэтин, плазминоген, протромбин. β-глобулины участвуют в транспорте фосфолипидов, холестерина, стероидных гормонов, катионов металлов. К этой фракции относится белок трансферрин, обеспечивающий транспорт железа, а также многие факторы свертывания крови. γ-глобулины включают в себя различные антитела или иммуноглобулины 5 классов: Jg A, Jg G, Jg М, Jg D и Jg Е, защищающие организм от вирусов и бактерий. К у-глобулинам относятся также аир – агглютинины крови, определяющие ее групповую принадлежность. Глобулины образуются в печени, костном мозге, селезенке, лимфатических узлах. Фибриноген – первый фактор свертывания крови. Под воздействием тромбина переходит в нерастворимую форму – фибрин, обеспечивая образование сгустка крови. Фибриноген образуется в печени. Белки и липопротеиды способны связывать поступающие в кровь лекарственные вещества. В связанном состоянии лекарства неактивны и образуют как бы депо. При уменьшении концентрации лекарственного препарата в сыворотке он отщепляется от белков и становится активным. Это надо иметь в виду, когда на фоне введения одних лекарственных веществ назначаются другие фармакологические средства. Введенные новые лекарственные вещества могут вытеснить из связанного состояния с белками ранее принятые лекарства, что приведет к повышению концентрации их активной формы. К органическим веществам плазмы крови относятся также небелковые азотсодержащие соединения (аминокислоты, полипептиды, мочевина, мочевая кислота, креатинин, аммиак). Общее количество небелкового азота в плазме, гак называемого остаточного азота, составляет 11 – 15 ммоль/л (30 – 40 мг%). Содержание остаточного азота в крови резко возрастает при нарушении функции почек. В плазме крови содержатся также безазотистые органические вещества: глюкоза 4,4 – 6,6 ммоль/л (80- 120 мг%), нейтральные жиры, липиды, ферменты, расщепляющие гликоген, жиры и белки, проферменты и ферменты, участвующие в процессах свертывания крови и фибринолиза. Неорганические вещества плазмы крови составляют 0,9- 1%. К этим веществам относятся в основном катионы Na+, Са2+, К+, Мg2+ и анионы Сl-, НРО42-, НСО3-. Содержание катионов является более жесткой величиной, чем содержание анионов. Ионы обеспечивают нормальную функцию всех клеток организма, в том числе клеток возбудимых тканей, обусловливают осмотическое давление, регулируют рН. В плазме постоянно присутствуют все витамины, микроэлементы, промежуточные продукты метаболизма (молочная и пировиноградная кислоты).
Форменные элементы крови
Эритроциты
В норме в крови у мужчин содержится 4,0 – 5,0x1012/л, или 4.000.000-5.000.000 эритроцитов в 1 мкл, у женщин 4,5x1012/л, или 4.500.000 в 1 мкл. Повышение количества эритроцитов в крови называется эритроцитозом, уменьшение эритропенией, что часто сопутствует малокровию, или анемии. При анемии может быть снижено или число эритроцитов, или содержание в них гемоглобина, или и то и другое. Как эритроцитозы, так и эритропении бывают ложными в случаях сгущения или разжижения крови и истинными. Эритроциты человека лишены ядра и состоят из стромы, заполненной гемоглобином, и белково-липидной оболочки. Эритроциты имеют преимущественно форму двояковогнутого диска диаметром 7,5 мкм, толщиной на периферии 2,5 мкм, в центре – 1,5 мкм. Эритроциты такой формы называются нормоцитами. Особая форма эритроцитов приводит к увеличению диффузионной поверхности, что способствует лучшему выполнению основной функции эритроцитов – дыхательной. Специфическая форма обеспечивает также прохождение эритроцитов через узкие капилляры. Лишение ядра не требует больших затрат кислорода на собственные нужды и позволяет более полноценно снабжать организм кислородом.Эритроциты выполняют в организме следующие функции: 1. основной функцией является дыхательная – перенос кислорода от альвеол легких к тканям и углекислого газа от тканей к легким; 2. регуляция рН крови благодаря одной из мощнейших буферных систем крови – гемоглобиновой; 3. питательная – перенос на своей поверхности аминокислот от органов пищеварения к клеткам организма; 4. защитная – адсорбция на своей поверхности токсических веществ; 5. участие в процессе свертывания крови за счет содержания факторов свертывающей и противосвертывающей систем крови; 6. эритроциты являются носителями разнообразных ферментов (холинэстераза, угольная ангидраза, фосфатаза) и витаминов (В1, В2, В6, аскорбиновая кислота); 7. эритроциты несут в себе групповые признаки крови.
Гемоглобин и его соединения
Гемоглобин – особый белок хромопротеида, благодаря которому эритроциты выполняют дыхательную функцию и поддерживают рН крови. У мужчин в крови содержится в среднем 130–160 г/л гемоглобина, у женщин – 120–150 г/л. Гемоглобин состоит из белка глобина и 4 молекул гема. Гем имеет в своем составе атом железа, способный присоединять или отдавать молекулу кислорода. При этом валентность железа, к которому присоединяется кислород, не изменяется, т. е. железо остается двухвалентным. Гемоглобин, присоединивший к себе кислород, превращается в оксигемоглобин. Это соединение непрочное. В виде оксигемоглобина переносится большая часть кислорода. Гемоглобин, отдавший кислород, называется восстановленным, или дезоксигемоглобином. Гемоглобин, соединенный с углекислым газом, носит название карбгемоглобина. Это соединение также легко распадается. В виде карбгемоглобина переносится 20% углекислого газа. В особых условиях гемоглобин может вступать в соединение и с другими газами. Соединение гемоглобина с угарным газом (СО) называется карбоксигемоглобином. Карбоксигемоглобин является прочным соединением. Гемоглобин блокирован в нем угарным газом и неспособен осуществлять перенос кислорода. Сродство гемоглобина к угарному газу выше его сродства к кислороду, поэтому даже небольшое количество угарного газа в воздухе является опасным для жизни. При некоторых патологических состояниях, например, при отравлении сильными окислителями (бертолетовой солью, перманганатом калия и др.) образуется прочное соединение гемоглобина с кислородом – метгемоглобин, в котором происходит окисление железа, и оно становится трехвалентным. В результате этого гемоглобин теряет способность отдавать кислород тканям, что может привести к гибели человека. В скелетных и сердечной мышцах находится мышечный гемоглобин, называемый миоглобином. Он играет важную роль в снабжении кислородом работающих мышц. Имеется несколько форм гемоглобина, отличающихся строением белковой части – глобина. У плода содержится гемоглобин F. В эритроцитах взрослого человека преобладает гемоглобин А (90%). Различия в строении белковой части определяют сродство гемоглобина к кислороду. У фетального гемоглобина оно намного больше, чем у гемоглобина А. Это помогает плоду не испытывать гипоксии при относительно низком парциальном напряжении кислорода в его крови. Ряд заболеваний связан с появлением в крови патологических форм гемоглобина. Наиболее известной наследственной патологией гемоглобина является серповидноклеточная анемия. Форма эритроцитов напоминает серп. Отсутствие или замена нескольких аминокислот в молекуле глобина при этом заболевании приводит к существенному нарушению функции гемоглобина. В клинических условиях принято вычислять степень насыщения эритроцитов гемоглобином. Это так называемый цветовой показатель. В норме он равен 1. Такие эритроциты называются нормохромными. При цветовом показателе более 1,1 эритроциты гиперхромные, менее 0,85 – гипохромные. Цветовой показатель важен для диагностики анемий различной этиологии.Гемолиз
Процесс разрушения оболочки эритроцитов и выход гемоглобина в плазму крови называется гемолизом. При этом плазма окрашивается в красныйцвет и становится прозрачной – «лаковая кровь». Различают несколько видов гемолиза. Осмотический гемолиз может возникнуть в гипотонической среде. Концентрация раствора NaCl, при которой начинается гемолиз, носит название осмотической резистентности эритроцитов. Для здоровых людей границы минимальной и максимальной стойкости эритроцитов находятся в пределах от 0,4 до 0,34%. Химический гемолиз может быть вызван хлороформом, эфиром, разрушающими белково-липидную оболочку эритроцитов. Биологический гемолиз встречается при действии ядов змей, насекомых, микроорганизмов, при переливании несовместимой крови под влиянием иммунных гемолизинов. Температурный гемолиз возникает при замораживании и размораживании крови в результате разрушения оболочки эритроцитов кристалликами льда. Механический гемолиз происходит при сильных механических воздействиях на кровь, например встряхивании ампулы с кровью.Скорость оседания эритроцитов (СОЭ)
Скорость оседания эритроцитов у здоровых мужчин составляет 2–10 мм в час, у женщин – 2–15 мм в час. СОЭ зависит от многих факторов: количества, объема, формы и величины заряда эритроцитов, их способности к агрегации, белкового состава плазмы. В большей степени СОЭ зависит от свойств плазмы, чем эритроцитов. СОЭ увеличивается при беременности, стрессе, воспалительных, инфекционных и онкологических заболеваниях, при уменьшении числа эритроцитов, при увеличении содержания фибриногена. СОЭ снижается при увеличении количества альбуминов. Многие стероидные гормоны (эстрогены, глюкокортикоиды), а также лекарственные вещества (салицилаты) вызывают повышение СОЭ.Эритропоэз
Образование эритроцитов, или эритропоэз, происходит в красном костном мозге. Эритроциты вместе с кроветворной тканью носят название «красного ростка крови», или эритрона. Для образования эритроцитов требуются железо и ряд витаминов. Железо организм получает из гемоглобина разрушающихся эритроцитов и с пищей. Трехвалентное железо пищи с помощью вещества, находящегося в слизистой кишечника, превращается в двухвалентное железо. С помощью белка трансферрина железо, всосавшись, транспортируется плазмой в костный мозг, где оно включается в молекулу гемоглобина. Избыток железа депонируется в печени в виде соединения с белком – ферритина или с белком и липоидом – гемосидерина. При недостатке железа развивается железодефицитная анемия. Для образования эритроцитов требуются витамин В12 (цианокобаламин) и фолиевая кислота. Витамин В12 поступает в организм с пищей и называется внешним фактором кроветворения. Для его всасывания необходимо вещество (гастромукопротеид), которое вырабатывается железами слизистой оболочки пилорического отдела желудка и носит название внутреннего фактора кроветворения Касла. При недостатке витамина В12 развивается В12-дефицитная анемия. Это может быть или при недостаточном его поступлении с пищей (печень, мясо, яйца, дрожжи, отруби), или при отсутствии внутреннего фактора (резекция нижней трети желудка). Считается, что витамин В12 способствует синтезу глобина. Витамин В12 и фолиевая кислота участвуют в синтезе ДНК в ядерных формах эритроцитов. Витамин В2 (рибофлавин) необходим для образования липидной стромы эритроцитов. Витамин В6 (пиридоксин) участвуете образовании гема. Витамин С стимулирует всасывание железа из кишечника, усиливает действие фолиевой кислоты. Витамин Е (а-токоферол) и витамин РР (пантотеновая кислота) укрепляют липидную оболочку эритроцитов, защищая их от гемолиза. Для нормального эритропоэза необходимы микроэлементы. Медь помогает всасыванию железа в кишечнике и способствует включению железа в структуру гема. Никель и кобальт участвуют в синтезе гемоглобина и гемсодержащих молекул, утилизирующих железо. В организме 75% цинка находится в эритроцитах в составе фермента карбоангидразы. Недостаток цинка вызывает лейкопению. Селен, взаимодействуя с витамином Е, защищает мембрану эритроцита от повреждения свободными радикалами. Физиологическими регуляторами эритропоэза являются эритропоэтины, образующиеся главным образом в почках, а также в печени, селезенке и в небольших количествах постоянно присутствующие в плазме крови здоровых людей. Эритропоэтины усиливают пролиферацию клеток-предшественников эритроидного ряда – КОЕ-Э (колониеобразующая единица эритроцитарная) и ускоряют синтез гемоглобина. Они стимулируют синтез информационной РНК, необходимой для образования энзимов, которые участвуют в формировании гема и глобина. Эритропоэтины увеличивают также кровоток в сосудах кроветворной ткани и увеличивают выход в кровь ретикулоцитов. Продукция эритропоэтинов стимулируется при гипоксии различного происхождения: пребывание человека в горах, кровопотеря, анемия, заболевания сердца и легких. Эритропоэз активируется мужскими половыми гормонами, что обусловливает большее содержание эритроцитов в крови у мужчин, чем у женщин. Стимуляторами эритропоэза являются соматотропный гормон, тироксин, катехоламины, интерлейкины. Торможение эритропоэза вызывают особые вещества – ингибиторы эритропоэза, образующиеся при увеличении массы циркулирующих эритроцитов, например у спустившихся с гор людей. Тормозят эритропоэз женские половые гормоны (эстрогены), кейлоны. Симпатическая нервная система активирует эритропоэз, парасимпатическая – тормозит. Нервные и эндокринные влияния на эритропоэз осуществляются, по-видимому, через эритропоэтины. Об интенсивности эритропоэза судят по числу ретикулоцитов – предшественников эритроцитов. В норме их количество составляет 1–2%. Созревшие эритроциты циркулируют в крови в течение 100–120 дней. Разрушение эритроцитов происходит в печени, селезенке, в костном мозге посредством клеток мононуклеарной фагоцитарной системы. Продукты распада эритроцитов также являются стимуляторами кроветворения.Лейкоциты
Лейкоциты, или белые кровяные тельца, представляют собой бесцветные клетки, содержащие ядро и протоплазму, размером от 8 до 20 мкм. Количество лейкоцитов в периферической крови взрослого человека колеблется в пределах 4,0–9,0•109/л, или 4000 – 9000 в 1 мкл. Увеличение количества лейкоцитов в крови называется лейкоцитозом, уменьшение – лейкопенией. Лейкоцитозы могут быть физиологическими и патологическими (реактивными). Среди физиологических лейкоцитозов различают пищевой, миогенный, эмоциональный, а также лейкоцитоз, возникающий при беременности. Физиологические лейкоцитозы носят перераспределительный характер и, как правило, не достигают высоких показателей. При патологических лейкоцитозах происходит выброс клеток из органов кроветворения с преобладанием молодых форм. В наиболее тяжелой форме лейкоцитоз наблюдается при лейкозах. Лейкоциты, образующиеся при этом заболевании в избыточном количестве, как правило, малодифференцированы и не способны выполнять свои физиологические функции, в частности, защищать организм от патогенных бактерий. Лейкопения наблюдается при повышении радиоактивного фона, при применении некоторых фармакологических препаратов. Особенно выраженной она бывает в результате поражения костного мозга при лучевой болезни. Лейкопения встречается также при некоторых тяжелых инфекционных заболеваниях (сепсис, милиарный туберкулез). При лейкопениях происходит резкое угнетение защитных сил организма в борьбе с бактериальной инфекцией. Лейкоциты в зависимости от того, однородна ли их протоплазма или содержит зернистость, делят на 2 группы: зернистые, или гранулоциты, и незернистые, или агранулоциты. Гранулоциты в зависимости от гистологических красок, какими они окрашиваются, бывают трех видов: базофилы (окрашиваются основными красками), эозинофилы (кислыми красками) и нейтрофилы (и основными, и кислыми красками). Нейтрофилы по степени зрелости делятся на метамиелоциты (юные), палочкоядерные и сегментоядерные. Агранулоциты бывают двух видов: лимфоциты и моноциты. В клинике имеет значение не только общее количество лейкоцитов, но и процентное соотношение всех видов лейкоцитов, получившее название лейкоцитарной формулы, или лейкограммы. При ряде заболеваний характер лейкоцитарной формулы меняется. Увеличение количества юных и палочкоядерных нейтрофилов называется сдвигом лейкоцитарной формулы влево. Он свидетельствует об обновлении крови и наблюдается при острых инфекционных и воспалительных заболеваниях, а также при лейкозах. Все виды лейкоцитов выполняют в организме защитную функцию. Однако осуществление ее различными видами лейкоцитов происходит по-разному. Нейтрофилы являются самой многочисленной группой. Основная их функция – фагоцитоз бактерий и продуктов распада тканей с последующим перевариванием их при помощи лизосомных ферментов (протеазы, пептидазы, оксидазы, дезоксирибонуклеазы). Нейтрофилы первыми приходят в очаг повреждения. Так как они являются сравнительно небольшими клетками, то их называют микрофагами. Нейтрофилы оказывают цитотоксическое действие, а также продуцируют интерферон, обладающий противовирусным действием. Активированные нейтрофилы выделяют арахидоновую кислоту, которая является предшественником лейкотриенов, тромбоксанов и простагландинов. Эти вещества играют важную роль в регуляции просвета и проницаемости кровеносных сосудов и в запуске таких процессов, как воспаление, боль и свертывание крови. По нейтрофилам можно определить пол человека, так как у женского генотипа имеются круглые выросты – «барабанные палочки». Эозинофилы также обладают способностью к фагоцитозу, но это не имеет серьезного значения из-за их небольшого количества в крови. Основной функцией эозинофилов является обезвреживание и разрушение токсинов белкового происхождения, чужеродных белков, а также комплекса антиген-антитело. Эозинофилы продуцируют фермент гистаминазу, который разрушает гистамин, освобождающийся из поврежденных базофилов и тучных клеток при различных аллергических состояниях, глистных инвазиях, аутоиммунных заболеваниях. Эозинофилы осуществляют противоглистный иммунитет, оказывая на личинку цитотоксическое действие. Поэтому при этих заболеваниях увеличивается количество эозинофилов в крови (эозинофилия). Эозинофилы продуцируют плазминоген, который является предшественником плазмина – главного фактора фибринолитической системы крови. Содержание эозинофилов в периферической крови подвержено суточным колебаниям, что связано с уровнем глюкокортикоидов. В конце второй половины дня и рано утром их на 20% меньше среднесуточного уровня, а в полночь – на 30% больше. Базофилы продуцируют и содержат биологически активные вещества (гепарин, гистамин и др.), чем и обусловлена их функция в организме. Гепарин препятствует свертыванию крови в очаге воспаления. Гистамин расширяет капилляры, что способствует рассасыванию и заживлению. В базофилах содержатся также гиалуроновая кислота, влияющая на проницаемость сосудистой стенки; фактор активации тромбоцитов (ФАТ); тромбоксаны, способствующие агрегации тромбоцитов; лейкотриены и простагландины. При аллергических реакциях (крапивница, бронхиальная астма, лекарственная болезнь) под влиянием комплекса антиген-антитело происходит дегрануляция базофилов и выход в кровь биологически активных веществ, в том числе гистамина, что определяет клиническую картину заболеваний. Моноциты обладают выраженной фагоцитарной функцией. Это самые крупные клетки периферической крови и их называют макрофагами. Моноциты находятся в крови 2–3 дня, затем они выходят в окружающие ткани, где, достигнув зрелости, превращаются в тканевые макрофаги (гистиоциты). Моноциты способны фагоцитировать микробы в кислой среде, когда нейтрофилы не активны. Фагоцитируя микробы, погибшие лейкоциты, поврежденные клетки тканей, моноциты очищают место воспаления и подготавливают его для регенерации. Моноциты синтезируют отдельные компоненты системы комплемента. Активированные моноциты и тканевые макрофаги продуцируют цитотоксины, интерлейкин (ИЛ-1), фактор некроза опухолей (ФНО), интерферон, тем самым осуществляя противоопухолевый, противовирусный, противомикробный и противопаразитарный иммунитет; участвуют в регуляции гемопоэза. Макрофаги принимают участие в формировании специфического иммунного ответа организма. Они распознают антиген и переводят его в так называемую иммуногенную форму (презентация антигена). Моноциты продуцируют как факторы, усиливающие свертывание крови (тромбоксаны, тромбопластины), так и факторы, стимулирующие фибринолиз (активаторы плазминогена). Лимфоциты являются центральным звеном иммунной системы организма. Они осуществляют формирование специфического иммунитета, синтез защитных антител, лизис чужеродных клеток, реакцию отторжения трансплантата, обеспечивают иммунную память. Лимфоциты образуются в костном мозге, а дифференцировку проходят в тканях. Лимфоциты, созревание которых происходит в вилочковой железе, называются Т-лимфоцитами (тимусзависимые). Различают несколько форм Т-лимфоцитов. Т-киллеры (убийцы) осуществляют реакции клеточного иммунитета, лизируя чужеродные клетки, возбудителей инфекционных заболеваний, опухолевые клетки, клетки-мутанты. Т-хелперы (помощники), взаимодействуя с В-лимфоцитами, превращают их в плазматические клетки, т. е. помогают течению гуморального иммунитета. Т-супрессоры (угнетатели) блокируют чрезмерные реакции В-лимфоцитов. Имеются также Т-хелперы и Т-супрессоры, регулирующие клеточный иммунитет. Т-клетки памяти хранят информацию о ранее действующих антигенах. В-лимфоциты (бурсозависимые) проходят дифференцировку у человека в лимфоидной ткани кишечника, нёбных и глоточных миндалин. В-лимфоциты осуществляют реакции гуморального иммунитета. Большинство В-лимфоцитов являются антителопродуцентами. В-лимфоциты в ответ на действие антигенов в результате сложных взаимодействий с Т-лимфоцитами и моноцитами превращаются в плазматические клетки. Плазматические клетки вырабатывают антитела, которые распознают и специфически связывают соответствующие антигены. Различают 5 основных классов антител, или иммуноглобулинов: IgA, IgG, IgM, IgE, IgD. Среди В-лимфоцитов также выделяют клетки-киллеры, хелперы, супрессоры и клетки иммунологической памяти. О-лимфоциты (нулевые) не проходят дифференцировку и являются как бы резервом Ти В-лимфоцитов.Лейкопоэз
Все лейкоциты образуются в красном костном мозге из единой стволовой клетки. Предшественники лимфоцитов первыми ответвляются от общего древа стволовых клеток; формирование лимфоцитов происходит во вторичных лимфатических органах. Лейкопоэз стимулируется специфическими ростовыми факторами, которые воздействуют на определенные предшественники гранулоцитарного и моноцитарного рядов. Продукция гранулоцитов стимулируется гранулоцитарным колониестимулирующим фактором (КСФ-Г), образующимся в моноцитах, макрофагах, Т-лимфоцитах, а угнетается – кейлонами и лактоферрином, секретируемыми зрелыми нейтрофилами; простагландинами Е. Моноцитопоэз стимулируется моноцитарным колониестимулирующим фактором (КСФ-М), катехоламинами. Простагландины Е, аи p-интерфероны, лактоферрии тормозят продукцию моноцитов. Большие дозы гидрокортизона препятствуют выходу моноцитов из костного мозга. Важная роль в регуляции лейкопоэза принадлежит интерлейкинам. Одни из них усиливают рост и развитие базофилов (ИЛ-3) и эозинофилов (ИЛ-5), другие стимулируют рост и дифференцировку Ти В-лимфоцитов (ИЛ-2,4,6,7). Лейкопоэз стимулируют продукты распада самих лейкоцитов и тканей, микроорганизмы и их токсины, некоторые гормоны гипофиза, нуклеиновые кислоты. Жизненный цикл разных видов лейкоцитов различен. Одни живут часы, дни, недели, другие на протяжении всей жизни человека. Лейкоциты разрушаются в слизистой оболочке пищеварительного тракта, а также в ретикулярной ткани.Тромбоциты
Тромбоциты, или кровяные пластинки – плоские клетки не-правильной округлой формы диаметром 2–5 мкм. Тромбоциты человека не имеют ядер. Количество тромбоцитов в крови человека составляет 180-320х109/л, или 180.000-320.000 в 1 мкл. Имеют место суточные колебания: днем тромбоцитов больше, чем ночью. Увеличение содержания тромбоцитов в периферической крови называется тромбоцитозом, уменьшение – тромбоцитопенией. Главной функцией тромбоцитов является участие в гемостазе. Тромбоциты способны прилипать к чужеродной поверхности (адгезия), а также склеиваться между собой (агрегация) под влиянием разнообразных причин. Тромбоциты продуцируют и выделяют ряд биологически активных веществ: серотоиин, адреналин, норадреналин, а также вещества, получившие название пластинчатых факторов свертывания крови. Тромбоциты способны выделять из клеточных мембран арахидоновую кислоту и превращать ее в тромбоксаны, которые, в свою очередь, повышают агрегационную активность тромбоцитов. Эти реакции происходят под действием фермента циклооксигеназы. Тромбоциты способны к передвижению за счет образования псевдоподий и фагоцитозу инородных тел, вирусов, иммунных комплексов, тем самым, выполняя защитную функцию. Тромбоциты содержат большое количество серотонина и гистамина, которые влияют на величину просвета и проницаемость капилляров, определяя тем самым состояние гистогематических барьеров. Тромбоциты образуются в красном костном мозге из гигантских клеток мегакариоцитов. Продукция тромбоцитов регулируется тромбоцитопоэтинами. Тромбоцитопоэтины образуются в костном мозге, селезенке, печени. Различают тромбоцитопоэтины кратковременного и длительного действия. Первые усиливают отщепление тромбоцитов от мегакариоцитов и ускоряют их поступление в кровь. Вторые способствуют дифференцировке и созреванию мегакариоцитов. Активность тромбоцитопоэтинов регулируется интерлейкинами (ИЛ-6 и ИЛ-11). Количество тромбоцитопоэтинов повышается при воспалении, необратимой агрегации тромбоцитов. Продолжительность жизни тромбоцитов составляет от 5 до 11 дней. Разрушаются кровяные пластинки в клетках системы макрофагов.Система гемостаза
Кровь циркулирует в кровеносном русле в жидком состоянии. При травме, когда нарушается целостность кровеносных сосудов, кровь должна свертываться. За все это в организме человека отвечает система PACK – регуляции агрегатного состояния крови. Эта регуляция осуществляется сложнейшими механизмами, в которых принимают участие факторы свертывающей, противосвертывающей и фибринолитической систем крови. В здоровом организме эти системы взаимосвязаны. Изменение функционального состояния одной из систем сопровождается компенсаторными сдвигами в деятельности другой. Нарушение функциональных взаимосвязей может привести к тяжелым патологическим состояниям организма, заключающимся или в повышенной кровоточивости, или во внутрисосудистом тромбообразовании.К факторам, поддерживающим кровь в жидком состоянии, относятся следующие: 1. внутренние стенки сосудов и форменные элементы крови заряжены отрицательно; 2. эндотелий сосудов секретирует простациклин ПГИ-2 – ингибитор агрегации тромбоцитов, антитромбин III, активаторы фибринолиза; 3. факторы свертывающей системы крови находятся в сосудистом русле в неактивном состоянии; 4. наличие антикоагулянтов; 5. большая скорость кровотока.
Свертывающие механизмы
Свертывание крови (гемокоагуляция) – это жизненно важная защитная реакция, направленная на сохранение крови в сосудистой системе и предотвращающая гибель организма от кровопотери при травме сосудов. Основные положения ферментативной теории свертывания крови были разработаны А. Шмидтом более 100 лет назад. В остановке кровотечения участвуют: сосуды, ткань, окружающая сосуды, физиологически активные вещества плазмы, форменные элементы крови, главная роль принадлежит тромбоцитам. И всем этим управляет нейрогуморальный регуляторный механизм. Физиологически активные вещества, принимающие участие в свертывании крови и находящиеся в плазме, называются плазменными факторами свертывания крови. Они обозначаются римскими цифрами в порядке их хронологического открытия. Некоторые из факторов имеют название, связанное с фамилией больного, у которого впервые обнаружен дефицит соответствующего фактора. К плазменным факторам свертывания крови относятся: 1ф – фибриноген, 2ф – протромбин, 3ф – тканевой тромбопластин, 4ф – ионы кальция, 5ф – Ас-глобулин (accelerance – ускоряющий), или проакцелерин, 6ф – исключен из номенклатуры, 7ф – проконвертин, 8ф – антигемофильный глобулин А, 9ф – антигемофильный глобулин В, или фактор Кристмаса, 10ф – фактор Стюарта – Прауэра, 11ф – плазменный предшественник тромбопластина, или антигемофильный глобулин С, 12ф – контактный фактор, или фактор Хагемана, 13ф – фибринстабилизирующий фактор, или фибриназа, 14ф – фактор Флетчера (прокалликреин), 15ф – фактор Фитцджеральда – Фложе (высокомолекулярный кининоген – ВМК). Большинство плазменных факторов свертывания крови образуется в печени. Для синтеза некоторых из них (II, VII, IX, X) необходим витамин К, содержащийся в растительной пище и синтезируемый микрофлорой кишечника. При недостатке или снижении активности факторов свертывания крови может наблюдаться патологическая кровоточивость. Это может происходить при тяжелых и дегенеративных заболеваниях печени, при недостаточности витамина К. Витамин К является жирорастворимым витамином, поэтому его дефицит может обнаружиться при угнетении всасывания жиров в кишечнике, например при снижении желчеобразования. Эндогенный дефицит витамина К наблюдается также при подавлении кишечной микрофлоры антибиотиками. Ряд заболеваний, при которых имеется дефицит плазменных факторов, носит наследственный характер. Примером являются различные формы гемофилии, которыми болеют только мужчины, но передают их женщины. Вещества, находящиеся в тромбоцитах, получили название тромбоцитарных, или пластинчатых, факторов свертывания крови. Их обозначают арабскими цифрами. К наиболее важным тромбоцитарным факторам относятся: ПФ-3 (тромбоцитарный тромбопластин) – липидно-белковый комплекс, на котором как на матрице происходит гемокоагуляция, ПФ-4 – антигепариновый фактор, ПФ-5 – благодаря которому тромбоциты способны к адгезии и агрегации, ПФ-6 (тромбостенин) – актиномиозиновый комплекс, обеспечивающий ретракцию тромба, ПФ-10 – серотонин, ПФ-11 – фактор агрегации, представляющий комплекс АТФ и тромбоксана. Аналогичные вещества открыты и в эритроцитах, и в лейкоцитах. При переливании несовместимой крови, резус-конфликте матери и плода происходит массовое разрушение эритроцитов и выход этих факторов в плазму, что является причиной интенсивного внутрисосудистого свертывания крови. При многих воспалительных и инфекционных заболеваниях также возникает диссеминированное (распространенное) внутрисосудистое свертывание крови (ДВС-синдром), причиной которого являются лейкоцитарные факторы свертывания крови. По современным представлениям в остановке кровотечения участвуют 2 механизма: сосудисто-тромбоцитарный и коагуляционный.Сосудисто-тромбоцитарный гемостаз
Благодаря этому механизму происходит остановка кровотечения из мелких сосудов с низким артериальным давлением. При травме наблюдается рефлекторный спазм поврежденных кровеносных сосудов, который в дальнейшем поддерживается сосудосуживающими веществами (серотонин, норадреналин, адреналин), освобождающимися из тромбоцитов и поврежденных клеток тканей. Внутренняя стенка сосудов в месте повреждения изменяет свой заряд с отрицательного на положительный. Благодаря способности к адгезии под влиянием фактора Виллебранда, содержащегося в субэндотелии и кровяных пластинках, отрицательно заряженные тромбоциты прилипают к положительно заряженной раневой поверхности. Практически одновременно происходит агрегация – скучивание и склеивание тромбоцитов с образованием тромбоцитарной пробки, или тромба. Сначала под влиянием АТФ, АДФ и адреналина тромбоцитов и эритроцитов образуется рыхлая тромбоцитарная пробка, через которую проходит плазма (обратимая агрегация). Затем тромбоциты теряют свою структурность и сливаются в однообразную массу, образуя пробку, непроницаемую для плазмы (необратимая агрегация). Эта реакция протекает под действием тромбина, образующегося в небольших количествах под действием тканевого тромбопластина. Тромбин разрушает мембрану тромбоцитов, что ведет к выходу из них серотонина, гистамина, ферментов, факторов свертывания крови. Пластинчатый фактор 3 дает начало образованию тромбоцитарной протромбиназы, что приводит к образованию на агрегатах тромбоцитов небольшого количества нитей фибрина, среди которых задерживаются эритроциты и лейкоциты. После образования тромбоцитарного тромба происходит его уплотнение и закрепление в поврежденном сосуде за счет ретракции кровяного сгустка. Ретракция осуществляется под влиянием тромбостенина тромбоцитов за счет сокращения актин-миозинового комплекса тромбоцитов. Тромбоцитарная пробка образуется в целом в течение 1 – 3 минут с момента повреждения, и кровотечение из мелких сосудов останавливается. В крупных сосудах тромбоцитарный тромб не выдерживает высокого давления и вымывается. Поэтому в крупных сосудах гемостаз может быть осуществлен путем формирования более прочного фибринового тромба, для образования которого необходим ферментативный коагуляционный механизм.Коагуляционный гемостаз
Свертывание крови – это цепной ферментативный процесс, в котором последовательно происходит активация факторов свертывания и образование их комплексов. Сущность свертывания крови заключается в переходе растворимого белка крови фибриногена в нерастворимый фибрин, в результате чего образуется прочный фибриновый тромб. Процесс свертывания крови осуществляется в 3 последовательные фазы.Первая фаза
Первая фаза является самой сложной и продолжительной. Во время этой фазы происходит образование активного ферментативного комплекса – протромбиназы, являющейся активатором протромбина. В образовании этого комплекса принимают участие тканевые и кровяные факторы. В результате формируются тканевая и кровяная протромбиназы. Образование тканевой протромбиназы начинается с активации тканевого тромбопластина, образующегося при повреждении стенок сосуда и окружающих тканей. Вместе с VII фактором и ионами кальция он активирует X фактор. В результате взаимодействия активированного X фактора с V фактором и с фосфолипидами тканей или плазмы образуется тканевая протромбиназа. Этот процесс длится 5–10 секунд. Образование кровяной протромбиназы начинается с активации XII фактора при его контакте с волокнами коллагена поврежденных сосудов. В активации и действии XII фактора участвуют также высокомолекулярный кининоген (ф XV) и калликреин (ф XIV). Затем XII фактор активирует XI фактор, образуя с ним комплекс. Активный XI фактор совместно с IV фактором активирует IX фактор, который, в свою очередь, активирует VIII фактор. Затем происходит активация X фактора, который образует комплекс с V фактором и ионами кальция, чем и заканчивается образование кровяной протромбиназы. В этом также участвует тромбоцитарный фактор 3. Этот процесс длится 5–10 минут.Вторая фаза.
Во время этой фазы под влиянием протромбиназы происходит переход протромбина в активный фермент тромбин. В этом процессе принимают участие факторы IV, V, X.Третья фаза.
В эту фазу растворимый белок крови фибриноген превращается в нерастворимый фибрин, образующий основу тромба. Вначале под влиянием тромбина происходит образование фибрин-мономера. Затем с участием ионов кальция образуется растворимый фибрин-полимер (фибрин «S», soluble). Под влиянием фибринстабилизирующего фактора XIII происходит образование не-растворимого фибрин-полимера (фибрин «I», insoluble), устойчивого к фибринолизу. В фибриновых нитях оседают форменные элементы крови, в частности эритроциты, и формируется кровяной сгусток, или тромб, который закупоривает рану. После образования сгустка начинается процесс ретракции, т. е. уплотнения и закрепления тромба в поврежденном сосуде. Это происходит с помощью сократительного белка тромбоцитов тромбостенина и ионов кальция. Через 2 – 3 часа сгусток сжимается до 25 – 50% от своего первоначального объема и идет отжатие сыворотки, т. е. плазмы, лишенной фибриногена. За счет ретракции тромб становится более плотным и стягивает края раны.Фибринолиз
Фибринолиз – это процесс расщепления фибринового сгустка, в результате которого происходит восстановление просвета сосуда. Фибринолиз начинается одновременно с ретракцией сгустка, но идет медленнее. Это тоже ферментативный процесс, который осуществляется под влиянием плазмина (фибринолизина). Плазмин находится в плазме крови в неактивном состоянии в виде плазминогена. Под влиянием кровяных и тканевых активаторов плазминогена происходит его активация. Высокоактивным тканевым активатором является урокиназа. Кровяные активаторы находятся в крови в неактивном состоянии и активируются адреналином, лизокиназами. Плазмин расщепляет фибрин на отдельные полипептидные цепи, в результате чего происходит лизис (растворение) фибринового сгустка. Если нет условий для фибринолиза, то возможна организация тромба, т. е. замещение его соединительной тканью. Иногда тромб может оторваться от места своего образования и вызвать закупорку сосуда в другом месте (эмболия). У здоровых людей активация фибринолиза всегда происходит вторично в ответ на усиление гемокоагуляции. Под влиянием ингибиторов фибринолиз может тормозиться.Противосвертывающие механизмы
Наряду с веществами, способствующими свертыванию крови, в кровотоке находятся вещества, препятствующие гемокоагуляции. Они называются естественными антикоагулянтами. Одни антикоагулянты постоянно находятся в крови. Это первичные антикоагулянты. Вторичные антикоагулянты образуются в процессе свертывания крови и фибринолиза. К первичным антикоагулянтам относят антитромбопластины, антитромбины, гепарин. Антитромбопластины обладают антитромбопластиновым и антипротромбиназным действием. Анти-тромбины связывают тромбин. Антитромбин III является плазменным кофактором гепарина. Без гепарина антитромбин III может лишь очень медленно инактивировать тромбин в крови. Гепарин, образуя комплекс с антитромбином III, переводит его в антитромбин, обладающий способностью молниеносно связывать тромбин в крови. Активированный антитромбин III блокирует активацию и превращение в активную форму факторов XII, XI, X, IX. Гепарин образуется в тучных клетках и базофильных лейкоцитах. Его особенно много в печени, легких, сердце и мышцах. Впервые был выделен из печени. Примером вторичных антикоагулянтов является антитромбин I, или фибрин, который адсорбирует и инактивирует тромбин. Продукты деградации фибрина нарушают полимеризацию фибрин-мономера, блокируют фибринмономер, угнетают агрегацию тромбоцитов.К факторам, ускоряющим процесс свертывания крови, относятся: 1. тепло, так как свертывание крови является ферментативным процессом; 2. ионы кальция, так как они участвуют во всех фазах гемокоагуляции; 3. соприкосновение крови с шероховатой поверхностью (поражение сосудов атеросклерозом, сосудистые швы в хирургии); 4. механические воздействия (давление, раздробление тканей, встряхивание емкостей с кровью, так как это приводит к разрушению форменных элементов крови и выходу факторов, участвующих в свертывании крови).
К факторам, замедляющим и предотвращающим гемокоагуляцию, относятся: 1. понижение температуры; 2. цитрат и оксалат натрия (связывают ионы кальция); 3. гепарин (подавляет все фазы гемокоагуляции); 4. гладкая поверхность (гладкие швы при сшивании сосудов в хирургии, покрытие силиконом или парафинирование канюль и емкостей для донорской крови).
Группы крови
Учение о группах крови возникло в связи с проблемой переливания крови. В 1901 г. К. Ландштейнер обнаружил в эритроцитах людей агглютиногены Л и В. В плазме крови находятся агглютинины акр (гамма-глобулины). Согласно классификации К. Ландштейнера и Я. Янского в зависимости от наличия или отсутствия в крови конкретного человека агглютиногенов и агглютининов различают 4 группы крови. Эта система получила название АВО. Группы крови в ней обозначаются цифрами и теми агглютиногенами, которые содержатся в эритроцитах данной группы. Групповые антигены – это наследственные врожденные свойства крови, не меняющиеся в течение всей жизни человека. Агглютининов в плазме крови новорожденных нет. Они образуются в течение первого года жизни ребенка под влиянием веществ, поступающих с пищей, а также вырабатываемых кишечной микрофлорой, к тем антигенам, которых нет в его собственных эритроцитах.Таблица. Группы крови
| Группа | Агглютиногены | Агглютинины |
|---|---|---|
| I группа (0) | - | α, β |
| II группа (А) | А | β |
| III группа (В) | В | α |
| IV группа (АВ) | АВ | - |
Система резус
К. Ландштейнером и А. Винером в 1940 г. в эритроцитах обезьяны макаки-резуса был обнаружен антиген, который они назвали резус-фактором. Этот антиген находится и в крови 85% людей белой расы. У некоторых народов, например, эвенов резус-фактор встречается в 100%. Кровь, содержащая резус-фактор, называется резус-положительной (Rh+). Кровь, в которой резус-фактор отсутствует, называется резус-отрицательной (Rh-). Резус-фактор передается по наследству. В настоящее время известно, что система резус включает много антигенов. Наиболее активными в антигенном отношении являются антиген D, затем следуют С, Е, d, с, е. Они и чаще встречаются. У аборигенов Австралии в эритроцитах не выявлен ни один антиген системы резус. Система резус, в отличие от системы АВО, не имеет в норме соответствующих агглютининов в плазме. Однако если кровь резус-положительного донора перелить резус-отрицательному реципиенту, то в организме последнего образуются специфические антитела по отношению к резус-фактору – антирезус-агглютинины. При повторном переливании резус-положительной крови этому же человеку у него произойдет агглютинация эритроцитов, т. е. возникает резус-конфликт, протекающий по типу гемотрасфузионного шока. Поэтому резус-отрицательным реципиентам можно переливать только резус-отрицательую кровь. Резус-конфликт также может возникнуть при беременности, если кровь матери резусотрицательная, а кровь плода резус-положительная. Резус-агглютиногены, проникая в организм матери, могут вызвать выработку у нее антител. Однако значительное поступление эритроцитов плода в организм матери наблюдается только в период родовой деятельности. Поэтому первая беременность может закончиться благополучно. При последующих беременностях резус-положительным плодом антитела проникают через плацентарный барьер, повреждают ткани и эритроциты плода, вызывая выкидыш или тяжелую гемолитическую анемию у новорожденных. С целью иммунопрофилактики резус-отрицательной женщине сразу после родов или аборта вводят концентрированные анти-О-антитела. Кроме агглютиногенов системы АВО и резус-фактора в последние годы на мембране эритроцитов обнаружены и другие агглютиногены, которые определяют группы крови в данной системе. Таких антигенов насчитывается более 400. Наиболее важными антигенными системами считаются MNSs, Р, Лютеран (Ьи), Льюис (Le), Даффи (Fy) и др. Наибольшее значение для клиники переливания крови имеют система АВО и резус-фактор. Лейкоциты также имеют более 90 антигенов. Лейкоциты содержат антигены главного локуса НЛА – антигены гистосовместимости, которые играют важную роль в трансплантационном иммунитете. Любое переливание крови – это сложнейшая операция по своей иммунологии. Поэтому переливать цельную кровь надо только по жизненным показаниям, когда кровопотеря превышает 25% от общего объема. Если острая кровопотеря менее 25% от общего объема, необходимо вводить плазмозаменители (кристаллоиды, коллоиды), так как в данном случае более важно восстановление объема. В других ситуациях более целесообразно переливать тот компонент крови, который необходим организму. Например, при анемии – эритроцитарную массу, при тромбоцитопении – тромбоцитарную массу, при инфекциях, септическом шоке – гранулоциты.Фармакологическая коррекция нарушений гемопоэза и гемостаза
Средства, влияющие на гемопоэз
При лейкопениях, вызванных рентгено- и радиотерапией, химиотерапией злокачественных новообразований, а также при лейкопениях, сопровождающих различные заболевания, применяют средства для стимуляции лейкопоэза. С этой целью используют колониестимулирующие факторы гранулоцитов человека. Например, фармакологический препарат граноцит (активное вещество – ленограстим) является рекомбинантным человеческим гранулоцитарным колониестимулирующим фактором. Он оказывает стимулирующее действие на клетки костного мозга и вызывает значительное нарастание в периферической крови лейкоцитов, главным образом нейтрофилов. Препарат лейкомас (активное вещество – молграмостим) является рекомбинантным человеческим гранулоцитарно-макрофагальным колониестимулирующим фактором. Он образуется штаммом Escherichia coli, несущим полученную с помощью генной инженерии плазмиду, содержащую ген гранулоцитарно-макрофагального колониестимулирующего фактора человека. Лейкомас обладает поливалентным действием на различные ростки кроветворения: активирует зрелые миелоидные клетки, стимулирует пролиферацию и дифференцировку клеток-предшественников кроветворной системы, что приводит к образованию гранулоцитов, моноцитов и Т-лимфоцитов. Стимуляторами лейкопоэза являются также такие фармакологические препараты, как пентоксил, лейкоген. Для стимуляции эритропоэза при анемиях применяют рекомбинантный эритропоэтин человека – эпрекс. Он синтезируется в клетках млекопитающих, в которые встроен ген, кодирующий эритропоэтин человека. По биологическим и иммунологическим свойствам он идентичен эритропоэтину человека, выделяемому из мочи. Этот препарат оказывает выраженный эффект при анемии, обусловленной хроническими заболеваниями почек. Для лечения анемий, в зависимости от их этиологии, применяют различные антианемические препараты, влияющие на эритропоэз. Так, например, для лечения железодефицитных анемий используют препараты железа (железа глюконат, сульфат, фурамат, феррум лек для парентерального введения), а также аскорбиновую кислоту, улучшающую всасывание железа, препараты, содержащие кобальт (коамид), последний способствует усвоению организмом железа. Для лечения В12-дефицитной анемии применяют витамин В12 (цианокобаламин), для лечения анемии, вызванной дефицитом фолиевой кислоты, – фолиевую кислоту.Средства, влияющие на гемостаз
В разных областях медицины применяют лекарственные средства, понижающие (противосвертывающие) или повышающие (антигеморрагические) свертываемость крови.Противосвертывающие и антитромботические средства.
Для профилактики тромбообразования и развития тромбоэмболии, часто возникающих после оперативных вмешательств,инфаркта миокарда, а также других заболеваниях применяют вещества, ингибирующие свертывание крови. К противосвертывающим веществам относятся антикоагулянты, фибринолитические средства и антиагрегантные препараты. Антикоагулянты в основном препятствуют образованию нитей фибрина, тромбообразованию, способствуют прекращению роста уже возникших тромбов. Они делятся на 2 группы: антикоагулянты прямого и непрямого действия. К антикоагулянтам прямого действия относятся различные препараты естественных противосвертывающих факторов – гепарина и антитромбина III. Они действуют быстро и кратковременно. К антикоагулянтам непрямого действия относятся синкумар, фенилин, пелентан. Они являются антагонистами витамина К, необходимого для образования в печени протромбина. Эти вещества действуют только в организме и длительно. Фибринолитические средства вызывают разрушение образовавшихся нитей фибрина; они способствуют в основном рассасыванию свежих тромбов. Фибринолитические средства также делят на вещества прямого и непрямого действия. Представителем препаратов прямого действия является фибринолизин. В качестве препаратов второй группы применяют активаторы фибринолиза – препараты стрептокиназы (белка из р-гемолитического стрептококка А) и протеолитический фермент урокиназу. Антиагреганты ингибируют агрегацию тромбоцитов и эритроцитов, уменьшают их способность к склеиванию и прилипанию (адгезии) к эндотелию кровеносных сосудов. Антиагреганты способны не только предупреждать агрегацию, но и вызывать дезагрегацию уже агрегированных кровяных пластинок. Выраженное антиагрегационное действие оказывают нестероидные противовоспалительные препараты, из которых широкое применение в целях профилактики тромбообразования имеет ацетилсалициловая кислота. Ацетилсалициловая кислота снижает ферментативную активность циклооксигеназы и тем самым тормозит синтез тромбоксанов, повышающих агрегационную активность тромбоцитов. Антигеморрагичесие и гемостатические средства. В качестве антигеморрагических и гемостатических средств используют вещества различного механизма действия. При кровотечениях, связанных с повышением фибринолитической активности крови, применяют ингибиторы фибринолиза. К этой группе веществ относят как ингибиторы перехода плазминогена в плазмин за счет блокады активаторов плазминогена (аминокапроновая кислота), так и ингибиторы протеиназ плазмы, в частности плазмина (трасилол, контрикал: действующее вещество апротинин). При геморрагическом синдроме с гипопротромбинемией, вызванном, например, нарушением функции печени, используют препараты витамина К (викасол, фитоменадион). Из плазмы крови доноров получают естественный компонент свертывающей системы крови фибриноген. Активатором образования тромбопластина является лекарственное средство этамзилат. При недостатке факторов свертывания крови (например, при гемофилии) применяют гемате II (фактор свертывания VIII и фактор Виллебранда) при гемофилии А и фактор свертывания IX человеческий – при гемофилии В. В составе комбинированой гемостатической терапии применяют кальция хлорид. В качестве местных средств для остановки кровотечения используют пленку и губку фибринные изогенные, желпластан и др.Глава 7. Крово- и лимфообращение
Доставка кислорода и питательных веществ к тканям и клеткам млекопитающих животных и человека, а также выведение продуктов их жизнедеятельности обеспечиваются кровью, циркулирующей по замкнутой сердечно-сосудистой системе, состоящей из сердца и двух кругов кровообращения: большого и малого. Большой круг кровообращения начинается от левого желудочка сердца, из которого артериальная кровь поступает в аорту. Пройдя по артериям, артериолам, капиллярам всех органов, кроме легких, она отдает им кислород и питательные вещества, а забирает углекислоту и продукты метаболизма. Затем кровь собирается в венулы и вены и через верхнюю и нижнюю полые вены поступает в правое предсердие. Малый круг кровообращения начинается с правого желудочка сердца, откуда венозная кровь направляется в легочную артерию. Пройдя через легочные капилляры, кровь освобождается от углекислоты, оксигенируется и уже в качестве артериальной поступает через легочные вены в левое предсердие.Физиология сердца
Свойства сердечной мышцы
Сердечная мышца обладает следующими свойствами: 1. автоматией – способностью сердца ритмически сокращаться под влиянием импульсов, возникающих в нем самом; 2. возбудимостью – способностью сердца приходить в состояние возбуждения под действием раздражителя; 3. проводимостью – способностью сердечной мышцы проводить возбуждение; 4. сократимостью – способностью изменять свою форму и величину под действием раздражителя, а также растягивающей силы или крови.Автоматия
Субстратом автоматии в сердце является специфическая мышечная ткань, или проводящая система сердца, которая состоит из синусно-предсердного (синоатриального) (СА) узла, расположенного в стенке правого предсердия у места впадения в него верхней полой вены, предсердно-желудочкового (атриовентрикулярного^ узла, расположенного в межпредсердной перегородке на границе предсердий и желудочков. От атриовентрикулярного узла начинается пучок Гиса. Пройдя в толщу межжелудочковой перегородки, он делится на правую и левую ножки, заканчивающиеся конечными разветвлениями – волокнами Пуркинье. Верхушка сердца не обладает автоматией, а лишь сократимостью, так как в ней отсутствуют элементы проводящей системы сердца. В нормальных условиях водителем ритма, или пейсмекером, является синоатриальный узел. Частота разрядов синоатриального узла в покое составляет 70 в 1 минуту. Атриовентрикулярный узел – это водитель ритма второго порядка с частотой 40 -50 в 1 минуту. Он берет на себя роль водителя ритма, если по каким-либо причинам возбуждение от СА не может перейти на предсердия при атриовентрикулярной блокаде или при нарушении проводящей системы желудочков. Если поражены все основные водители ритма, то очень редкие импульсы (20 имп/с) могут возникать в волокнах Пуркинье – это водитель ритма 3-го порядка. Следовательно, существует градиент автоматии сердца, согласно которому степень автоматии тем выше, чем ближе расположен данный участок проводящей системы к синусному узлу.Электрическая активность клеток миокарда и проводящей системы сердца
Потенциал действия кардиомиоцитов начинается с быстрой риверсии мембранного потенциала, составляющего -90 мВ и создаваемого за счет К+-потенциала, до пика ПД (+ 30 мВ) (рис.11). Это фаза быстрой деполяризации, обусловленная коротким значительным повышением проницаемости для Na+, который лавинообразно устремляется в клетку. Фаза быстрой деполяризации очень короткая и составляет всего 1 -2 мс. Начальный вход Na+ быстро инактивируется, однако деполяризация мембраны продолжается за счет активации медленных натрий-кальциевых каналов, а вход Са2+ приводит к развитию плато ПД – это специфическая особенность клеток миокарда. В этот период быстрые натриевые каналы инактивируются и клетка становится абсолютно невозбудима. Это фаза абсолютной рефрактерности. Одновременно происходит активация калиевых каналов, а выходящие из клетки ионы К+ создают фазу быстрой реполяризации мембраны. Ускорение процесса реполяризации происходит за счет закрытия кальциевых каналов. В конце периода реполяризации постепенно закрываются калиевые каналы и реактивируются натриевые. Это приводит к восстановлению возбудимости кардиомиоцита и возникновению относительной рефрактерной фазы. Длительность ПД кардиомиоцита составляет 200–400 мс. Калий-натриевый насос, создающий потенциал покоя или мембранный потенциал миокардиоцита, может быть инактивирован под действием сердечных гликозидов (препараты наперстянки, строфантина), которые приводят также к повышению внутриклеточной концентрации Na+, снижению интенсивности обмена внутриклеточного Са2+ на внеклеточный Na+, накоплению Са2+ в клетке. В результате сократимость миокарда становится больше. Ее можно увеличить и за счет повышения внеклеточной концентрации Са2+ и с помощью веществ (адреналин, норадреналин), ускоряющих вход Са2+ во время ПД. Если удалить Са2+ из внешней среды или заблокировать вход Са2+ во время ПД с помощью таких веществ – антагонистов кальция, как верапамил, нифедипин и др., то сократимость сердца уменьшается. Клетки проводящей системы сердца и, в частности, клетки пейсмекера, обладающие автоматией, в отличие от клеток рабочего миокарда-кардиомиоцитов могут спонтанно деполяризоваться до критического уровня. В таких клетках за фазой реполяризации следует фаза медленной диастолической деполяризации (МДД), которая приводит к снижению МП до порогового уровня и возникновению ПД. МДД – это местное, нераспространяющееся возбуждение, в отличие от ПД, который является распространяющимся возбуждением.Таким образом, пейсмекерные клетки отличаются от кардиомиоцитов: 1. низким уровнем МП – около 50 – 70 мВ 2. наличием МДД 3. близкой к пикообразному потенциалу формой ПД, 4. низкой амплитудой ПД – 30 – 50 мВ без явления риверсии (овершута).
Особенности электрической активности пейсмекерных клеток обусловлены целым рядом процессов, происходящих на их мембране. Во-первых, эти клетки даже в условиях «покоя» имеют повышенную проницаемость для ионов Na+, что приводит к снижению МП. Во-вторых, в период реполяризации на мембране открываются только медленные натрий-кальциевые каналы, так как быстрые натриевые каналы из-за низкого МП уже инактивированы. В клетках синоатриального узла в период реполяризации быстро инактивируются открытые калиевые каналы, но повышается натриевая проницаемость, на фоне которой и возникает МДД, а затем и ПД. Потенциал действия синоатриального узла распространяется на все остальные отделы проводящей системы сердца. Таким образом, синоатриальный узел навязывает всем «ведомым» отделам проводящей системы свой ритм. Если возбуждение но поступает от главного пейсмекера, то «латентные» водители ритма, т. е. клетки сердца, обладающие автоматией, берут на себя функцию нового пейсмекера, в них также зарождается МДД и ПД, а сердце продолжает свою работу.
Возбудимость
Во время развития фаз ПД и сокращения сердечной мышцы меняется уровень ее возбудимости. Периоду быстрой реполяризации и плато, а также всему периоду сокращения сердечной мышцы соответствует фаза абсолютной рефрактерности (см. рис. 11), когда мышца абсолютно невозбудима и не отвечает даже па сверхпороговые раздражители. Ее длительность – 0,27 с. Концу периода реполяризации и фазе расслабления соответствует фаза относительной рефрактерности, когда возбудимость начинает восстанавливаться, но еще не достигла исходных значений. В этот период лишь сверхпороговые стимулы могут вызвать сокращение мышцы сердца. Длительность относительной рефрактерной фазы – 0,03 с. В период восстановления МП и в конце расслабления сердечная мышца находится в состоянии повышенной, или супернормальной, возбудимости. Эту фазу называют еще периодом экзальтации, когда сердечная мышца отвечает даже на подпороговые стимулы. Рефрактерность обусловлена инактивацией быстрых натриевых каналов и соответствует развитию ПД, поэтому продолжительность рефрактерного периода, как правило, связана с длительностью ПД. Местные анестетики, подавляя быстрые натриевые каналы и замедляя восстановление проницаемости после инактивации, вызывают удлинение рефрактерного периода, но не влияют на продолжительность ПД. Поскольку очередное сокращение возможно только по окончании периода абсолютной рефрактерности предшествующего ПД, сердечная мышца, в отличие от скелетной, не отвечает на повторные раздражения, т. е. она не способна к тетанусу. Таким образом, длительная абсолютная рефрактерная фаза и короткая фаза супернормальной возбудимости сердечной мышцы исключают для нее состояние тетануса, которое бы мешало нагнетательной функции сердца, поэтому сердечная мышца работает в одиночном режиме.
Однако если повторное сверхпороговое раздражение нанести в фазу расслабления очередного сокращения, которое совпадает с периодом относительной рефрактерности, возникает внеочередное сокращение, или экстрасистола. В зависимости от того, где возникает новый, или «эктопический», очаг возбуждения, различают синусовую, предсердную и желудочковую экстрасистолы. Желудочковая экстрасистола отличается следующей за ней более продолжительной, чем обычно, компенсаторной паузой. Она появляется в результате выпадения очередного нормального сокращения. При этом импульсы, возникшие в синоатриальном узле, поступают к миокарду желудочков, когда они еще находятся в состоянии абсолютной рефрактерной фазы экстрасистолы. При синусовых и предсердных экстрасистолах компенсаторная пауза отсутствует.
Экстрасистолию могут вызвать также изменения ионного состава крови и внеклеточной жидкости. Так, снижение внеклеточной концентрации К+ (ниже 4 ммоль/л) повышает активность пейсмекера и приводит к активации гетерогенных очагов возбуждения и как следствие – к нарушению ритма. Большие дозы алкоголя, курение табака могут спровоцировать экстрасистолию. Гипоксия (недостаток кислорода в тканях) значительно изменяет метаболизм в кардиомиоцитах и может привести к появлению экстрасистол. В период полового созревания, у спортсменов в результате перетренировок также могут возникать единичные экстрасистолы. Экстрасистолию могут вызвать изменения со стороны вегетативной нервной системы и коры больших полушарий.
Если в норме частота сердечных сокращений колеблется от 60 до 80 в 1 мин, то ее урежение до 40 – 50 в 1 мин называется брадикардией, а учащение свыше 90- 100 – тахикардией. Брадикардия отмечается во время сна и у спортсменов в состоянии покоя, а тахикардия – при интенсивной мышечной деятельности и эмоциональном напряжении.
У некоторых молодых людей в норме наблюдаются изменения сердечного ритма, связанные с актом дыхания, – дыхательная аритмия, которая заключается в том, что частота сокращений сердца на вдохе увеличивается, а на выдохе и во время дыхательной паузы уменьшается.
При нарушении проводимости и возбудимости сердца происходят изменения ритма работы предсердий и желудочков, названные трепетанием и мерцанием (фибрилляция). При этом предсердия и желудочки сокращаются асинхронно с частотой от 300 до 600 в 1 минуту, возбуждение возникает в различных участках сердечной мышцы. Подобное нарушение ритма наблюдается при инфаркте миокарда, а также при отравлении фармакологическими препаратами (наперстянка, хлороформ, барий). У человека фибрилляция, как правило, приводит к смерти, если не принять срочные меры. Фибрилляцию можно прекратить непосредственным воздействием на сердце мощного электрического разряда (напряжением в несколько киловольт), после чего синхронность сокращений предсердий и желудочков восстанавливается.
Таким образом, длительная абсолютная рефрактерная фаза и короткая фаза супернормальной возбудимости сердечной мышцы исключают для нее состояние тетануса, которое бы мешало нагнетательной функции сердца, поэтому сердечная мышца работает в одиночном режиме.
Однако если повторное сверхпороговое раздражение нанести в фазу расслабления очередного сокращения, которое совпадает с периодом относительной рефрактерности, возникает внеочередное сокращение, или экстрасистола. В зависимости от того, где возникает новый, или «эктопический», очаг возбуждения, различают синусовую, предсердную и желудочковую экстрасистолы. Желудочковая экстрасистола отличается следующей за ней более продолжительной, чем обычно, компенсаторной паузой. Она появляется в результате выпадения очередного нормального сокращения. При этом импульсы, возникшие в синоатриальном узле, поступают к миокарду желудочков, когда они еще находятся в состоянии абсолютной рефрактерной фазы экстрасистолы. При синусовых и предсердных экстрасистолах компенсаторная пауза отсутствует.
Экстрасистолию могут вызвать также изменения ионного состава крови и внеклеточной жидкости. Так, снижение внеклеточной концентрации К+ (ниже 4 ммоль/л) повышает активность пейсмекера и приводит к активации гетерогенных очагов возбуждения и как следствие – к нарушению ритма. Большие дозы алкоголя, курение табака могут спровоцировать экстрасистолию. Гипоксия (недостаток кислорода в тканях) значительно изменяет метаболизм в кардиомиоцитах и может привести к появлению экстрасистол. В период полового созревания, у спортсменов в результате перетренировок также могут возникать единичные экстрасистолы. Экстрасистолию могут вызвать изменения со стороны вегетативной нервной системы и коры больших полушарий.
Если в норме частота сердечных сокращений колеблется от 60 до 80 в 1 мин, то ее урежение до 40 – 50 в 1 мин называется брадикардией, а учащение свыше 90- 100 – тахикардией. Брадикардия отмечается во время сна и у спортсменов в состоянии покоя, а тахикардия – при интенсивной мышечной деятельности и эмоциональном напряжении.
У некоторых молодых людей в норме наблюдаются изменения сердечного ритма, связанные с актом дыхания, – дыхательная аритмия, которая заключается в том, что частота сокращений сердца на вдохе увеличивается, а на выдохе и во время дыхательной паузы уменьшается.
При нарушении проводимости и возбудимости сердца происходят изменения ритма работы предсердий и желудочков, названные трепетанием и мерцанием (фибрилляция). При этом предсердия и желудочки сокращаются асинхронно с частотой от 300 до 600 в 1 минуту, возбуждение возникает в различных участках сердечной мышцы. Подобное нарушение ритма наблюдается при инфаркте миокарда, а также при отравлении фармакологическими препаратами (наперстянка, хлороформ, барий). У человека фибрилляция, как правило, приводит к смерти, если не принять срочные меры. Фибрилляцию можно прекратить непосредственным воздействием на сердце мощного электрического разряда (напряжением в несколько киловольт), после чего синхронность сокращений предсердий и желудочков восстанавливается.
Проводимость и сократимость
Между клетками проводящей системы и рабочим миокардом имеются тесные контакты в виде нексусов, поэтому возбуждение, возникшее в одном участке сердца, проводится без затухания (без декремента) в другой. Скорость распространения возбуждения от предсердий к желудочкам составляет 0,8–1,0 м/с. Проходя атриовентрикулярный узел, возбуждение задерживается на 0,04 с. Далее, распространившись по пучку Гиса и волокнам Пуркинье, возбуждение охватывает мускулатуру желудочков со скоростью 0,75–4,0 м/с. Таким образом, мышечная ткань сердца ведет себя как функциональный синцитий. Благодаря этой особенности сердце, в отличие от скелетной мышцы, подчиняется закону «все или ничего». Это означает, что на раздражение возрастающей силы, начиная от порогового, мышца сердца отвечает сразу возбуждением всех волокон, т. е. амплитуда сокращений одинакова. Если раздражитель подпороговый, то она совсем не реагирует. Однако если раздражать сердечную мышцу током возрастающей частоты, оставив его силу постоянной, то каждое увеличение частоты раздражителя вызовет возрастающее сокращение сердечной мышцы – феномен «treppe» – лестницы. Это явление можно объяснить попаданием каждого последующего импульса в фазу повышенной возбудимости и накоплением ионов Са2+ в области миофибрилл, что и дает усиление ответной реакции. Сокращение сердца, как и у скелетных мышц, запускается ПД. Однако если у скелетной мышцы ПД составляет всего несколько миллисекунд и предшествует сокращению, то у сердечной ПД и фазы сокращения перекрывают друг друга. ПД заканчивается только после начала фазы расслабления. Это одна из особенностей электромеханического сопряжения сердечной мышцы. Другая особенность состоит в том, что существует взаимосвязь между внутриклеточным депо Са2+ и Са2+ внеклеточной среды. Как упоминалось выше, во время ПД Са2+ входит в клетку из внеклеточной среды и увеличивает длительность ПД, а значит, и рефрактерного периода, тем самым создаются условия для пополнения внутриклеточных запасов кальция, участвующего в последующих сокращениях сердца.Сердечный цикл
Сократительная деятельность сердца связана с работой клапанов и давлением в его полостях. Эти изменения носят фазный характер и составляют основу сердечного цикла, длительность которого равна 0,8 с, но может меняться в зависимости от частоты сердечных сокращений. Чем больше частота сердечных сокращений, тем короче сердечный цикл и наоборот. Сердечный цикл состоит из 3 основных фаз: систолы предсердий, систолы желудочков и общей паузы или диастолы. Систола предсердий длится 0,1 с, при этом атриовентрикулярные клапаны открыты, а полулунные закрыты, давление в предсердиях равно 5–8 мм рт.ст. Систола предсердий заканчивается закрытием атриовентрикулярных клапанов и начинается систола желудочков, ее длительность – 0,33 с. Систола желудочков, в свою очередь, делится на период напряжения и период изгнания крови. Период напряжения – 0,08 с. Он также состоит из 2 фаз: асинхронного сокращения – промежутка времени от начала возбуждения и сокращения кардиомиоцитов до закрытия атриовентрикулярных клапанов, после чего давление в полостях желудочков быстро растет до 60 – 80 мм рт.ст. и начинается фаза изометрического сокращения. С моментом закрытия атриовентрикулярных клапанов совпадает возникновение I систолического тона сердца. При закрытых полулунных и атриовентрикулярных клапанах длина волокон не изменяется, а увеличивается только напряжение в полостях желудочков, в результате давление в них резко возрастает, становясь выше, чем в аорте и легочной артерии, полулунные клапаны открываются, а атриовентрикулярные остаются закрытыми, и кровь устремляется в эти сосуды. Начинается период изгнания крови, его длительность – 0,25 с. Он состоит из фазы быстрого изгнания и фазы медленного изгнания крови. Давление в желудочках составляет: в левом – 120–130 мм рт.ст., в правом – до 25 – 30 мм рт.ст. Диастола желудочков, длящаяся 0,47 с, начинается с протодиастолического периода (0,04 с) – это промежуток времени от начала падения давления внутри желудочков до момента закрытия полулунных клапанов, после которого давление в желудочках продолжает падать, а атриовентрикулярные клапаны еще не открыты – это период изометрического расслабления желудочков. Моменту закрытия полулунных клапанов соответствует воз-никновение II диастолического тона сердца. Как только давление в желудочках снизится до 0, открываются атриовентрикулярные клапаны и кровь из предсердий поступает в желудочки. Это период наполнения желудочков кровью, который длится 0,25 с и делится на фазы быстрого (0,08 с) и медленного (0,17 с) наполнения. Периоду наполнения, сопровождающемуся колебаниями стенок желудочков, соответствует возникновение III тона сердца. В конце фазы медленного наполнения наступает систола предсердий, в результате за 0,1 с «выжимается» около 40 мл крови из предсердий в желудочки (пресистолический период), что ведет к появлению IV тона сердца, после чего начинается новый цикл сокращения желудочков. Итак, в результате сократительной деятельности сердца и работы клапанов возникают 4 тона сердца. Из них I – систолический длительностью 0,11 с и II – диастолический длительностью 0,07 с. Эти тоны можно прослушать и зарегистрировать. III тон соответствует началу наполнения желудочков и вибрации их стенок при быстром притоке крови, хорошо прослушивается у детей, его можно зарегистрировать. IV тон обусловлен сокращением предсердий, он только регистрируется. За одну систолу при ритме сокращений 70 – 75 в 1 мин сердце выбрасывает в аорту 60 – 70 мл крови – это систолический объем крови (СО). Умножив его на число сердечных сокращений (ЧСС) в 1 мин, получим минутный объем крови (МОК), равный 4,5 -5,0 л, т. е. количество крови, выбрасываемое сердцем за 1 мин.МОК= СО•ЧСС.
В покое не вся кровь во время систолы изгоняется из желудочков, остается «резервный объем», который может быть использован для увеличения сердечного выброса. В настоящее время рассчитывают величину сердечного индекса – это отношение МОК в л/мин к поверхности тела в м2. Для «стандартного» мужчины он равен 3 л/мин-м2.
Электрокардиография
Вокруг возбужденного сердца возникает электрическое поле, которое можно зарегистрировать с поверхности тела в виде электрокардиограммы. Электрические потенциалы прежде всего возникают в возбужденном синоатриальном узле. Этот участок становится электроотрицательным по отношению к невозбужденному, заряженному положительно. Это и приводит к появлению электрических потенциалов и дальнейшему их распространению по проводящей системе сердца, миокарду предсердий и желудочков. Электрокардиограмма отражает процесс возникновения возбуждения и его проведение по сердцу, но не его сокращение. В нормальной электрокардиограмме различают пять зубцов: Р, Q, R, S, Т (рис.12). Возникновение зубца Р обусловлено распространением возбуждения в предсердиях – это алгебраическая сумма электрических потенциалов, возникающих в предсердиях. Зубец Q соответствует возбуждению сосочковых мышц. Зубец R – возбуждению оснований желудочков, зубец S – верхушки сердца. Зубец Т отражает процесс реполяризации желудочков и состояние метаболизма миокарда. Он очень изменчив и может искажаться при различного рода интоксикациях, например, при инфекциях (дизентерия и др.), отравлениях химическими ядами, при гипоксии, инфаркте миокарда, диабете.
Итак, различают предсердный комплекс, куда входит зубец Р, и сегмент PQ, а также желудочковый комплекс QRS и сегмент ST. Интервал PQ от начала зубца Р до начала зубца О отражает время проведения возбуждения от предсердий к желудочкам, в норме он равен 0,12–0,18 с.
При нарушении проведения импульсов из предсердий к желудочкам, вызванном или органическими изменениями в проводящей системе, или отравлением сердечными глюкозидами, увеличением содержания ионов К +, снижением МП, а также гипоксией возникает неполная атриовентрикулярная блокада. При этом не все импульсы периодически проводятся к желудочкам или их проведение задерживается, тогда интервал PQ становится больше 0,18 с.
При полном нарушении проводимости между предсердиями и желудочками возникает полная атриовентрикулярная блокада – предсердия и желудочки сокращаются независимо друг от друга: предсердия в синусном ритме, желудочки – в ритме пейсмекера 2-го или 3-го порядка.
Длительность комплекса QRS составляет 0,06–0,1 с. Его уширение является признаком нарушения внутрижелудочковой проводимости. Интервал ОТ составляет 0,36 с и зависит от частоты сердечных сокращений. Чем больше частота, тем короче интервал. Амплитуда зубцов ЭКГ следующая: Р‹0,25 мВ; 0‹1/47; R+S›0,6MB; Т= от 1/6 до 2/3R.
Для регистрации ЭКГ используют 3 стандартных биполярных отведения от конечностей (треугольник Эйнтховена), 1-е отведение: правая рука-левая рука; 2-е отведение: правая рука-левая нога; 3-е отведение: левая рука-левая нога. Кроме того, регистрируют 3 усиленных униполярных отведения: aVR – активный электрод на правой руке, aVL – активный электрод на левой руке, aVF – активный электрод на левой поте и 6 униполярных грудных отведений по Вильсону – V1-V6.
При биполярных отведениях по Эйптховеиу точки, от которых отводят потенциалы, совпадают с вершинами равностороннего треугольника, стороны которого и представляют собой оси отведений. С помощью треугольника Эйнтховена можно установить величину электродвижущей силы сердца, а значит, и высоту зубцов ЭКГ. Высота зубца R во 2-м отведении в нормограмме равна сумме зубца R в 1-м и 3-м отведении.
Электрокардиограмма отражает процесс возникновения возбуждения и его проведение по сердцу, но не его сокращение. В нормальной электрокардиограмме различают пять зубцов: Р, Q, R, S, Т (рис.12). Возникновение зубца Р обусловлено распространением возбуждения в предсердиях – это алгебраическая сумма электрических потенциалов, возникающих в предсердиях. Зубец Q соответствует возбуждению сосочковых мышц. Зубец R – возбуждению оснований желудочков, зубец S – верхушки сердца. Зубец Т отражает процесс реполяризации желудочков и состояние метаболизма миокарда. Он очень изменчив и может искажаться при различного рода интоксикациях, например, при инфекциях (дизентерия и др.), отравлениях химическими ядами, при гипоксии, инфаркте миокарда, диабете.
Итак, различают предсердный комплекс, куда входит зубец Р, и сегмент PQ, а также желудочковый комплекс QRS и сегмент ST. Интервал PQ от начала зубца Р до начала зубца О отражает время проведения возбуждения от предсердий к желудочкам, в норме он равен 0,12–0,18 с.
При нарушении проведения импульсов из предсердий к желудочкам, вызванном или органическими изменениями в проводящей системе, или отравлением сердечными глюкозидами, увеличением содержания ионов К +, снижением МП, а также гипоксией возникает неполная атриовентрикулярная блокада. При этом не все импульсы периодически проводятся к желудочкам или их проведение задерживается, тогда интервал PQ становится больше 0,18 с.
При полном нарушении проводимости между предсердиями и желудочками возникает полная атриовентрикулярная блокада – предсердия и желудочки сокращаются независимо друг от друга: предсердия в синусном ритме, желудочки – в ритме пейсмекера 2-го или 3-го порядка.
Длительность комплекса QRS составляет 0,06–0,1 с. Его уширение является признаком нарушения внутрижелудочковой проводимости. Интервал ОТ составляет 0,36 с и зависит от частоты сердечных сокращений. Чем больше частота, тем короче интервал. Амплитуда зубцов ЭКГ следующая: Р‹0,25 мВ; 0‹1/47; R+S›0,6MB; Т= от 1/6 до 2/3R.
Для регистрации ЭКГ используют 3 стандартных биполярных отведения от конечностей (треугольник Эйнтховена), 1-е отведение: правая рука-левая рука; 2-е отведение: правая рука-левая нога; 3-е отведение: левая рука-левая нога. Кроме того, регистрируют 3 усиленных униполярных отведения: aVR – активный электрод на правой руке, aVL – активный электрод на левой руке, aVF – активный электрод на левой поте и 6 униполярных грудных отведений по Вильсону – V1-V6.
При биполярных отведениях по Эйптховеиу точки, от которых отводят потенциалы, совпадают с вершинами равностороннего треугольника, стороны которого и представляют собой оси отведений. С помощью треугольника Эйнтховена можно установить величину электродвижущей силы сердца, а значит, и высоту зубцов ЭКГ. Высота зубца R во 2-м отведении в нормограмме равна сумме зубца R в 1-м и 3-м отведении.
Сосудистая система
Классификация сосудов. Основы гемодинамики
По своим функциональным характеристикам сосуды большого и малого кругов кровообращения делятся на следующие группы: 1. Амортизирующие сосуды эластического типа. К ним относятся аорта, легочная артерия, крупные артерии. Их функция выражается в сглаживании (амортизации) резкого подъема артериального давления во время систолы. За счет эластических свойств этих сосудов создается непрерывный кровоток, как во время систолы, так и диастолы. Во время систолы одна часть кинетической энергии, создаваемой сердцем, затрачивается на продвижение крови, другая преобразуется в потенциальную энергию растянутых сосудов аорты и крупных артерий, образующих эластическую «компрессионную камеру». Во время диастолы потенциальная энергия растянутого сосуда снова переходит в кинетическую энергию движения крови. Благодаря этому эффекту и обеспечивается непрерывное течение крови. 2. Резистивные сосуды (сосуды сопротивления). К ним относятся средние и мелкие артерии, артериолы, прекапилляры и прекапиллярные сфинктеры. Эти сосуды имеют хорошо развитую гладкомышечную стенку, за счет которой просвет сосуда может резко уменьшаться и создавать большое сопротивление кровотоку. Этими свойствами особенно обладают артериолы, которые называют «кранами сосудистой системы». 3. Обменные сосуды. К ним относятся капилляры, в которых происходят обменные процессы между кровью и тканевой жидкостью. 4. Емкостные сосуды – это вены, благодаря своей растяжимости они способны вмещать 70 – 80% всей крови. 5. Артериовснозные анастомозы (шунты) – это сосуды, соединяющие артериальную и венозную части сосудистой системы, минуя капиллярную сеть.Движение крови по кровеносным сосудам подчиняется законам гемодинамики, являющейся частью гидродинамики – науки о движении жидкостей по трубкам. Основным условием кровотока является градиент давления между различными отделами сосудистой системы. Давление в сосудах создается работой сердца. Кровь течет из области высокого давления в область низкого. При движении ей приходится преодолевать сопротивление, создаваемое, во-первых, трением частиц крови друг о друга, во-вторых, трением частиц крови о стенки сосуда. Особенно велико это сопротивление в артериолах и прекапиллярах. Сопротивление (R) в кровеносном сосуде можно определить по формуле Пуазейля.
R=8lη/πr4
В соответствии с законами гидродинамики количество жидкости (крови), протекающей через поперечное сечение сосуда за единицу времени (мл/с), или объемная скорость кровотока (О), прямо пропорциональна разности давления в начале (P1) сосудистой системы – в аорте и в ее конце (Р2), т. е. в полых венах, и обратно пропорциональна сопротивлению (Д) току жидкости.
Q=(P1-P2)/R
В связи с замкнутостью кровеносной системы объемная скорость кровотока во всех ее отделах (во всех артериях, всех капиллярах, всех венах) одинакова. Зная объемную скорость кровотока, можно рассчитать линейную скорость или расстояние, проходимое частицей крови за единицу времени:
V = Q/πr2.
В отличие от объемной, линейная скорость изменяется по ходу сосудистого русла и обратно пропорциональна суммарному по-перечному сечению всех сосудов данного калибра. Самое узкое место в сосудистой системе – это аорта, поэтому она имеет самую большую линейную скорость кровотока – 50 – 60 см/с. В артериях она равна 20 – 40 см/с, в артериолах – 5 мм/с, в венах – 7 – 20 см/с; самый широкий суммарный просвет, в 500 – 600 раз превышающий диаметр аорты, имеют капилляры, поэтому линейная скорость в них минимальная – 0,5 мм/с. Помимо объемной и линейной скорости кровотока, существует еще один гемодинамический показатель – время кругооборота крови – это время, в течение которого частица крови пройдет и большой и малый круг кровообращения, оно составляет 20- 25 с. У здорового человека в возрасте 20 – 40 лет в плечевой артерии оно равно 110 – 120 мм рт.ст. Во время диастолы АД снижает- Основным гемодинамическим показателем является артериальное давление (АД), уровень которого по ходу сосудистого русла падает неравномерно (рис. 13) и зависит от ряда факторов, главный из которых – работа сердца. Во время систолы АД повышается – это систолическое, или максимальное, давление.
 Диастолическое, или минимальное, давление, равное 70 – 80 мм рт.ст. Разницу между систолическим и диастолическим давлением составляет пульсовое давление – 40 мм рт.ст. Различают еще среднее давление, или равнодействующую изменений давления во время систолы и диастолы. Оно равно 100 мм рт.ст. АД прежде всего зависит от работы сердца. Остановка сердца приводит к быстрому падению АД до 0.
На уровень давления влияет количество циркулирующей крови. При кровопотере давление снижается. АД зависит также от эластичности сосудистой стенки. Поэтому у пожилых людей (после 50 лет) в связи с потерей эластичности сосуда АД повышается до 140/90 мм рт.ст.
Сопротивление сосуда, которое изменяется в зависимости от его просвета, влияет на уровень АД. Так, прием сосудосуживающих препаратов приводит к увеличению сопротивления в сосуде и повышению АД.
Увеличение вязкости крови повышает артериальное давление, уменьшение – снижает.
Возраст определяет величину АД. У новорожденных систолическое давление равно 70 – 80 мм рт.ст, у ребенка первых лет жизни – 80- 120, подростка – 110–120, у взрослого человека 20–40 лет 110/70–120/80, после 50 лет 140–150/90 мм рт.ст. Физические упражнения повышают давление до 180 мм рт.ст. и более, особенно систолическое. Во время сна давление падает на 15 – 20 мм рт.ст.
Прием пищи, эмоции повышают систолическое давление. На уровень АД влияет положение тела в пространстве, так как сосудистая система находится в поле силы тяжести. В вертикальном положении давление, создаваемое работой сердца, складывается с гидростатическим давлением. Поэтому давление в сосудах, расположенных ниже сердца, больше чем давление в сосудах, расположенных выше сердца. При горизонтальном положении эти различия нивелируются. Так, в вертикальном положении в сосудах стопы, т. е. на 125 см ниже сердца, гидростатическое давление составляет 90 мм рт.ст. Сложив его со средним АД, получим: 100 + 90= 190 мм рт.ст. В артериях головного мозга (на 40 см выше сердца) АД снижается на 30 мм рт.ст., составляя 100–30 = 70 мм рт.ст.
В настоящее время существуют два способа измерения АД. Первый – кровавый, прямой, применяется в остром эксперименте на животных, второй – бескровный, непрямой, используется для измерения давления на плечевой артерии у человека.
На кривой давления (рис.14), записанной на сонной артерии животного, различают волны 3 порядков: волны первого порядка, или пульсовые, обусловленные деятельностью сердца, волны второго порядка, или дыхательные, вдох сопровождается понижением АД, а выдох – повышением.
Диастолическое, или минимальное, давление, равное 70 – 80 мм рт.ст. Разницу между систолическим и диастолическим давлением составляет пульсовое давление – 40 мм рт.ст. Различают еще среднее давление, или равнодействующую изменений давления во время систолы и диастолы. Оно равно 100 мм рт.ст. АД прежде всего зависит от работы сердца. Остановка сердца приводит к быстрому падению АД до 0.
На уровень давления влияет количество циркулирующей крови. При кровопотере давление снижается. АД зависит также от эластичности сосудистой стенки. Поэтому у пожилых людей (после 50 лет) в связи с потерей эластичности сосуда АД повышается до 140/90 мм рт.ст.
Сопротивление сосуда, которое изменяется в зависимости от его просвета, влияет на уровень АД. Так, прием сосудосуживающих препаратов приводит к увеличению сопротивления в сосуде и повышению АД.
Увеличение вязкости крови повышает артериальное давление, уменьшение – снижает.
Возраст определяет величину АД. У новорожденных систолическое давление равно 70 – 80 мм рт.ст, у ребенка первых лет жизни – 80- 120, подростка – 110–120, у взрослого человека 20–40 лет 110/70–120/80, после 50 лет 140–150/90 мм рт.ст. Физические упражнения повышают давление до 180 мм рт.ст. и более, особенно систолическое. Во время сна давление падает на 15 – 20 мм рт.ст.
Прием пищи, эмоции повышают систолическое давление. На уровень АД влияет положение тела в пространстве, так как сосудистая система находится в поле силы тяжести. В вертикальном положении давление, создаваемое работой сердца, складывается с гидростатическим давлением. Поэтому давление в сосудах, расположенных ниже сердца, больше чем давление в сосудах, расположенных выше сердца. При горизонтальном положении эти различия нивелируются. Так, в вертикальном положении в сосудах стопы, т. е. на 125 см ниже сердца, гидростатическое давление составляет 90 мм рт.ст. Сложив его со средним АД, получим: 100 + 90= 190 мм рт.ст. В артериях головного мозга (на 40 см выше сердца) АД снижается на 30 мм рт.ст., составляя 100–30 = 70 мм рт.ст.
В настоящее время существуют два способа измерения АД. Первый – кровавый, прямой, применяется в остром эксперименте на животных, второй – бескровный, непрямой, используется для измерения давления на плечевой артерии у человека.
На кривой давления (рис.14), записанной на сонной артерии животного, различают волны 3 порядков: волны первого порядка, или пульсовые, обусловленные деятельностью сердца, волны второго порядка, или дыхательные, вдох сопровождается понижением АД, а выдох – повышением.
 По мере снижения давления в манжетке, звуковые явления, создаваемые завихрениями крови в еще пережатой артерии, про-слушиваются достаточно хорошо. Затем они исчезают, так как сосуд открыт как во время систолы, так и во время диастолы, препятствий для прохождения крови нет. Момент исчезновения тонов Короткова соответствует диастолическому, или минимальному, давлению.
По мере снижения давления в манжетке, звуковые явления, создаваемые завихрениями крови в еще пережатой артерии, про-слушиваются достаточно хорошо. Затем они исчезают, так как сосуд открыт как во время систолы, так и во время диастолы, препятствий для прохождения крови нет. Момент исчезновения тонов Короткова соответствует диастолическому, или минимальному, давлению.
Артериальный пульс
Артериальный пульс – это ритмические колебания стенки артерии, связанные с повышением давления во время систолы. Деятельность сердца создает два вида движения в артериальной системе: пульсовую волну и пульсирующее течение крови, или линейную скорость кровотока (в артериях она не более 50 см/с). Пульсовая волна возникает в аорте во время фазы изгнания крови и распространяется со скоростью 4–6 м/с. Периферических артерий мышечного типа (например, лучевой) она достигает со скоростью 8–12 м/с. С возрастом эластичность артерий снижается и скорость распространения пульсовой волны (СРПВ) возрастает. Она может увеличиваться при повышении АД в связи с увеличением напряжения сосудистой стенки. СРПВ претерпевает значительные изменения под действием лекарственных препаратов. Артериальный пульс можно зарегистрировать с помощью приборов сфигмографов. Кривая пульса называется сфигмограммой. Различают центральный пульс – пульс на аорте и прилегающих к ней артериях (сонной, подключичной) и периферический – пульс на лучевой, бедренной и других артериях. На кривой центрального пульса (рис.15) имеется восходящая часть – анакрота, обусловленная повышением давления и растяжением стенки артерии в начале фазы изгнания. В конце периода изгнания перед закрытием полулунных клапанов происходит внезапное падение давления в аорте, при этом регистрируется выемка, или инцизура. Далее происходит захлопывание полулунных клапанов и возникает вторичная волна повышения давления. Ей соответствует дикротический подъем, или зубец, после которого регистрируется катакрота – спад пульсовой кривой, обусловленный диастолой сердца и падением давления в желудочках.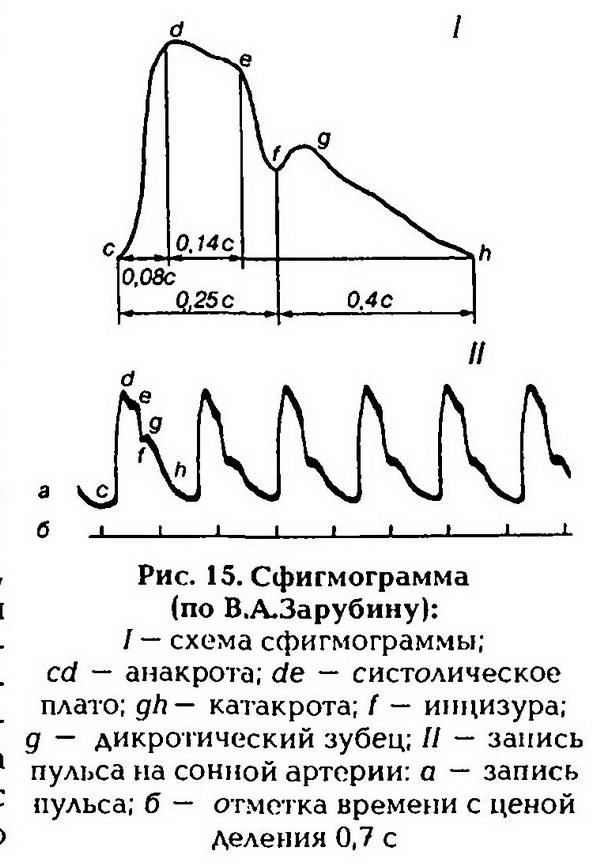 Центральный пульс отличается от периферического, тем что, начиная от вершины подъема кривой, может регистрироваться систолическое плато, образованное ударной и остаточной систолической волнами.
На кривой периферического пульса анакротический подъем более медленный, дикротический зубец менее выражен и является результатом интерференции центральных и периферических волн.
Артериальный пульс отражает состояние сердечно-сосудистой системы и имеет несколько характеристик: частоту, ритм, быстроту, амплитуду, напряжение и форму. Частота пульса у здорового человека соответствует частоте сердечных сокращений. В покое она равна 60 -80 в 1 минуту. Если пульс менее 60 в 1 минуту – это брадикардия, более 80 – тахикардия. Повышение температуры тела на 1°С сопровождается учащением пульса на 8 ударов в 1 минуту.
Ритм пульса может быть правильным – это ритмичный пульс или неправильным – аритмичный (например, дыхательная аритмия).
Быстрота пульса отражает скорость, с которой происходит повышение давления в артерии во время подъема пульсовой волны и снижение во время ее спада. Различают быстрый и медленный пульс, оба вида пульса наблюдаются при патологии аортальных клапанов и аорты.
Амплитуда пульса – это амплитуда колебаний стенки сосуда, зависящая от систолического объема сердца, а также от эластичности сосудов: чем они более эластичны, тем меньше амплитуда пульса.
Напряжение пульса определяется тем сопротивлением стенки артерии, которая противодействует нажиму давящего пальца. Различают твердый и мягкий пульс. При высоком АД пульс становится твердым, «проволочным».
По форме пульс может быть дикротическим или анакротическим в зависимости от степени выраженности дикротического зубца.
Центральный пульс отличается от периферического, тем что, начиная от вершины подъема кривой, может регистрироваться систолическое плато, образованное ударной и остаточной систолической волнами.
На кривой периферического пульса анакротический подъем более медленный, дикротический зубец менее выражен и является результатом интерференции центральных и периферических волн.
Артериальный пульс отражает состояние сердечно-сосудистой системы и имеет несколько характеристик: частоту, ритм, быстроту, амплитуду, напряжение и форму. Частота пульса у здорового человека соответствует частоте сердечных сокращений. В покое она равна 60 -80 в 1 минуту. Если пульс менее 60 в 1 минуту – это брадикардия, более 80 – тахикардия. Повышение температуры тела на 1°С сопровождается учащением пульса на 8 ударов в 1 минуту.
Ритм пульса может быть правильным – это ритмичный пульс или неправильным – аритмичный (например, дыхательная аритмия).
Быстрота пульса отражает скорость, с которой происходит повышение давления в артерии во время подъема пульсовой волны и снижение во время ее спада. Различают быстрый и медленный пульс, оба вида пульса наблюдаются при патологии аортальных клапанов и аорты.
Амплитуда пульса – это амплитуда колебаний стенки сосуда, зависящая от систолического объема сердца, а также от эластичности сосудов: чем они более эластичны, тем меньше амплитуда пульса.
Напряжение пульса определяется тем сопротивлением стенки артерии, которая противодействует нажиму давящего пальца. Различают твердый и мягкий пульс. При высоком АД пульс становится твердым, «проволочным».
По форме пульс может быть дикротическим или анакротическим в зависимости от степени выраженности дикротического зубца.
Микроциркуляция
Термином «микроциркуляция» обозначают ток крови и лимфы по мельчайшим кровеносным и лимфатическим сосудам, питающим любой орган, а также транспорт воды, газов и различных веществ (в том числе и лекарственных) между микрососудами и интерстициальным пространством.Микрососуды – это главное звено сосудистой системы. Они выполняют целый ряд функций: 1. Участвуют в перераспределении крови в организме в зависимости от его потребностей. 2. Создают условия для обмена веществ между кровью и тканями. 3. Играют компенсаторно-приспособительную роль при воздействии экстремальных факторов среды – переохлаждение, перегревание и др.
В состав внугриорганного микроциркуляторного русла входят следующие сосуды: артериолы, прекапилляры, или метаартериолы, прекапиллярные сфинктеры, капилляры, посткапиллярные венулы, венулы и артериовенозные анастомозы. К кровеносным сосудам, расположенным в интерстициальном пространстве, примыкают замкнутые лимфатические капилляры и мелкие лимфатические сосуды. Совокупность всех вышеперечисленных элементов микроциркуляторного русла называется микроциркуляторной единицей, или «модулем» (рис.16). Артериолы аметром 70 мкм, содержат кольцевой слой гладких мышц, сокращение которых создает значительное сопротивление кровотоку, поэтому их называют резистивными сосудами. Их функция – регуляция уровня АД в артериях. При уменьшении просвета артериолы АД в артериях увеличивается, при увеличении падает. И. М. Сеченов. Схема артериовенозного назвал артериолы «кранами сосудистой системы».
 Прекапилляры, или метаартериолы, имеют диаметр от 7 до 16 мкм. В них отсутствуют эластические элементы, но их мышечные клетки обладают автоматией, т. е. способностью спонтанно генерировать импульсы. Их особенность – большая чувствительность к химическим веществам, в том числе к сосудосуживающим и сосудорасширяющим.
Каждый прекапилляр заканчивается прекапиллярным сфинктером. Это последнее звено, в котором встречаются гладкомышечные клетки. От состояния сфинктера зависит число открытых и закрытых капилляров и появление так называемых «плазменных» капилляров, по которым протекает только плазма без форменных элементов, например, после кровопотери, при малокровии. Прекапиллярные сфинктеры также находятся преимущественно под контролем гуморальных факторов и химических веществ, растворенных в крови. Так, хорошо известный антагонист кальция – нифедипин (коринфар), а также бета-адреноблокатор – анаприлин (обзидан) расширяют прекапиллярные сфинктеры, улучшают капиллярную фильтрацию и снижают артериальное давление.
Капилляры – самое важное звено в системе микроциркуляции, это обменные сосуды, обеспечивающие переход газов, воды, питательных веществ из сосудистого русла в ткани и из тканей в сосуды. Всего у человека 40 млрд капилляров. Капилляры – это тончайшие сосуды диаметром 5 – 7 мкм и длиной от 0,5 до 1,1 мм. Они тесно примыкают к клеткам органов и тканей, образуя обширную обменную поверхность, равную 1000 – 1500 м2, хотя в них и содержится всего 200 – 250 мл крови. Капилляр не имеет сократительных элементов, у него 2 оболочки: внутренняя – эндотелиальная и наружняя – базальная, в которую впаяны клетки-перициты.
Прекапилляры, или метаартериолы, имеют диаметр от 7 до 16 мкм. В них отсутствуют эластические элементы, но их мышечные клетки обладают автоматией, т. е. способностью спонтанно генерировать импульсы. Их особенность – большая чувствительность к химическим веществам, в том числе к сосудосуживающим и сосудорасширяющим.
Каждый прекапилляр заканчивается прекапиллярным сфинктером. Это последнее звено, в котором встречаются гладкомышечные клетки. От состояния сфинктера зависит число открытых и закрытых капилляров и появление так называемых «плазменных» капилляров, по которым протекает только плазма без форменных элементов, например, после кровопотери, при малокровии. Прекапиллярные сфинктеры также находятся преимущественно под контролем гуморальных факторов и химических веществ, растворенных в крови. Так, хорошо известный антагонист кальция – нифедипин (коринфар), а также бета-адреноблокатор – анаприлин (обзидан) расширяют прекапиллярные сфинктеры, улучшают капиллярную фильтрацию и снижают артериальное давление.
Капилляры – самое важное звено в системе микроциркуляции, это обменные сосуды, обеспечивающие переход газов, воды, питательных веществ из сосудистого русла в ткани и из тканей в сосуды. Всего у человека 40 млрд капилляров. Капилляры – это тончайшие сосуды диаметром 5 – 7 мкм и длиной от 0,5 до 1,1 мм. Они тесно примыкают к клеткам органов и тканей, образуя обширную обменную поверхность, равную 1000 – 1500 м2, хотя в них и содержится всего 200 – 250 мл крови. Капилляр не имеет сократительных элементов, у него 2 оболочки: внутренняя – эндотелиальная и наружняя – базальная, в которую впаяны клетки-перициты.
Различают три типа капилляров: 1. Соматический – эндотелий капилляра не имеет фенестр и пор, а базальный слой непрерывный (капилляры скелетных и гладких мыщц, кожи, коры больших полушарий). Капилляры данного типа непроницаемы или почти непроницаемы для крупных молекул белка, но хорошо пропускают воду и растворенные в ней минеральные вещества. 2. Висцеральный – имеет фенестрированный эндотелий и сплошную базальную мембрану. Этот тип капилляров расположен в органах (почки, кишечник, эндокринные железы), секретирующих и всасывающих большие количества воды с растворенными в ней веществами. 3. Синусоидный – это капилляры с большим диаметром, между эндотелиоцитами имеются щели, базальная мембрана прерывиста или может полностью отсутствовать. Через их стенки хорошо проникают макромолекулы и форменные элементы крови. Такого типа капилляры находятся в печени, костном мозге, се-лезенке.
Количество функционирующих капилляров зависит от состояния органа. Так, в покое открыто только 25 – 35% всех капилляров. Кровь поступает в капилляр под давлением 30 мм рт.ст., а выходит под давлением 10 мм рт.ст. и течет по капилляру с очень маленькой скоростью, всего 0,5 мм/с, что создает благоприятные условия для протекания обменных процессов между кровью и тканями. Посткапиллярные венулы – это первое звено емкостной части микроциркуляторного русла. Наряду с эндотелиальными и гладкомышечными клетками в стенке вен появляются соединительно-тканные элементы, придающие ей большую растяжимость. Диаметр этих сосудов составляет от 12 мкм до 1 мм, давление – 10 мм рт.ст., скорость кровотока – 0,6–1 мм/с. Посткапиллярные венулы наряду с капиллярами относят к обменным сосудам, через стенку которых способны проходить высокомолекулярные вещества.
Артериовенозные анастомозы, или шунты – это сосуды, соединяющие артериолу с венулой, минуя или в обход капиллярной сети. Они находятся в коже, легких, почках, печени, имеют гладкомышечные элементы и, в отличие от других сосудов, большое количество рецепторов и нервных окончаний, обеспечивающих регуляцию кровотока. Основные функции анастомозов заключаются: 1. в перераспределении крови к работающему органу, 2. оксигенации венозной крови; 3. поддержании постоянной температуры в данном органе или участке тела – терморегуляторная функция; 4. увеличении притока крови к сердцу.
В системе микроциркуляции различают два вида кровотока: 1. Медленный, транскапиллярный, преобладает в состоянии покоя, обеспечивает обменные процессы. 2. Быстрый, юкстакапиллярный, через артериовенозные анастомозы, преобладает в состоянии функциональной активности, например, в мышцах при физической нагрузке. Так, 1 мл крови проходит через капилляры за 6 ч, а через артериовенозные анастомозы – всего за 2 с.
Транссосудистый обмен веществ
В механизме перехода веществ через сосудистую стенку в межтканевое пространство и из межтканевого пространства в сосуд играют роль следующие процессы: фильтрация, реабсорбция, диффузия и микропиноцитоз. Фильтрация и реабсорбция основаны, с одной стороны, на разности гидростатического давления в капилляре и в окружающих тканях, с другой – на разности онкотического давления плазмы крови, создаваемого белками, и онкотического давления в тканях. Кровь поступает в артериальную часть капилляра под давлением 30 мм рт.ст. – это гидростатическое давление. В межклеточной жидкости оно составляет около 3 мм рт.ст. Онкотическое давление плазмы крови равно 25 мм рт.ст., а межклеточной жидкости – 4 мм рт.ст. В артериальном конце капилляра способствует фильтрации гидростатическое давление (30 мм рт.ст. -3 мм рт.ст. = 27 мм рт.ст. – это фильтрационное давление). В то же время препятствует фильтрации онкотическое давление, однако оно остается таким же в венозной части капилляра и способствует реабсорбции, т. е. переходу веществ из межтканевого пространства в капилляр (25 мм рт.ст. – 4 мм рт.ст. = 21 мм рт.ст. – реабсорбционное давление). Сниженное гидростатическое давление (10 мм рт.ст.) не играет решающей роли и не мешает реаб-сорбции. Значит, в венозной части капилляра способствует реабсорбции онкотическое давление. Фильтрация увеличивается при общем повышении артериального давления, расширении резистивных сосудов во время мышечной деятельности, изменении положения тела (переходе из горизонтального в вертикальное), увеличении объема циркулирующей крови после вливания питательных растворов. Фильтрация возрастает также при снижении онкотического давления (при снижении количества белка в плазме – гипопротеинемии). Увеличивают реабсорбцию падение АД, кровопотеря, сужение резистивных сосудов, повышение онкотического давления. Некоторые вещества, такие, например, как кинины, гистамин, выделяющиеся при аллергических реакциях, воспалении и ожогах, могут повысить проницаемость капилляров, способствовать выходу жидкости в интерстициальное пространство и возникновению отеков. Однако в связи с малой растяжимостью интерстициального пространства и удалением лишней жидкости через лимфатические сосуды отеки встречаются не так часто, как могли бы быть в действительности. В среднем из капилляра в ткани фильтруется около 20 л жидкости в сутки, а реабсорбируется, т. е. возвращается из тканей в венозную часть кровеносной системы – около 18 л, остальные 2 л идут на образование лимфы. Диффузия основана на градиенте концентрации веществ по обе стороны капилляра. Преимущественно с помощью диффузии из сосуда в ткани попадают лекарственные препараты, кислород. Для кислорода имеется большой градиент парциального давления: в артериальной части капилляра – 100 мм рт.ст. и в тканях – 0 мм рт.ст., что создает условия для перехода кислорода в ткани. Через стенку капилляра свободно диффундируют жирорастворимые вещества, например, такие как спирт. Другие растворенные в воде вещества ограничены величиной пор в сосуде. Через маленькие поры хорошо проходят вода, NaCl, но хуже глюкоза и другие вещества; через большие поры, расположенные в основном в посткапиллярных венулах, могут проходить крупные молекулы белка и, в частности, иммунные белки. Следующий механизм переноса веществ – это микропиноцитоз. В отличие от фильтрации и диффузии, это активный транспорт с помощью везикул, расположенных в эндотелиальной клетке, способной «узнавать» циркулирующие в крови молекулы и адсорбировать их на своей поверхности. После чего везикулы захватывают молекулы веществ и транспортируют их на другую поверхность капилляра. С помощью микропиноцитоза переносятся, например, гамма-глобулины, миоглобин, гликоген.Движение крови в венах
Вены обладают большей растяжимостью, чем артерии, благодаря незначительной толщине мышечного слоя, поэтому они способны вмещать 80% всего количества крови, играя роль депо крови. Основная функция венозной системы – это возврат крови к сердцу и наполнение его полостей во время диастолы. Скорость течения крови в периферических венах составляет 6–14 см/с, в полых венах – 20 см/с.Движению крови в венах и возврату крови к сердцу способствует ряд факторов: 1. Главный фактор – это градиент давления в начале и конце венозной системы, равный 2 -4 мм рт. ст. 2. Остаточная сила сердца – vis a tergo – играет роль в движении крови по посткапиллярным венулам. 3. Присасывающее действие самого сердца во время диастолы – давление в полостях сердца в эту фазу равно 0 мм рт.ст. 4. Отрицательное давление в грудной полости. Во время вдоха особенно повышается градиент давления между брюшными и грудными венами, что приводит к увеличению венозного притока к последним. 5. Наличие в венах клапанов, препятствующих обратному току крови от сердца. 6. «Мышечный насос» – сокращение скелетных мышц и сдавливание вен, проходящих в их толще, при этом кровь выдавливается по направлению к сердцу. 7. Перистальтика кишечника, способствующая движению крови в венах брюшной полости.
Венозное давление
Кровь течет по венам под низким давлением. В посткапиллярных венулах оно равно 15 – 20 мм рт.ст., а в мелких венах – уже 12- 15 мм рт.ст., в венах, расположенных вне грудной полости, – 5 -9 мм рт.ст.; в полых венах – от 1 до 3 мм рт.ст. Часто давление в венах измеряется в миллиметрах водного столба (1 мм рт.ст. = 13,6 мм вод.ст.). Давление в венах, расположенных вблизи грудной клетки, например в яремной вене, в момент вдоха может быть отрицательным. Поэтому при ранениях шеи необходимо опасаться засасывания атмосферного воздуха в вены и развития воздушной эмболии. Различают также центральное венозное давление (ЦВД), или давление в правом предсердии, влияющее на величину венозного возврата крови к сердцу, а значит, и на систолический объем. ЦВД у здорового человека в покое составляет 40–120 мм вод.ст., увеличиваясь к вечеру на 10 – 30 мм вод.ст. Кашель, натуживание кратковременно могут увеличить ЦВД (выше 100 мм рт.ст.). Вдох сопровождается уменьшением ЦВД вплоть до отрицательных величин, а выдох – увеличением. Минимальное среднее давление в правом предсердии составляет 5–10 мм вод.ст., максимальное – 100 – 120 мм вод.ст. Существует определенная зависимость между ЦВД и количеством притекающей к сердцу крови. При снижении ЦВД от 0 до 4 мм рт.ст. венозный приток возрастает на 20 – 30%. Еще большее снижение ЦВД приводит к спадению вен, впадающих в грудную клетку, а приток крови к сердцу при этом не возрастает. И наоборот, повышение ЦВД хотя бы на 1 мм рт.ст. снижает приток крови на 14%. Можно искусственно увеличить возврат крови к сердцу с помощью внутривенных вливаний кровезаменителей, которые приведут к повышению ЦВД.Венный пульс
В периферических венах пульсовые колебания давления крови отсутствуют и отмечаются лишь в венах, расположенных около сердца, например яремной вене. Они передаются ретроградно и отражают изменения давления в правом предсердии. На кривой венного пульса – флебограмме (рис.17), зарегистрированной на яремной вене, различают три положительные волны: волна а – связана с сокращением правого предсердия, вторая положительная волна с, обусловлена выпячиванием атриовентрикулярного клапана в правое предсердие в начале систолы желудочков и толчком пульсирующей сонной артерии. Затем наблюдается быстрое падение кривой. Первая отрицательная волна х (коллапс) связана с разряжением в предсердиях в начале систолы желудочков и усиленным притоком крови из вены. После провала начинается третья положительная волна v – вентрикулярная, совпадающая с фазой изометрического расслабления, при этом атриовентрикулярный клапан еще не открыт, кровь переполняет предсердие и затрудняет отток крови из вен в предсердие. Далее следует вторая отрицательная волна у, отражающая фазу быстрого наполнения кровью желудочка и быстрого опорожнения вен. Изменения венного пульса наблюдаются, например, при недостаточности трехстворчатого клапана.
Первая отрицательная волна х (коллапс) связана с разряжением в предсердиях в начале систолы желудочков и усиленным притоком крови из вены. После провала начинается третья положительная волна v – вентрикулярная, совпадающая с фазой изометрического расслабления, при этом атриовентрикулярный клапан еще не открыт, кровь переполняет предсердие и затрудняет отток крови из вен в предсердие. Далее следует вторая отрицательная волна у, отражающая фазу быстрого наполнения кровью желудочка и быстрого опорожнения вен. Изменения венного пульса наблюдаются, например, при недостаточности трехстворчатого клапана.
Нейрогуморальная регуляция кровообращения
Регуляция деятельности сердца
Сердце – это мощный насос, перекачивающий по кровеносным сосудам около 10 т крови в сутки. Организм испытывает на себе за свою жизнь все невзгоды окружающей среды, и чтобы помочь ему адаптироваться к новым условиям, сердце также должно перестроить свою работу. Это достигается за счет деятельности ряда регуляторных механизмов.Условно их можно разделить на 2 группы: 1. внутрисердечные 2. внесердечные, или экстракардиальные.
Внутрисердечные механизмы регуляции
Эти механизмы делятся на 3 группы: 1. внутриклеточные 2. гемодинамические (гетеро- и гомеометрические) 3. внутрисердечные периферические рефлексы.Внутриклеточные механизмы регуляции имеют место, например, у спортсменов. Регулярная мышечная нагрузка приводит к усилению синтеза сократительных белков миокарда и появлению так называемой рабочей (физиологической) гипертрофии – утолщению стенок сердца и увеличению его размеров. Так, если масса нетренированного сердца составляет 300 г, то у спортсменов она увеличивается до 500 г. Гемодинамические, или миогенные, механизмы регуляции обеспечивают постоянство систолического объема крови. Сила сокращений сердца зависит от его кровенаполнения, т. е. от исходной длины мышечных волокон и степени их растяжения во время диастолы. Чем больше растянуты волокна, тем больше приток крови к сердцу, что приводит к увеличению силы сердечных сокращений во время систолы – это «закон сердца» (закон Франка- Стерлинга). Такой тип гемодинамической регуляции называется гетерометрическим. Она объясняется способностью Са2+ выходить из саркоплазматического ретикулума. Чем больше растянут саркомер, тем больше выделяется Са2+ и тем больше сила сокращений сердца. Этот механизм саморегуляции включается при перемене положения тела, при резком увеличении объема циркулирующей крови (при переливании), а также при фармакологической блокаде симпатической нервной системы бета-симпатолитиками. Другой тип миогенной саморегуляции работы сердца – гомеометрический не зависит от исходной длины кардиомиоцитов. Сила сердечных сокращений может возрастать при увеличении частоты сокращений сердца. Чем чаще оно сокращается, тем выше амплитуда его сокращений («лестница» Боудича). При повышении давления в аорте до определенных пределов возрастает противонагрузка на сердце, происходит увеличение силы сердечных сокращений (феномен Анрепа). Внутрисердечные периферические рефлексы относятся к третьей группе механизмов регуляции. В сердце независимо от нервных элементов экстракардиального происхождения функционирует внутриорганная нервная система, образующая миниатюрные рефлекторные дуги, в состав которых входят афферентные нейроны, дендриты которых начинаются на рецепторах растяжения на волокнах миокарда и коронарных сосудов, вставочные и эфферентные нейроны (клетки Догеля I, II и III порядка), аксоны которых могут заканчиваться на миокардиоцитах, расположенных в другом отделе сердца. Так, увеличение притока крови к правому предсердию и растяжение его стенок приводит к усилению сокращения левого желудочка. Этот рефлекс можно заблокировать с помощью, например, местных анестетиков (новокаина) и ганглиоблокаторов (беизогексония). Эфферентный нейрон внутрисердечной рефлекторной дуги может быть общим с эфферентным нейроном парасимпатического нерва (п. vagus), который иннервирует сердечную мышцу. Внесердечные (эстракардиальные) механизмы регуляции Эти механизмы также работают по рефлекторному принципу, в них главную роль играют парасимпатическая нервная система (п. vagus) и симпатическая нервная система (n. sympaticus). Рефлекторная дуга экстракардиального рефлекса начинается от механорецепторов предсердий – А-рецепторов, реагирующих на сокращение мускулатуры предсердий и их напряжение, и Врецепторов, возбуждающихся в конце систолы желудочков и реагирующих на пассивное растяжение мускулатуры предсердий (увеличение внутрисердечного давления). От этих рецепторов начинаются афферентные пути, которые представлены миелинизированными волокнами, идущими в составе блуждающего нерва. Другая группа афферентных нервных волокон отходит от свободных нервных окончаний густого субэндокардиального сплетения безмякотных волокон, находящихся под эндокардом. Они идут в составе симпатических нервов. Афферентные волокна, идущие в составе блуждающего нерва, достигают продолговатого мозга, где находится центр блуждающего нерва. Его называют ингибирующим сердечным центром, в нем расположены первые, или преганглионарные, нейроны, регулирующие работу сердца. Аксоны этих нейронов, составляющих блуждающий нерв, достигают сердца, в их окончаниях выделяется ацетилхолин, который через Н-холинорецепторы передает возбуждение на интрамуральный нейрон, или ганглий. В нем находится второй нейрон – постганглионарный, аксон которого иннервирует проводящую систему сердца и коронарные сосуды, контактируя с М – холинорецепторами. Волокна правого блуждающего нерва иннервируют синоатриальный узел, левого – атриовентрикулярный. Блуждающий нерв не иннервирует желудочки. Симпатические нервы равномерно иннервируют все отделы сердца, включая желудочки. Первые нейроны находятся в боковых рогах грудных сегментов спинного мозга (Т1–Т5). Их преганглионарные волокна прерываются в шейных и верхних грудных симпатических узлах и звездчатом ганглии, где находятся вторые нейроны, от которых отходят постганглионарные волокна, выделяющие в своих окончаниях адреналин и но радреналин. Контактируя с бета-адренорецепторами, они передают свои влияния на сердечную мышцу.
Характер влияний блуждающих и симпатических нервов на работу сердца
Различают четыре типа влияний блуждающего и симпатического нервов на работу сердца: 1. инотропное – на силу сердечных сокращений (инос-сила); 2. хронотропное – на частоту сердечных сокращений (хронос-время); 3. батмотропное – на возбудимость сердечной мышцы; 4. дромотропное – на проводимость импульсов по сердечной мышце.Впервые тормозное влияние блуждающих нервов на работу сердца было показано братьями Вебер в 1845 г. Раздражение периферического конца перерезанного блуждающего нерва приводит к уменьшению амплитуды сердечных сокращений, т. е. к отрицательному инотропному эффекту, урежению сердечных сокращений – отрицательному хронотропному, уменьшению возбудимости и проводимости – отрицательному батмотропному и дромотропному эффектам. Сильное раздражение блуждающего нерва вызывает остановку сердца в диастоле. Механизм отрицательного влияния блуждающего нерва на частоту сердечных сокращений можно представить в виде цепочки следующих друг за другом процессов: стимуляция блуждающего нерва выделение в его окончаниях ацетилхолина взаимодействие с М-холинорецепторами увеличение проницаемости мембраны клеток пейсмекера для ионов К+ и уменьшение для Са2+ замедление МДД увеличение мембранного потенциала отрицательный хронотропный эффект. При сильном раздражении блуждающего нерва может возникнуть гиперполяризация клеток синоатриального узла и полная остановка сердца. При продолжающемся раздражении блуждающего нерва прекратившиеся сокращения могут вновь восстановиться – это феномен ускользания сердца из-под влияния блуждающего нерва. Отрицательное влияние блуждающего нерва на сердце может быть снято с помощью атропина – блокатора М-холинорецепторов. Кроме того, ацетилхолин очень быстро разрушается ферментом ацетилхолинэстеразой (АХЭ), поэтому эффект нерва кратковременный. Существует такое понятие, как тонус вагуса – это постоянное тормозное влияние блуждающего нерва на сердце, особенно в состоянии покоя, т. е. в ночное время («ночь – царство вагуса»). Наличие тонуса блуждающего нерва доказывается полной денервацией сердца, после чего оно будет работать чаще, чем до денервации. Впервые влияние симпатического нерва на сердце было описано братьями Цион (1867 г.), Раздражение периферического конца перерезанного симпатического нерва оказывает на сердце положительный ино-, хроно-, батмо-, дромотропный эффект. При этом цепь процессов такова: стимуляция симпатического нерва выделение в его окончаниях норадреналина взаимодействие с бета-адренорецепторами на мембране клеток синоатриального узла повышение проницаемости для Na+ и Са2+ уменьшение МП ускорение МДД положительный хронотропный эффект. Положительное влияние симпатической нервной системы на сердце можно уменьшить или устранить с помощью бета-блокаторов, например обзидана. Свое влияние симпатические нервы, в отличие от блуждающего, оказывают не в покое, а при физическом или эмоциональном напряжении, в экстремальной ситуации. При чрезмерной активности симпатической нервной системы могут появиться эктопические очаги возбуждения в сердце, что приведет к возникновению экстрасистол. И. П. Павлов (1887 г.) обнаружил в составе симпатического нерва волокна, раздражение которых увеличивало силу сердечных сокращений, не изменяя при этом их частоту. Эти волокна были названы усиливающим, или трофическим, нервом, так как стимулировали обменные процессы и питание сердечной мышцы. В настоящее время стало известно, что при раздражении нервов, иннервирующих сердце, в синаптическую щель, помимо основных медиаторов, выделяются и другие биологически активные вещества, в частности пептиды. Они обладают модулирующим действием в отношении основного медиатора. Так, опиоидные пептиды (энкефалины и эндорфины) угнетают эффекты раздражения блуждающего нерва, а пептид дельта-сна усиливает вагусную брадикардию.
Гуморальная регуляция деятельности сердца
На работу сердца прежде всего влияют медиаторы ацетилхолин, выделяющийся в окончаниях парасимпатических нервов, он тормозит деятельность сердца, а также адреналин и норадреналин – медиаторы симпатических нервов, оказывающие на сердце положительный ино- и хронотропный эффекты. Ацетилхолин был открыт Отто Леви в 1921 г. в эксперименте на изолированных сердцах лягушки. Положительное, подобное адреналину, влияние на сердце было отмечено у дофамина. Кортикостероиды, ангиотензин, серото)1ин оказывают положительный инотропный эффект. Глюкагон, активируя аденилатциклазу, увеличивает силу и частоту сердечных сокращений. Тироксин и трийодтиронин оказывают положительный хронотропный эффект, кортикостероиды и ангиотензин – положительный инотропный. Аденозин расширяет коронарные сосуды, увеличивает коронарный кровоток в 6 раз, оказывая положительное инотропное и хронотропное влияние на сердце. Ионы Са2+ увеличивают силу сокращений и повышают возбудимость сердечной мышцы за счет активации фосфорилазы. Передозировка ионов Са2+ вызывает остановку сердца в систоле. Небольшое повышение концентрации ионов К+ в крови (до 4 ммоль/л) снижает МП и увеличивает проницаемость для этих ионов. Возбудимость миокарда и скорость проведения возбуждения при этом возрастают. Если увеличить концентрацию К+ в 2 раза, то возбудимость и проводимость сердца резко снижаются и может произойти его остановка в диастоле. Если ионов К+ недостает (гипокалиемия), что наблюдается при приеме диуретиков, которые выводят вместе с водой и К+, то возникает аритмия сердца и, в частности, экстрасистолия, поэтому одновременно с диуретиками необходимо принимать препараты, сберегающие К+ (например, панангин). Предсердия вырабатывают атриопептид, или натрийуретический гормон, в ответ на растяжение их стенок. Он расслабляет гладкомышечные клетки мелких сосудов, повышает диурез, выделяет натрий с мочой (натрийурез), уменьшает объем циркулирующей крови, подавляет секрецию ренина, тормозит эффекты ангиотензина II и альдостерона, снижает артериальное давление.Регуляция тонуса сосудов
Механизмы, регулирующие сосудистый тонус, можно условно разделить: 1. на местные, периферические, регулирующие кровоток в отдельном органе или участке ткани независимо от центральной регуляции 2. центральные, поддерживающие уровень АД и системное кровообращение.Местные регуляторные механизмы
Они реализуются уже на уровне эндотелия сосудов, который обладает способностью вырабатывать и выделять биологически активные вещества, способные расслаблять или сокращать гладкие мышцы сосудов в ответ на повышение АД, а также механические или фармакологические воздействия. Эндотелий сосуда рассматривается как эндокринная железа, способная выделять свой секрет, который затем действует на гладкую мышцу сосуда и изменяет ее тонус. К веществам, синтезируемым эндотелием, относится расслабляющий фактор (ВЭФР) – нестабильное соединение, одним из которых может быть оксид азота (NO), другое вещество – эндотелии, вазоконстрикторный пептид, полученный из эндотелиоцитов аорты свиньи. Он состоит из 21 аминокислотного остатка, выделяется в ответ на различные физиологические и фармакологические воздействия. Если полностью денервировать сосуд, он хотя и расширится, но будет сохранять некоторое напряжение своей стенки за счет базального, или миогенного, тонуса гладких мышц. Этот тонус создается благодаря автоматии гладкомышечных клеток сосудов, которые имеют нестабильно поляризованную мембрану, облегчающую возникновение спонтанных ПД в этих клетках. Увеличение АД растягивает клеточную мембрану, что увеличивает спонтанную активность гладких мышц и приводит к повышению их тонуса. Базальный тонус особенно выражен в сосудах микроциркуляторного русла, преимущественно в прекапиллярах, обладающих автоматией. Он поддерживается также за счет химической информации как от эндотелия сосудистой стенки при ее растяжении, так и от различных веществ, растворенных в крови, т. е. находится преимущественно под влиянием гуморальной регуляции.Центральные механизмы регуляции
Эти механизмы обеспечиваются волокнами, иннервирующими сосудистую стенку, а также влияниями центральной нервной системы. Вазоконстрикторный эффект симпатических нервов был впервые показан А. Вальтером (1842 г.) на плавательной перепонке лягушки, сосуды которой расширились при перерезке седалищного нерва, содержащего в себе симпатические волокна, и Клодом Бернаром (1851 г.), перерезавшим на шее у кролика с одной стороны симпатический нерв. В результате сосуды уха на стороне перерезки нерва расширились, а ухо стало красным и горячим. Раздражение периферического конца перерезанного симпатического нерва привело к резкому сужению сосудов, а ухо стало бледным и холодным. Для сосудов брюшной полости главный вазоконстриктор – это чревный нерв, в составе которого проходят симпатические волокна. Значит, симпатический нерв – основной вазоконстриктор, поддерживающий тонус сосудов на том или ином уровне в зависимости от количества импульсов, поступающих по его волокнам к сосуду. Свое влияние на сосуды симпатический нерв оказывает через норадреналин, выделяющийся в его окончаниях, и альфа-адренорецепторы, расположенные в сосудистых стенках, в результате происходит сужение сосуда. Если вазоконстрикторный эффект симпатической нервной системы носит общий системный характер, то вазодилататорный является чаще местной реакцией. Нельзя утверждать, что парасимпатическая нервная система расширяет все сосуды. Известны лишь несколько парасимпатических нервов, расширяющих сосуды только тех органов, которые они иннервируют. Так, раздражение барабанной струны – веточки парасимпатического лицевого нерва – расширяет сосуды подчелюстной железы и увеличивает в пей кровоток. Вазодилататорный эффект был получен при раздражении других парасимпатических нервов: языкоглоточного, расширяющего сосуды миндалин, околоушной железы, задней трети языка; верхнегортанного нерва – веточки блуждающего нерва, расширяющего сосуды слизистой гортани и щитовидной железы; тазового нерва, расширяющего сосуды органов малого таза. В окончаниях вышеперечисленных нервов выделялся медиатор ацетилхолин (холинергические волокна), который контактировал с М-холинорецепторами и вызывал расширение сосудов. Среди симпатических волокон есть холинергические, в окончаниях которых выделяется не норадреналин, а ацетилхолин, их раздражение вызывает не сужение, а расширение сосудов таких органов, как сердца и скелетных мышц, и эффект от раздражения блокируется атропином. Стимуляция задних корешков спинного мозга в эксперименте приводит к расширению сосудов данного сегмента тела. Раздражая кожу, например, горчичниками, можно получить местное расширение сосудов и покраснение данного участка кожи по типу аксон-рефлекса, реализуемого в пределах двух разветвлений одного аксона и без участия центральной нервной системы.Гуморальная регуляция сосудистого тонуса
Гуморальная регуляция просвета сосудов осуществляется за счет химических, растворенных в крови веществ, к которым относятся гормоны общего действия, местные гормоны, медиаторы и продукты метаболизма. Их можно разделить на две группы: сосудосуживающие и сосудорасширяющие вещества. К сосудосуживающим веществам относятся: гормоны мозгового слоя надпочечников – адреналин и норадреналин. Адреналин в малых дозах (1 х 10–7 г/мл) повышает АД, суживая сосуды всех органов, кроме сосудов сердца, мозга, поперечно-полосатой мускулатуры, в которых находятся бета-адренорецепторы. Норадреналин – сильный вазоконстриктор, взаимодействующий с альфа-адренорецепторами. Разнонаправленный характер влияния катехоламинов (адреналина и норадреналина) на гладкие мышцы сосудов объясняется наличием разных типов адренорецепторов – альфа и бета. Возбуждение альфа-адренорецепторов приводит к сокращению мускулатуры сосудов, а возбуждение бета-адренорецепторов – к ее расслаблению. Норадреалин контактирует в основном с альфаадренорецепторами, а адреналин – и с альфа и с бета. Если в сосудах преобладают альфа-адренорецепторы, то адреналин их суживает, а если преобладают бета-адренорецепторы, то он их расширяет. Кроме того, порог возбуждения бета-адренорецепторов ниже, чем альфа-рецепторов, поэтому в низких концентрациях адреналин в первую очередь контактирует с бета-адренорецепторами и вызывает расширение сосудов, а в высоких – их сужение. Вазопрессин, или антидиуретический гормон – гормон задней доли гипофиза, суживающий мелкие сосуды и, в частности, артериолы, особенно при значительном падении артериального давления. Альдостерон – минералокортикоид – гормон коры надпочечников, повышает чувствительность гладких мышц сосудов к вазоконстрикторным агентам, усиливает прессорное действие ангиотензина II. Серотонин – образуется в слизистой кишечника и в некоторых отделах головного мозга, содержится в тромбоцитах, суживает поврежденный сосуд и препятствует кровотечению. Он оказывает мощное сосудосуживающее влияние на артерии мягкой мозговой оболочки и может играть роль в возникновении их спазмов (приступы мигрени). Ренин – образуется в юкстагломерулярном комплексе почки, особенно много при ее ишемии.Он расщепляет альфа-2 – глобулин плазмы – ангиотензиноген и превращает его в малоактивный декапептид – ангиотензин I, который под влиянием фермента дипептидкарбоксипептидазы превращается в очень активное сосудосуживающее вещество – ангиотензин II, повышающее АД (почечная гипертония). Ангиотензин II – мощный стимулятор выработки альдостерона, повышающего содержание в организме Na+ и внеклеточной жидкости. В таких случаях говорят о работе ренин-ангиотензин-альдостероновой системы или механизма. Последний имеет большое значение для нормализации уровня кровяного давления при кровопотере. Эндотелии – вырабатывается эндотелием сосудов, оказывает сосудосуживающий эффект при снижении АД. Ионы Са2+ суживают сосуды. К сосудорасширяющим веществам относятся: медиатор ацетилхолин, а также так называемые местные гормоны. Один из них – гистамин – образуется в слизистой оболочке желудка и кишечника, в коже, скелетной мускулатуре (во время работы) и в других органах. Содержится в базофилах и тучных клетках поврежденных тканей и выделяется при реакциях антиген-антитело. Расширяет артериолы и венулы, увеличивает проницаемость капилляров. Брадикинин выделен из экстрактов поджелудочной железы, легких. Он расширяет сосуды скелетных мышц, сердца, спинного и головного мозга, слюнных и потовых желез, увеличивает проницаемость капилляров. Простагландины, простациклины и тромбоксан образуются во многих органах и тканях. Они синтезируются из полиненасыщенных жирных кислот арахидоновой и линолевой. Простагландины (PG) – это гормоноподобные вещества. Разные группы и подгруппы этих веществ оказывают различный эффект на сосуды. Так, PGA, и PGA2 вызывают расширение артерий чревной области. Медуллин (PGA2), выделенный из мозгового вещества почек, снижает АД, увеличивает почечный кровоток, выделение почками воды, Na+ и К +. Простагландины PGE расширяют сосуды при внутриартериальном введении и тормозят выделение норадреналина из окончаний симпатических нервов. PGF суживают сосуды и повышают АД. Тромбоксан оказывает сосудосуживающий эффект. Продукты метаболизма – молочная и пировиноградная кислоты оказывают местный вазодилататорный эффект. СО2 расширяет сосуды мозга, кишечника, скелетной мускулатуры. Аденозин расширяет коронарные сосуды. NO (оксид азота) расширяет коронарные сосуды. Ионы К+ и Na+ расширяют сосуды.Центры кровообращения
Образования, имеющие отношение к центрам кровообращения, располагаются на разных уровнях центральной нервной системы.Спинальный уровень
Спинальный уровень регуляции сердечной деятельности находится в боковых рогах (Т1-Т5) спинного мозга – это симпатические преганглионарные нейроны. В звездчатом симпатическом ганглии локализованы постганглионарные симпатические нейроны, аксоны которых иннервируют сердечную мышцу. Раздражение вышеперечисленных структур стимулирует сердечную деятельность. Сосудистый тонус регулируется центрами, расположенными в боковых рогах спинного мозга, – это симпатические пре-ганглионарные нейроны, пара- и превертебральные ганглии – постганглионарные нейроны. Если перерезать у животного спинной мозг между последним шейным и первым грудным сегментами, то в первый момент про-изойдет резкое падение АД, но через неделю кровяное давление восстанавливается за счет деятельности симпатических центров боковых рогов спинного мозга, приобретающих при гипоксии, вызванной кровопогерей, самостоятельное значение.Бульварный уровень.
В продолговатом мозге находится главный центр регуляции сердечной деятельности (ингибирующий центр), состоящий из группы нейронов, относящихся к ядру блуждающего нерва и оказывающих на сердце тормозное влияние, а также группы нейронов, связанных со спинальными (стимулирующими) центрами. Кроме того, в продолговатом мозге располагается главный сосудодвигательный центр. Прессорные нейроны локализованы преимущественно в латеральных областях продолговатого мозга, депрессорные – в медиальных.Гипоталамический уровень.
Раздражение передней группы ядер вызывает торможение сердечной деятельности и вазодилататорный эффект, раздражение задней группы – стимуляцию работы сердца и вазокопстрикторный эффект. Корковый уровень обеспечивает регуляцию сердечной деятельности и сосудистых реакций (условных и безусловных) в ответ на внешние раздражения. Стимуляция некоторых отделов коры больших полушарий вызывает различные реакции со стороны сердечно-сосудистой системы. При раздражении моторной и премоторной зон коры возникают преимущественно прессорные реакции и ускорение ритма сердечных сокращений. Стимуляция поясной извилины приводит к депрессорному эффекту, а раздражение некоторых точек около орбитальных областей островка височной коры вызывает как прессорные, так и депрессорные реакции.Рефлекторная регуляция деятельности сердца и сосудистого тонуса
Рефлекторные влияния на деятельность сердца и тонус сосудов могут возникать при раздражении различных рецепторов, расположенных как в самом сердце и сосудистой системе, так и в различных органах.Условно все сердечно-сосудистые рефлексы можно разделить на собственные и сопряженные. 1. Собственные рефлексы берут свое начало в самом сердце или в кровеносных сосудах и заканчиваются на сердце и сосудах. 2. Сопряженные рефлексы начинаются в других органах и заканчиваются на сердце и сосудах.
Собственные рефлексы можно разделить: 1. на рефлексы с сердца на сердце 2. рефлексы с сосудов на сердце и сосуды.
Так, при повышении давления в правом предсердии и устье полых вен происходит возбуждение барорецепторов этих зон, затем стимуляция симпатических центров спинного мозга и рефлекторная тахикардия, при этом сердце выбрасывает больше крови, в результате давление в правом предсердии снижается (рефлекс Бейнбриджа). В группе рефлексов с сосудов на сердце и сосуды выделяют два главных рефлекса: аортальный и синокаротидный. Повышение артериального давления приводит к возбуждению барорецепторов дуги аорты. Далее возбуждение по депрессорному, или аортальному, нерву, открытому И. Ф. Ционом и К. Людвигом (1866 г.), достигает продолговатого мозга, где находятся центры сердечной деятельности (центр блуждающего нерва) и сосудодвигательный центр. Импульсы по центробежным эфферентным волокнам блуждающего нерва поступают к сердцу и тормозят его работу. Одновременно происходит расширение сосудов, получивших импульсацию по вазодилататорам из сосудодвигательного центра продолговатого мозга. Брадикардия и расширение сосудов приводят к падению давления. При снижении артериального давления в аортальной зоне частота импульсов, идущих в продолговатый мозг по депрессорному нерву, уменьшается. Это тормозит центр блуждающего нерва, увеличивает тонус симпатических нервов и рефлекторно повышает артериальное давление. Вторая сосудистая рефлексогенная зона была описана Г. Герингом (1923 г.). Раздражение барорецепторов каротидного синуса в области бифуркации сонной артерии на наружную и внутреннюю при повышении артериального давления приводит к возбуждению синокаротидного нерва, идущего в составе языкоглоточного нерва. Далее импульсы достигают центра блуждающего нерва и сосудодвигательного центра в продолговатом мозге, затем происходят те же изменения деятельности сердца и просвета сосудов, что и при аортальном рефлексе. К сопряженным рефлексам (с органов на сердце) относится рефлекс Гольца – это рефлекторная брадикардия вплоть до полной остановки сердца в результате стимуляции механорецепторов брюшины и органов брюшной полости при ударе в эпигастральную область. Центростремительные пути этого рефлекса проходят в составе чревного нерва в спинной и продолговатый мозг, где они достигают ядер блуждающего нерва и по его эфферентным волокнам – сердца. Урежение частоты сердечных сокращений на 10–20 в 1 минуту можно получить при надавливании на глазные яблоки – это также вагальный рефлекс Даньини-Ашнера. Рефлекторные изменения работы сердца и повышение артериального давления наблюдаются при болевых раздражениях кожи (экстерорецепторов), внутренних органов (интерорецепторов), при эмоциях, мышечной работе.
Методы исследования сердечно-сосудистой системы
Фонокардиография – метод регистрации тонов (1,2,3,4), а в патологии – шумов сердца посредством преобразования с помощью микрофона звуковых колебаний в электрические. Баллистокардиография – метод регистрации движений тела человека, обусловленных сокращением сердца и выбросом крови в крупные сосуды. Динамокардиография – метод регистрации смещений центра тяжести грудной клетки, отражающих движения сердца в грудной клетке и перемещение массы крови из полостей сердца в сосуды. Векторкардиография – регистрация изменений направления электрической оси сердца, обладающей свойствами векторной величины с помощью электронно-лучевой трубки. Эхокардиография – регистрация ультразвуковых колебаний, отраженных от различных поверхностей сердца. Позволяет судить о расстоянии между различными структурами, находящимися в радиусе ультразвукового луча, об изменениях размеров сердца, движении клапанов. Реография – запись изменений сопротивления тканей проходящему через них электрическому току. Вследствие увеличения кровенаполнения тканей (при систоле) происходит повышение их электропроводности и уменьшение электрического сопротивления. Уменьшение кровенаполнения (при диастоле) приводит к обратным явлениям. По форме реограмма напоминает кривую объемного пульса. Реография используется для определения изменений регионарного сосудистого тонуса, скорости кровотока и скорости распространения пульсовой волны. Плетизмография – регистрация изменений объема органа, связанных с колебаниями его кровенаполнения. Во время систолы приток крови к органу увеличивается, происходит и увеличение его объема. Во время диастолы наблюдаются обратные явления. Плетизмография используется для оценки тонуса периферических сосудов, изменений систолического объема крови, определения скорости распространения пульсовой волны. С помощью метода окклюзионной плетизмографии можно измерить объемную скорость кровотока.Коронарное кровообращение
Коронарный кровоток составляет 250 мл/мин, или 4–5% от МОК. При максимальной физической нагрузке он может возрастать в 4–5 раз. Обе коронарные артерии отходят от аорты. Правая коронарная артерия снабжает кровью большую часть правого желудочка, заднюю стенку левого желудочка и некоторые отделы межжелудочковой перегородки. Левая коронарная артерия питает остальные отделы сердца. Отток венозной крови от левого желудочка осуществляется преимущественно в венозный синус, открывающийся в правое предсердие (75% всей крови). От правого желудочка кровь оттекает по передним сердечным венам и венам Тебезия непосредственно в правое предсердие. При ослаблении сердечной деятельности или сократительной способности миокарда возможен обратный кровоток из полостей сердца в коронарные сосуды с помощью сосудов Вьессана и вен Тебезия. Внутренний слой стенки коронарных сосудов продуцирует эластин, способствующий образованию атеросклеротических бляшек. Средний слой вырабатывает кейлоны, тормозящие продукцию эластина. Нарушение выработки кейлонов приводит к образованию атеросклеротических бляшек. Коронарный кровоток зависит от фаз сердечного цикла. Во время систолы интенсивность коронарного кровотока (особенно в миокарде левого желудочка) снижается, а во время диастолы возрастает. Это связано с периодическим сжатием мускулатурой сердца коронарных сосудов во время систолы и расслаблением во время диастолы. Для миокарда характерны высокая объемная скорость кровотока и большая растяжимость коронарных сосудов. Коронарный кровоток зависит от давления в аорте. При повышении давления в аорте коронарный кровоток увеличивается, при снижении – уменьшается. Повышение артериального давления в правой половине сердца препятствует венозному оттоку крови из коронарных сосудов и уменьшению кровотока по ним – «легочное сердце» (при воспалении легких, туберкулезе легких).Регуляция коронарного кровотока
Гипоксия – один из важнейших факторов, регулирующих коронарный кровоток. Сердечная мышца экстрагирует из притекающей крови О2 (60–70%). Потребление кислорода миокардом составляет 4–10 мл на 100 г его массы в 1 минуту, при повышении нагрузки на сердце оно возрастает, но не за счет увеличения экстракции О2 , а за счет увеличения коронарного кровотока. Снижение О2 на 5% приводит к расширению коронарных сосудов. При аноксии (прекращении доставки О2 к сердцу) его сокращения постепенно ослабевают, полости сердца расширяются и через 6–10 минут наступает остановка сердца, которая вначале сопровождается биохимическими изменениями: падением содержания АТФ и креатинфосфата, накоплением лактата, который не расщепляется до СО2 и воды. После 30-минутной аноксии наступают структурные необратимые нарушения в мышце сердца: 30 минут – это предел реанимации. При удушье предел реанимации короче (8–10 мин), так как возникают необратимые изменения головного мозга. Увеличение МОК приводит к улучшению коронарного кровотока. Несильное раздражение симпатических нервов улучшает метаболизм сердечной мышцы и коронарный кровоток, сильное раздражение вызывает констрикторный эффект на сосудах сердца и боли в сердце. Стимуляция парасимпатических нервов (блуждающего нерва) приводит к слабому расширению коронарных сосудов и одновременно к отрицательному инотропному эффекту, ухудшению коронарного кровотока и к смерти, особенно ночью, когда превалирует тонус блуждающего нерва. Положительный хронотропный эффект (тахикардия) уменьшает коронарный кровоток, положительный инотропный эффект улучшает коронарный кровоток. Адреналин и норадреналин увеличивают коронарный кровоток, ацетилхолин – уменьшает, брадикинин, простагландины – расширяют коронарные сосуды и улучшают в них кровоток. Аналогичное положительное влияние оказывает аденозин, молочная кислота, СО2, Н+ ионы, Са2+, NO (окись азота). Передозировка ионов К+ ухудшает коронарный кровоток и приводит к остановке сердца.Лимфатическая система
Лимфатические сосуды – это дренажная система, по которой тканевая жидкость оттекает в кровеносное русло. Лимфатическая система человека начинается с замкнутых, в отличие от кровеносных, лимфатических капилляров, пронизывающих все ткани, за исключением эпидермиса кожи, центральной нервной системы, паренхимы селезенки, хрящей, плаценты, хрусталика и оболочек глазного яблока. Диаметр лимфатического капилляра – 20–40 мкм, его стенка состоит из одного слоя эндотелия и связана с помощью коллагеновых волокон с окружающей соединительной тканью, что препятствует спадению стенок лимфатического капилляра при изменении внутритканевого давления. Через стенку лимфатического капилляра хорошо проходят электролиты, углеводы, жиры и белки. Далее капилляры переходят во внутриорганные мелкие лимфатические сосуды. Выйдя из органа, последние пронизывают один или два лимфатических узла – «фильтры», задерживающие наиболее крупные частицы, находящиеся в лимфе. Затем лимфатические сосуды соединяются в более крупные стволы, образующие правый и грудной лимфатический протоки. Грудной проток собирает 3/4 лимфы всего тела, за исключением правой половины головы и шеи, правой руки и правой половины грудной клетки, которые питаются правым лимфатическим протоком. Оба протока впадают в подключичные вены. В лимфатических сосудах имеются клапаны. Участок лимфососуда между двумя клапанами называется лимфангионом. Это морфофункциональпая единица лимфатической системы, состоящая из мышечной «манжетки» и двух клапанов – дистального и проксимального. Лимфатические сосуды – это система коллекторов, представляющих собой цепочку лимфангионов. Лимфатические сосуды могут спонтанно сокращаться с частотой от 10 до 20 в 1 мин. Эти сокращения представляют собой последовательные, ритмические сокращения лимфангионов, напоминающие сердечный цикл, в котором имеется систола и диастола. В результате происходит перемещение лимфы по сосудам. Движению лимфы способствуют дыхательные движения, сокращения мышц, сердца, перистальтика кишечника. Лимфатические сосуды находятся в состоянии тонуса, который поддерживается местными гуморальными и нервными механизмами.Функции лимфатической системы
Лимфатическая система выполняет следующие функции: 1. Возврат белков, электролитов и воды из интерстиция в кровь. За одни сутки в кровоток лимфа возвращает 100 г белка. При массивной кровопотере увеличивается поступление лимфы в кровь. При перевязке или закупорке лимфатического сосуда развивается лимфатический отек ткани (скопление жидкости в тканях). 2. Резорбтивная функция. Через поры в лимфатических капиллярах в лимфу проникают коллоидные вещества, крупномолекулярные соединения, лекарственные препараты, частицы погибших клеток. В последние годы при лечении тяжелых воспалительных процессов и раковых заболеваний используют эндолимфотерапию, т. е. введение лекарственных препаратов непосредственно в лимфатическую систему. 3. Барьерная функция осуществляется за счет лимфоузлов, задерживающих инородные частицы, микроорганизмы и опухолевые клетки (метастазирование в лимфоузлы). 4. Участие в энергетическом и пластическом обмене веществ. Лимфа приносит в кровь продукты метаболизма, витамины, электролиты и другие вещества. 5. Участие в жировом обмене. Жиры из кишечника после их всасывания поступают в лимфатические сосуды, затем в кровеносную систему и в жировые депо в виде хиломикронов. 6. Иммунобиологическая функция. В лимфоузлах образуются плазматические клетки, вырабатывающие антитела. Там же находятся Т- и В-лимфоциты, отвечающие за иммунитет. 7. Участие в обмене жирорастворимых витаминов (А, Е, К), которые сначала всасываются в лимфу, а затем в кровь.Лимфообразование
Лимфа образуется в результате перехода (резорбции) интерстициальной жидкости с растворенными в ней веществами в лимфатические капилляры, которые вновь переходят в кровеносную систему. Транспорт жидкости с растворенными в ней веществами можно представить в виде следующей схемы: кровеносное русло-›интерстиций-›лимфатические сосуды-жровеносное русло. Из 20 л жидкости, выходящей из кровеносного русла в интерстициальное пространство, 2–4 л в виде лимфы по лимфатическим сосудам возвращается в кровеносную систему.К факторам, способствующим лимфообразованию, относятся: 1. Разность гидростатического давления в кровеносном сосуде, межтканевом пространстве и лимфатическом капилляре. Так, повышение артериального давления в капилляре способствует фильтрации жидкости из капилляра в ткань и лимфатический сосуд. Давление лимфы в области грудного протока составляет 11 – 12 мм вод.ст. При форсированном дыхании оно возрастает до 35 – 40 см вод.ст. 2. Разность онкотического и осмотического давления в кровеносном сосуде и межтканевом пространстве. Повышение онкотического давления плазмы снижает образование лимфы. 3. Состояние проницаемости эндотелия кровеносных и лимфатических капилляров. Очень проницаемы капилляры печени, поэтому большая часть лимфы образуется в печени, после чего она поступает в грудной проток. Макромолекулы и частицы диаметром 3 – 50 мкм проникают через эндотелий с помощью пиноцитоза (белки, хиломикроны).
Нервная регуляция лимфообразования
Лимфатические сосуды имеют как адренергическую, так и холинергическую иннервацию, представленную в местах расположения клапанов и при переходе сосуда малого калибра в более крупный. Роль нервных влияний состоит в модуляции спонтанных ритмических сокращений лимфангиона. Возбуждение симпатической нервной системы приводит к сокращению лимфангиона, а парасимпатических – в основном к расслаблению.Гуморальная регуляция лимфотока и лимфообразования
Адреналин – усиливает ток лимфы по лимфатическим сосудам брыжейки и повышает давление в грудной полости. Гистамин – усиливает лимфообразование за счет увеличения проницаемости кровеносных капилляров, стимулирует сокращение гладких мышц лимфангионов. Гепарин – действует на лимфатические сосуды так же, как и гистамин. Серотонин – сокращает просвет грудного протока. АТФ – тормозит спонтанные сокращения грудного протока и брыжеечных лимфососудов. Недостаток или отсутствие ионов Са2+ в крови тормозит сокращения лимфатических сосудов. Гипоксия и наркоз подавляют активность сосудов.Состав лимфы
В организме содержится 1,5 – 2 л лимфы. Ее удельный вес 1010–1023, рН 8,4–9,2. Осмотическое давление немного выше, чем плазмы, онкотическое ниже, так как в лимфе меньше белка. Общий белок составляет 25–56,1 г/л, альбумины – 15,0–40,0 г/л, глобулины 10,0–16,0 г/л, фибриноген – 1,5–4,6 г/л. Содержание белка значительно варьирует в зависимости от проницаемости кровеносных капилляров: 60 г/л – в печени, 30 – 40 г/л – в желудочно-кишечном тракте. Липиды в виде хиломикронов составляют у голодного животного 626 мг%, а после приема пищи лимфа приобретает белый цвет и похожа на молоко («млечный сок»). В лимфе много хлора – 92,0–140,7 ммоль/л и бикарбонатов – 114,3–137,5 ммоль/л. Она содержит ферменты диастазу и липазу. В лимфе имеются в основном лимфоциты, количество которых варьирует в течение суток от 1 до 22 х 109/л, мало моноцитов и гранулоцитов. Эритроциты отсутствуют, при повышении капиллярной проницаемости эритроциты могут появиться в лимфе, тогда она приобретает кровянистый вид. Лейкоцитарная формула лимфы (по Б. Н. Ткаченко): лимфоциты – 90%, моноциты – 5%, сегментоядерные нейтрофилы – 1%, эозинофилы – 2%, другие клетки – 2%, тромбоциты – 5–35х109 л. В связи с тем, что лимфа содержит фибриноген, она может свернуться. Время свертывания лимфы составляет 10- 15 минут.Фармакологическая коррекция нарушений некоторых физиологических показателей системы кровообращения
Средства, влияющие на возбудимость, проводимость сердечной мышцы и ритм сердечных сокращений
Сердечный ритм зависит от автоматии, возбудимости и проводимости сердечной мышцы. Аритмии – нарушения ритма деятельности сердца. Они могут возникать вследствие повышения или угнетения автоматии в синоатриальном узле, а также в результате повышения автоматии или в эктопическом, или в латентном водителе ритма. Увеличение автоматии синоатриального узла называется синусовой тахикардией, уменьшение – синусовой брадикардией. Одной из причин возникновения аритмий может быть так называемый «механизм повторного входа возбуждения» (reentrумеханизм), который имеет место при пароксизмальной тахикардии, мерцании и трепетании предсердий и желудочков, экстрасистолии. Нарушение проводимости – наиболее частая причина возникновения аритмий, включает в себя замедление или блокаду проведения импульсов, о которых говорилось выше. Для лечения аритмий используют антиаритмические препараты, которые по механизму действия делят на пять групп. К первой группе относят препараты с мембраностабилизирующим действием (уменьшают проницаемость клеточной мембраны и нарушают транспорт К+, Na+ и Са2+, блокируют ацетилхолин). Эти вещества угнетают автоматию клеток синоатриального узла и эктопических водителей ритма, снижают возбудимость волокон Пуркинье и миофибрилл, уменьшают скорость проведения импульсов через атриовентрикулярный узел и волокна Пуркинье, увеличивают продолжительность ПД и абсолютной рефрактерной фазы. К этой группе препаратов относят хинидин, новокаинамид, ритмодан и др. Их принимают при мерцательной аритмии, трепетании предсердий, пароксизмальной тахикардии, частой предсердной и желудочковой экстрасистолии, желудочковой тахикардии. Препараты К+ – панангин, аспаркам, хлорид калия приводят к снижению мембранного потенциала миоцитов и уменьшению скорости проведения импульсов в миофибриллах. Их назначают при аритмиях, связанных с гипокалиемией, и при аритмиях, вызванных передозировкой дигиталиса. Ко второй группе антиаритмических препаратов относят лидокаин, мекситил, пропафенон и др. В отличие от хинидина, эти препараты уменьшают рефрактерный период, повышают скорость проведения импульсов, не влияя на сократимость миокарда. Кроме того, они обладают местноанестезирующим действием и показаны при остром инфаркте миокарда. Их используют для лечения желудочковой экстрасистолии и профилактики фибрилляции желудочков сердца. Антиаритмические препараты третьей группы – это блокаторы бета-адренергических рецепторов. Они уменьшают автоматик) предсердий и желудочков, снижают атриовентрикулярную и внутрижелудочковую проводимость, укорачивают время реполяризации. Их назначают при желудочковой экстрасистолии, трепетании и мерцании предсердий. К препаратам этой группы относят обзидан, оксипренолол, аптин, вискен. Антиаритмические препараты четвертой группы обладают антиаритмическими свойствами, не влияя на мембраны за счет блокады постганглионарной симпатической передачи импульсов. Они укорачивают ПД и абсолютный рефрактерный период. Представителем этой группы является препарат кордарон. Его назначают при пароксизмальных аритмиях, синусной тахикардии, трепетании предсердий, желудочковой тахикардии и экстрасистолии. К пятой группе антиаритмических препаратов относят антагонисты кальция, например верапамил (изоптин, финоптин). Он тормозит трансмембранный ток Са2+ внутри сердечной клетки, уменьшает спонтанную активность синоатриального узла.Средства, влияющие на сократимость сердечной мышцы
МОК зависит от силы сердечных сокращений и, в частности, от величины систолы. При сердечно-сосудистой недостаточности, возникающей, например, при декомпенсированных пороках сердца, сила сердечных сокращений и систолический выброс крови уменьшаются, диурез падает, наступают явления застоя и отеки, нарушается доставка кислорода к тканям, возникает цианоз и одышка. К препаратам, влияющим на сократимость сердечной мышцы при явлениях сердечно-сосудистой недостаточности, относятся сердечные гликозиды, содержащиеся в ряде растений: разные виды наперстянки (Digitalis), горицвета (Adonis vemalis), ландыша (Convallaria majalis), строфанта (Strophanthus gratus) и др. В клинике используются следующие препараты, содержащие в своем составе сердечные гликозиды: дигитоксин, дигоксин, адонизид, коргликон, строфантин К.Под влиянием терапевтических доз сердечных гликозидов наблюдается: 1. усиление и укорочение систолы, 2. удлинение диастолы, длительный отдых необходим для восстановления сократительной способности миокарда. В результате ритм сердца замедляется, улучшается приток крови к желудочкам, увеличивается систолический объем крови. Замедление ритма сердца связывают с возбуждением центра блуждающего нерва, получившего информацию от сосудистых рефлексогенных зон аорты и легочной артерии, которые раздражались при усилении под действием гликозидов пульсовой волны; 3. улучшение тканевого обмена сердечной мышцы и понижение возбудимости проводящей системы сердца замедляют атриовентрикулярную проводимость и проводимость по пучку Гиса. Вызываемое гликозидами усиление сокращений миокарда способствует изгнанию крови из желудочков, лучшей оксигенации тканей, уменьшению застойных явлений и снятию отеков.
Большие дозы сердечных гликозидов могут вызвать чрезмерное угнетение проводимости сердечной мышцы и полную блокаду сердца. При этом сердце будет сокращаться в более редком ритме атриовентрикулярного узла, который может прерываться экстрасистолией и даже полной остановкой сердца. На ЭКГ это будет проявляться в уменьшении величины зубца Т, укорочении интервала QRST, увеличении интервала P-Q и расстояния между циклами (R-R), а также брадикардией.
Средства, улучшающие коронарный кровоток и метаболизм миокарда
Коронарный кровоток обеспечивает сердечную мышцу кислородом. Нарушение кровоснабжения и метаболизма миокарда является одной из причин ишемической болезни сердца (ИБС), приступов стенокардии, инфаркта миокарда. Действие лекарственных препаратов должно быть направлено на повышение способности коронарной системы доставлять кровь в ишеминизированный участок сердца, уменьшение потребности миокарда в кислороде и на устранение болей в области сердца (антиангинальное действие). В число этих препаратов входят органические нитраты, антагонисты кальция, бета-адреноблокаторы и спазмолитические средства. Основной представитель группы органических нитратов – это нитроглицерин и его современные лекарственные формы: нитросорбит, нитрогранулог, сустак, нитронг, оказывающие пролонгированное действие. В отличие от нитроглицерина, они пред-назначены не для купирования приступа стенокардии, а для его профилактики. Нитроглицерин используется в основном сублингвально (эффект наступает через 1–2 мин). Нитроглицерин действует на центральную гемодинамику, тормозит влияние симпатической нервной системы на сосудистый тонус, выступая в качестве периферического вазодилататора. Он оказывает прямое расширяющее действие на коллатерали коронарных артерий, в результате улучшается коронарный кровоток. Препарат уменьшает венозный приток крови к сердцу, при этом снижается давление в правом предсердии и системе легочной вены, уменьшается периферическое сосудистое сопротивление, в результате нагрузка на миокард и его потребность в кислороде становятся меньше, коронарный кровоток улучшается и исчезает болевая импульсация от ишемического очага в сердечной мышце – боли прекращаются.Средства, нормализующие кровяное давление
Гипотензивные препараты.
К ним относятся вещества, снижающие системное артериальное давление.По механизму действия они делятся на три группы: 1. нейротропные средства, ингибирующие влияния симпатической нервной системы на сосудистый тонус 2. миотропные средства, влияющие непосредственно на гладкую мускулатуру сосудов 3. средства, влияющие на гуморальную регуляцию сосудистого тонуса.
К первой группе относят также препараты: 1. влияющие на сосудодвигательные центры головного мозга (клофелин, метилдофа, гуанфацин) 2. блокирующие проведение нервных импульсов на уровне вегетативных ганглиев (бензогексоний, пентамин) 3. блокирующие пресинаптические окончания адренергических нейронов – симпатолитические средства (октадин, резерпин) 4. угнетающие альфаи бета-адренорецепторы (фентоламин, тропафен, анаприлин).
Ко второй группе миотропных средств относят некоторые спазмолитические препараты (папаверин, но-шпа), но они оказывают слабое гипотензивное действие и назначаются в сочетании с другими средствами, а также периферические вазодилататоры (апрессин, миноксидил). К третьей группе гипотензивных средств относят антагонисты кальциевых каналов (нифедипин), агонисты (открыватели) калиевых каналов, повышающие мембранный потенциал, приводящие к гиперполяризации мембраны и снижению возбудимости клетки (кромакалим). Блокаторы ангиотензин-конвертирующего фермента (каптоприл, эналаприл) и антагонисты альдостерона (спиронолактон) относят к новой группе гипотензивных препаратов. В лечении гипертонической болезни помимо гипотензивных средств используют диуретики, антигипертензивное действие которых основано на уменьшении объема циркулирующей плазмы крови и ослаблении вазоконстрикторного эффекта симпатической нервной системы на сосудистую стенку.
Гипертензивные препараты.
Для повышения АД при гипотепзии используют кардиотонические препараты (строфантин), симпатомиметические (норадреналин, мезатон и др.), дофа-минергические (дофамин), аналептические (камфора, кордиамин). Наиболее эффективным является ангиотензинамид – экзогенный лиганд ангиотензиновых рецепторов.Средства, влияющие на метаболизм сосудистой стенки и ее проницаемость
Для лечения заболеваний периферических сосудов, нарушения их проницаемости при заболеваниях вен с застойными и воспалительными явлениями, трофических язвах, ангиопатиях используют ангиопротекторы – вещества, улучшающие микроциркуляцию, нормализующие проницаемость сосудов, уменьшающие отечность тканей сосудов, улучшающие метаболизм сосудистой стенки. К ним относятся препараты пармидин, трибенозид, троксевазин и препараты группы витамина Р. Механизм действия ангиопротекторов основан на их ингибирующем влиянии на активность гиалуронидазы, торможении биосинтеза простагландинов, антибрадикининовом действии.Глава 8. Физиология дыхания
Человек и все высокоорганизованные живые существа нуждаются для своей нормальной жизнедеятельности в постоянном поступлении к тканям организма кислорода, который используется в сложном биохимическом процессе окисления питательных веществ, в результате чего выделяется энергия и образуется двуокись углерода и вода. Дыхание – синоним и неотъемлемый признак жизни. «Пока дышу – надеюсь», утверждали древние римляне, а греки называли атмосферу «пастбищем жизни». Человек в день съедает примерно 1,24 кг пищи, выпивает 2 л воды, но вдыхает свыше 9 кг воздуха (более 10 000 л). Дыхание – это совокупность процессов, обеспечивающих потребление организмом кислорода и выделение двуокиси углерода. В условиях покоя в организме за 1 минуту потребляется в среднем 250 – 300 мл О2 и выделяется 200 – 250 мл СО2. При физической работе большой мощности потребность в кислороде существенно возрастает и максимальное потребление кислорода (МПК) достигает у высокотренированных людей около 6 – 7 л/мин. Дыхание осуществляет перенос О2 из атмосферного воздуха к тканям организма, а в обратном направлении производит удаление СО2 из организма в атмосферу.Различают несколько этапов дыхания: 1. Внешнее дыхание – обмен газов между атмосферой и альвеолами. 2. Обмен газов между альвеолами и кровью легочных капилляров. 3. Транспорт газов кровью – процесс переноса О2 от легких к тканям и СО2 от тканей – к легким. 4. Обмен О2 и СО2 между кровью капилляров и клетками тканей организма. 5. Внутреннее, или тканевое, дыхание – биологическое окисление в митохондриях клетки.
Состав и свойства дыхательных сред
Дыхательной средой для человека является атмосферный воздух, состав которого отличается постоянством. В 1 л сухого воздуха содержится 780 мл азота, 210 мл кислорода и 0,3 мл двуокиси углерода (табл. 1). Остальные 10 мл приходятся на инертные газы – аргон, неон, гелий, криптон, ксенон и водород.Таблица 1. Содержание и парциальное давление (напряжение) кислорода и углекислого газа в различных средах
| Среда | Кислород | Углекислый газ | ||||
|---|---|---|---|---|---|---|
| % | мм рт.ст. | мл/л | % | мм рт.ст. | мл/л | |
| Вдыхаемый воздух | 20,93 | 159 | 209,3 | 0,03 | 0,2 | 0,3 |
| Выдыхаемый воздух | 16,0 | 121 | 160,0 | 4,5 | 34 | 45 |
| Альвеолярный воздух | 14,0 | 100 | 140,0 | 5,5 | 40 | 55 |
| Артериальная кровь | - | 100–96 | 200,0 | - | 40 | 560–540 |
| Венозная кровь | - | 40 | 140–160 | - | 46 | 580 |
| Ткань | - | 10–15 | - | - | 60 | - |
| Около митохондрий | - | 0,1–1 | - | - | 70 | - |
Внешнее дыхание
Внешнее дыхание осуществляется благодаря изменениям объема грудной клетки и сопутствующим изменениям объема легких. Во время вдоха объем грудной клетки увеличивается, а во время выдоха – уменьшается.В дыхательных движениях участвуют: 1. Дыхательные пути, которые по своим свойствам являются слегка растяжимыми, сжимаемыми и создают поток воздуха. Дыхательная система состоит из тканей и органов, обеспечивающих легочную вентиляцию и легочное дыхание (воздухоносные пути, легкие и элементы костно-мышечной системы). К воздухоносным путям, управляющим потоком воздуха, от-носятся: нос, полость носа, носоглотка, гортань, трахея, бронхи и бронхиолы. Легкие состоят из бронхиол и альвеолярных мешочков, а также из артерий, капилляров и вен легочного круга кровообращения. К элементам костно-мышечной системы, связанным с дыханием, относятся ребра, межреберные мышцы, диафрагма и вспомогательные дыхательные мышцы. Нос и полость носа служат проводящими каналами для воздуха, где он нагревается, увлажняется и фильтруется. Полость носа выстлана богато васкулиризированной слизистой оболочкой. В верхней части полости носа лежат обонятельные рецепторы. Носовые ходы открываются в носоглотку. Гортань лежит между трахеей и корнем языка. У нижнего конца гортани начинается трахея и спускается в грудную полость, где делится на правый и левый бронхи. Установлено, что дыхательные пути от трахеи до концевых дыхательных единиц (альвеол) ветвятся (раздваиваются) 23 раза. Первые 16 «поколений» дыхательных путей – бронхи и бронхиолы выполняют проводящую функцию. «Поколения» 17 – 22 – респираторные бронхиолы и альвеолярные ходы, составляют переходную (транзиторную) зону, и только 23-е «поколение» является дыхательной респираторной зоной и целиком состоит из альвеолярных мешочков с альвеолами. Общая площадь поперечного сечения дыхательных путей по мере ветвления возрастает более чем в 4,5 тысячи раз. Правый бронх обычно короче и шире левого. 2. Эластическая и растяжимая легочная ткань. Респираторный отдел представлен альвеолами. В легких имеется три типа альпеолоцитов (пневмоцитов), выполняющих разную функцию. Альвеолоциты второго типа осуществляют синтез липидов и фосфолипидов легочного сурфактанта. Общая площадь альвеол у взрослого человека достигает 80 – 90 м2, т. е. примерно в 50 раз превышает поверхность тела человека. 3. Грудная клетка, состоящая из пассивной костно-хрящевой основы, которая соединена соединительными связками и дыхательными мышцами, осуществляющими поднятие и опускание ребер и движения купола диафрагмы. За счет большого количества эластической ткани легкие, обладая значительной растяжимостью и эластичностью, пассивно следуют за всеми изменениями конфигурации и объема грудной клетки.
Чем больше разность между давлением воздуха внутри и снаружи легкого, тем больше они будут растягиваться. Для иллюстрации этого положения служит модель Дондерса (рис. 18).
 Существуют два механизма, вызывающие изменение объема грудной клетки: поднятие и опускание ребер и движения купола диафрагмы. Дыхательные мышцы подразделяются на инспираторные и экспираторные.
Инспираторными мышцами являются диафрагма, наружные межреберные и межхрящевые мышцы. При спокойном дыхании объем грудной клетки изменяется в основном за счет сокращения диафрагмы и перемещения ее купола. Опусканию диафрагмы всего на 1 см соответствует увеличение емкости грудной полости примерно на 200–300 мл. При глубоком форсированном дыхании участвуют дополнительные мышцы вдоха: трапециевидные, передние лестничные и грудино-ключично-сосцевидные мышцы. Они включаются в активный процесс дыхания при значительно больших величинах легочной вентиляции, например, при восхождении альпинистов на большие высоты или при дыхательной недостаточности, когда в процесс дыхания вступают почти все мышцы туловища.
Экспираторными мышцами являются внутренние межреберные и мышцы брюшной стенки, или мышцы живота. Каждое ребро способно вращаться вокруг оси, проходящей через две точки подвижного соединения с телом и поперечным отростком соответствующего позвонка.
Верхние отделы грудной клетки на вдохе расширяются преимущественно в переднезаднем направлении, а нижние отделы больше расширяются в боковых направлениях, так как ось вращения нижних ребер занимает сагиттальное положение.
В фазу вдоха наружные межреберные мышцы, сокращаясь, поднимают ребра, а в фазу выдоха ребра опускаются благодаря активности внутренних межреберных мышц.
При обычном спокойном дыхании выдох осуществляется пассивно, поскольку грудная клетка и легкие спадаются – стремятся занять после вдоха то положение, из которого они были выведены сокращением дыхательных мышц. Однако при кашле, рвоте, натуживании мышцы выдоха активны.
При спокойном вдохе увеличение объема грудной клетки составляет примерно 500 – 600 мл. Движение диафрагмы во время дыхания обусловливает до 80% вентиляции легких. У спортсменов высокой квалификации во время глубокого дыхания купол диафрагмы может смещаться до 10–12 см.
Существуют два механизма, вызывающие изменение объема грудной клетки: поднятие и опускание ребер и движения купола диафрагмы. Дыхательные мышцы подразделяются на инспираторные и экспираторные.
Инспираторными мышцами являются диафрагма, наружные межреберные и межхрящевые мышцы. При спокойном дыхании объем грудной клетки изменяется в основном за счет сокращения диафрагмы и перемещения ее купола. Опусканию диафрагмы всего на 1 см соответствует увеличение емкости грудной полости примерно на 200–300 мл. При глубоком форсированном дыхании участвуют дополнительные мышцы вдоха: трапециевидные, передние лестничные и грудино-ключично-сосцевидные мышцы. Они включаются в активный процесс дыхания при значительно больших величинах легочной вентиляции, например, при восхождении альпинистов на большие высоты или при дыхательной недостаточности, когда в процесс дыхания вступают почти все мышцы туловища.
Экспираторными мышцами являются внутренние межреберные и мышцы брюшной стенки, или мышцы живота. Каждое ребро способно вращаться вокруг оси, проходящей через две точки подвижного соединения с телом и поперечным отростком соответствующего позвонка.
Верхние отделы грудной клетки на вдохе расширяются преимущественно в переднезаднем направлении, а нижние отделы больше расширяются в боковых направлениях, так как ось вращения нижних ребер занимает сагиттальное положение.
В фазу вдоха наружные межреберные мышцы, сокращаясь, поднимают ребра, а в фазу выдоха ребра опускаются благодаря активности внутренних межреберных мышц.
При обычном спокойном дыхании выдох осуществляется пассивно, поскольку грудная клетка и легкие спадаются – стремятся занять после вдоха то положение, из которого они были выведены сокращением дыхательных мышц. Однако при кашле, рвоте, натуживании мышцы выдоха активны.
При спокойном вдохе увеличение объема грудной клетки составляет примерно 500 – 600 мл. Движение диафрагмы во время дыхания обусловливает до 80% вентиляции легких. У спортсменов высокой квалификации во время глубокого дыхания купол диафрагмы может смещаться до 10–12 см.
Внутриплевральное и внутрилегочное давление
Внутригрудное пространство, в котором находятся легкие, герметично замкнуто и с внешней средой не сообщается. Легкие окружены листками плевры: париетальный листок плотно спаян со стенками грудной клетки, диафрагмы, а висцеральный – с наружной поверхностью ткани легкого. Листки плевры увлажнены небольшим количеством серозной жидкости, играющей роль своеобразной смазки, облегчающей трение – скольжение листков при дыхательных движениях. Внутриплевральное давление, или давление в герметично замкнутой плевральной полости между висцеральными и париетальными листками плевры, в норме является отрицательным относительно атмосферного. При открытых верхних дыхательных путях давление во всех отделах легких равно атмосферному. Перенос атмосферного воздуха в легкие происходит при появлении разницы давлений между внешней средой и альвеолами легких. При каждом вдохе объем легких увеличивается, давление заключенного в них воздуха, или внутрилегочное давление, становится ниже атмосферного, и воздух засасывается в легкие. При выдохе объем легких уменьшается, внутрилегочное давление повышается и воздух выталкивается из легких в атмосферу. Внутриплевральное давление обусловлено эластической тягой легких или стремлением легких уменьшить свой объем. При обычном спокойном дыхании внутриплевральное давление ниже атмосферного: в инспирацию – на 6 -8 см вод. ст., а в экспирацию – на 4 -5 см вод. ст. Прямые измерения показали, что внутриплевральное давление в апикальных частях легких ниже, чем в прилегающих к диафрагме базальных отделах легких. В положении стоя этот градиент практически линейный и не изменяется в процессе дыхания (рис.19). Важным фактором, влияющим на эластические свойства и растяжимость легких, является поверхностное натяжение жидкости в альвеолах. Спадению альвеол препятствует антиателектатический фактор, или сурфактант, выстилающий внутреннюю поверхность альвеол, препятствующий их спадению, а также выходу жидкости на поверхность альвеол из плазмы капилляров легкого. Синтез и замена поверхностно-активного вещества – сурфактанта происходит довольно быстро, поэтому нарушение кровотока в легких, воспаление и отеки, курение, острая кислородная недостаточность (гипоксия) или избыток кислорода (гипероксия), а также различные токсические вещества, в том числе некоторые фармакологические препараты (жирорастворимые анестетики), могут снизить его запасы и увеличить поверхностное натяжение жидкости в альвеолах. Все это ведет к их ателектазу, или спадению. В профилактике и лечении ателектазов определенное значение имеют аэрозольные ингаляции лекарственных средств, содержащих фосфолипидный компонент, например лецитин, который способствует восстановлению сурфактанта.
Пневмотораксом называется поступление воздуха в межплевральное пространство, возникающее при проникающих ранениях грудной клетки, нарушающих герметичность плевральной полости. При этом легкие спадаются, так как внутриплевральное давление становится одинаковым с атмосферным. У человека левая и правая плевральные полости не сообщаются, и благодаря этому односторонний пневмоторакс, например слева, не ведет к прекращению легочного дыхания правого легкого. Двусторонний открытый пневмоторакс несовместим с жизнью.
Важным фактором, влияющим на эластические свойства и растяжимость легких, является поверхностное натяжение жидкости в альвеолах. Спадению альвеол препятствует антиателектатический фактор, или сурфактант, выстилающий внутреннюю поверхность альвеол, препятствующий их спадению, а также выходу жидкости на поверхность альвеол из плазмы капилляров легкого. Синтез и замена поверхностно-активного вещества – сурфактанта происходит довольно быстро, поэтому нарушение кровотока в легких, воспаление и отеки, курение, острая кислородная недостаточность (гипоксия) или избыток кислорода (гипероксия), а также различные токсические вещества, в том числе некоторые фармакологические препараты (жирорастворимые анестетики), могут снизить его запасы и увеличить поверхностное натяжение жидкости в альвеолах. Все это ведет к их ателектазу, или спадению. В профилактике и лечении ателектазов определенное значение имеют аэрозольные ингаляции лекарственных средств, содержащих фосфолипидный компонент, например лецитин, который способствует восстановлению сурфактанта.
Пневмотораксом называется поступление воздуха в межплевральное пространство, возникающее при проникающих ранениях грудной клетки, нарушающих герметичность плевральной полости. При этом легкие спадаются, так как внутриплевральное давление становится одинаковым с атмосферным. У человека левая и правая плевральные полости не сообщаются, и благодаря этому односторонний пневмоторакс, например слева, не ведет к прекращению легочного дыхания правого легкого. Двусторонний открытый пневмоторакс несовместим с жизнью.
Вентиляция легких и легочные объемы
Величина легочной вентиляции определяется глубиной дыхания и частотой дыхательных движений. Количественной характеристикой легочной вентиляции служит минутный объем дыхания (МОД) – объем воздуха, проходящий через легкие за 1 минуту. В покое частота дыхательных движений человека составляет примерно 16 в 1 минуту, а объем выдыхаемого воздуха – около 500 мл. Умножив частоту дыхания в 1 минуту на величину дыхательного объема, получим МОД, который у человека в покое составляет в среднем 8 л/мин. Максимальная вентиляция легких (МВЛ) – объем воздуха, который проходит через легкие за 1 минуту во время максимальных по частоте и глубине дыхательных движений. Максимальная вентиляция возникает во время интенсивной работы, при недостатке содержания О2 (гипоксия) и избытке СО2 (гиперкапния) во вдыхаемом воздухе. В этих условиях МОД может достигать 150 – 200 л в 1 минуту. Объем воздуха в легких и дыхательных путях зависит от конституционально-антропологических и возрастных характеристик человека, свойств легочной ткани, поверхностного натяжения альвеол, а также силы, развиваемой дыхательными мышцами. Для оценки вентиляционной функции легких, состояния дыхательных путей, изучения паттерна (рисунка) дыхания применяются различные методы исследования: пневмография, спирометрия, спирография, пневмоскрин. С помощью спирографа можно определить и записать величины легочных объемов воздуха, проходящих через воздухоносные пути человека (рис. 20). При спокойном вдохе и выдохе через легкие проходит сравнительно небольшой объем воздуха. Это дыхательный объем (АО), который у взрослого человека составляет примерно 500 мл. При этом акт вдоха проходит несколько быстрее, чем акт выдоха. Обычно за 1 минуту совершается 12- 16 дыхательных циклов. Такой тип дыхания обычно называется «эйпноэ» или «хорошее дыхание».
При форсированном (глубоком) вдохе человек может дополнительно вдохнуть еще определенный объем воздуха. Этот резервный объем вдоха (РОвд) – максимальный объем воздуха, который способен вдохнуть человек после спокойного вдоха. Величина резервного объема вдоха составляет у взрослого человека примерно 1,8–2,0 л.
После спокойного выдоха человек может при форсированном выдохе дополнительно выдохнуть еще определенный объем воздуха. Это резервный объем выдоха (РОвыд), величина которого составляет в среднем 1,2–1,4 л.
Объем воздуха, который остается в легких после максимального выдоха и в легких мертвого человека, – остаточный объем легких (ОО). Величина остаточного объема составляет 1,2 – 1,5 л. У аборигенов высокогорья из-за бочкообразной грудной клетки сохраняются более высокие величины этого показателя, благодаря чему удается сохранить в организме необходимое содержание СО2, достаточное для регуляции дыхания в этих условиях.
При спокойном вдохе и выдохе через легкие проходит сравнительно небольшой объем воздуха. Это дыхательный объем (АО), который у взрослого человека составляет примерно 500 мл. При этом акт вдоха проходит несколько быстрее, чем акт выдоха. Обычно за 1 минуту совершается 12- 16 дыхательных циклов. Такой тип дыхания обычно называется «эйпноэ» или «хорошее дыхание».
При форсированном (глубоком) вдохе человек может дополнительно вдохнуть еще определенный объем воздуха. Этот резервный объем вдоха (РОвд) – максимальный объем воздуха, который способен вдохнуть человек после спокойного вдоха. Величина резервного объема вдоха составляет у взрослого человека примерно 1,8–2,0 л.
После спокойного выдоха человек может при форсированном выдохе дополнительно выдохнуть еще определенный объем воздуха. Это резервный объем выдоха (РОвыд), величина которого составляет в среднем 1,2–1,4 л.
Объем воздуха, который остается в легких после максимального выдоха и в легких мертвого человека, – остаточный объем легких (ОО). Величина остаточного объема составляет 1,2 – 1,5 л. У аборигенов высокогорья из-за бочкообразной грудной клетки сохраняются более высокие величины этого показателя, благодаря чему удается сохранить в организме необходимое содержание СО2, достаточное для регуляции дыхания в этих условиях.
Различают следующие емкости легких: 1. общая емкость легких (ОЕЛ) – объем воздуха, находящегося в легких после максимального вдоха – все четыре объема; 2. жизненная емкость легких (ЖЕЛ) включает в себя дыхательный объем, резервный объем вдоха, резервный объем выдоха. ЖЕЛ – это объем воздуха, выдохнутого из легких после максимального вдоха при максимальном выдохе. ЖЕЛ = ОЕЛ – остаточный объем легких. ЖЕЛ составляет у мужчин 3,5 – 5,0 л, у женщин – 3,0–4,0 л; 3. емкость вдоха (ЕВД) равна сумме дыхательного объема и резервного объема вдоха, составляет в среднем 2,0–2,5 л; 4. функциональная остаточная емкость (ФОЕ) – объем воздуха в легких после спокойного выдоха. В легких при спокойном вдохе и выдохе постоянно содержится примерно 2500 мл воздуха, заполняющего альвеолы и нижние дыхательные пути. Благодаря этому газовый состав альвеолярного воздуха сохраняется на постоянном уровне.
Исследование легочных объемов и емкостей как важнейших показателей функционального состояния легких имеет большое медико-физиологическое значение не только для диагностики заболеваний (ателектаз, рубцовые изменения легких, поражения плевры), но и для экологического мониторинга местности и оценки состояния функции дыхания популяции в экологически неблагополучных зонах. Для сопоставимости результатов измерений газовых объемов и емкостей материалы исследований должны быть приведены к стандартному состоянию BTPS, т. е. соотноситься с условиями в легких, где температура альвеолярного воздуха соответствует температуре тела, кроме того, воздух находится при определенном давлении и насыщен водяными парами. Воздух, находящийся в воздухоносных путях (полость рта, носа, глотки, трахеи, бронхов и бронхиол), не участвует в газообмене, и поэтому пространство воздухоносных путей называют вредным или мертвым дыхательным пространством. Во время спокойного вдоха объемом 500 мл в альвеолы поступает только 350 мл вдыхаемого атмосферного воздуха. Остальные 150 мл задерживаются в анатомическом мертвом пространстве. Составляя в среднем треть дыхательного объема, мертвое пространство снижает на эту величину эффективность альвеолярной вентиляции при спокойном дыхании. В тех случаях, когда при выполнении физической работы дыхательный объем увеличивается в несколько раз, объем анатомического мертвого пространства практически не влияет на эффективность альвеолярной вентиляции. При некоторых патологических состояниях – при анемии, легочной эмболии или эмфиземе могут возникать очаги – зоны альвеолярного мертвого пространства. В подобных зонах легких не происходит газообмена.
Газообмен и транспорт газов
Газообмен О2 и СО2 через альвеолярно-капиллярную мембрану происходит с помощью диффузии, которая осуществляется в два этапа. На первом этапе диффузионный перенос газов происходит через аэрогематический барьер, на втором – происходит связывание газов в крови легочных капилляров, объем которой оставляет 80- 150 мл при толщине слоя крови в капиллярах всего 5 – 8 мкм. Плазма крови практически не препятствует диффузии газов, в отличие от мембраны эритроцитов. Структура легких создает благоприятные условия для газообмена: дыхательная зона каждого легкого содержит около 300 млн альвеол и примерно такое же число капилляров, имеет площадь 40–140 м2 при толщине аэрогематического барьера всего 0,3- 1,2 мкм. Особенности диффузии газов количественно харктеризуются через диффузионную способность легких. Для О2 диффузионная способность легких – это объем газа, переносимого из альвеол в кровь в 1 минуту при градиенте альвеолярно-капиллярного давления газа, равном 1 мм рт.ст. Движение газов происходит в результате разницы парциальных давлений. Парциальное давление – это та часть давления, которую составляет данный газ из общей смеси газов. Пониженное давление О2 в ткани способствует движению кислорода к ней. Для СО2 градиент давления направлен в обратную сторону, и СО2 с выдыхаемым воздухом уходит в окружающую среду. Изучение физиологии дыхания фактически сводится к изучению этих градиентов и того, как они поддерживаются. Градиент парциального давления кислорода и углекислого газа это сила, с которой молекулы этих газов стремятся проникнуть через альвеолярную мембрану в кровь. Парциальное напряжение газа в крови или тканях – это сила, с которой молекулы растворимого газа стремятся выйти в газовую среду. На уровне моря атмосферное давление составляет в среднем 760 мм рт.ст., а процентное содержание кислорода – около 21%. В этом случае рО2 в атмосфере составляет: 760х21/100=159 мм рт.ст. При вычислении парциального давления газов в альвеолярном воздухе следует учитывать, что в этом воздухе присутствуют пары воды (47 мм рт.ст.). Поэтому это число вычитают из значения атмосферного давления, и на долю парциального давления газов приходится (760 – 47) = 713 мм рт.ст. При содержании кислорода в альвеолярном воздухе, равном 14 %, его парциальное давление будет 100 мм рт. ст. При содержании двуокиси углерода, равном 5,5%, парциальное давление СО2 составит примерно 40 мм рт.ст. В артериальной крови парциальное напряжение кислорода достигает почти 100 мм рт.ст., в венозной крови – около 40 мм рт.ст., а в тканевой жидкости, в клетках – 10 -15 мм рт.ст. Напряжение углекислого газа в артериальной крови составляет около 40 мм рт.ст., в венозной – 46 мм рт.ст., а в тканях – до 60 мм рт.ст. Газы в крови находятся в двух состояниях: физически растворенном и химически связанном. Растворение происходит в соответствии с законом Генри, согласно которому количество газа, растворенного в жидкости, прямо пропорционально парциальному давлению этого газа над жидкостью. На каждую единицу парциального давления в 100 мл крови растворяется 0,003 мл О2, или 3 мл/л крови. Каждый газ имеет свой коэффициент растворимости. При температуре тела растворимость СО2 в 25 раз больше, чем О2. Из-за хорошей растворимости углекислоты в крови и тканях СО2 переносится в 20 раз легче, чем О2. Стремление газа переходить из жидкости в газовую фазу называют напряжением газа. В обычных условиях в 100 мл крови находится в растворенном состоянии всего 0,3 мл О2 и 2,6 мл СО2. Такие величины не могут обеспечить запросы организма в О2. Газообмен кислорода между альвеолярным воздухом и кровью происходит благодаря наличию концентрационного градиента О2 между этими средами. Транспорт кислорода начинается в капиллярах легких, где основная масса поступающего в кровь О2 вступает в химическую связь с гемоглобином. Гемоглобин способен избирательно связывать О2 и образовывать оксигемоглобин (НвО2). Один грамм гемоглобина связывает 1,36- 1,34 мл О2, а в 1 литре крови содержится 140- 150 г гемоглобина. На 1 грамм гемоглобина приходится 1,39 мл кислорода. Следовательно, в каждом литре крови максимально возможное содержание кислорода в химически связанной форме составит 190 – 200 мл О2, или 19 об% – это кислородная емкость крови. Кровь человека содержит примерно 700 – 800 г гемоглобина и может связывать 1 л кислорода. Под кислородной емкостью крови понимают количество О2, которое связывается кровью до полного насыщения гемоглобина. Изменение концентрации гемоглобина в крови, например, при анемиях, отравлениях ядами изменяет ее кислородную емкость. При рождении в крови у человека более высокие значения кислородной емкости и концентрации гемоглобина. Насыщение крови кислородом выражает отношение количества связанного кислорода к кислородной емкости крови, т. е. под насыщением крови О2 подразумевается процент оксигемоглобина по отношению к имеющемуся в крови гемоглобину. В обычных условиях насыщение О., составляет 95 – 97%. При дыхании чистым кислородом насыщение крови О2 достигает 100%, а при дыхании газовой смесью с низким содержанием кислорода процент насыщения падает. При 60 – 65% наступает потеря сознания. Зависимость связывания кислорода кровью от его парциального давления можно представить в виде графика, где по оси абсцисс откладывается рО2 в крови, по ординате – насыщение гемоглобина кислородом. Этот график – криваядиссоциации оксигемоглобина, или сатурационная кривая, показывает, какая доля гемоглобина в данной крови связана с О2 при том или ином его парциальном давлении, а какая – диссоциирована, т. е. свободна от кислорода. Кривая диссоциации имеет S-образную форму. Плато кривой характерно для насыщенной О2 (сатурированной) артериальной крови, а крутая нисходящая часть кривой – венозной, или десатурированной, крови в тканях (рис. 21). Сродство кислорода к гемоглобину и способность отдавать О2 в тканях зависит от метаболических потребностей клеток организма и регулируется важнейшими факторами метаболизма тканей, вызывающими смещение кривой диссоциации. К этим факторам относятся: концентрация водородных ионов, температура, парциальное напряжение углекислоты и соединение, которое накапливается в эритроцитах – это 2,3-дифосфоглицератфосфат (ДФГ). Уменьшение рН крови вызывает сдвиг кривой диссоциации вправо, а увеличение рН крови – сдвиг кривой влево. Вследствие повышенного содержания СО2 в тканях рН также меньше, чем в плазме крови. Величина рН и содержание СО2 в тканях организма изменяют сродство гемоглобина к О2. Их влияние на кривую диссоциации оксигемоглобина называется эффектом Бора (Х. Бор, 1904). При повышении концентрации водородных ионов и парциального напряжения СО2 в среде сродство гемоглобина к кислороду снижается. Этот «эффект» имеет важное приспособительное значение: СО2 в тканях поступает в капилляры, поэтому кровь при том же рО2 способна освободить больше кислорода. Образующийся при расщеплении глюкозы метаболит 2,3-ДФГ также снижает сродство гемоглобина к кислороду.
На кривую диссоциации оксигемоглобина оказывает влияние также и температура. Рост температуры значительно увеличивает скорость распада оксигемоглобина и уменьшает сродство гемоглобина к О2. Увеличение температуры в работающих мышцах способствует освобождению О2. Связывание О2 гемоглобином снижает сродство его аминогрупп к СО2 (эффект Холдена). Диффузия СО2 из крови в альвеолы обеспечивается за счет поступления растворенного в плазме крови СО2 (5- 10%), из гидрокарбонатов (80 – 90%) и, наконец, из карбаминовых соединений эритроцитов (5 – 15%), которые способны диссоциировать.
Углекислый газ в крови находится в трех фракциях: физически растворенный, химически связанный в виде бикарбонатов и химически связанный с гемоглобином в виде карбогемоглобина. В венозной крови углекислого газа содержится всего 580 мл. При этом на долю физически растворенного газа приходится 25 мл, на долю карбогемоглобина – около 45 мл, на долю бикарбонатов – 510 мл (бикарбонатов плазмы – 340 мл, эритроцитов – 170 мл). В артериальной крови содержание угольной кислоты меньше.
От парциального напряжения физически растворенного углекислого газа зависит процесс связывания СО2 кровью. Углекислота поступает в эритроцит, где имеется фермент карбоангидраза, который может в 10 000 раз увеличить скорость образования угольной кислоты. Пройдя через эритроцит, угольная кислота превращается в бикарбонат и переносится к легким.
Эритроциты переносят в 3 раза больше СО2, чем плазма. Белки плазмы составляют 8 г на 100 см3 крови, гемоглобина же содержится в крови 15 г на 100 см3. Большая часть СО2 транспортируется в организме в связанном состоянии в виде гидрокарбонатов и карбаминовых соединений, что увеличивает время обмена СО2.
Кроме физически растворенного в плазме крови молекулярного СО2 из крови в альвеолы легких диффундирует СО2, который высвобождается из карбаминовых соединений эритроцитов благодаря реакции окисления гемоглобина в капиллярах легкого, а также из гидрокарбонатов плазмы крови в результате их быстрой диссоциации с помощью содержащегося в эритроцитах фермента карбоангидразы. Этот фермент в плазме отсутствует. Бикарбонаты плазмы для освобождения СО2 должны сначала проникнуть в эритроциты, чтобы подвергнуться действию карбоангидразы. В плазме находится бикарбонат натрия, а в эритроцитах – бикарбонат калия. Мембрана эритроцитов хорошо проницаема для СО2, поэтому часть СО2 быстро диффундирует из плазмы внутрь эритроцитов. Наибольшее количество бикарбонатов плазмы крови образуется при участии карбоангидразы эритроцитов.
Следует отметить, что процесс выведения СО2 из крови в альвеолы легкого менее лимитирован, чем оксигенация крови, так как молекулярный СО2 легче проникает через биологические мембраны, чем О2.
Различные яды, ограничивающие транспорт О2, такие как СО, нитриты, ферроцианиды и многие другие, практически не действуют на транспорт СО2. Блокаторы карбоангидразы также никогда полностью не нарушают образование молекулярного СО2. И наконец, ткани обладают большой буферной емкостью, но не защищены от дефицита О2. Выведение СО2 легкими может нарушиться при значительном уменьшении легочной вентиляции (гиповентиляции) в результате заболевания легких, дыхательных путей, интоксикации или нарушении регуляции дыхания. Задержка СО2 приводит к дыхательному ацидозу – уменьшению концентрации бикарбонатов, сдвигу рН крови в кислую сторону. Избыточное выведение СО2 при гипервентиляции во время интенсивной мышечной работы, при восхождении на большие высоты может вызвать дыхательный алкалоз, сдвиг рН крови в щелочную сторону.
Сродство кислорода к гемоглобину и способность отдавать О2 в тканях зависит от метаболических потребностей клеток организма и регулируется важнейшими факторами метаболизма тканей, вызывающими смещение кривой диссоциации. К этим факторам относятся: концентрация водородных ионов, температура, парциальное напряжение углекислоты и соединение, которое накапливается в эритроцитах – это 2,3-дифосфоглицератфосфат (ДФГ). Уменьшение рН крови вызывает сдвиг кривой диссоциации вправо, а увеличение рН крови – сдвиг кривой влево. Вследствие повышенного содержания СО2 в тканях рН также меньше, чем в плазме крови. Величина рН и содержание СО2 в тканях организма изменяют сродство гемоглобина к О2. Их влияние на кривую диссоциации оксигемоглобина называется эффектом Бора (Х. Бор, 1904). При повышении концентрации водородных ионов и парциального напряжения СО2 в среде сродство гемоглобина к кислороду снижается. Этот «эффект» имеет важное приспособительное значение: СО2 в тканях поступает в капилляры, поэтому кровь при том же рО2 способна освободить больше кислорода. Образующийся при расщеплении глюкозы метаболит 2,3-ДФГ также снижает сродство гемоглобина к кислороду.
На кривую диссоциации оксигемоглобина оказывает влияние также и температура. Рост температуры значительно увеличивает скорость распада оксигемоглобина и уменьшает сродство гемоглобина к О2. Увеличение температуры в работающих мышцах способствует освобождению О2. Связывание О2 гемоглобином снижает сродство его аминогрупп к СО2 (эффект Холдена). Диффузия СО2 из крови в альвеолы обеспечивается за счет поступления растворенного в плазме крови СО2 (5- 10%), из гидрокарбонатов (80 – 90%) и, наконец, из карбаминовых соединений эритроцитов (5 – 15%), которые способны диссоциировать.
Углекислый газ в крови находится в трех фракциях: физически растворенный, химически связанный в виде бикарбонатов и химически связанный с гемоглобином в виде карбогемоглобина. В венозной крови углекислого газа содержится всего 580 мл. При этом на долю физически растворенного газа приходится 25 мл, на долю карбогемоглобина – около 45 мл, на долю бикарбонатов – 510 мл (бикарбонатов плазмы – 340 мл, эритроцитов – 170 мл). В артериальной крови содержание угольной кислоты меньше.
От парциального напряжения физически растворенного углекислого газа зависит процесс связывания СО2 кровью. Углекислота поступает в эритроцит, где имеется фермент карбоангидраза, который может в 10 000 раз увеличить скорость образования угольной кислоты. Пройдя через эритроцит, угольная кислота превращается в бикарбонат и переносится к легким.
Эритроциты переносят в 3 раза больше СО2, чем плазма. Белки плазмы составляют 8 г на 100 см3 крови, гемоглобина же содержится в крови 15 г на 100 см3. Большая часть СО2 транспортируется в организме в связанном состоянии в виде гидрокарбонатов и карбаминовых соединений, что увеличивает время обмена СО2.
Кроме физически растворенного в плазме крови молекулярного СО2 из крови в альвеолы легких диффундирует СО2, который высвобождается из карбаминовых соединений эритроцитов благодаря реакции окисления гемоглобина в капиллярах легкого, а также из гидрокарбонатов плазмы крови в результате их быстрой диссоциации с помощью содержащегося в эритроцитах фермента карбоангидразы. Этот фермент в плазме отсутствует. Бикарбонаты плазмы для освобождения СО2 должны сначала проникнуть в эритроциты, чтобы подвергнуться действию карбоангидразы. В плазме находится бикарбонат натрия, а в эритроцитах – бикарбонат калия. Мембрана эритроцитов хорошо проницаема для СО2, поэтому часть СО2 быстро диффундирует из плазмы внутрь эритроцитов. Наибольшее количество бикарбонатов плазмы крови образуется при участии карбоангидразы эритроцитов.
Следует отметить, что процесс выведения СО2 из крови в альвеолы легкого менее лимитирован, чем оксигенация крови, так как молекулярный СО2 легче проникает через биологические мембраны, чем О2.
Различные яды, ограничивающие транспорт О2, такие как СО, нитриты, ферроцианиды и многие другие, практически не действуют на транспорт СО2. Блокаторы карбоангидразы также никогда полностью не нарушают образование молекулярного СО2. И наконец, ткани обладают большой буферной емкостью, но не защищены от дефицита О2. Выведение СО2 легкими может нарушиться при значительном уменьшении легочной вентиляции (гиповентиляции) в результате заболевания легких, дыхательных путей, интоксикации или нарушении регуляции дыхания. Задержка СО2 приводит к дыхательному ацидозу – уменьшению концентрации бикарбонатов, сдвигу рН крови в кислую сторону. Избыточное выведение СО2 при гипервентиляции во время интенсивной мышечной работы, при восхождении на большие высоты может вызвать дыхательный алкалоз, сдвиг рН крови в щелочную сторону.
Регуляция внешнего дыхания
В соответствии с метаболическими потребностями дыхательная система обеспечивает газообмен О2 и СО2 между окружающей средой и организмом. Эту жизненно важную функцию регулирует сеть многочисленных взаимосвязанных нейронов ЦНС, расположенных в нескольких отделах мозга и объединяемых в комплексное понятие «дыхательный центр» (рис. 22). При воздействии на его структуры нервных и гуморальных стимулов происходит приспособление функции дыхания к меняющимся условиям внешней среды. Структуры, необходимые для возникновения дыхательного ритма, впервые были обнаружены в продолговатом мозге. Перерезка продолговатого мозга в области дна IV желудочка приводит к прекращению дыхания. Поэтому под главным дыхательным центром понимают совокупность нейронов специфических дыхательных ядер продолговатого мозга.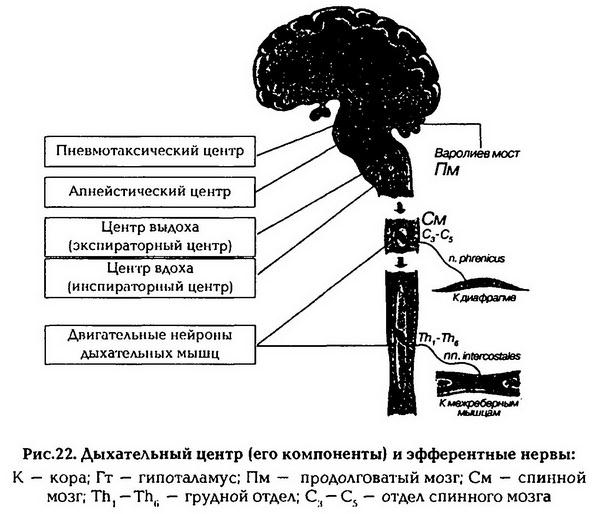 Дыхательный центр управляет двумя основными функциями; двигательной, которая проявляется в виде сокращения дыхательных мышц, и гомеостатической, связанной с поддержанием постоянства внутренней среды организма при сдвигах в ней содержания О2 и СО2 Двигательная, или моторная, функция дыхательного центра заключается в генерации дыхательного ритма и его паттерна. Благодаря этой функции осуществляется интеграция дыхания с другими функциями. Под паттерном дыхания следует иметь в виду длительность вдоха и выдоха, величину дыхательного объема, минутного объема дыхания. Гомеостатическая функция дыхательного центра поддерживает стабильные величины дыхательных газов в крови и внеклеточной жидкости мозга, адаптирует дыхательную функцию к условиям измененной газовой среды и другим факторам среды обитания.
Дыхательный центр управляет двумя основными функциями; двигательной, которая проявляется в виде сокращения дыхательных мышц, и гомеостатической, связанной с поддержанием постоянства внутренней среды организма при сдвигах в ней содержания О2 и СО2 Двигательная, или моторная, функция дыхательного центра заключается в генерации дыхательного ритма и его паттерна. Благодаря этой функции осуществляется интеграция дыхания с другими функциями. Под паттерном дыхания следует иметь в виду длительность вдоха и выдоха, величину дыхательного объема, минутного объема дыхания. Гомеостатическая функция дыхательного центра поддерживает стабильные величины дыхательных газов в крови и внеклеточной жидкости мозга, адаптирует дыхательную функцию к условиям измененной газовой среды и другим факторам среды обитания.
Локализация и функциональные свойства дыхательных нейронов
В передних рогах спинного мозга на уровне С3–С5 располагаются мотонейроны, образующие диафрагмальный нерв. Мотонейроны, иннервирующие межреберные мышцы, находятся в передних рогах на уровнях Т2-Т10 (Т2–Т6 – мотонейроны инспираторных мышц, Т8–Т10 – экспираторных). Установлено, что одни мотонейроны регулируют преимущественно дыхательную, а другие – преимущественно познотоническую активность межреберных мышц. Нейроны бульварного дыхательного центра располагаются на дне IV желудочка в медиальной части ретикулярной формации продолговатого мозга и образуют дорсальную и вентральную дыхательные группы. Дыхательные нейроны, активность которых вызывает инспирацию или экспирацию, называются соответственно инспираторными и экспираторными нейронами. Между группами нейронов, управляющими вдохом и выдохом, существуют реципрокные отношения. Возбуждение экспираторного центра сопровождается торможением в инспираторном центре и наоборот. Инспираторные и экспираторные нейроны, в свою очередь, делятся на «ранние» и «поздние». Каждый дыхательный цикл начинается с активизации «ранних» инспираторных нейронов, затем возбуждаются «поздние» инспираторные нейроны. Также последовательно возбуждаются «ранние» и «поздние» экспираторные нейроны, которые тормозят инспираторные нейроны и прекращают вдох. Современные исследования показали, что в продолговатом мозге нет четкого деления на инспираторный и экспираторный отделы, а есть скопления дыхательных нейронов с определенной функцией. Спонтанная активность нейронов дыхательного центра начинает появляться к концу периода внутриутробного развития. Возбуждение дыхательного центра у плода появляется благодаря пейсмекерным свойствам сети дыхательных нейронов продолговатого мозга. По мере формирования синаптических связей дыхательного центра с различными отделами ЦНС пейсмекерный механизм дыхательной активности постепенно теряет свое физиологическое значение. В варолиевом мосту находятся ядра дыхательных нейронов, образующих пневмотаксический центр. Считается, что дыхательные нейроны моста участвуют в механизме смены вдоха и выдоха и регулируют величину дыхательного объема. Дыхательные нейроны продолговатого мозга и варолиева моста связаны между собой восходящими и нисходящими нервными путями и функционируют согласованно. Получив импульсы от инспирагорного центра продолговатого мозга, пневмотаксический центр посылает их к экспираторному центру продолговатого мозга, возбуждая последний. Инспираторные нейроны тормозятся. Разрушение мозга между продолговатым мозгом и мостом удлиняет фазу вдоха. Гипоталамические ядра координируют связь дыхания с кровообращением. Определенные зоны коры больших полушарий осуществляют произвольную регуляцию дыхания в соответствии с особенностями влияния на организм факторов внешней среды и связанными с этим гомеостатическими сдвигами. Таким образом, мы видим, что управление дыханием – сложнейший процесс, осуществляемый множеством нейронных структур. В процессе управления дыханием осуществляется четкая иерархия различных компонентов и структур дыхательного центра.Рефлекторная регуляция дыхания
Нейроны дыхательного центра имеют связи с многочисленными механорецепторами дыхательных путей и альвеол легких и рецепторов сосудистых рефлексогенных зон. Благодаря этим связям осуществляется весьма многообразная, сложная и биологически важная рефлекторная регуляция дыхания и ее координация с другими функциями организма. Различают несколько типов механорецепторов: медленно адаптирующиеся рецепторы растяжения легких, ирритантные быстро адаптирующиеся механорецепторы и J-рецепторы – «юкстакапиллярные» рецепторы легких. Медленно адаптирующиеся рецепторы растяжения легких расположены в гладких мышцах трахеи и бронхов. Эти рецепторы возбуждаются при вдохе, импульсы от них по афферентным волокнам блуждающего нерва поступают в дыхательный центр. Под их влиянием тормозится активность инспираторных нейронов продолговатого мозга. Вдох прекращается, начинается выдох, при котором рецепторы растяжения неактивны. Рефлекс торможения вдоха при растяжении легких называется рефлексом Геринга – Брейера. Этот рефлекс контролирует глубину и частоту дыхания. Он является примером регуляции по принципу обратной связи. После перерезки блуждающих нервов дыхание становится редким и глубоким. Ирритантные быстро адаптирующиеся механорецепторы, локализованные в слизистой оболочке трахеи и бронхов, возбуждаются при резких изменениях объема легких, при растяжении или спадении легких, при действии на слизистую трахеи и бронхов механических или химических раздражителей. Результатом раздражения ирритантных рецепторов является частое, поверхностное дыхание, кашлевой рефлекс, или рефлекс бронхоконстрикции. J-рецепторы – «юкстакапиллярные» рецепторы легких находятся в интерстиции альвеол и дыхательных бронхов вблизи от капилляров. Импульсы от J-рецепторов при повышении давления в малом круге кровообращения, или увеличении объема интерстициальной жидкости в легких (отек легких), или эмболии мелких легочных сосудов, а также при действии биологически активных веществ (никотин, простагландины, гистамин) по медленным волокнам блуждающего нерва поступают в дыхательный центр – дыхание становится частым и поверхностным (одышка). Важное биологическое значение, особенно в связи с ухудшением экологических условий и загрязнением атмосферы, имеют защитные дыхательные рефлексы – чихание и кашель. Чихание. Раздражение рецепторов слизистой оболочки полости носа, например, пылевыми частицами или газообразными наркотическими веществами, табачным дымом, водой вызывает сужение бронхов, брадикардию, снижение сердечного выброса, сужение просвета сосудов кожи и мышц. Различные механические и химические раздражения слизистой оболочки носа вызывают глубокий сильный выдох – чихание, способствующее стремлению избавиться от раздражителя. Афферентным путем этого рефлекса является тройничный нерв. Кашель возникает при раздражении механои хеморецепторов глотки, гортани, трахеи и бронхов. При этом после вдоха сильно сокращаются мышцы выдоха, резко повышается внутригрудное и внутрилегочное давление (до 200 мм рт. ст.), открывается голосовая щель, и воздух из дыхательных путей под большим напором высвобождается наружу и удаляет раздражающий агент. Кашлевой рефлекс является основным легочным рефлексом блуждающего нерва.Рефлексы с проприорецепторов дыхательных мышц
От мышечных веретен и сухожильных рецепторов Гольджи, расположенных в межреберных мышцах и мышцах живота, импульсы поступают в соответствующие сегменты спинного мозга, затем в продолговатый мозг, центры головного мозга, контролирующие состояние скелетных мышц. В результате происходит регуляция силы сокращений в зависимости от исходной длины мышц и оказываемого им сопротивления дыхательной системы. Рефлекторная регуляция дыхания осуществляется также периферическими и центральными хеморецепторами, что изложено в разделе гуморальной регуляции.Гуморальная регуляция дыхания
Главным физиологическим стимулом дыхательных центров является двуокись углерода. Регуляция дыхания обусловливает поддержание нормального содержания СО2 в альвеолярном воздухе и артериальной крови. Возрастание содержания СО2 в альвеолярном воздухе на 0,17% вызывает удвоение МОД, а вот снижение О2 на 39 – 40% не вызывает существенных изменений МОД. При повышении в замкнутых герметических кабинах концентрации СО2 до 5 -8% у обследуемых наблюдалось увеличение легочной вентиляции в 7 -8 раз. При этом концентрация СО2 в альвеолярном воздухе существенно не возрастала, так как основным признаком регуляции дыхания является необходимость регуляции объема легочной вентиляции, поддерживающей постоянство состава альвеолярного воздуха. Деятельность дыхательного центра зависит от состава крови, поступающей в мозг по общим сонным артериям. В 1890 г. это было показано Фредериком в опытах с перекрестным кровообращением. У двух собак, находившихся под наркозом, перерезали и соединяли перекрестно сонные артерии и яремные вены. При этом голова первой собаки снабжалась кровью второй собаки и наоборот. Если у одной из собак, например у первой, перекрывали трахею и таким путем вызывали асфиксию, то гиперпноэ развивалось у второй собаки. У первой же собаки, несмотря на увеличение в артериальной крови напряжения СО2 и снижение напряжения О2, развивалось апноэ, так как в ее сонную артерию поступала кровь второй собаки, у которой в результате гипервентиляции снижалось напряжение СО2 в артериальной крови. Двуокись углерода, водородные ионы и умеренная гипоксия вызывают усиление дыхания. Эти факторы усиливают деятельность дыхательного центра, оказывая влияние на периферические (артериальные) и центральные (медулярные) хеморецепторы, регулирующие дыхание. Артериальные хеморецепторы находятся в каротидных синусах и дуге аорты. Они расположены в специальных тельцах, обильно снабжаемых артериальной кровью. Аортальные хеморецепторы на дыхание влияют слабо и большее значение имеют для регуляции кровообращения. Артериальные хеморецепторы являются уникальными рецепторными образованиями, на которые гипоксия оказывает стимулирующее влияние. Афферентные влияния каротидных телец усиливаются также при повышении в артериальной крови напряжения двуокиси углерода и концентрации водородных ионов. Стимулирующее действие гипоксии и гиперкапнии на хеморецепторы взаимно усиливается, тогда как в условиях гипероксии чувствительность хеморецепторов к двуокиси углерода резко снижается. Артериальные хеморецепторы информируют дыхательный центр о напряжении О2 и СО2 в крови, направляющейся к мозгу. После перерезки артериальных (периферических) хеморецепторов у подопытных животных исчезает чувствительность дыхательного центра к гипоксии, но полностью сохраняется реакция дыхания на гиперкапнию и ацидоз. Центральные хеморецепторы расположены в продолговатом мозге латеральнее пирамид. Перфузия этой области мозга раствором со сниженным рН резко усиливает дыхание, а при высоком рН дыхание ослабевает, вплоть до апноэ. То же происходит при охлаждении или обработке этой поверхности продолговатого мозга анестетиками. Центральные хеморецепторы, оказывая сильное влияние на деятельность дыхательного центра, существенно изменяют вентиляцию легких. Установлено, что снижение рН спинномозговой жидкости всего на 0,01 сопровождается увеличением легочной вентиляции на 4 л/мин. Центральные хеморецепторы реагируют на изменение напряжения СО2 в артериальной крови позже, чем периферические хеморецепторы, так как для диффузии СО2 из крови в спинномозговую жидкость и далее в ткань мозга необходимо больше времени. Гиперкапния и ацидоз стимулируют, а гипокапния и алкалоз – тормозят центральные хеморецепторы. Для определения чувствительности центральных хеморецепторов к изменению рН внеклеточной жидкости мозга, изучения синергизма и антагонизма дыхательных газов, взаимодействия системы дыхания и сердечно-сосудистой системы используют метод возвратного дыхания. При дыхании в замкнутой системе выдыхаемый СО2 вызывает линейное увеличение концентрации СО2 и одновременно повышается концентрация водородных ионов в крови, а также во внеклеточной жидкости мозга. Совокупность дыхательных нейронов следовало бы рассматривать как созвездие структур, осуществляющих центральный механизм дыхания. Таким образом, вместо термина «дыхательный центр» правильнее говорить о системе центральной регуляции дыхания, которая включает в себя структуры коры головного мозга, определенные зоны и ядра промежуточного, среднего, продолговатого мозга, варолиева моста, нейроны шейного и грудного отделов спинного мозга, центральные и периферические хеморецепторы, а также механорецепторы органов дыхания. Своеобразие функции внешнего дыхания состоит в том, что она одновременно и автоматическая, и произвольно управляемая.Дыхание в измененных условиях
В различных условиях среды обитания системы нейрогуморальной регуляции дыхания и кровообращения функционируют в тесном взаимодействии как единая кардиореспираторная система. Особенно четко это проявляется при интенсивной физической нагрузке и в условиях гипоксии – недостаточном снабжении организма кислородом. В процессе жизнедеятельности в организме возникают различные виды гипоксии, имеющие эндогенную и экзогенную природу.Дыхание при физической нагрузке
Во время выполнения физической работы мышцам необходимо большое количество кислорода. Потребление О2 и продукция СО2 возрастают при физической нагрузке в среднем в 15 – 20 раз. Обеспечение организма кислородом достигается сочетанным усилением функции дыхания и кровообращения. Уже в начале мышечной работы вентиляция легких быстро увеличивается. В возникновении гиперпноэ в начале физической работы периферические и центральные хеморецепторы как важнейшие чувствительные структуры дыхательного центра еще не участвуют. Уровень вентиляции в этот период регулируется сигналами, поступающими к дыхательному центру главным образом из гипота-ламуса, лимбической системы и двигательной зоны коры большого мозга, а также раздражением проприорецепторов работающих мышц. По мере продолжения работы к нейрогенным стимулам присоединяются гуморальные воздействия, вызывающие дополнительный прирост вентиляции. При тяжелой физической работе на уровень вентиляции оказывают влияние также повышение температуры, артериальная двигательная гипоксия и другие лимитирующие факторы. Таким образом, наблюдаемые при физической работе изменил дыхания обеспечиваются сложным комплексом нервных и гуморальных механизмов. Однако из-за индивидуально лимитирующих факторов биомеханики дыхания, особенностей экопортрета человека, не всегда удается при выполнении одной и той же нагрузки полностью объяснить точное соответствие вентиляции легких уровню метаболизма в мышцах.Дыхание при гипоксии
Гипоксией (кислородной недостаточностью) называется состояние, наступающее в организме при неадекватном снабжении тканей и органов кислородом или при нарушении утилизации в них кислорода в процессе биологического окисления. Исходя из этого достаточно точного определения гипоксии, все гипоксические состояния целесообразно разделить на экзогенные и эндогенные (см. схему). Экзогенная гипоксия развивается в результате действия измененных (в сравнении с обычными) факторов внешней среды. Эндогенная гипоксия возникает при различных физиологических и патологических изменениях в различных функциональных системах организма. Реакция внешнего дыхания на гипоксию зависит от продолжительности и скорости нарастания гипоксического воздействия, степени потребления кислорода (покой и физическая нагрузка), индивидуальных особенностей организма и совокупности генетически обусловленных свойств и наследственных морфофункциональных признаков (экопортрет коренных жителей высокогорья и популяции различных этнических групп). Наблюдаемая в условиях кислородной недостаточности первоначальная гипоксическая стимуляция дыхания приводит к вымыванию углекислоты из крови и развитию дыхательного алкалоза. Гипоксия сочетается с гипокапнией. В свою очередь, это способствует увеличению рН внеклеточной жидкости мозга. Центральные хеморецепторы реагируют на подобный сдвиг рН в цереброспинальной жидкости мозга резким снижением своей активности. Это вызывает настолько существенное торможение нейронов дыхательного центра, что он становится нечувствительным к стимулам, исходящим от периферических хеморецепторов. Наступает своеобразная гипоксическая «глухота». Несмотря на сохраняющуюся гипоксию, постепенно гиперпноэ сменяется непроизвольной гиповентиляцией, что в определенной мере способствует также сохранению физиологически необходимого количества углекислоты. Реакция на гипоксию у коренных жителей высокогорья и у горных животных практически отсутствует, и, по мнению многих авторов, у жителей равнин гипоксическая реакция также исчезает после продолжительной (не менее 3 – 5 лет) их адаптации к условиям высокогорья. Основными факторами долговременной акклиматизации к условиям высокогорья являются: повышение содержания углекислоты и понижение содержания кислорода в крови на фоне снижения чувствительности периферических хеморецепторов к гипоксии, увеличения плотности капиллляров и относительно высокого уровня утилизации тканями О2 из крови (рис. 23). У горцев также возрастают диффузионная способность легких и кислородная емкость крови за счет роста концентрации гемоглобина. Одним из механизмов, позволяющих горцам в условиях гипоксии повысить отдачу кислорода тканям и сохранить углекислоту, является способность повышенного образования у них метаболита глюкозы – 2,3 дифосфоглицерата. Этот метаболит снижает сродство гемоглобина к кислороду. Предметом интенсивных физиологических исследований как в эксперименте, так и в различных природно-климатических и производственных условиях является изучение функционального взаимодействия систем регуляции дыхания и кровообращения. Обе системы имеют общие рефлексогенные зоны в сосудах, которые посылают афферентные сигналы к специализированным нейронам основного чувствительного ядра продолговатого мозга – ядра одиночного пучка. Здесь же в непосредственной близости находятся дорсальное ядро дыхательного центра и сосудодвигательный центр. Особо следует отметить, что легкие являются единственным органом, куда поступает весь минутный объем крови. Это обеспечивает не только газотранспортную функцию, но и роль своеобразного фильтра, который определяет состав биологически активных веществ в крови и их метаболизм.
Предметом интенсивных физиологических исследований как в эксперименте, так и в различных природно-климатических и производственных условиях является изучение функционального взаимодействия систем регуляции дыхания и кровообращения. Обе системы имеют общие рефлексогенные зоны в сосудах, которые посылают афферентные сигналы к специализированным нейронам основного чувствительного ядра продолговатого мозга – ядра одиночного пучка. Здесь же в непосредственной близости находятся дорсальное ядро дыхательного центра и сосудодвигательный центр. Особо следует отметить, что легкие являются единственным органом, куда поступает весь минутный объем крови. Это обеспечивает не только газотранспортную функцию, но и роль своеобразного фильтра, который определяет состав биологически активных веществ в крови и их метаболизм.
Дыхание при высоком атмосферном давлении
Во время водолазных и кессонных работ человек находится под давлением выше атмосферного на 1 атм на каждые 10 м погружения. В этих условиях увеличивается количество газов, растворенных в крови, и особенно азота. При быстром подъеме водолаза на поверхность физически растворенные в крови и тканях газы не успевают выделиться из организма и образуют пузырьки – кровь «закипает». Кислород и углекислый газ быстро связываются кровью и тканями. Особую опасность представляют пузырьки азота, которые разносятся кровью и закупоривают мелкие сосуды (газовая эмболия), что сопровождается тяжелыми повреждениями ЦНС, органов зрения, слуха, сильными болями в мышцах и в области суставов, потерей сознания. Такое состояние, возникающее при быстрой декомпрессии, называется кессонной болезнью. Пострадавшего необходимо вновь поместить в среду с высоким давлением, а затем постепенно производить декомпрессию. Вероятность возникновения кессонной болезни может быть значительно снижена при дыхании специальными газовыми смесями, например гелиево-кислородной. Гелий почти нерастворим в крови, он быстрее диффундирует из тканей.Патологические типы дыхания
Паттерн дыхания существенно меняется при нарушении функции структур мозга, участвующих в регуляции процесса дыхания, а также в условиях гипоксии, гиперкапнии и при их сочетании (рис. 24). 1. Эйпноэ. 2. Гиперпноэ 3. Апноэ 4. Дыхание Чейна-Стокса 5. Дыхание Биота 6. Апнейзис 7. ГаспингРазличают несколько типов патологического дыхания. Гаспинг, или терминальное редкое дыхание, которое проявляется судорожными вдохами-выдохами. Оно возникает при резкой гипоксии мозга или в период агонии.
 Атактическое дыхание, т. е. неравномерное, хаотическое, нерегулярное дыхание. Наблюдается при сохранении дыхательных нейронов продолговатого мозга, но при нарушении связи с дыхательными нейронами варолиева моста.
Апнейстическое дыхание. Апнейзис – нарушение процесса смены вдоха на выдох: длительный вдох, короткий выдох и снова – длительный вдох.
Дыхание типа Чейна – Стокса: постепенно возрастает амплитуда дыхательных движений, потом сходит на нет и после паузы (апноэ) вновь постепенно возрастает. Возникает при нарушении работы дыхательных нейронов продолговатого мозга, часто наблюдается во время сна, а также при гипокапнии.
Дыхание Биота проявляется в том, что между нормальными дыхательными циклами «вдох-выдох» возникают длительные паузы – до 30 с. Такое дыхание развивается при повреждении дыхательных нейронов варолиева моста, но может появиться в горных условиях во время сна в период адаптации.
При дыхательной апраксии больной не способен произвольно менять ритм и глубину дыхания, но обычный паттерн дыхания у него не нарушен. Это наблюдается при поражении нейронов лобных долей мозга.
При нейрогенной гипервентиляции дыхание частое и глубокое. Возникает при стрессе, физической работе, а также при нарушениях структур среднего мозга.
Все виды паттернов дыхания, в том числе и патологические, возникают при изменении работы дыхательных нейронов продолговатого мозга и варолиева моста. Наряду с этим могут развиваться вторичные изменения дыхания, связанные с различной патологией или воздействием на организм экстремальных факторов внешней среды. Например, застой крови в малом круге кровообращения, гипертензия малого круга или амнезия вызывают учащение дыхания (тахипноэ). Дыхание типа Чейна -Стокса часто развивается при сердечной недостаточности. Метаболический ацидоз, как правило, вызывает брадипноэ.
Атактическое дыхание, т. е. неравномерное, хаотическое, нерегулярное дыхание. Наблюдается при сохранении дыхательных нейронов продолговатого мозга, но при нарушении связи с дыхательными нейронами варолиева моста.
Апнейстическое дыхание. Апнейзис – нарушение процесса смены вдоха на выдох: длительный вдох, короткий выдох и снова – длительный вдох.
Дыхание типа Чейна – Стокса: постепенно возрастает амплитуда дыхательных движений, потом сходит на нет и после паузы (апноэ) вновь постепенно возрастает. Возникает при нарушении работы дыхательных нейронов продолговатого мозга, часто наблюдается во время сна, а также при гипокапнии.
Дыхание Биота проявляется в том, что между нормальными дыхательными циклами «вдох-выдох» возникают длительные паузы – до 30 с. Такое дыхание развивается при повреждении дыхательных нейронов варолиева моста, но может появиться в горных условиях во время сна в период адаптации.
При дыхательной апраксии больной не способен произвольно менять ритм и глубину дыхания, но обычный паттерн дыхания у него не нарушен. Это наблюдается при поражении нейронов лобных долей мозга.
При нейрогенной гипервентиляции дыхание частое и глубокое. Возникает при стрессе, физической работе, а также при нарушениях структур среднего мозга.
Все виды паттернов дыхания, в том числе и патологические, возникают при изменении работы дыхательных нейронов продолговатого мозга и варолиева моста. Наряду с этим могут развиваться вторичные изменения дыхания, связанные с различной патологией или воздействием на организм экстремальных факторов внешней среды. Например, застой крови в малом круге кровообращения, гипертензия малого круга или амнезия вызывают учащение дыхания (тахипноэ). Дыхание типа Чейна -Стокса часто развивается при сердечной недостаточности. Метаболический ацидоз, как правило, вызывает брадипноэ.
Негазообменные функции воздухоносных путей и легких
Воздухоносные пути: полость носа, носоглотка, гортань, трахея, бронхи помимо газотранспортной выполняют целый ряд других функций. В них происходит согревание, увлажнение, очищение воздуха, регуляция его объема за счет способности мелких бронхов изменять свой просвет, а также рецепция вкусовых и обонятельных раздражителей. Эндотелиальные клетки слизистой оболочки полости носа выбрасывают за сутки до 500 – 600 мл секрета. Этот секрет участвует в выведении из дыхательных путей инородных частиц и способствует увлажнению вдыхаемого воздуха. Слизистая оболочка трахеи и бронхов продуцирует в сутки до 100 – 150 мл секрета. Их выведение осуществляется реснитчатым эпителием трахеи и бронхов. Каждая клетка мерцательного эпителия имеет около 200 ресничек, которые совершают координированные колебательные движения частотой 800- 1000 в 1 минуту. Наибольшая частота колебаний ресничек наблюдается при температуре 37°С, снижение температуры вызывает угнетение их двигательной активности. Вдыхание табачного дыма и других газообразных наркотических и токсических веществ вызывает торможение активности мерцательного эпителия. Слизистая оболочка трахеи выделяет такие биологически активные вещества, как пептиды, серотонин, дофамин, норадреналин. Альвеолоциты 1-го порядка вырабатывают поверхностно-активное стабилизирующее вещество сурфактант, о котором упоминалось выше. Снижение продукции сурфактанта приводит к ателектазу – спадению стенок альвеол и выключению определенной доли легкого из газообмена. Подобные нарушения системы дыхания возникают при изменении микроциркуляции и питания легкого, курении, воспалении и отеке, при гипероксии, длительном применении жирорастворимых анестетиков, продолжительной искусственной вентиляции легких и ингаляции чистого кислорода. Нарушения секреторной функции бронхиальных желез и М-холинорецепторов бронхиальной мускулатуры приводит к бронхоспазму, связанному с повышением тонуса кольцевой мускулатуры бронхов и активным выделением жидкого секрета бронхиальных желез, затрудняющему поступление воздуха в легкие. При раздражении Р2-адренорецепторов, например, адреналином, а не норадреналином, взаимодействующим с отсутствующими в мускулатуре бронхов α-адренорецепторами, возникает снижение тонуса бронхов и их расширение. Легкие выполняют фильтрационно-защитную функцию. Аль-веолярные макрофаги фагоцитируют попавшие к ним пылевые частицы, микроорганизмы и вирусы. В бронхиальной слизи содержатся также лизоцим, интерферон, протеазы, иммуноглобулин и другие компоненты. Легкие являются не только механическим фильтром, очищающим кровь от разрушенных клеток, сгустков фибрина и других частиц, но и метаболизируют их с помощью своей ферментативной системы. Легочная ткань принимает участие в липидном и белковом обмене, синтезируя фосфолипиды и глицерин и окисляя своими липопротеазами эмульгированные жиры, жирные кислоты и глицериды до углекислого газа с выделением большого количества энергии. Легкие синтезируют белки, входящие в состав сурфактанта. В легких синтезируются вещества, относящиеся к свертывающей (тромбопластин) и противосвертывающей (гепарин) системам. Гепарин, растворяя тромбы, способствует свободному кровообращению в легких. Легкие принимают участие в водно-солевом обмене, удаляя за сутки 500 мл воды. В то же время легкие могут поглощать воду, которая поступает из альвеол в легочные капилляры. Вместе с водой легкие способны пропускать крупномолекулярные вещества, например, лекарственные препараты, которые вводятся непосредственно в легкие в виде аэрозолей или жидкостей через интубационную трубку. В легких подвергаются биотрансформации, инактивации, детоксикации, ферментативному расщеплению и концентрации различные биологически активные вещества и лекарственные препараты, которые затем выводятся из организма. Так, в легких подвергаются инактивации: ацетилхолин, норадреналин, серотонин, брадикинин, простагландины Е1, Е2, F. Ангиотензин I превращается в легких в ангиотензин II.Фармакологическая коррекция патологии органов дыхания
Для восстановления функций дыхательной системы используют стимуляторы дыхания, которые подразделяют на три группы: 1. средства, непосредственно активирующие центр дыхания (коразол, кофеин, этимизол); 2. средства, стимулирующие дыхание рефлекторно, через Н-холинорецепторы синокаротидной зоны (цититон, лобелин и др.); 3. средства смешанного типа действия (СО2, кордиамин), у которых центральный эффект дополняется стимулирующим влиянием на хеморецепторы синокаротидной зоны.Стимуляторы дыхания применяют при отравлении наркотическими средствами, большими дозами анальгетиков, окисью углерода, при асфиксии новорожденных и для восстановления легочной вентиляции в посленаркозном периоде.
Противокашлевые средства делятся на две группы: 1. средства центрального действия 2. средства периферического действия.
К первой группе относятся препараты кодеин, диолан. Они угнетают центр кашля в продолговатом мозге. В связи с развитием привыкания и лекарственной зависимости использование препаратов данной группы в настоящее время ограничено. Во вторую группу входят либексин, действующий как анестетик слизистой оболочки верхних дыхательных путей, и бронхолитики.
Группа отхаркивающих средств, т. е. способствующих удалению мокроты из легочных путей при различных бронхолегочных заболеваниях, делится на две подгруппы: 1. стимулирующие от-харкивание (секретомоторные); 2. муколитические (бронхосекретолитические).
Секретомоторные препараты усиливают активность мерцательного эпителия и перистальтические движения бронхиол, способствуя продвижению и выведению мокроты из нижних отделов дыхательных путей. Их также условно делят на средства рефлекторного действия (препараты термопсиса, истода, алтея, терпингидрат), которые раздражают рецепторы слизистой желудка и через центральную нервную систему рефлекторно влияют на бронхи и бронхиальные железы, а также средства резорбтивного действия (йодид натрия и калия, натрия гидрокарбонат и др.). Последние стимулируют бронхиальные железы и вызывают непосредственное разжижение (дегидратацию) мокроты. Действие группы муколитических препаратов (бромгексин, амброксол) основано на активации ферментов, способных разрывать дисульфидные связи кислых мукополисахаридов геля мокроты, а также на их специфической способности стимулировать выработку сурфактанта, регулирующего реологические свойства бронхолегочного секрета и облегчающего его выведение из дыхательных путей. В настоящее время стали применять искусственные поверхностно-активные вещества, замещающие природный сурфактант при заболеваниях легких, дефиците сурфактанта у новорожденных. К ним относится альвеофакт, полученный из легких крупного рогатого скота. Бронхолитические средства используют для профилактики и устранения бронхоспазма (например, при бронхиальной астме).
К этим веществам относятся: 1. β2-адреномиметики; 2. М-холиноблокаторы; 3. спазмолитики миотропного действия; 4. блокаторы а-адренергических рецепторов: фентоламин, пирроксан; 5. простагландины группы Е.
Из группы β2-адреномиметиков наибольшей активностью обладает изадрин, стимулирующий β2-адренорецепторы бронхов и устраняющий бронхоспазм. β2-Адренорецепторы бронхиол возбуждает сальбутамол. Для купирования приступов бронхиальной астмы широко используют адреналин, влияющий на α и β (β1- и β2)-адренорецепторы, но он действует непродолжительно. Менее активен, но действует более пролонгирование эфедрин (аи радреномиметик) и его производные – теофедрин, солутан и др. Бронхолитическими свойствами обладают М-холиноблокаторы (атропин и платифиллин). Из миотропных спазмолитиков, действующих непосредственно на гладкую мускулатуру бронхов, используют эуфиллин, теофиллин, оказывающие бронхолитическое действие.
Глава 9. Пищеварение
Для нормальной жизнедеятельности организму необходим пластический и энергетический материал. Эти вещества поступают в организм с пищей. Но только минеральные соли, вода и витамины усваиваются человеком в том виде, в котором они находятся в пище. Белки, жиры и углеводы попадают в организм в виде сложных комплексов, и для того чтобы всосаться и подвергнуться усвоению, требуется сложная физическая и химическая переработка пищи. При этом компоненты пищи должны утратить свою видовую специфичность, иначе они будут приняты системой иммунитета как чужеродные вещества. Для этих целей и служит система пищеварения. Пищеварение – совокупность физических, химических и физиологических процессов, обеспечивающих обработку и превращение пищевых продуктов в простые химические соединения, способные усваиваться клетками организма. Эти процессы идут в определенной последовательности во всех отделах пищеварительного тракта (полости рта, глотке, пищеводе, желудке, тонкой и толстой кишке с участием печени и желчного пузыря, поджелудочной железы), что обеспечивается регуляторными механизмами различного уровня. Последовательная цепь процессов, приводящая к расщеплению пищевых веществ до мономеров, способных всасываться, носит название пищеварительного конвейера. В зависимости от происхождения гидролитических ферментов пищеварение делят на 3 типа: собственное, симбионтное и аутолитическое. Собственное пищеварение осуществляется ферментами, синтезированными железами человека или животного. Симбионтное пищеварение происходит под влиянием ферментов, синтезированных симбионтами макроорганизма (микроорганизмами) пищеварительного тракта. Так происходит переваривание клетчатки пищи в толстой кишке. Аутолитическое пищеварение осуществляется под влиянием ферментов, содержащихся в составе принимаемой пищи. Материнское молоко содержит ферменты, необходимые для его створаживания. В зависимости от локализации процесса гидролиза питательных веществ различают внутриклеточное и внеклеточное пищеварение. Внутриклеточное пищеварение представляет собой процесс гидролиза веществ внутри клетки клеточными (лизосомальными) ферментами. Вещества поступают в клетку путем фагоцитоза и пиноцитоза. Внутриклеточное пищеварение характерно для простейших животных. У человека внутриклеточное пищеварение встречается в лейкоцитах и клетках лимфо-ретикулогистиоцитарной системы. У высших животных и человека пищеварение осуществляется внеклеточно. Внеклеточное пищеварение делят на дистантное (полостное) и контактное (пристеночное, или мембранное). Дистантное (полостное) пищеварение осуществляется с помощью ферментов пищеварительных секретов в полостях желудочно-кишечного тракта на расстоянии от места образования этих ферментов. Контактное (пристеночное, или мембранное) пищеварение (A. M. Уголев) происходит в тонкой кишке в зоне гликокаликса, на поверхности микроворсинок с участием ферментов, фиксированных на клеточной мембране и заканчивается всасыванием – транспортом питательных веществ через энтероцит в кровь или лимфу.Функции желудочно-кишечного тракта
Секреторная функция связана с выработкой железистыми клетками пищеварительных соков: слюны, желудочного, поджелудочного, кишечного соков и желчи. Двигательная, или моторная, функция осуществляется мускулатурой пищеварительного аппарата на всех этапах процесса пищеварения и заключается в жевании, глотании, перемешивании и передвижении пищи по пищеварительному тракту и удалении из организма непереваренных остатков. К моторике также относятся движения ворсинок и микроворсинок. Всасывательная функция осуществляется слизистой оболочкой желудочно-кишечного тракта. Из полости органа в кровь или лимфу поступают продукты расщепления белков, жиров, углеводов (аминокислоты, глицерин и жирные кислоты, моносахариды), вода, соли, лекарственные вещества. Инкреторная, или внутрисекреторная, функция заключается в выработке ряда гормонов, оказывающих регулирующее влияние на моторную, секреторную и всасывательную функции желудочно-кишечного тракта. Это гастрин, секретин, холецистокинин-панкреозимин, мотилин и др. Экскреторная функция обеспечивается выделением пищеварительными железами в полость желудочно-кишечного тракта продуктов обмена (мочевина, аммиак, желчные пигменты), воды, солей тяжелых металлов, лекарственных веществ, которые затем удаляются из организма. Органы желудочно-кишечного тракта выполняют и ряд других непищеварительных функций, например, участие в водно-солевом обмене, в реакциях местного иммунитета, гемопоэзе, фибринолизе и т. д.Общие принципы регуляциипроцессов пищеварения
Функционирование пищеварительной системы, сопряжение моторики, секреции и всасывания регулируются сложной системой нервных и гуморальных механизмов. Выделяют три основных механизма регуляции пищеварительного аппарата: центральный рефлекторный, гуморальный и локальный, т. е. местный. Значимость этих механизмов в различных отделах пищеварительного тракта не одинакова. Центральные рефлекторные влияния (условно-рефлекторные и безусловно-рефлекторные) в большей мере выражены в верхней части пищеварительного тракта. По мере удаления от ротовой полости их участие снижается, однако возрастает роль гуморальных механизмов. Особо выражено это влияние на деятельность желудка, двенадцатиперстной кишки, поджелудочной железы, желчеобразование и желчевыведение. В тонкой и особенно толстой кишке проявляются преимущественно локальные механизмы регуляции (механические и химические раздражения). Пища оказывает активирующее воздействие на секрецию и моторику пищеварительного аппарата непосредственно в месте действия и в каудальном направлении. В краниальном направлении она, напротив, вызывает торможение. Афферентная импульсация поступает от механо-, хемо-, осмо- и терморецепторов, находящихся в стенке пищеварительного тракта к нейронам интра- и экстрамуральных ганглиев, спинного и головного мозга. Из этих нейронов по эфферентным вегетативным волокнам импульсы следуют в органы пищеварительной системы к клеткам-эффекторам: гландулоцитам, миоцитам, энтероцитам. Регуляция процессов пищеварения осуществляется симпатическим, парасимпатическим и внутриорганным отделами вегетативной нервной системы. Внутриорганный отдел представлен рядом нервных сплетений, из которых наибольшее значение в регуляции функций желудочно-кишечного тракта имеют межмышечное (ауэрбаховское) и подслизистое (мейснеровское) сплетения. С их помощью осуществляются местные рефлексы, замыкающиеся на уровне интрамуральных ганглиев. В симпатических преганглионарных нейронах выделяются ацетилхолин, энкефалин, нейротензин; в постсинаптических – норадреналин, ацетилхолин, ВИП, в парасимпатических преганглионарных нейронах – ацетилхолин и энкефалин; постганглионарных – ацетилхолин, энкефалин, ВИП. В качестве медиаторов в желудке и кишечнике выступают также гастрин, соматостатин, субстанция Р, холецистокинин. Основными возбуждающими моторику и секрецию желудочно-кишечного тракта нейронами являются холинергические, тормозными – адренергические. Большую роль в гуморальной регуляции пищеварительными функциями играют гастроинтестинальные гормоны. Эти вещества продуцируются эндокринными клетками слизистой оболочки желудка, двенадцатиперстной кишки, поджелудочной железы и представляют собой пептиды и амины. По общему для всех этих клеток свойству поглощать аминный предшественник и карбоксилировать его эти клетки объединены в АПУД-систему. Гастроинтестинальные гормоны оказывают регуляторные влияния на клетки-мишени различными способами: эндокринным (доставляются к органам-мишеням общим и региональным кровотоком) и паракринным (диффундируют через интерстициальную ткань к рядом или близко расположенной клетке). Некоторые из этих веществ продуцируются нервными клетками и играют роль нейротрансмиттеров. Гастроинтестинальные гормоны участвуют в регуляции секреции, моторики, всасывания, трофики, высвобождения других регуляторных пептидов, а также оказывают общие эффекты: изменения в обмене веществ, деятельности сердечно-сосудистой и эндокринной систем, пищевом поведении (табл.2).Таблица 2. Эндокриннные пептиды в ЖКТ
| Гормон | Место образования | Эффекты |
|---|---|---|
| Гастрин | Антральный отдел желудка и проксимальный отдел тонкой кишки (G-клетки) | Усиление секреции соляной кислоты и пепсиногена желудком и сока поджелудочной железы. Стимуляция моторики желудка, тонкой и толстой кишки, желчного пузыря |
| Гастрон | Антральный отдел желудка (G-клетки) | Торможение секреции желудочного сока |
| Бульбогасгрон | Антральный отдел желудка (G-клетки) | Торможение секреции и моторики желудка |
| Энтерогастрон | Проксимальный отдел тонкой кишки (ЕСl-клетки) | Торможение секреции и моторики желудка |
| Секретин | Тонкая кишка, преимущественно в проксимальном отделе (S-клетки) | Увеличение секреции бикарбонатов поджелудочной железой, торможение секреции соляной кислоты в желудке, усиление желчеобразования и секвеции тонкой кишки. Торможение моторики желудка, усиление моторики кишечника и сокращения пилорического сфинктера |
| Холецистокинин-панкреозимин (ХЦК-ПЗ) | Тонкая кишка, преимущественно проксимальный отдел (I-клетки) | Усиление моторики желчного пузыря и секреции ферментов поджелудочной железой, торможение секреции соляной кислоты в желудке и его моторики, усиление секреции пепсиногена, стимуляция моторики тонкой и толстой кишки, расслабление сфинктера Одди, Угнетение аппетита |
| Гастроингибирующий (или желудочный ингибирующий) пептид (ГИП или ЖИП) | Тонкая кишка (К-клетки) | Глюкозозависимое усиление высвобождения поджелудочной железой инсулина. Уменьшение секреции и моторики желудка путем торможения высвобождения гастрина. Стимуляция секреции кишечного сока, угнетение всасывания электролитов в тонкой кишке |
| Бомбезин | Желудок и проксимальный отдел тонкой кишки (Р-клетки) | Стимуляция секреции желудка путем усиления высвобождения гастрина. Усиление сокращений желчного пузыря, секреции ферментов поджелудочной железой путем стимуляции высвобождения ХЦК-ПЗ, усиление высвобождения энтероглюкагопа, пейротепзипа и ПП |
| Соматостатин | Желудок, тонкая кишка, преимущественно проксимальный отдел, (D-клетки) поджелудочная железа | Торможение выделения секретина, ГИПа, мотилина, гастрина, инсулина и глюкагона |
| Мотилин | Тонкая кишка, преимущественно проксимальный отдел (ЕС2-клетки) | Усиление моторики желудка и тонкой кишки, усиление секреции пепсиногена желудком |
| Панкреатический пептид (ПП) | Поджелудочная железа (ПП-клетки) | Антагонист ХЦК-ПЗ. Уменьшение секреции ферментов и бикарбонатов поджелудочной железой, усиление пролиферации слизистой оболочки тонкой кишки, поджелудочной железы и печени, усиление моторики желудка. Участие в обмене углеводов и липидов |
| Гистамин | Желудочно-кишечныйтракт (ECL-клетки) | Стимуляция секреции соляной кислоты желудком, сокаподжелудочной железы. Усиление моторики желудка и кишечника. Расширение кровеносных капилляров |
| Нейротензин | Тонкая кишка, преимущественно дистальный отдел (N-клетки) | Уменьшение секреции соляной кислоты желудком, усиление секреции поджелудочной железы |
| Субстанция Р | Тонкая кишка (ЕСl-клетки) | Усиление моторики кишечника, слюноотделения, торможение высвобождения инсулина и всасывания натрия |
| Вилликинин | Проксимальный отделтонкой кишки (ЕСl-клетки) | Стимуляция сокращений ворсинок топкой кишки |
| Энкефалин | Тонкая кишка, немного в поджелудочной железе (G-клетки) | Торможение секреции ферментов поджелудочной железой |
| Энтероглюкагон | Тонкая кишка (ЕСl-клетки) | Мобилизация углеводов. Торможение секреции желудка и поджелудочной железы, моторики желудка и кишечника. Пролиферация слизистой оболочки тонкой кишки (индукция гликогенолиза, липолиза, глюконеогенеза и кетогенеза |
| Серотонин | Желудочно-кишечный тракт (ЕС1, ЕС2-клетки) | Торможение выделения соляной кислоты в желудке, стимуляция выделения пепсина. Стимуляция секреции поджелудочпой железы, желчевыделения, кишечной секреции |
| Вазоактивный интестинальный пептид (ВИП) | Желудочно-кишечный тракт (Д1-клетки) | Расслабление гладких мышц кровеносных сосудов, желчного пузыря, сфинктеров. Торможение секреции желудка, усиление секреции бикарбонатов поджелудочной железой и кишечной секреции. Торможение дейсгвия ХЦК-ПЗ |
Пищеварение в полости рта
Пищеварение начинается в ротовой полости, где происходит механическая и химическая обработка пищи. Механическая обработка заключается в измельчении пищи, смачивании ее слюной и формировании пищевого комка. Химическая обработка происходит за счет ферментов, содержащихся в слюне. В полость рта впадают протоки трех пар крупных слюнных желез: околоушных, подчелюстных, подъязычных и множества мелких желез, находящихся на поверхности языка и в слизистой оболочке нёба и щек. Околоушные железы и железы, расположенные на боковых поверхностях языка, – серозные (белковые). Их секрет содержит много воды, белка и солей. Железы, расположенные на корне языка, твердом и мягком нёбе, относятся к слизистым слюнным железам, секрет которых содержит много муцина. Подчелюстные и подъязычные железы являются смешанными.Состав и свойства слюны
Слюна, находящаяся в ротовой полости, является смешанной. Ее рН равна 6,8–7,4. У взрослого человека за сутки образуется 0,5–2 л слюны. Она состоит из 99% воды и 1% сухого остатка. Сухой остаток представлен органическими и неорганическими веществами. Среди неорганических веществ – анионы хлоридов, бикарбонатов, сульфатов, фосфатов; катионы натрия, калия, кальция магния, а также микроэлементы: железо, медь, никель и др. Органические вещества слюны представлены в основном белками. Белковое слизистое вещество муцин склеивает отдельные частицы пищи и формирует пищевой комок. Основными ферментами слюны являются амилаза и мальтаза, которые действуют только в слабощелочной среде. Амилаза расщепляет полисахариды (крахмал, гликоген) до мальтозы (дисахарида). Мальтаза действует на мальтозу и расщепляет ее до глюкозы. В слюне в небольших количествах обнаружены также и другие ферменты: гидролазы, оксиредуктазы, трансферазы, протеазы, пептидазы, кислая и щелочная фосфатазы. В слюне содержится белковое вещество лизоцим (мурамидаза), обладающее бактерицидным действием. Пища находится в полости рта всего около 15 секунд, поэтому здесь не происходит полного расщепления крахмала. Но пищеварение в ротовой полости имеет очень большое значение, так как является пусковым механизмом для функционирования желудочно-кишечного тракта и дальнейшего расщепления пищи.Функции слюны
Слюна выполняет указанные ниже функции. Пищеварительная функция – о ней было сказано выше.Экскреторная функция.
В составе слюны могут выделяться некоторые продукты обмена, такие как мочевина, мочевая кислота, лекарственные вещества (хинин, стрихнин), а также вещества, поступившие в организм (соли ртути, свинца, алкоголь).Защитная функция.
Слюна обладает бактерицидным действием благодаря содержанию лизоцима. Муцин способен нейтрализовать кислоты и щелочи. В слюне находится большое количество иммуноглобулинов, что защищает организм от патогенной микрофлоры. В слюне обнаружены вещества, относящиеся к системе свертывания крови: факторы свертывания крови, обеспечивающие местный гемостаз; вещества, препятствующие свертыванию крови и обладающие фибринолитической активностью; вещество, стабилизирующее фибрин. Слюна защищает слизистую оболочку полости рта от пересыхания.Трофическая функция.
Слюна является источником кальция, фосфора, цинка для формирования эмали зуба.Регуляция слюноотделения
При поступлении пищи в ротовую полость происходит раздражение механо-, термо- и хеморецепторов слизистой оболочки. Возбуждение от этих рецепторов по чувствительным волокнам язычного (ветвь тройничного нерва) и языкоглоточного нервов, барабанной струны (ветвь лицевого нерва) и верхнегортанного нерва (ветвь блуждающего нерва) поступает в центр слюноотделения в продолговатом мозге. От слюноотделительного центра по эфферентным волокнам возбуждение доходит до слюнных желез и железы начинают выделять слюну. Эфферентный путь представлен парасимпатическими и симпатическими волокнами. Парасимпатическая иннервация слюнных желез осуществляется волокнами языкоглоточного нерва и барабанной струны, симпатическая иннервация – волокнами, отходящими от верхнего шейного симпатического узла. Тела преганглионарных нейронов находятся в боковых рогах спинного мозга на уровне II-IV грудных сегментов. Ацетилхолин, выделяющийся при раздражении парасимпатических волокон, иннервирующих слюнные железы, приводит к отделению большого количества жидкой слюны, которая содержит много солей и мало органических веществ. Норадреналин, выделяющийся при раздражении симпатических волокон, вызывает отделение небольшого количества густой, вязкой слюны, которая содержит мало солей и много органических веществ. Такое же действие оказывает адреналин. Субстанция Р стимулирует секрецию слюны. СО2 усиливает слюнообразование. Болевые раздражения, отрицательные эмоции, умственное напряжение тормозят секрецию слюны. Слюноотделение осуществляется не только с помощью безусловных, но и условных рефлексов. Вид и запах пищи, звуки, связанные с приготовлением пищи, а также другие раздражители, если они раньше совпадали с приемом пищи, разговор и воспоминание о пище вызывают условно-рефлекторное слюноотделение. Качество и количество отделяемой слюны зависят от особенностей пищевого рациона. Например, при приеме воды слюна почти не отделяется. В слюне, выделяющейся на пищевые вещества, содержится значительное количество ферментов, она богата муцином. При попадании в ротовую полость несъедобных, отвергаемых веществ выделяется жидкая и обильная слюна, бедная органическими соединениями.Пищеварение в желудке
Пища из ротовой полости поступает в желудок, где она подвергается дальнейшей химической и механической обработке. Кроме того, желудок является пищевым депо. Механическая обработка пищи обеспечивается моторной деятельностью желудка, химическая осуществляется за счет ферментов желудочного сока. Размельченные и химически обработанные пищевые массы в смеси с желудочным соком образуют жидкий или полужидкий химус. Желудок выполняет следующие функции: секреторную, моторную, всасывательную (эти функции будут описаны ниже), экскреторную (выделение мочевины, мочевой кислоты, креатипина, солей тяжелых металлов, йода, лекарственных веществ), инкреторную (образование гормонов гастрина и гистамина), гомеостатическую (регуляция рН), участие в гемопоэзе (выработка внутреннего фактора Касла).Секреторная функция желудка
Секреторная функция желудка обеспечивается железами, находящимися в его слизистой оболочке. Различают три вида желез: кардиальные, фундальные (собственные железы желудка) и пилорические (железы привратника). Железы состоят из главных, париетальных (обкладочных), добавочных клеток и мукоцитов. Главные клетки вырабатывают пепсиногены, париетальные – соляную кислоту, добавочные и мукоциты – мукоидный секрет. Фундальные железы содержат все три типа клеток. Поэтому в состав сока фундального отдела желудка входят ферменты и много соляной кислоты и именно этот сок играет ведущую роль в желудочном пищеварении.Состав и свойства желудочного сока
У взрослого человека в течение суток образуется и выделяется около 2 – 2,5 л желудочного сока. Желудочный сок имеет кислую реакцию (рН 1,5- 1,8). В его состав входят вода – 99% и сухой остаток – 1%. Сухой остаток представлен органическими и неорганическими веществами. Главный неорганический компонент желудочного сока – соляная кислота, которая находится в свободном и связанном с протеинами состоянии.Соляная кислота выполняет ряд функций: 1. способствует денатурации и набуханию белков в желудке, что облегчает их последующее расщепление пепсинами; 2. активирует пепсиногены и превращает их в пепсины; 3. создает кислую среду, необходимую для действия ферментов желудочного сока; 4. обеспечивает антибактериальное действие желудочного сока; 5. способствует нормальной эвакуации пищи из желудка: открытию пилорического сфинктера со стороны желудка и закрытию со стороны 12-перстной кишки; 6. возбуждает панкреатическую секрецию.
Кроме того, в желудочном соке содержатся следующие неорганические вещества: хлориды, бикарбонаты, сульфаты, фосфаты, натрий, калий, кальций, магний и др. В состав органических веществ входят протеолитические ферменты, главную роль среди которых играют пепсины. Пепсины выделяются в неактивной форме в виде пепсиногенов. Под влиянием соляной кислоты они активируются. Оптимум протеазной активности находится при рН 1,5–2,0. Они расщепляют белки до альбумоз и пептонов. Гастриксин гидролизует белки при рН 3,2–3,5. Реннин (химозин) вызывает створаживание молока в присутствии ионов кальция, так как переводит растворимый белок казеиноген в нерастворимую форму – казеин. В желудочном соке имеются также и непротеолитические ферменты. Желудочная липаза мало активна и расщепляет только эмульгированные жиры. В желудке продолжается гидролиз углеводов под влиянием ферментов слюны. Это становится возможным потому, что пищевой комок, попавший в желудок, пропитывается кислым желудочным соком постепенно. И в это время во внутренних слоях пищевого комка в щелочной среде продолжается действие ферментов слюны. В состав органических веществ входит лизоцим, обеспечивающий бактерицидные свойства желудочного сока. Желудочная слизь, содержащая муцин, защищает слизистую оболочку желудка от механических и химических раздражений и от самопереваривания. В желудке вырабатывается гастромукопротеид, или внутренний фактор Касла. Только при наличии внутреннего фактора возможно образование комплекса с витамином В12, участвующего в эритропоэзе. В желудочном соке содержатся также аминокислоты, мочевина, мочевая кислота.
Регуляция желудочной секреции
Железы желудка вне процесса пищеварения выделяют только слизь и пилорический сок. Отделение желудочного сока начинается при виде, запахе пищи, поступлении ее в ротовую полость. Процесс желудочного сокоотделения можно разделить на несколько фаз: сложно-рефлекторную (мозговую), желудочную и кишечную. Сложно-рефлекторная (мозговая) фаза включает условно-рефлекторный и безусловно-рефлекторный механизмы. Условно-рефлекторное отделение желудочного сока происходит при раз-дражении обонятельных, зрительных, слуховых рецепторов (запах, вид пищи, звуковые раздражители, связанные с приготовлением пищи, разговорами о пище). В результате синтеза афферентных зрительных, слуховых и обонятельных раздражений в таламусе, гипоталамусе, лимбической системе и коре больших полушарий головного мозга повышается возбудимость нейронов пищеварительного бульбарного центра и создаются условия для запуска секреторной активности желудочных желез. Сок, выделяющийся при этом, И. П. Павлов назвал запальным, или аппетитным. Безусловно-рефлекторное желудочное сокоотделение начинается с момента попадания пищи в ротовую полость и связано с возбуждением рецепторов ротовой полости, глотки, пищевода. Импульсы по афферентным волокнам язычного (V пара черепномозговых нервов), языкоглоточного (IX пара) и верхнего гортанного (X пара) нервов поступают в центр желудочного сокоотделения в продолговатом мозге. От центра импульсы по эфферентным волокнам блуждающего нерва передаются к железам желудка, что приводит к усилению секреции. Сок, выделяющийся в первую фазу желудочной секреции, обладает большой протеолитической активностью и имеет большое значение для пищеварения, так как благодаря ему желудок оказывается заранее подготовленным к приему пищи. Торможение секреции желудочного сока происходит за счет раздражения эфферентных симпатических волокон, идущих из центров спинного мозга. Желудочная фаза секреции наступает с момента попадания пищи в желудок. Эта фаза реализуется за счет блуждающего нерва, внутриорганного отдела нервной системы и гуморальных факторов. Желудочная секреция в эту фазу обусловлена раздражением пищей рецепторов слизистой желудка, откуда импульсы передаются по афферентным волокнам блуждающего нерва в продолговатый мозг, а затем по эфферентным волокнам блуждающего нерва поступают к секреторным клеткам. Блуждающий нерв оказывает свое влияние на желудочную секрецию несколькими путями: прямой контакт с главными, обкладочными и добавочными клетками желудочных желез (возбуждение ацетилхолином Мхолинорецепторов), через внутриорганную нервную систему и через гуморальное звено, так как волокна блуждающего нерва иннервируют G-клетки пилорической части желудка, которые продуцируют гастрин. Гастрин повышает активность главных, но в большей степени обкладочных клеток. В то же время продукция гастрина увеличивается под влиянием экстрактивных веществ мяса, овощей, продуктов переваривания белков, бомбезина. Снижение рН в антральном отделе желудка уменьшает высвобождение гастрина. Под влиянием блуждающего нерва повышается также секреция гистамина ЕС2-клетками желудка. Гистамин, взаимодействуя с Н2-гистаминовыми рецепторами обкладочных клеток, повышает секрецию желудочного сока высокой кислотности с низким содержанием пепсинов. К числу химических веществ, способных оказывать непосредственное влияние на секрецию желез слизистой оболочки желудка, относятся экстрактивные вещества мяса, овощей, спирты, продукты расщепления белков (альбумозы и пептоны). Кишечная фаза секреции начинается при переходе химуса из желудка в кишечник. Химус воздействует на хемо-, осмо-, механорецепторы кишечника и рефлекторно изменяет интенсивность желудочной секреции. В зависимости от степени гидролиза пищевых веществ, в желудок поступают сигналы, повышающие желудочную секрецию или, наоборот, тормозящие. Стимуляция осуществляется за счет местных и центральных рефлексов и реализуется через блуждающий нерв, внутриорганную нервную систему и гуморальные факторы (выделение гастрина G-клетками двенадцатиперстной кишки). Эта фаза характеризуется длительным скрытым периодом, большой продолжительностью. Кислотность желудочного сока в этот период низкая. Торможение желудочной секреции происходит за счет выделения секретина, ХЦКПЗ, которые угнетают секрецию соляной кислоты, но усиливают секрецию пепсиногенов. Уменьшают продукцию соляной кислоты также глюкагон, ЖИП, ВИП, нейротензин, соматостатин, серотонин, бульбогастрон, продукты гидролиза жира.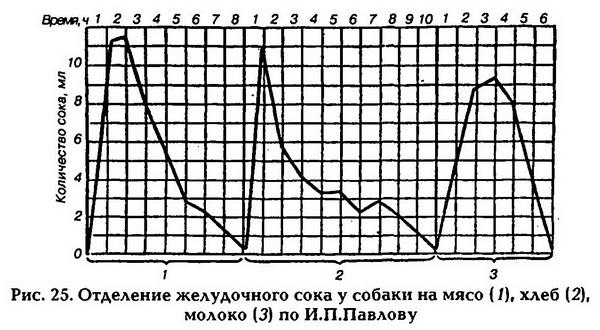 Продолжительность секреторного процесса, количество, переваривающая способность желудочного сока, его кислотность находятся в строгой зависимости от характера пищи, что обеспечивается нервными и гуморальными влияниями. Доказательством наличия такой зависимости являются классические опыты, проведенные в лаборатории И. П. Павлова на собаках с изолированным малым желудочком. Животные получали хлеб в качестве углеводной пищи, нежирное мясо, содержащее в основном белки, и молоко, в состав которого входят белки, жиры и углеводы. Самое большое количество желудочного сока вырабатывалось при употреблении мяса, среднее – хлеба, малое – молока (за счет содержащихся жиров). Длительность секреции сока также была различной: на хлеб – в течение 10 ч, на мясо – 8 ч, на молоко – 6 ч (рис. 25). Переваривающая сила сока убывала в следующем порядке: мясо, хлеб, молоко; кислотность: мясо, молоко, хлеб. Установлено также, что желудочный сок с высокой кислотностью лучше расщепляет белки животного происхождения, а с низкой кислотностью – растительного. Эти данные используются при назначении диеты у больных с гипо- и гиперсекрецией желудочных желез. Так, пациентам с гиперсекрецией рекомендуется молочная диета, с гипосекрецией – овощная и мясная с высоким содержанием экстрактивных веществ.
Продолжительность секреторного процесса, количество, переваривающая способность желудочного сока, его кислотность находятся в строгой зависимости от характера пищи, что обеспечивается нервными и гуморальными влияниями. Доказательством наличия такой зависимости являются классические опыты, проведенные в лаборатории И. П. Павлова на собаках с изолированным малым желудочком. Животные получали хлеб в качестве углеводной пищи, нежирное мясо, содержащее в основном белки, и молоко, в состав которого входят белки, жиры и углеводы. Самое большое количество желудочного сока вырабатывалось при употреблении мяса, среднее – хлеба, малое – молока (за счет содержащихся жиров). Длительность секреции сока также была различной: на хлеб – в течение 10 ч, на мясо – 8 ч, на молоко – 6 ч (рис. 25). Переваривающая сила сока убывала в следующем порядке: мясо, хлеб, молоко; кислотность: мясо, молоко, хлеб. Установлено также, что желудочный сок с высокой кислотностью лучше расщепляет белки животного происхождения, а с низкой кислотностью – растительного. Эти данные используются при назначении диеты у больных с гипо- и гиперсекрецией желудочных желез. Так, пациентам с гиперсекрецией рекомендуется молочная диета, с гипосекрецией – овощная и мясная с высоким содержанием экстрактивных веществ.
Пищеварение в тонкой кишке
В тонкой кишке происходят основные процессы переваривания пищевых веществ. Особенно велика роль ее начального отдела – двенадцатиперстной кишки. В процессе пищеварения здесь участвуют панкреатический, кишечный соки и желчь. С помощью ферментов, входящих в состав панкреатического и кишечного соков, происходит гидролиз белков, жиров и углеводов.Состав и свойства панкреатического сока
Внешнесекреторная деятельность поджелудочной железы заключается в образовании и выделении в двенадцатиперстную кишку 1,5 – 2,0 л панкреатического сока. В состав поджелудочного сока входят вода и сухой остаток (0,12%), который представлен неорганическими и органическими веществами. В соке содержатся катионы Na+, Са2+, К+, Мg2+ и анионы Сl-, SO32-, НРО42- Особенно много в нем бикарбонатов, благодаря которым рН сока равна 7,8–8,5. Ферменты поджелудочного сока активны в слабощелочной среде. Панкреатический сок представлен протеолитическими, липолитическими и амилолитическими ферментами, переваривающими белки, жиры, углеводы и нуклеиновые кислоты. Альфа-амилаза, липаза и нуклеаза секретируются в активном состоянии; протеазы – в виде проэнзимов. Альфа-амилаза поджелудочной железы расщепляет полисахариды до олиго-, ди- и моносахаридов. Нуклеиновые кислоты расщепляются рибои дезоксирибонуклеазами. Панкреатическая липаза, активная в присутствии солей желчных кислот, действует на липиды, расщепляя их до моноглицеридов и жирных кислот. На липиды действуют также фосфолипаза А и эстераза. В присутствии ионов кальция гидролиз жиров усиливается. Протеолитические ферменты секретируются в виде проэнзимов – трипсиногена, химотрипсиногена, прокарбоксипептидазы, проэластазы. Под влиянием энтерокиназы двенадцатиперстной кишки трипсиноген превращается в трипсин. Затем сам трипсин действует автокаталитически на оставшееся количество трипсиногена и на другие пропептидазы, превращая их в активные ферменты. Трипсин, химотрипсин, эластаза расщепляют премущественно внутренние пептидные связи белков пищи, в результате чего образуются низкомолекулярные пептиды и аминокислоты. Карбоксипептидазы А и В расщепляют С-концевые связи в белках и пептидах.Регуляция секреции поджелудочной железы
Регуляция поджелудочной экзокринной секреции осуществляется нервными и гуморальными механизмами. Блуждающий нерв усиливает секрецию поджелудочной железы. Симпатические нервы уменьшают количество секрета, но усиливают синтез органических веществ (бета-адренергический эффект). Снижение секреции происходит также и за счет уменьшения кровоснабжения поджелудочной железы путем сужения кровеносных сосудов (альфа-адренергический эффект). Напряженная физическая и умственная работа, боль, сон вызывают торможение секреции. Гастроинтестинальные гормоны, секретин и ХЦК-ПЗ усиливают секрецию поджелудочного сока. Секретин стимулирует выделение сока, богатого бикарбонатами, ХЦК-ПЗ – богатого ферментами. Секрецию поджелудочной железы усиливают гастрин, серотонин, бомбезин, инсулин, соли желчных кислот. Химоденин стимулирует секрецию химотрипсиногена. Тормозящее действие оказывают ЖИП, ПП, глюкагон, кальцитонин, соматостатин, энкефалин.Выделяют 3 фазы панкреатической секреции: 1. сложно-рефлекторную 2. желудочную 3. кишечную.
На отделение сока поджелудочной железы влияет характер принятой пищи. Эти влияния опосредованы через соответствующие гастроинтестинальные гормоны. Так, пищевые продукты, усиливающие секрецию соляной кислоты в желудке (экстрактивные вещества мяса, овощей, продукты переваривания белков), стимулируют выработку секретина, а значит, приводят к выделению поджелудочного сока, богатого бикарбонатами. Продукты начального гидролиза белков и жиров стимулируют секрецию ХЦК-ПЗ, который, в свою очередь, способствует выделению сока с большим количеством ферментов. Таким образом, при длительном преобладании в пищевом рационе только углеводов, или белков, или жиров происходит и соответствующее изменение ферментного состава панкреатического сока. Поджелудочная железа обладает и внутрисекреторной актив-ностью, продуцируя инсулин, глюкагон, соматостатин, панкреа-тический полипептид, серотонин, ВИП, гастрин, энкефалин, калликреин, липоксин и ваготонин.
Состав и свойства кишечного сока
Кишечный сок представляет собой секрет желез, расположенных в слизистой оболочке вдоль всей тонкой кишки (дуоденальных, или бруннеровых желез, кишечных крипт, или либеркюновых желез, кишечных эпителиоцитов, бокаловидных клеток, клеток Панета). У взрослого человека за сутки отделяется 2 – 3 л кишечного сока, рН от 7,2 до 9,0. Сок состоит из воды и сухого остатка, который представлен неорганическими и органическими веществами. Из неорганических веществ в соке содержится много бикарбонатов, хлоридов, фосфатов натрия, кальция, калия. В состав органических веществ входят белки, аминокислоты, слизь. В кишечном соке находится более 20 ферментов, обеспечивающих конечные стадии переваривания всех пищевых веществ. Это энтерокиназа, пептидазы, щелочная фосфатаза, нуклеаза, липаза, фосфолипаза, амилаза, лактаза, сахараза. Встречаются наследственные и приобретенные дефициты кишечных ферментов, расщепляющих углеводы (дисахаридаз), что приводит к непереносимости соответствующих дисахаридов. Например, у многих людей, особенно народов Азии и Африки, выявлена лактазная недостаточность. Основная часть ферментов поступает в кишечный сок при отторжении клеток слизистой оболочки кишки. Значительное количество ферментов адсорбируется на поверхности эпителиальных клеток кишки, осуществляя пристеночное пищеварение.Регуляция кишечной секреции
Регуляция деятельности желез тонкой кишки осуществляется местными нервно-рефлекторными механизмами, а также гуморальными влияниями и ингредиентами химуса. Механическое раздражение слизистой оболочки тонкой кишки вызывает выделение жидкого секрета с малым содержанием ферментов. Местное раздражение слизистой кишки продуктами переваривания белков, жиров, соляной кислотой, панкреатическим соком вызывает отделение кишечного сока, богатого ферментами. Усиливают кишечное сокоотделение ГИП, ВИП, мотилин. Гормоны энтерокринин и дуокринин, выделяемые слизистой оболочкой тонкой кишки, стимулируют соответственно секрецию либеркюновых и бруннеровых желез. Тормозное действие оказывает соматостатин.Полостное и пристеночное пищеварение в тонкой кишке
В тонкой кишке различают два вида пищеварения: полостное и пристеночное. Полостное пищеварение происходит с помощью ферментов пищеварительных секретов, поступающих в полость тонкой кишки (поджелудочный сок, желчь, кишечный сок). В результате полостного пищеварения крупномолекулярные вещества (полимеры) гидролизуются в основном до стадии олигомеров. Дальнейший их гидролиз идет в зоне, прилегающей к слизистой оболочке и непосредственно на ней. Пристеночное пищеварение в широком смысле происходит в слое слизистых наложений, находящемся над гликокаликсом, зоне гликокаликса и на поверхности микроворсинок. Слой слизистых наложений состоит из слизи, продуцируемой слизистой оболочкой тонкой кишки и слущивающегося кишечного эпителия. В этом слое находится много ферментов поджелудочной железы и кишечного сока. Питательные вещества, проходя через слой слизи, подвергаются воздействию этих ферментов. Гликокаликс адсорбирует из полости тонкой кишки ферменты пищеварительных соков, которые осуществляют промежуточные стадии гидролиза всех основных питательных веществ. Продукты гидролиза поступают на апикальные мембраны энтероцитов, в которые встроены кишечные ферменты, осуществляющие собственное мембранное пищеварение, в результате которого образуются мономеры, способные всасываться. Благодаря близкому расположению встроенных в мембрану собственных кишечных ферментов и транспортных систем, обеспечивающих всасывание, создаются условия для сопряжения процессов конечного гидролиза питательных веществ и начала их всасывания. Для мембранного пищеварения характерна следующая зависимость: секреторная активность эпителиоцитов убывает от крипты к вершине кишечной ворсинки. В верхней части ворсинки идет в основном гидролиз дипептидов, у основания – дисахаридов. Пристеночное пищеварение зависит от ферментного состава мембран энтероцитов, сорбционных свойств мембраны, моторики тонкой кишки, от интенсивности полостного пищеварения, диеты. На мембранное пищеварение оказывают влияние гормоны надпочечников (синтез и транслокация ферментов).Пищеварение в толстой кишке
Из тонкой кишки химус через илеоцекальный сфинктер (баугиниеву заслонку) переходит в толстую кишку. Роль толстой кишки в процессе переваривания пищи небольшая, так как пища почти полностью переваривается и всасывается в тонкой кишке, за исключением растительной клетчатки. В толстой кишке происходят концентрирование химуса путем всасывания воды, формирование каловых масс и удаление их из кишечника. Здесь также происходит всасывание электролитов, водорастворимых витаминов, жирных кислот, углеводов.Секреторная функция толстой кишки
Железы слизистой оболочки толстой кишки выделяют небольшое количество сока (рН 8,5 – 9,0), который содержит в основном слизь, отторгнутые эпителиальные клетки и небольшое количество ферментов (пептидазы, липаза, амилаза, щелочная фосфатаза, катепсин, нуклеаза) со значительно меньшей активностью, чем в тонкой кишке. Однако при нарушении пищеварения вышележащих отделов пищеварительного тракта толстая кишка способна их компенсировать путем значительного повышения секреторной активности. Регуляция сокоотделения в толстой кишке обеспечивается местными механизмами. Механическое раздражение слизистой оболочки кишечника усиливает секрецию в 8 – 10 раз.Микрофлора толстой кишки
Существенную роль в процессе пищеварения в толстой кишке играет нормальная микрофлора. Анаэробная микрофлора преобладает над аэробной. Микрофлора толстой кишки осуществляет конечное разложение остатков непереваренных пищевых веществ, расщепляет волокна клетчатки; участвует в метаболизме липидов, желчных и жирных кислот, билирубина, холестерина; инактивирует ферменты, например, щелочную фосфатазу, трипсин, амилазу, поступающие из тонкой кишки в составе химуса; сбраживает углеводы до кислых продуктов (молочной и уксусной кислоты); синтезирует витамины К и группы В в толстой кишке; участвует в создании общего иммунитета; подавляет размножение патогенных микробов. Под воздействием микробов сохранившиеся белки подвергаются гнилостному разложению с образованием токсичных соединений: индола, скатола, фенола. Образующиеся при брожении кислые продукты препятствуют гниению, поэтому сбалансированное питание уравновешивает процессы гниения и брожения. При некоторых заболеваниях, а также в результате длительного лечения антибактериальными препаратами происходит нарушение нормальной микрофлоры и размножение патогенной, что приводит к развитию осложнений (дисбактериоз).Моторика пищеварительного тракта
Моторная функция желудочно-кишечного тракта осуществляется во всех его отделах и заключается в измельчении пищи в ходе жевания, перемешивании и продвижении пищи по пищеварительному тракту, сокращении и расслаблении сфинктеров, движении ворсинок и микроворсинок тонкой кишки, удалении непереваренных остатков пищи. На оральном и аборальном концах моторика осуществляется с участием произвольных поперечно-полосатых мышц, в других отделах желудочно-кишечного тракта – с участием гладкой мускулатуры. Поэтому процессы жевания, глотания и дефекации подчиняются сознательному контролю. Сфинктеры выполняют роль клапанов, обеспечивающих движение пищевого содержимого в каудальном направлении и однонаправленное движение пищеварительных соков. В пищеварительном тракте насчитывается около 35 сфинктеров.Жевание
Этот процесс состоит в механической обработке пищи между верхними и нижними рядами зубов за счет движений нижней челюсти по отношению к верхней неподвижной. Жевательные движения осуществляются специальными жевательными мышцами, мимическими, а также мышцами языка. В процессе жевания про-исходит измельчение пищи, смешивание ее со слюной и формирование пищевого комка, создаются условия для возникновения вкусовых ощущений. Пища, поступая в ротовую полость, раздражает механо-, термо- и хеморецепторы ее слизистой оболочки. Возбуждение от этих рецепторов по афферентным волокнам в основном тройничного нерва передается в чувствительные ядра продолговатого мозга, зрительный бугор и кору больших полушарий. От ствола мозга и зрительного бугра коллатерали отходят к ретикулярной формации. В акте жевания также принимают участие проприорецепторы жевательных мышц и механорецепторы опорного аппарата зуба – парадонта. В результате анализа и синтеза поступившей информации принимается решение о съедобности попавших в ротовую полость веществ. Несъедобная пища отвергается, съедобная – остается в полости рта. Совокупность нейронов различных отделов мозга, управляющих актом жевания, называется жевательным центром. От двигательных ядер ретикулярной формации ствола мозга по эфферентным волокнам тройничного, подъязычного и лицевого нервов импульсы поступают к мышцам, обеспечивающим жевание. В результате происходят движения нижней челюсти. Мышцы языка и щек подают и удерживают пищу между зубами.Глотание
Пищевой комок из полости рта проводится через пищевод в желудок. Это осуществляется посредством акта глотания, который является рефлекторным процессом и состоит из ротовой, глоточной и пищеводной фаз. Ротовая фаза (произвольная) состоит в том, что пищевой комок перемещается на корень языка и раздражает механорецепторы мягкого нёба, корня языка и задней стенки глотки, вызывающие глоточную фазу. Возбуждение от этих рецепторов по афферентным волокнам тройничного, языкоглоточного и верхнего гортанного нервов передается в центр глотания продолговатого мозга. Отсюда по эфферентным волокнам тройничного, подъязычного, языкоглоточного и блуждающих нервов импульсы поступают к мышцам, участвующим в акте глотания. Если обработать корень языка и глотку раствором кокаина, то глотание не происходит, так как «выключаются» рецепторы. Во время глоточной фазы (быстрая непроизвольная) перекрываются пути для попадания пищевого комка в носовые и дыхательные пути. Это происходит за счет сокращения мышц, приподнимающих мягкое нёбо, и поднятия гортани. Центр глотания расположен в продолговатом мозге рядом с центром дыхания и находится с ним в реципрокных отношениях, поэтому при глотании дыхание задерживается. Пищеводная (медленная непроизвольная) фаза заключается в открытии глоточно-пищеводного сфинктера и поступлении пищевого комка в пищевод. По пищеводу пищевой комок передвигается в сторону желудка благодаря перистальтическому сокращению мышц пищевода. У пищевода имеются два основных гладкомышечных слоя: продольный наружный и циркулярный внутренний. В области кардии находится нижний пищеводный сфинктер (кардиальный сфинктер), который при приближении пищевого комка расслабляется и пищевой комок входит в желудок. Обратному переходу химуса из желудка в пищевод препятствуют острый угол впадения пищевода в желудок, косые циркулярные мышцы желудка и диафрагмально-пищеводная связка.Моторная функция желудка
Моторная функция желудка способствует перемешиванию пищи с желудочным соком, продвижению и порционному поступлению содержимого желудка в двенадцатиперстную кишку. Она обеспечивается работой гладкой мускулатуры. Мышечная оболочка желудка состоит из трех слоев гладких мышц: внешнего продольного, среднего кругового и внутреннего косого. В пилорической части желудка волокна кругового и продольного слоев образуют сфинктер. Для некоторых мышечных клеток внутреннего косого слоя характерно наличие пейсмекерной активности. Пустой желудок обладает некоторым тонусом. Периодически происходит его сокращение (голодная моторика), которое сменяется состоянием покоя. Этот вид сокращения мышц связан с ощущением голода. Сразу после приема пищи происходит релаксация гладких мышц стенки желудка (пищевая рецептивная релаксация). Спустя некоторое время, что зависит от вида пищи, начинается сокращение желудка. Различают перистальтические, систолические и тонические сокращения желудка. Перистальтические движения осуществляются за счет сокращения циркулярных мышц желудка. Сокращения мышц начинаются на большой кривизне в непосредственной близости от пищевода, где локализуется кардиальный водитель ритма. В препилорической части локализуется второй водитель ритма. Сокращения мышц дистальной части антрального отдела и пилоруса представляют собой систолические сокращения. Эти движения обеспечивают переход содержимого желудка в двенадцатиперстную кишку. Тонические сокращения обусловлены изменением тонусамышц. В желудке возможны также и антиперистальтические движения, которые наблюдаются при акте рвоты. Рвота – это сложнорефлекторный координированный двигательный процесс, в нормальных условиях выполняющий защитную функцию, в результате которой из организма удаляются вредные для него вещества.Эвакуация химуса из желудка в двенадцатиперстную кишку
Содержимое желудка поступает в двенадцатиперстную кишку отдельными порциями благодаря сокращению мускулатуры желудка и открытию сфинктера привратника. Открытие пилорического сфинктера происходит вследствие раздражения рецепторов слизистой пилорической части желудка соляной кислотой. Перейдя в двенадцатиперстную кишку, НС1, находящаяся в химусе, воздействует на хеморецепторы слизистой кишки, что приводит к рефлекторному закрытию пилорического сфинктера (запирательный пилорический рефлекс). После нейтрализации кислоты в двенадцатиперстной кишке щелочным дуоденальным соком пилорический сфинктер снова открывается. Скорость перехода содержимого желудка в двенадцатиперстную кишку зависит от состава, объема, консистенции, осмотического давления, температуры и рН желудочного содержимого, степени наполнения двенадцатиперстной кишки, состояния сфинктера привратника. Жидкость переходит в двенадцатиперстную кишку сразу после поступления в желудок. Содержимое желудка переходит в двенадцатиперстную кишку только тогда, когда его консистенция становится жидкой или полужидкой. Углеводная пища эвакуируется быстрее, чем пища, богатая белками. Жирная пища переходит в двенадцатиперстную кишку с наименьшей скоростью. Время полной эвакуации смешанной пищи из желудка составляет 6–10 часов.Моторная функция тонкой кишки
За счет двигательной активности наружных продольных и внутренних (кольцевых) мышц тонкой кишки происходит перемешивание химуса с соком поджелудочной железы и кишечным соком и продвижение химуса по тонкой кишке. В тонкой кишке различают несколько видов движений: ритмическая сегментация, маятникообразные, перистальтические, тонические сокращения. Ритмическая сегментация обеспечивается сокращением кольцевых мышц. В результате этих сокращений образуются поперечные перехваты, которые делят кишку (и пищевую кашицу) на небольшие сегменты, что способствует лучшему растиранию химуса и перемешиванию его с пищеварительными соками. Маятникообразные движения обусловлены сокращением кольцевых и продольных мышц кишечника. В результате последовательных сокращений кольцевых и продольных мышц отрезок кишки то укорачивается и расширяется, то удлиняется и суживается. Это приводит к перемещению химуса то в одну, то в другую сторону, наподобие маятника, что способствует тщательному перемешиванию химуса с пищеварительными соками. Перистальтические движения обусловлены согласованными сокращениями продольного и циркулярного слоев мышц. За счет сокращения кольцевых мышц верхнего отрезка кишки происходит выдавливание химуса в одновременно расширяющийся за счет сокращения продольных мышц нижний участок. Перистальтические движения обеспечивают продвижение химуса по кишечнику. Все сокращения происходят на фоне общего тонуса стенок кишки. Отсутствие тонуса мышц (атония) при парезах делает невозможным любой вид сокращений. Кроме того, в течение всего процесса пищеварения наблюдается постоянное сокращение и расслабление ворсинок кишки, что обеспечивает соприкосновение их с новыми порциями химуса, улучшает всасывание и отток лимфы.Моторная функция толстой кишки
Моторная функция толстой кишки обеспечивает резервную функцию, т. е. накопление кишечного содержимого и периодическое удаление каловых масс из кишечника. Кроме того, моторная активность кишки способствует всасыванию воды. В толстой кишке наблюдаются следующие виды сокращений: перистальтические, антиперистальтические, пропульсивные, маятникообразные, ритмическая сегментация. Наружный продольный слой мышц располагается в виде полос и находится в постоянном тонусе. Сокращения отдельных участков циркулярного мышечного слоя образуют складки и вздутия (гаустры). Обычно волны гаустрации медленно проходят по толстой кишке. Три-четыре раза в сутки возникает сильная пропульсивная перистальтика, которая продвигает содержимое кишки в дистальном направлении.Регуляция моторики желудочно-кишечного тракта
Регуляция моторной функции пищеварительного тракта осуществляется нейрогуморальными механизмами. Активация блуждающего нерва усиливает перистальтику пищевода и расслабляет тонус кардии желудка. Симпатические волокна оказывают противоположный эффект. Кроме того, регуляция моторики осуществляется межмышечным, или ауэрбаховским, сплетением. Блуждающие нервы возбуждают моторную активность желудка, симпатические – угнетают. Большое значение в регуляции моторики желудка имеет внутриорганный отдел вегетативной нервной системы (ауэрбаховское сплетение) за счет местных периферических рефлексов. Возбуждающим действием на сократительную активность гладкой мускулатуры желудка обладают гастрин, гистамин, серотонин, мотилин, инсулин, ионы калия. Торможение моторики желудка вызывают энтерогастрон, адреналин, норадреналин, секретин, глюкагон, ХЦК-ПЗ, ЖИП, ВИП, бульбогастрон. Механическое раздражение кишечника пищевыми веществами приводит к рефлекторному торможению двигательной активности желудка (энтерогастральный рефлекс). Особенно выражен этот рефлекс при поступлении в двенадцатиперстную кишку жира и соляной кислоты. Двигательная активность тонкой кишки регулируется миогенными, нервными и гуморальными механизмами. Спонтанная двигательная активность гладких мышц кишечника обусловлена их автоматией. Известны два «датчика ритма» кишечных сокращений, один из которых находится у места впадения общего желчного протока в двенадцатиперстную кишку, другой – в подвздошной кишке. Организованная фазная сократительная деятельность стенки кишки осуществляется также с помощью нейронов ауэрбаховского нервного сплетения, которые обладают ритмической фоновой активностью. Эти механизмы находятся под влиянием нервной системы и гуморальных факторов. Парасимпатические нервы в основом возбуждают, а симпатические – тормозят сокращения тонкой кишки. Эффекты раздражения вегетативных нервов зависят от исходного состояния мышц, частоты и силы раздражения. Большое значение для регуляции моторики тонкой кишки имеют рефлексы с различных отделов пищеварительного тракта, которые можно разделить на возбуждающие и тормозные. К возбуждающим рефлексам относятся пищеводно-кишечный, желудочно-кишечный и кишечно-кишечный, к тормозным – кишечнокишечный, ректоэнтеральный, а также рецепторное торможение тонкой кишки (рецепторная релаксация) во время еды, которое затем сменяется усилением ее моторики. Рефлекторные дуги этих рефлексов замыкаются как на уровне интрамуральных ганглиев внутриорганного отдела вегетативной нервной системы, так и на уровне ядер блуждающих нервов в продолговатом мозге и в узлах симпатической нервной системы. Моторика тонкой кишки зависит от физических и химических свойств химуса. Грубая пища, содержащая большое количество клетчатки, жиры стимулируют двигательную активность тонкой кишки. Усиливают моторику кислоты, щелочи, концентрированные растворы солей, продукты гидролиза, особенно жиров. Гуморальные вещества осуществляют регуляцию моторики кишки, или непосредственно влияя на миоциты или на энтеральные нейроны. Стимулируют моторику вазопрессин, окситоцин, брадикинин, серотонин, гистамин, гастрин, мотилин, ХЦК-ПЗ, вещество Р, тормозят – секретин, ВИП, ГИП. Регуляция двигательной активности толстой кишки осуществляется преимущественно внутриорганным отделом вегетативной нервной системы: интрамуральными нервными сплетениями (ауэрбаховским и мейсснеровским). В стимуляции моторной деятельности толстой кишки существенную роль играют рефлексы при раздражении рецепторов пищевода, желудка, тонкой кишки, а также и самой толстой кишки. Раздражение рецепторов прямой кишки тормозит моторику толстой кишки. Коррекция местных рефлексов происходит вышележащими центрами ВНС. Симпатические нервные волокна, проходящие в составе чревных нервов, тормозят моторику; парасимпатические, идущие в составе блуждающих и тазовых нервов, – усиливают. Механические и химические раздражители повышают двигательную активность и ускоряют продвижение химуса по кишке. Поэтому, чем больше в пище клетчатки, тем выраженнее моторная активность толстой кишки. Серотонин, адреналин, глюкагон тормозят моторику толстой кишки, кортизон – стимулирует.Акт дефекации и его регуляция
Каловые массы удаляются с помощью акта дефекации, представляющего сложнорефлекторный процесс опорожнения дистального отдела толстой кишки через задний проход. При наполнении ампулы прямой кишки калом и повышении в ней давления до 40 – 50 см вод.ст. происходит раздражение механо- и барорецепторов. Возникшие при этом импульсы по афферентным волокнам тазового (парасимпатического) и срамного (соматического) нервов направляются в центр дефекации, который расположен в поясничной и крестцовой частях спинного мозга (непроизвольный центр дефекации). Из спинного мозга по эфферентным волокнам тазового нерва импульсы идут к внутреннему сфинктеру, вызывая его расслабление, и одновременно усиливают моторику прямой кишки. Произвольный акт дефекации осуществляется при участии коры больших полушарий, гипоталамуса и продолговатого мозга, которые оказывают свой эффект через центр непроизвольной дефекации в спинном мозге. От альфа-мотонейронов крестцового отдела спинного мозга по соматическим волокнам срамного нерва импульсы поступают к наружному (произвольному) сфинктеру, тонус которого вначале повышается, а при увеличении силы раздражения тормозится. Одновременно происходит сокращение диафрагмы и брюшных мышц, что ведет к уменьшению объема брюшной полости и повышению внутрибрюшного давления, что способствует акту дефекации. Продолжительность эвакуации, т. е. время, в течение которого происходит освобождение кишок от содержимого, у здорового человека достигает 24 – 36 часов. Парасимпатические нервные волокна, идущие в составе тазовых нервов, тормозят тонус сфинктеров, усиливают моторику прямой кишки и стимулируют акт дефекации. Симпатические нервы повышают тонус сфинктеров и тормозят моторику прямой кишки.Методы изучения функций пищеварительного тракта
Изучение секреторной и моторной деятельности желудочно-кишечного тракта проводится как на человеке, так и в эксперименте на животных. Особую роль играют хронические исследования, когда животному предварительно производится соответствующая операция и после восстановительного периода изучаются функции желудочно-кишечного тракта. В основе этих операций лежит принцип максимального сохранения нервных и сосудистых связей, обеспечивающих выполнение функций того или иного органа. Для изучения секреторной активности применяют выведение на кожу выводных протоков желез, или фистульный метод. Фистула – это искусственно созданное сообщение между полостью органа и внешней средой. Фистульные методы исследования дают возможность получать чистые пищеварительные соки с последующим изучением их состава и переваривающих свойств натощак, после кормления или другой стимуляции секреции; изучать моторную, секреторную и всасывательную функции органов пищеварения; изучать механизмы регуляции деятельности пищеварительных желез. В. А. Басовым (1842 г.) была впервые проведена операция наложения фистулы желудка. Однако с помощью этого метода нельзя было получить чистый желудочный сок. И. П. Павловым и Е. О. Шумовой-Симаковской (1889 г.) был разработан метод «мнимого кормления», когда животному с фистулой желудка одновременно делалась эзофаготомия (перерезка пищевода). Когда собака ела, пища выпадала из отверстия пищевода, а в желудке выделялся чистый желудочный сок, который собирался из фистулы. Этот метод дает возможность изучать рефлекторную деятельность желез желудка при раздражении рецепторов полости рта. Однако он не позволяет исследовать влияние самой пищи и продуктов расщепления, находящихся в желудке, на секрецию желудочных желез. Р. Гейденгайном была разработана операция изолированного желудочка, которая давала возможность получить чистый желудочный сок. Но эта операция не учитывала топографию нервов, иннервирующих желудок. При формировании изолированного желудочка нервы перерезались, а желудочек оказывался денервированным. Этим методом можно было изучать только гуморальную фазу желудочной секреции. И. П. Павлов, учтя недостатки методики Р. Гейденгайна, предложил способ операции изолированного желудочка без перерезки нервов, иннервирующих желудок, что дало возможность изучать желудочную секрецию на протяжении всего периода пищеварения. Для изучения секреторной активности других желез производятся операции наложения фистулы слюнных желез, поджелудочной железы, кишечника. Секреторную и моторную активность кишечника можно исследовать с помощью изолированных отрезков кишки, один или оба конца которых выводят наружу. Для изучения секреторной и моторной функций желудокно-кишечного тракта у человека используются зондовые и беззондовые методы. Зондовые методы (зондирование желудка, 12-перстной кишки) позволяют определить объем и состав секрета как натощак, так и после стимуляции пищеварительных желез пищей и различными фармакологическими препаратами (гистамином, пентагастрином при оценке желудочной секреции и серно-кислой магнезией при исследовании желчевыведения). В последние годы широко используются эндоскопические методы исследования желудка и кишечника, которые позволяют наряду с визуальным наблюдением за слизистой оболочкой получать биопсийный материал. При беззондовых методах учитывают содержание в крови и выделение с мочой веществ, освободившихся из принятых препаратов под действием на них пищеварительных секретов. О функциональном состоянии пищеварительных желез также можно судить по активности их ферментов в крови и моче. Разработан также метод эндорадиозондирования. Радиокапсула, проглоченная внутрь, может передавать информацию в виде радиосигналов о параметрах содержимого различных отделов желудочно-кишечного тракта, например рН и др. Радиокапсула с датчиком давления используется для изучения моторной активности пищеварительного тракта. Для изучения моторной функции пищеварительного аппарата применяются также методы мастикациографии (графическая регистрация жевательных движений нижней челюсти) и электрогастрографии (регистрация с поверхности передней брюшной стенки биотоков желудка, возникающих при его сокращении). В клинике также широко используются методы рентгенологического исследования с помощью рентгеноконтрастных веществ, радиоизотопное сканирование, УЗИ печени и желчного пузыря. Оценка гидролиза и всасывания в клинической практике производится биохимическими методами определения веществ при даче исходных продуктов.Физиологические основы голода и насыщения
Потребность в питательных веществах выражается в состоянии голода и создает мотивацию поиска и поедания пищи. Совокупность нейронов различных отделов центральной нервной системы, которые определяют пищевое поведение и регулируют пищеварительные функции человека и животного, составляют пищевой центр. Эти нейроны находятся в коре больших полушарий, в лимбической системе, ретикулярной формации, гипоталамусе, где локализуется центр голода. При возбуждении этих ядер у животного развивается гиперфагия – усиленное потребление пищи. Разрушение этих ядер приводит животное к отказу от пищи – афагии. В вентромедиальных ядрах гипоталамуса находится центр насыщения. При стимуляции этих нейронов у животного возникает афагия, при их разрушении – гиперфагия. Между центром голода и центром насыщения существуют реципрокные отношения, т. е. если один центр возбужден, то другой заторможен. Возбуждение или торможение этих ядер происходит в зависимости от содержания питательных веществ в крови, а также сигналов, поступающих от различных рецепторов. Существует несколько теорий, объясняющих возникновение чувства голода.Глюкостатическая теория – ощущение голода связано со снижением уровня глюкозы в крови. Аминоацидостатическая – чувство голода создается понижением содержания в крови аминокислот. Липостатическая – нейроны пищевого центра возбуждаются недостатком жирных кислот и триглицеридов в крови. Метаболическая – раздражителем нейронов пищевого центра являются продукты метаболизма цикла Кребса. Термостатическая – снижение температуры крови вызывает чувство голода. Локальная теория – чувство голода возникает в результате импульсации от механорецепторов желудка при его «голодных» сокращениях.
Насыщение возникает в результате возбуждения нейронов центра насыщения. Выделяют первичное, или сенсорное, насыщение и вторичное, или обменное. Сенсорное насыщение связано с торможением латеральных ядер гипоталамуса импульсами от ре-цепторов рта, желудка, возбуждаемых принимаемой пищей. В то же время возбуждение нейронов вентромедиальных ядер гипоталамуса приводит к поступлению в кровь питательных веществ из депо. Вторичное, обменное, или истинное, насыщение наступает через 1,5 – 2 часа с момента приема пищи, когда в кровь поступают продукты гидролиза питательных веществ. Гормоны желудочно-кишечного тракта также играют важную роль в возникновении чувства голода и насыщения. Холецистокинин, соматостатин, бомбезин и другие снижают потребление пищи. Пентагастрин, окситоцин и другие способствуют формированию чувства голода.
Лекарственные средства, применяемые при нарушении секреторной функции пищеварительного тракта
Широкое применение в клинике нашли лекарственные средства, тормозящие кислотно-пепсиновую секрецию желудочных желез. Эти препараты используются при язвенных поражениях желудка и двенадцатиперстной кишки. В качестве антисекреторных препаратов применяют блокаторы Н2-гистаминовых рецепторов (циметидин) и М-холинолитики (атропин и его аналоги и избирательный блокатор М^холинорецепторов гастроцепин). При назначении неизбирательных М-холинолитиков за счет уменьшения секреции слюнных желез может наблюдаться сухость во рту. Снизить секрецию соляной кислоты можно также, ингибируя активность Na+, К+–АТФазы в мембранах париетальных клеток. Таким действием обладает препарат омепразол. Для нейтрализации соляной кислоты при гиперацидных гастритах применяют антацидные вещества, повышающие рН. В качестве антацидов используют различные сочетания гидроокиси алюминия и магния, например, в составе препарата альмагеля. Эти вещества обладают также адсорбирующими и обволакивающими свойствами. При различных нарушениях процессов пищеварения, связанных с недостаточной секреторной способностью желудка, кишечника, поджелудочной железы, расстройствах пищеварения вследствие нарушения диеты, применяют ферментные препараты. Эти лекарственные средства, как правило, являются комплексными препаратами, содержащими определенный набор различных ферментов. При недостаточной функции желудочных желез используют натуральный желудочный сок, получаемый от здоровых собак через фистулу желудка при мнимом кормлении, или препараты, содержащие протеолитические ферменты. Так, из слизистой оболочки желудка свиней получают основной протеолитический фермент пепсин. Имеются лекарственные средства, содержащие сумму протеолитических ферментов желудочного сока (абомин). Эти ферментные средства применяют обычно в сочетании с разведенной соляной (хлористоводородной) кислотой. Получены фармакологические препараты, содержащие амилолитические, протеолитические и липолитические ферменты. Так, например, ферментный препарат из поджелудочных желез убойного скота панкреатин содержит трипсин и амилазу. Комплексный препарат фестал содержит основные компоненты поджелудочной железы (амилазу, липазу, протеазу) и желчи. Препарат панзинорм форте содержит экстракт слизистой оболочки желудка (пепсин, катепсин), экстракт желчи, аминокислоты, трипсин, химотрипсин, амилазу, липазу. В качестве диагностического средства для определения секреторной способности и кислотообразующей функции желудка используют синтетический аналог гастрина – пентагастрин.Лекарственные средства, применяемые при нарушениях моторной функции пищеварительного тракта Учитывая, что ацетилхолин, выделяющийся в окончаниях холинергических нервов, иннервирующих органы пищеварения, вызывает повышение тонуса и перистальтики гладких мышц пищеварительного тракта, при атониях желудка и кишечника применяются фармакологические препараты, возбуждающие холинорецепторы и действующие как эндогенный ацетилхолин (холиномиметики, например, ацеклидин). Аналогичным действием обладают и вещества, инактивирующие фермент холинэстеразу, разрушающую ацетилхолин, что приводит к накоплению эндогенного ацетилхолина (антихолинэстеразные вещества, например прозерин). При заболеваниях желудочно-кишечного тракта, сопровождающихся спазмом гладких мышц (спастические колиты, пилороспазм, холециститы), применяются лекарственные вещества, напротив, понижающие тонус гладких мышц. Таким действием обладают спазмолитические средства (но-шпа) и холинолитические препараты (атропин, метацин).
Всасывание
Всасывание – это процесс транспорта переваренных пищевых веществ из полости желудочно-кишечного тракта в кровь, лимфу и межклеточное пространство Оно осуществляется на протяжении всего пищеварительного тракта, но в каждом отделе имеются свои особенности. В полости рта всасывание незначительное, так как пища там не задерживается, но некоторые вещества, например, цианистый калий, а также лекарственные препараты (эфирные масла, валидол, нитроглицерин и др.) всасываются в ротовой полости и очень быстро попадают в кровеносную систему, минуя кишечник и печень. Это находит применение как способ введения лекарственных веществ. В желудке всасываются некоторые аминокислоты, немного глюкозы, воды с растворенными в ней минеральными солями и довольно существенно всасывание алкоголя. Основное всасывание продуктов гидролиза белков, жиров и углеводов происходит в тонком кишечнике. Белки всасываются в виде аминокислот, углеводы – в виде моносахаридов, жиры – в виде глицерина и жирных кислот. Всасыванию нерастворимых в воде жирных кислот помогают водорастворимые соли желчных кислот. Всасывание питательных веществ в толстой кишке незначительно, там всасывается много воды, что необходимо для формирования кала, в небольшом количестве глюкоза, аминокислоты, хлориды, минеральные соли, жирные кислоты и жирорастворимые витамины A, D, Е, К. Вещества из прямой кишки всасываются так же, как и из ротовой полости, т. е. непосредственно в кровь, минуя портальную кровеносную систему. На этом основано действие так называемых питательных клизм. Что касается других отделов желудочно-кишечного тракта (желудка, тонкого и толстого кишечника), то всосавшиеся в них вещества вначале поступают по портальным венам в печень, а затем в общий кровоток. Лимфоотток от кишечника осуществляется по кишечным лимфатическим сосудам в млечную цистерну. Наличие клапанов в лимфатических сосудах препятствует возврату лимфы в сосуды, которая по грудному протоку поступает в верхнюю полую вену. Всасывание зависит от величины всасывательной поверхности. Особенно она велика в тонкой кишке и создается за счет складок, ворсинок и микроворсинок. Так, на 1 мм2 слизистой оболочки кишки приходится 30 – 40 ворсинок, а на каждый энтероцит – 1700 – 4000 микроворсинок. Каждая ворсинка – это микроорган, содержащий мышечные сократительные элементы, кровеносный и лимфатический микрососуды и нервное окончание. Микроворсинки покрыты слоем гликокаликса, состоящего из мукополисахаридных нитей, связанных между собой кальциевыми мостиками, и образующего слой толщиной 0,1 мкм. Это молекулярное сито или сеть, которая благодаря отрицательному заряду и гидрофильности пропускает к мембране микроворсинок низкомолекулярные вещества и препятствует переходу через нее высокомолекулярных веществ и ксенобиотиков. Гликокаликс вместе с покрывающей кишечный эпителий слизью адсорбирует из полости кишки гидролитические ферменты, необходимые для полостного гидролиза питательных веществ, которые затем транспортируются на мембрану микроворсинок. Большую роль во всасывании играют сокращения ворсинок, которые натощак сокращаются слабо, а при наличии в кишке химуса – до б сокращений в 1 минуту. В регуляции сокращения ворсинок принимает участие интрамуральная нервная система (подслизистое, мейснеровское сплетение). Экстрактивные вещества пищи, глюкоза, пептиды, некоторые аминокислоты усиливают сокращения ворсинок. Кислое содержимое желудка способствует образованию в тонкой кишке специального гормона – вилликинина, стимулирующего через кровоток сокращения ворсинок.Механизмы всасывания
Для всасывания микромолекул – продуктов гидролиза пита-тельных веществ, электролитов, лекарственных препаратов используются несколько видов транспортных механизмов. 1. Пассивный транспорт, включающий в себя диффузию, фильтрацию и осмос. 2. Облегченная диффузия. 3. Активный транспортДиффузия основана на градиенте концентрации веществ в полости кишечника, в крови или лимфе. Путем диффузии через слизистую оболочку кишечника переносятся вода, аскорбиновая кислота, пиридоксин, рибофлавин и многие лекарственные препараты. Фильтрация основана на градиенте гидростатического давления. Так, повышение внутрикишечного давления до 8–10 мм рт.ст. увеличивает в 2 раза скорость всасывания из тонкой кишки раствора поваренной соли. Способствует всасыванию увеличение моторики кишечника. Переходу веществ через полупроницаемую мембрану энтероцитов помогают осмотические силы. Если в желудочно-кишечный тракт ввести гипертонический раствор какой-либо соли (поваренной, английской и т. д.), то по законам осмоса жидкость из крови и окружающих тканей, т. е. из изотонической среды, будет всасываться в сторону гипертонического раствора, т. е. в кишечник, и оказывать очищающее действие. На этом основано действие солевых слабительных. По осмотическому градиенту всасываются вода, электролиты. Облегченная диффузия осуществляется также по градиенту концентрации веществ, но с помощью особых мембранных переносчиков, без затраты энергии и быстрее, чем простая диффузия. Так, с помощью облегченной диффузии переносится фруктоза. Активный транспорт осуществляется против электрохимического градиента даже при низкой концентрации этого вещества в просвете кишечника, при участии переносчика и требует затраты энергии. В качестве переносчика – транспортера чаще всего используется Na+, с помощью которого всасываются такие вещества, как глюкоза, галактоза, свободные аминокислоты, соли желчных кислот, билирубин, некоторые дии трипептиды. Путем активного транспорта всасываются также витамин В12, ионы кальция. Активный транспорт крайне специфичен и может угнетаться веществами, имеющими химическое сходство с субстратом. Тормозится активный транспорт при низкой температуре и недостатке кислорода. На процесс всасывания влияет рН среды. Оптимальная рН для всасывания – нейтральная. Многие вещества могут всасываться при участии как активного, так и пассивного транспорта. Все зависит от концентрации вещества. При низкой концентрации преобладает активный транспорт, а при высокой – пассивный. Некоторые высокомолекулярные вещества транспортируются путем эндоцитоза (пиноцитоза и фагоцитоза). Этот механизм заключается в том, что мембрана энтероцита окружает всасываемое вещество с образованием пузырька, который погружается в цитоплазму, а затем переходит к базальной поверхности клетки, где заключенное в пузырек вещество выбрасывается из энтероцита. Этот вид транспорта имеет значение при переносе у новорожденного белков, иммуноглобулинов, витаминов, ферментов грудного молока. Некоторые вещества, например, вода, электролиты, антитела, аллергены могут проходить через межклеточные пространства. Такой вид транспорта называется персорбцией.
Всасывание белков
Белки под действием пептидаз – ферментов желудочного, кишечного и панкреатического соков расщепляются до олигопептидов, а затем аминокислот и всасываются в кровь. В двенадцати-перстной кишке всасывается 50 – 60% белков пищи и 30% – по мере прохождения химуса до подвздошной кишки, т. е. основная масса белков всасывается в тонком кишечнике (80 – 90%) и только 10% – в толстом под действием бактерий. У новорожденных цельные белки матери (глобулины) поступают из кишечника прямо в кровь ребенка, где они и были обнаружены. Предполагается, что именно это обстоятельство обеспечивает иммунитет ребенка сразу после рождения. Аминокислоты всасываются с различной скоростью: быстрее всего всасываются аргинин, метионин, лецитин, медленнее – цистеин, фенилаланин, тирозин, а еще медленнее – аланин, серин, глютаминовая кислота. Некоторые иммуноглобулины всасываются путем пиноцитоза. Основной вид всасывания белка – с помощью активного транспорта, т. е. с тратой энергии фосфоросодержащих макроэргов и с участием переносчиков.Различают четыре системы переноса аминокислот: 1. система переноса нейтральных аминокислот (валина, фенилаланина, аланина) 2. система переноса основных аминокислот (аргинина, цистеина, лизина, орнитина 3. система переноса иминокислот (пролина) 4. система переноса бикарбоновых аминокислот (глутамйновой и аспарагина).
К дополнительной группе относится система для глицина. Натрий также принимает участие во всасывании белка. Различные аминокислоты одной группы ингибируют перенос друг друга, конкурируя за один и тот же переносчик (конкурентное ингибирование). Аминокислоты могут освобождаться из энтероцита также с помощью диффузии и облегченной диффузии, но эти два вида транспорта не являются для них основными. Возраст влияет на всасывание белка. Оно более интенсивно в молодом возрасте. Уровень белкового обмена, содержание аминокислот в крови, нервные и гуморальные факторы влияют на всасывание белков.
Всасывание углеводов
Углеводы всасываются в кишечнике только в виде моносахаридов. Наиболее интенсивно всасываются глюкоза и галактоза (гексозы), пентозы всасываются медленнее. Если употребляется пища, богатая углеводами, то их концентрация в просвете кишечника увеличивается и они всасываются путем пассивного транспорта. Но основной путь всасывания глюкозы и галактозы – активный транспорт, сопряженный с переносом натрия. Без натрия эти моносахариды всасываются в 100 раз медленнее, а против градиента концентрации транспорт глюкозы полностью прекращается. Процесс всасывания глюкозы происходит следующим образом. Аккумулируясь на наружной стороне мембраны энтероцита, обращенной в полость кишечника, глюкоза в присутствии натрия связывается с переносчиком, который по электрохимическому градиенту для натрия диффундирует к внутренней стороне мембраны. В цитоплазме он высвобождает натрий и глюкозу. Затем переносчик и натрий транспортируются снова к наружной стороне мембраны энтероцита, а накопившаяся в цитозоле глюкоза удаляется из клетки в сосуд по градиенту концентрации. Концентрация натрия поддерживается за счет работы энергозависимого натрий-калиевого насоса. Всасывание углеводов регулируется нейрогуморальными факторами. Парасимпатическая нервная система стимулирует, а симпатическая – тормозит всасывание углеводов. Спинной мозг, ствол мозга, подкорковые структуры и кора больших полушарий также могут влиять на всасывание углеводов. Гормоны коры надпочечников, гипофиза, щитовидной железы, серотонин, ацетилхолин усиливают всасывание, а гистамин и особенно соматостатин – замедляют.Всасывание жиров
Жиры после их гидролиза под действием липазы на глицерин и жирные кислоты всасываются наиболее активно в двенадцатиперстной кишке и проксимальном отделе тощей кишки. Жирные кислоты плохо растворимы в воде, но их делают водорастворимыми соли желчных кислот. На поверхности мембраны энтероцита образуется мицелла, в состав которой входят жирная кислота с длинными цепями, желчная кислота и глицерин. Затем мицелла проходит в мембрану энтероцита без траты энергии. Внутри мембраны жирные кислоты захватываются специальным транспортным белком. В цитозоле энтероцита глицерин и жирные кислоты снова превращаются в триглицериды, холестерин и фосфолипиды. Все три образовавшиеся вещества, заключенные в тонкую липопротеиновую оболочку, формируют мельчайшие жировые частицы диаметром 60–75 нм, которые называются хиломикронами. Последние, пройдя через базолатеральную мембрану клетки, попадают в межклеточное пространство, а затем в лимфатические сосуды. Помимо хиломикронов в энтероцитах образуются липопротеины очень низкой плотности, которые также попадают в лимфатические сосуды. Так как жиры в основном всасываются в лимфу, то через несколько часов после приема пищи от всасывания жира лимфа приобретает белый цвет, напоминая молоко (млечный сок). Всасывание липидов регулируется центральной нервной системой. Парасимпатическая нервная система усиливает, а симпатическая нервная система тормозит всасывание липидов. Стимулируют всасывание гормоны коры надпочечников, гипофиза и щитовидной железы, а также гормоны APUD-системы – секретин и ХЦК-ПЗ.Всасывание витаминов
Водорастворимые витамины всасываются в дистальном отделе тощей кишки и проксимальном отделе подвздошной кишки. Всасывание жирорастворимых витаминов A, D, Е, К происходит в средней части тощей кишки и целиком зависит от всасывания жиров, нарушение которого препятствует транспорту витаминов из кишечника в лимфу и кровь. Витамин А образует эфиры с жирными кислотами и поступает в лимфу в составе хиломикронов. Для всасывания жирорастворимых витаминов важно наличие желчных кислот. Витамин С и рибофлавин переносятся путем диффузии. Витамин В12 в комплексе с внутренним фактором Касла всасывается в подвздошной кишке.Всасывание воды и электролитов
В пищеварительный тракт за сутки с пищей и питьем поступает 2,0 – 2,5 л воды, остальные 6–7 л воды выделяются в составе слюны, желудочного, панкреатического и кишечного соков. Таким образом, в полость желудочно-кишечного тракта за сутки поступает до 9,5 л воды. Незначительная часть воды всасывается в желудке, а большая часть – в тонком и особенно в толстом кишечнике. Вода всасывается в основном пассивно за счет осмотического градиента, создаваемого активным транспортом натрия между просветом кишечника и межклеточным пространством. Все факторы, влияющие на транспорт Na+, изменяют и всасывание воды. Так, блокатор натриевого насоса оубаин подавляет всасывание воды. В результате поступления Na+ из полости кишечника в межклеточную жидкость последняя становится гипертонической и притягивает к себе воду из просвета кишечника. Ток воды создает в межклеточном пространстве градиент гидростатического давления, являющийся движущей силой передвижения воды и растворенных в ней веществ в сторону капилляров, базальная мембрана которых обладает большой проницаемостью. Кроме того, вода всасывается через межэпителиальные щели путем персорбции. Всасывание воды связано также с транспортом аминокислот и Сахаров, поэтому если подавить всасывание Сахаров флорицином, то замедляется и всасывание воды. Оптимальный рН для всасывания воды – 6,8. Наркоз (эфир, хлороформ) и ваготомия тормозят всасывание воды, которое зависит также от степени гидратации тканей. Об участии коры больших полушарий в механизмах всасывания воды свидетельствует условно-рефлекторное изменение ее всасывания. АКТГ усиливает всасывание воды и хлоридов, тироксин стимулирует всасывание воды. Некоторые гастроинтестинальные гормоны (гастрин, секретин, ХЦК-ПЗ, ВИП, бомбезин, серотонин) тормозят всасывание воды. Всасывание натрия осуществляется различными путями: пассивно по градиенту концентрации, активно за счет работы натриевых и натрий-калиевых насосов, а также путем персорбции через межклеточные щели. За одни сутки в желудочно-кишечном тракте всасывается более 1 моля натрия хлорида. Основное всасывание Na+ происходит в подвздошной и толстой кишке. От всасывания Na+ зависит транспорт аминокислот, глюкозы и других веществ. Всасывание Na+ регулируется минералокортикоидами и гормонами задней доли гипофиза, которые усиливают всасывание натрия. Угнетают этот процесс гастрин, секретин, ХЦК-ПЗ. Всасывание К+ осуществляется в тонком и толстом кишечнике за счет активного и пассивного транспорта по электрохимическому градиенту. Транспорт калия сопряжен с транспортом натрия. Хлориды всасываются в желудке и подвздошной кишке по типу активного и пассивного транспорта. Всасывание хлора связано с транспортом Na+, Са2+ и К+. Всасывание кальция происходит очень медленно с помощью специального переносчика – кальцийсвязывающего белка, синтез которого контролируется витамином D3. Последний образуется в коже под влиянием ультрафиолетового облучения. Этот процесс активируется желчными кислотами, некоторыми аминокислотами, натрием, антибиотиками. Паратгормон, гормоны щитовидной железы, гипофиза и надпочечников увеличивают всасывание кальция. Железо всасывается в тонком кишечнике путем активного транспорта. В энтероцитах содержится специальный переносчик железа, который транспортирует его внутрь клетки. Там он связывается со специфическим белком, который доставляет двухвалентное железо в кровь. В крови есть белок трансферритин, связывающий и доставляющий железо к месту его действия. Избыток железа вместе с ферритином поступает в просвет кишечника и выводится.Всасывание лекарственных препаратов
Механизмы всасывания лекарственных препаратов из полости желудочно-кишечного тракта различны: прежде всего это диффузия, этим способом всасывается большинство лекарственных препаратов, затем фильтрация и пиноцитоз. Некоторые лекарственные препараты всасываются путем активного транспорта. На процесс всасывания лекарств в желудке и кишечнике влияет целый ряд факторов. В первую очередь – это рН среды. Поэтому в желудке, где среда кислая, лучше всего всасываются лекарствакислоты, а лекарства-основания – в кишечнике. Кислая среда разрушает некоторые лекарства, например бензилпенициллин. Другим субстратом, действующим на всасывание лекарств, являются ферменты желудочно-кишечного тракта, которые способны инактивировать ряд белковых и полипептидных веществ (кортикотропины, вазопрессин, инсулин и др.), а также некоторые гормоны (прогестерон, тестостерон, альдостерон). Соли желчных кислот, в свою очередь, могут ускорять всасывание лекарств или, наоборот, замедлять его при образовании нерастворимых соединений. Моторика желудочно-кишечного тракта – один из факторов, лимитирующих скорость и полноту всасывания лекарственных препаратов. Количество пищи, ее состав, интервал времени между едой и приемом лекарств влияют на всасывание лекарств. Так, всасывание тетрациклинов, ампициллина нарушается под действием молока, солей железа, при высоком содержании углеводов, белков и жира в пище. Объем жидкости, принимаемой вместе с лекарствами, может вызвать или замедление, или ускорение всасывания.Печень
Печень – это железа внешней секреции, выделяющая свой секрет в двенадцатиперстную кишку. Свое название она получила от слова «печь», так как в печени самая высокая температура по сравнению с другими органами. Печень представляет собой сложнейшую «химическую лабораторию», в которой происходят процессы, связанные с образованием тепла. Печень принимает самое активное участие в пищеварении. Кроме пищеварительной печень выполняет целый ряд других важнейших функций, которые будут рассмотрены ниже. Через нее проходят почти все вещества, в том числе и лекарственные, которые так же, как и токсические продукты, обезвреживаютсяПищеварительная функция печени
Эту функцию можно разделить на секреторную, или желче-отделение (холерез) и экскреторную, или желчевыделение (холекинез). Желчеотделение происходит непрерывно и желчь накапливается в желчном пузыре, а желчевыделение – только во время пищеварения (через 3–12 мин после начала приема пищи). При этом желчь сначала выделяется из желчного пузыря, а затем из печени в двенадцатиперстную кишку. Поэтому принято говорить о печеночной и пузырной желчи. За сутки отделяется 500 – 1500 мл желчи. Она образуется в печеночных клетках – гепатоцитах, которые контактируют с кровеносными капиллярами. Из плазмы крови с помощью пассивного и активного транспорта в гепатоцит выходит ряд веществ: вода, глюкоза, креатинин, электролиты и др. В гепатоците образуются желчные кислоты и желчные пигменты, затем все вещества из гепатоцита секретируют в желчные капилляры. Далее желчь поступает в желчные печеночные протоки. Последние впадают в общий желчный проток, от которого отходит пузырный проток. Из общего желчного протока желчь попадает в двенадцатиперстную кишку.Состав желчи
Печеночная желчь имеет золотисто-желтый цвет, пузырная – темно-коричневый; рН печеночной желчи – 7,3 – 8,0, относительная плотность – 1,008–1,015; рН пузырной желчи – 6,0 – 7,0 за счет всасывания гидрокарбонатов, аотносительная плотность – 1,026–1,048. Желчь состоит из 98% воды и 2% сухого остатка, куда входят органические вещества: соли желчных кислот, желчные пигменты – билирубин и биливердин, холестерин, жирные кислоты, лецитин, муцин, мочевина, мочевая кислота, витамины А, В, С; незначительное количество ферментов: амилаза, фосфатаза, протеаза, каталаза, оксидаза, а также аминокислоты и глюкокортикоиды; неорганические вещества: Na+, К+, Са2+, Fe++, Сl-, HCО3-, SО4-, НРО42-. В желчном пузыре концентрация всех этих веществ в 5–6 раз больше, чем в печеночной желчи. Холестерин – 80% его образуется в печени, 10% – в тонком кишечнике, остальное – в коже. За сутки синтезируется около 1 г холестерина. Он принимает участие в образовании мицелл и хиломикронов и только 30% всасывается из кишечника в кровь. Если нарушается выведение холестерина (при заболевании печени или неправильной диете), то возникает гиперхолестеринемия, которая проявляется или в виде атеросклероза, или желчнокаменной болезни. Желчные кислоты синтезируются из холестерина. Взаимодействуя с аминокислотами глицином и таурином, образуют соли гликохолевой (80%) и таурохолевой кислот (20%). Они способствуют эмульгированию и лучшему всасыванию в кровь жирных кислот и жирорастворимых витаминов (A, D, Е, К). За счет гидрофильности и липофильности жирные кислоты способны образовывать мицеллы с жирными кислотами и эмульгировать последние. Желчные пигменты – билирубин и биливердин придают желчи специфическую желто-коричневую окраску. В печени, селезенке и костном мозге происходит разрушение эритроцитов и гемоглобина. Вначале из распавшегося гема образуется биливердин, а затем билирубин. Далее вместе с белком в нерастворенной в воде форме билирубин с кровью транспортируется в печень. Там, соединившись с глюкуроновой и серной кислотами, он образует водорастворимые конъюгаты, которые выделяются печеночными клетками в желчный проток и в двенадцатиперстную кишку, где от конъюгата под действием микрофлоры кишечника отщепляется глюкуроновая кислота и образуется стеркобилин, придающий калу соответствующую окраску, а после всасывания из кишечника в кровь, а затем в мочу – уробилин, окрашивающий мочу в желтый цвет. При поражении клеток печени, например, при инфекционном гепатите или закупорке желчных протоков камнями или опухолью, в крови накапливаются желчные пигменты, появляется желтая ркраска склер и кожи. В норме содержание билирубина в крови составляет 0,2–1,2 мг%, или 3,5- 19 мкмоль/л (если больше 2–3 мг%, возникает желтуха).Функции желчи
Желчь выполняет целый ряд важных функций. 1. Эмульгирует жиры, делая водорастворимыми жирные кислоты. 2. Способствует всасыванию триглицеридов и образованию мицелл и хиломикронов. 3. Активирует липазу. 4. Стимулирует моторику тонкого кишечника. 5. Инактивирует пепсин в двенадцатиперстной кишке. 6. Оказывает бактерицидное и бактериостатическое действие на кишечную флору. 7. Стимулирует пролиферацию и слущивание энтероцитов. 8. Усиливает гидролиз и всасывание белков и углеводов. 9. Стимулирует желчеобразование и желчевыделение.Регуляция желчеотделения и желчевыделения
Желчеотделение и желчевыделение усиливаются при стимуляции парасимпатических волокон и снижаются – при раздражении симпатических. Стимуляция парасимпатических нервных волокон вызывает сокращение тела желчного пузыря и расслабление сфинктера, в результате желчь выделяется в двенадцатиперстную кишку. Раздражение симпатических нервов сокращает сфинктер и расслабляет тело желчного пузыря – желчный пузырь не опорожняется. Рефлекторные изменения желчеобразования и желчевыделения наблюдаются при раздражении интерорецепторов пищеварительного тракта, а также при условно-рефлекторных воздействиях. К гуморальным желчегонным факторам относится сама желчь. Поэтому в состав таких хорошо известных препаратов, как аллохол, холензим, входит желчь. Усиливают секрецию желчи гастрин, ХЦК-ПЗ, секретин, простагландины. Некоторые пищевые продукты, такие как желтки, молоко, жирная пища, хлеб, мясо, стимулируют желчеобразование и желчевыделение. Вид, запах пищи, разговоры о пище, подготовка к ее приему вызывают соответствующие изменения в деятельности желчного пузыря и всего желчевыделительного аппарата. В первые 7 – 10 минут желчный пузырь сначала расслабляется, а затем сокращается и небольшая порция желчи через сфинктер Одди выходит в двенадцатиперстную кишку. После этого следует основной период опорожнения желчного пузыря. В результате его периодических сокращений, чередующихся с расслаблением, в двенадцатиперстную кишку выходит желчь вначале из общего желчного протока, затем пузырная и в последнюю очередь – печеночная. Желчевыделение стимулируется ХЦК-ПЗ, гастрином, секретином, бомбезином, ацетилхолином, гистамином. Тормозят желчевыделение глюкагон, кальцитонин, ВИП.Непищеварительные функции печени
Участие в углеводном обмене
Печень является органом, поддерживающим нормальный уровень сахара в крови за счет процессов гликогенеза – превращения глюкозы в гликоген с помощью гормона поджелудочной железы инсулина. Если количество глюкозы в крови уменьшается, то депонированный в печени гликоген снова превращается в глюкозу – это гликогенолиз. При уменьшении запасов углеводов в крови в печени под влиянием гормонов коры надпочечников – глюкокортикоидов гликоген может синтезироваться из аминокислот и жиров – это гликонеогенез.Участие в белковом обмене
В печени происходит метаболизм и анаболизм протеинов, дезаминирование аминокислот, обезвреживание аммиака и превращение его в мочевину, которая затем выводится почками, и креатинина. Печень продуцирует целый ряд плазменных белков: гамма-глобулины, альбумины, бета-глобулины.Участие в жировом обмене
Печень синтезирует жирные кислоты, триглицериды, фосфолипиды, холестерин, кетоновые тела, участвует в их метаболизме. Она экстрагирует липиды из крови в виде хиломикронов и отвечает за их окисление в других тканях. В печени синтезируются липопротеиды высокой и низкой плотности.Печень – депо витаминов
Печень принимает непосредственное участие в обмене и всасывании в кишечнике жирорастворимых витаминов A, D, Е. К. Каротин превращается в витамин А, который хранится в печени в течение 10 месяцев и высвобождается в кровь по мере его потребности. Витамин D хранится в печени от 3 до 4 месяцев, витамин В12 – от 1 года до нескольких лет. Печень депонирует также витамины В6 – пиридоксаль, рибофлавин, аскорбиновую, фолиевую и пантотеновую кислоты, витамин К. Кроме витаминов печень депонирует микроэлементы; железо в виде ферритина, медь, марганец, кобальт, цинк, молибден и ДР.Участие в свертывании крови
В печени синтезируются такие факторы свертывания крови, как фибриноген (1-й фактор), протромбин (2-й фактор), проакцелерин (5-й фактор), проконвертин (7-й фактор), антигемофильный глобулин В (9-й фактор), фактор Стюарта – Прауэр (10-й фактор).Печень – депо крови
Через печень проходит 29% от МОК. Печень участвует в перераспределительных реакциях кровеносной системы. Алкогольная интоксикация, отравление токсическими веществами вызывают цирроз печени – разрастание вокруг сосудов фиброзной ткани. Кроме того, застой крови в правом сердце, увеличение давления в системе воротной вены и полой вены вызывает переполнение кровью сосудов печени, в результате плазма выходит непосредственно через капсулу печени в брюшную полость. Это явление называется асцитом.Дезинтоксикационная функция печени
Эта функция состоит в инактивации и выведении лекарственных препаратов (например, сульфаниламидов, антибиотиков и др.), гормонов, вредных веществ: аммиака, индола, скатола, фенола, алкоголя, который метаболизируется в основном в печени, а затем выводится с мочой и калом.Биотрансформация лекарственных препаратов в печени
Пройдя через стенку желудка и кишечника, лекарственные препараты, прежде чем попасть в системное кровообращение, через портальную кровеносную систему проникают в печень, где они подвергаются метаболическим превращениям под действием ферментативных систем печени («эффект первичного превращения»). Поэтому дозы некоторых препаратов (пропранолол, аминазин, опиаты) при их приеме через желудочно-кишечный тракт должны быть больше, чем при внутривенном введении для достижения необходимого эффекта. Поскольку лекарства еще не попали в системное кровообращение, их первичные превращения в печени называют пресистемным метаболизмом, интенсивность которого зависит от скорости кровотока через печень. Для оценки пресистемного метаболизма используют формулу,f=1-Сlобщ/V
где f – часть принятой внутрь дозы, достигающей общего кровотока; Сlобщ – общий клиренс препарата; V – скорость печеночного кровотока.
Все лекарственные вещества делятся на две группы: 1. с высоким печеночным клиренсом 2. низким печеночным клиренсом.
Для препаратов 1-й группы характерна высокая степень их экстракции гепатоцитами из крови. Способность печени метаболизировать эти препараты зависит от кровотока печени. Печеночный клиренс препаратов 2-й группы зависит преимущественно от емкости ферментативных систем печени, под действием которых происходят превращения лекарственных веществ, и от скорости их связывания с белками плазмы крови (дифенин – высокая скорость связывания, теофиллин, парацетамол – низкая). Биотрансформация лекарственных препаратов проходит в две фазы: 1-я фаза – окисление, гидроксилирование – это микросомальные и немикросомальные реакции, в результате которых образуются группы –ОН, –СООН, –Н, Н2; 2-я фаза – соединение этих веществ с глюкуроновой кислотой, сульфатами, глицином и образованием водорастворимых конъюгатов, которые легко выводятся из организма с калом и мочой. Таким путем удаляются эстрогены, прогестерон, наркотики, амидопирин, салицилаты, антибиотики и другие препараты. Многие лекарственные вещества после их биотрансформации в печени в виде метаболитов или в неизмененном виде с помощью активных транспортных систем экскретируются в желчь. Часть этих веществ выводится с калом, другая, под действием ферментов желудочно-кишечного тракта и бактериальной микрофлоры превращается в соединения, которые вновь реабсорбируются плазмой крови и попадают снова в печень, где они проходят процесс метаболических превращений или цикл энтерогепатической циркуляции.
Гепатотропные средства
Лекарственные препараты, применяемые для лечения заболеваний печени и желчевыводящих путей, в настоящее время делят на три группы: 1. желчегонные 2. гепатопротекторные 3. холелитолитические средства.В свою очередь, в группу желчегонных входят препараты, усиливающие образование желчи и желчных кислот (холеретика или холесекретика – от греч. chole – желчь, ereto – раздражать), и препараты, способствующие выделению желчи из желчного пузыря в 12-перстную кишку (холагога или холекинетика – от греч. chole – желчь, ago – вести, гнать). К холеретикам относятся препараты, содержащие желчные кислоты и желчь: аллохол, ли обил, холензим и др., а также средства растительного происхождения (цветки бессмертника, кукурузные рыльца и др., а также ряд синтетических препаратов – оксафенамид, циквалон). Механизм действия холеретиков основан на раздражении слизистой кишечника и паренхимы печени, усилении моторики и секреции желудочно-кишечного тракта, что стимулирует образование желчи, а также на повышении осмотического градиента между желчью и кровью, который способствует фильтрации в желчные капилляры воды и электролитов, предупреждает образование желчных камней. Холекинетики действуют на тонус желчного пузыря, желчных путей и сфинктера Одди. Способствуют опорожнению желчного пузыря: магния сульфат, барбарис и др. Расслабление тонуса желчных путей вызывают такие спазмолитики, как папаверин, но-шпа и др. Кроме того, желчегонные препараты оказывают гепатопротекторное действие, облегчая отток желчи, уменьшая воспалительный процесс в гепатоцитах. К гепатопротекторам относятся препараты (легалон, лив-52, эссенциале и др.), повышающие устойчивость печени к патологическим воздействиям, способствующие восстановлению активности ее ферментативных систем, ингибирующие перекисное окисление липидов, – это витамины группы Р (рутин, кварцетин). Холелитолитические средства – это производные дезоксихолевой кислоты, снижающие содержание холестерина в желчи и растворяющие холестериновые камни в желчном пузыре (хенодиол, хенофалк).
Глава 10. Обмен веществ и энергии
В живых организмах любой процесс сопровождается передачей энергии. Энергию определяют как способность совершать работу. Специальный раздел физики, который изучает свойства и превращения энергии в различных системах, называется термодинамикой. Под термодинамической системой понимают совокупность объектов, условно выделенных из окружающего пространства. Термодинамические системы разделяют на изолированные, закрытые и открытые. Изолированными называют системы, энергия и масса которых не изменяется, т. е. они не обмениваются с окружающей средой ни веществом, ни энергией. Закрытые системы обмениваются с окружающей средой энергией, но не веществом, поэтому их масса остается постоянной. Открытыми системами называют системы, обменивающиеся с окружающей средой веществом и энергией. С точки зрения термодинамики живые организмы относятся к открытым системам, так как главное условие их существования – непрерывный обмен веществ и энергии. В основе процессов жизнедеятельности лежат реакции атомов и молекул, протекающие в соответствии с теми же фундаментальными законами, которые управляют такими же реакциями вне организма. Согласно первому закону термодинамики энергия не исчезает и не возникает вновь, а лишь переходит из одной формы в другую. Второй закон термодинамики утверждает, что вся энергия в конце концов переходит в тепловую энергию, и организация материи становится полностью неупорядоченной. В более строгой форме этот закон формулируется так: энтропия замкнутой системы может только возрастать, а количество полезной энергии (т. е. той, с помощью которой может быть совершена работа) внутри системы может лишь убывать. Под энтропией понимают степень неупорядоченности системы. Неизбежная тенденция к возрастанию энтропии, сопровождаемая столь же неизбежным превращением полезной химической энергии в бесполезную тепловую, заставляет живые системы захватывать все новые порции энергии (пищи), чтобы поддерживать свое структурное и функциональное состояние. Фактически способность извлекать полезную энергию из окружающей среды является одним из основных свойств, которые отличают живые системы от неживых, т. е. непрерывно идущий обмен веществ и энергии является одним из основных признаков живых существ. Чтобы противостоять увеличению энтропии, поддерживать свою структуру и функции, живые существа должны получать энергию в доступной для них форме из окружающей среды и возвращать в среду эквивалентное количество энергии в форме, менее пригодной для дальнейшего использования. Обмен веществ и энергии – это совокупность физических, химических и физиологических процессов превращения веществ и энергии в живых организмах, а также обмен веществами и энергией между организмом и окружающей средой. Обмен веществ у живых организмов заключается в поступлении из внешней среды различных веществ, в превращении и использовании их в процессах жизнедеятельности и в выделении образующихся продуктов распада в окружающую среду. Все происходящие в организме преобразования вещества и энергии объединены общим названием – метаболизм (обмен веществ). На клеточном уровне эти преобразования осуществляются через сложные последовательности реакций, называемые путями метаболизма, и могут включать тысячи разнообразных реакций. Эти реакции протекают не хаотически, а в строго определенной последовательности и регулируются множеством генетических и химических механизмов. Метаболизм можно разделить на два взаимосвязанных, но разнонаправленных процесса: анаболизм (ассимиляция) и катаболизм (диссимиляция). Анаболизм – это совокупность процессов биосинтеза органических веществ (компонентов клетки и других структур органов и тканей). Он обеспечивает рост, развитие, обновление биологических структур, а также накопление энергии (синтез макроэргов). Анаболизм заключается в химической модификации и перестройке поступающих с пищей молекул в другие более сложные биологические молекулы. Например, включение аминокислот в синтезируемые клеткой белки в соответствии с инструкцией, содержащейся в генетическом материале данной клетки. Катаболизм – это совокупность процессов расщепления сложных молекул до более простых веществ с использованием части из них в качестве субстратов для биосинтеза и расщеплением другой части до конечных продуктов метаболизма с образованием энергии. К конечным продуктам метаболизма относятся вода (у человека примерно 350 мл в день), двуокись углерода (около 230 мл/мин), окись углерода (0,007 мл/мин), мочевина (около 30 г/день), а также другие вещества, содержащие азот (примерно 6 г/день). Катаболизм обеспечивает извлечение химической энергии из содержащихся в пище молекул и использование этой энергии на обеспечение необходимых функций. Например, образование свободных аминокислот в результате расщепления по-ступающих с пищей белков и последующее окисление этих аминокислот в клетке с образованием СО2 и Н2О, что сопровождается высвобождением энергии. Процессы анаболизма и катаболизма находятся в организме в состоянии динамического равновесия (рис. 26). Преобладание анаболических процессов над катаболическими приводит к росту, накоплению массы тканей, а преобладание катаболических процессов ведет к частичному разрушению тканевых структур. Состояние равновесного или неравновесного соотношения анаболизма и катаболизма зависит от возраста (в детском возрасте преобладает анаболизм, у взрослых обычно наблюдается равновесие, в старческом возрасте преобладает катаболизм), состояния здоровья, выполняемой организмом физической или психоэмоциональной нагрузки.
Процессы анаболизма и катаболизма находятся в организме в состоянии динамического равновесия (рис. 26). Преобладание анаболических процессов над катаболическими приводит к росту, накоплению массы тканей, а преобладание катаболических процессов ведет к частичному разрушению тканевых структур. Состояние равновесного или неравновесного соотношения анаболизма и катаболизма зависит от возраста (в детском возрасте преобладает анаболизм, у взрослых обычно наблюдается равновесие, в старческом возрасте преобладает катаболизм), состояния здоровья, выполняемой организмом физической или психоэмоциональной нагрузки.
Превращение и использование энергии
В процессе обмена веществ постоянно происходит превращение энергии: энергия сложных органических соединений, поступивших с пищей, превращается в тепловую, механическую и электрическую. Человек и животные получают энергию из окружающей среды в виде потенциальной энергии, заключенной в химических связях молекул жиров, белков и углеводов. Все процессы жизнедеятельности обеспечиваются энергией за счет анаэробного и аэробного метаболизма. Получение энергии без участия кислорода, например, гликолиз, (расщепление глюкозы до молочной кислоты) называется анаэробным обменом. В ходе анаэробного расщепления глюкозы (гликолиза) или ее резервного субстрата гликогена (гликогенолиза) превращение 1 моля глюкозы в 2 моля лактата приводит к образованию 2 молей АТФ. Энергии, образующейся в ходе анаэробных процессов, недостаточно для осуществления активной жизни, реакции, происходящие с участием кислорода, энергетически более эффективны. Все процессы, генерирующие энергию с участием кислорода, называются аэробным обменом. При окислении сложных молекул химические связи разрываются, сначала органические молекулы распадаются до трехуглеродных соединений, которые включаются в цикл Кребса (цикл лимонной кислоты), а далее окисляются до СО2 и Н2О. Высвободившиеся в этих реакциях протоны и электроны вступают в цепь переноса электронов, в которой кислород служит конечным акцептором электронов. Биологическое окисление в сущности представляет собой «сгорание» вещества при низкой температуре, часть энергии, высвобождающейся при окислении, запасается в высокоэнергетических фосфатных связях аденозинтрифосфата (АТФ). АТФ является аккумулятором химической энергии и средством ее переноса, диффундируя в те места, где она требуется. Общее количество молекул АТФ, образующихся при полном окислении 1 моля глюкозы до СО2 и Н2О, составляет 25,5 молей. При полном окислении молекулы жиров образуется большее количество молей АТФ, чем при окислении молекулы углеводов. Динамика химических превращений, происходящих в клетках, изучается биологической химией. Задачей физиологии является определение общих затрат веществ и энергии организмом и того, как они должны восполняться с помощью полноценного питания. Энергетический обмен служит показателем общего состояния и физиологической активности организма. Единица измерения энергии, обычно применяемая в биологии и медицине, – калория (кал). Она определяется как количество энергии, необходимое для повышения температуры 1 г воды на ГС. В Международной системе единиц (СИ) при измерении энергетических величин используется джоуль (1 ккал = 4,19 кДж).Энергетический эквивалент пищи
Количество энергии, выделяемой при окислении какого-либо соединения, не зависит от числа промежуточных этапов его распада, т. е. от того, сгорело ли оно или окислилось в ходе катаболических процессов. Запас энергии в пище определяется в калориметрической бомбе – замкнутой камере, погруженной в водяную баню. Точно взвешенную пробу помещают в эту камеру, наполненную чистым О2, и поджигают. Количество выделившейся энергии определяется по изменению температуры воды, окружающей камеру. При окислении углеводов выделяется 17,17 кДж/г (4,1 ккал/г), окисление 1 г жира дает 38,96 кДж (9,3 ккал). Запасание энергии в форме жира является наиболее экономичным способом длительного хранения энергии в организме. Белки окисляются в организме не полностью. Аминогруппы отщепляются от молекулы белка и выводятся с мочой в форме мочевины. Поэтому при сжигании белка в калориметрической бомбе выделяется больше энергии, чем при его окислении в организме: при сжигании белка в калориметрической бомбе выделяется 22,61 кДж/г (5,4 ккал/г), а при окислении в организме – 17,17 кДж/г (4,1 ккал/г). Разница приходится на ту энергию, которая выделяется при сжигании мочевины.Определение уровня метаболизма
Почти половина всей энергии, получаемой в результате катаболизма, теряется в виде тепла в процессе образования молекул АТФ. Мышечное сокращение – процесс еще менее эффективный. Около 80% энергии, используемой при мышечном сокращении, теряется в виде тепла и только 20% превращается в механическую работу (сокращение мышцы). Если человек не совершает работу, то практически вся генерируемая им энергия теряется в форме тепла (например, у человека, лежащего в постели). Следовательно, величина теплопродукции является точным выражением величины обмена в организме человека. Для определения количества затрачиваемой организмом энергии применяют прямую и непрямую калориметрию. Первые прямые измерения энергетического обмена провели в 1788 г. Лавуазье и Лаплас. Прямая калориметрия заключается в непосредственном измерении тепла, выделяемого организмом. Для этого животное или человек помещается в специальную герметическую камеру, по трубам, проходящим через нее, протекает вода. Для вычисления теплопродукции используются данные о теплоемкости жидкости, ее объеме, протекающем через камеру за единицу времени, и разности температур поступающей в камеру и вытекающей жидкости. Непрямая калориметрия основана на том, что источником энергии в организме являются окислительные процессы, при которых потребляется кислород и выделяется углекислый газ. Поэтому энергетический обмен можно оценивать, исследуя газообмен. Наиболее распространен способ Дугласа – Холдейна, при котором в течение 10- 15 мин собирают выдыхаемый обследуемым человеком воздух в мешок из воздухонепроницаемой ткани (мешок Дугласа). Затем определяют объем выдохнутого воздуха и процентное содержание в нем О2 и СО2. По соотношению между количеством выделенного углекислого газа и количеством потребленного за данный период времени кислорода – дыхательному коэффициенту (ДК) – можно установить, какие вещества окисляются в организме. ДК при окислении белков равен 0,8, при окислении жиров – 0,7, а углеводов – 1,0. Каждому значению ДК соответствует определенный калорический эквивалент кислорода, т. е. то количество тепла, которое выделяется при окислении какого-либо вещества на каждый литр поглощенного при этом кислорода. Количество энергии на единицу потребляемого О2 зависит от типа окисляющихся в организме веществ. Калорический эквивалент кислорода при окислении углеводов равен 21 кДж на 1 л О2 (5 ккал/л), белков – 18,7 кДж (4,5 ккал), жиров – 19,8 кДж (4,74 ккал). Для косвенного определения интенсивности обмена могут быть использованы некоторые физиологические параметры, связанные с потреблением кислорода: частота дыханий и вентиляционный объем, частота сокращений сердца и минутный объем кровотока – все они отражают затраты энергии. Однако эти показатели недостаточно точны.Основной обмен
Интенсивность энергетического обмена значительно варьирует и зависит от многих факторов. Поэтому для сравнения энергетических затрат у разных людей была введена условная стандартная величина – основной обмен.Основной обмен (ОО) – это минимальные для бодрствующего организма затраты энергии, определенные в строго контролируемых стандартных условиях: 1. при комфортной температуре (18 – 20 градусов тепла); 2. в положении лежа (но обследуемый не должен спать); 3. в состоянии эмоционального покоя, так как стресс усиливает метаболизм; 4. натощак, т. е. через 12 – 16 ч после последнего приема пищи.
Основной обмен зависит от пола, возраста, роста и массы тела человека. Величина основного обмена в среднем составляет 1 ккал в 1 ч на 1 кг массы тела. У мужчин в сутки основной обмен приблизительно равен 1700 ккал, у женщин основной обмен на 1 кг массы тела примерно на 10% меньше, чем у мужчин, у детей он больше, чем у взрослых, и с увеличением возраста постепенно снижается.
Правило поверхности.
У млекопитающих величина основного обмена, рассчитанная на 1 кг массы тела, сильно различается: чем меньше животное, тем выше обмен. Если пересчитать интенсивность обмена на 1 м2 поверхности тела, то полученные величины отличаются не столь значительно. Макс Рубнер в 1868 г. установил, что затраты энергии (интенсивность обмена) пропорциональны величине поверхности тела. Это объясняется необходимостью поддерживать постоянную температуру, соотношением теплопродукции и теплоотдачи, так как при относительно большой поверхности теряется больше тепла. У человека отношение основного обмена к поверхности тела оказалось величиной сравнительно постоянной. Ежедневная продукция тепла на 1 м2 поверхности тела у человека равна 3559–5234 кДж (850–1250 ккал). Правило поверхности лишь относительно верно, о чем свидетельствует тот факт, что у индивидуумов с одинаковой поверхностью тела интенсивность метаболизма может значительно различаться. Это связано с особенностями метаболизма, состоянием нервной, эндокринной и других систем.Суточный расход энергии
Суточный расход энергии у здорового человека значительно превышает величину основного обмена и складывается из следующих компонентов: основного обмена; рабочей прибавки, т. е. энергозатрат, связанных с выполнением той или иной работы; специфического-динамического действия пищи. Совокупность компонентов суточного расхода энергии составляет рабочий обмен. Мышечная работа существенно изменяет интенсивность обмена. Чем интенсивнее выполняемая работа, тем выше затраты энергии. Степень энергетических затрат при различной физической активности определяется коэффициентом физической активности – отношением общих энергозатрат на все виды деятельности в сутки к величине основного обмена. По этому принципу все население делится на 5 групп. Для людей, выполняющих легкую работу сидя, нужно 2400 – 2600 ккал в сутки, работающих с большей мышечной нагрузкой, требуется 3400 – 3600 ккал, выполняющих тяжелую мышечную работу – 4000 – 5000 ккал и выше. У тренированных спортсменов при кратковременных интенсивных упражнениях величина рабочего обмена может в 20 раз превосходить основной обмен. Потребление кислорода при физической нагрузке не отражает общего расхода энергии, так как часть ее тратится на гликолиз (анаэробный) и не требует затраты кислорода. Разность между потребностью в О2 и его потреблением составляет энергию, получаемую в результате анаэробного распада, и называется кислородным долгом. Потребление О2 и после окончания мышечной работы остается высоким, так как в это время происходит возвращение кислородного долга. Кислород затрачивается на превращение главного побочного продукта анаэробного метаболизма – молочной кислоты в пировиноградную, на фосфорилирование энергетических соединений (креатинфосфат) и восстановление запасов О2 в мышечном миоглобине. Прием пищи усиливает энергетический обмен (специфическое динамическое действие пищи). Белковая пища повышает интенсивность обмена на 25 – 30%, а углеводы и жиры – на 10% или меньше. Во время сна интенсивность метаболизма почти на 10% ниже основного обмена. Разница между бодрствованием в состоянии покоя и сном объясняется тем, что во время сна мышцы расслаблены. При гиперфункции щитовидной железы основной обмен повышается, а при гипофункции – понижается. Понижение основного обмена происходит при недостаточности функций половых желез и гипофиза. При умственном труде энерготраты значительно ниже, чем при физическом. Даже очень интенсивный умственный труд, если он не сопровождается движениями, вызывает повышение затрат энергии лишь на 2–3% по сравнению с полным покоем. Однако если умственная активность сопровождается эмоциональным возбуждением, энерготраты могут быть заметно большими. Пережитое эмоциональное возбуждение может вызывать в течение нескольких последующих дней повышение обмена на 11 – 19%.Обмен веществ
Обмен веществ начинается с поступления питательных веществ в желудочно-кишечный тракт и воздуха в легкие. Первым этапом обмена веществ являются ферментативные процессы расщепления белков, жиров и углеводов до растворимых в воде аминокислот, моно- и дисахаридов, глицерина, жирных кислот и других соединений, происходящие в различных отделах желудочно-кишечного тракта, а также всасывание этих веществ в кровь и лимфу. Вторым этапом обмена являются транспорт питательных веществ и кислорода кровью к тканям и те сложные химические превращения веществ, которые происходят в клетках. В них одновременно осуществляются расщепление питательных веществ до конечных продуктов метаболизма, синтез ферментов, гормонов, составных частей цитоплазмы. Расщепление веществ сопровождается выделением энергии, которая используется для процессов синтеза и обеспечения работы каждого органа и организма в целом. Третьим этапом является удаление конечных продуктов распада из клеток, их транспорт и выделение почками, легкими, потовыми железами и кишечником. Превращение белков, жиров, углеводов, минеральных веществ и воды происходит в тесном взаимодействии друг с другом. В метаболизме каждого из них имеются свои особенности, а физиологическое значение их различно, поэтому обмен каждого из этих веществ принято рассматривать отдельно.Обмен белков
Белки используются в организме в первую очередь в качестве пластических материалов. Потребность в белке определяется тем его минимальным количеством, которое будет уравновешивать его потери организмом. Белки находятся в состоянии непрерывного обмена и обновления. В организме здорового взрослого человека количество распавшегося за сутки белка равно количеству вновь синтезированного. Десять аминокислот из 20 (валин, лейцин, изолейцин, лизин, метионин, триптофан, треонин, фенилаланин, аргинин и гистидин) в случае их недостаточного поступления с пищей не могут быть синтезированы в организме и называются незаменимыми. Другие десять аминокислот (заменимые) могут синтезироваться в организме. Из аминокислот, полученных в процессе пищеварения, синтезируются специфические для данного вида, организма и для каждого органа белки. Часть аминокислот используются как энергетический материал, т. е. подвергаются расщеплению. Сначала они дезаминируются – теряют группу -NH2, В результате образуются аммиак и кетокислоты. Аммиак является токсическим веществом и обезвреживается в печени путем превращения в мочевину. Кетокислоты после ряда превращений распадаются на СО2 и Н2О. Скорость распада и обновления белков организма различна – от нескольких минут до 180 суток (в среднем 80 суток). О количестве белка, подвергшегося распаду за сутки, судят по количеству азота, выводимого из организма человека. В 100 г белка содержится 16 г азота. Таким образом, выделение организмом 1 г азота соответствует распаду 6,25 г белка. За сутки из организма взрослого человека выделяется около 3,7 г азота, т. е. масса разрушившегося белка составляет 3,7 х 6,25 = 23 г, или 0,028 – 0,075 г азота на 1 кг массы тела в сутки (коэффициент изнашивания Рубнера). Если количество азота, поступающего в организм с пищей, равно количеству азота, выводимого из организма, то организм находится в состоянии азотистого равновесия. Если в организм поступает азота больше, чем выделяется, то это свидетельствует о положительном азотистом балансе (ретенция азота). Он возникает при увеличении массы мышечной ткани (интенсивные физические нагрузки), в период роста организма, беременности, во время выздоровления после тяжелого заболевания. Состояние, при котором количество выводимого из организма азота превышает его поступление в организм, называют отрицательным азотистым балансом. Оно возникает при питании неполноценными белками, когда в организм не поступают какие-либо из незаменимых аминокислот, при белковом или полном голодании. Необходимо потребление не менее 0,75 г белка на 1 кг массы тела в сутки, что для взрослого здорового человека массой 70 кг составляет не менее 52,5 г полноценного белка. Для надежной стабильности азотистого баланса рекомендуется принимать с пищей 85 – 90 г белка в сутки. У детей, беременных и кормящих женщин эти нормы должны быть выше. Физиологическое значение в данном случае означает, что белки в основном выполняют пластическую функцию, а углеводы – энергетическую.Обмен липидов
Липиды являются сложными эфирами глицерина и высших жирных кислот. Жирные кислоты бывают насыщенными и ненасыщенными (содержащими одну и более двойных связей). Липиды играют в организме энергетическую и пластическую роль. За счет окисления жиров обеспечивается около 50% потребности в энергии взрослого организма. Жиры служат резервом питания организма, их запасы у человека в среднем составляют 10 – 20% от массы тела. Из них около половины находятся в подкожной жировой клетчатке, значительное количество откладывается в большом сальнике, околопочечной клетчатке и между мышцами. В состоянии голода, при действии на организм холода, при физической или психоэмоциональной нагрузке происходит интенсивное расщепление запасенных жиров. В условиях покоя после приема пищи происходит ресинтез и отложение липидов в депо. Главную энергетическую роль играют нейтральные жиры – триглицериды, а пластическую осуществляют фосфолипиды, холестерин и жирные кислоты, которые выполняют функции структурных компонентов клеточных мембран, входят в состав липопротеидов, являются предшественниками стероидных гормонов, желчных кислот и простагландинов. Липидные молекулы, всосавшиеся из кишечника, упаковываются в эпителиоцитах в транспортные частицы (хиломикроны), которые через лимфатические сосуды поступают в кровоток. Под действием липопротеидлипазы эндотелия капилляров главный компонент хиломикронов – нейтральные триглицериды – расщепляются до глицерина и свободных жирных кислот. Часть жирных кислот может связываться с альбумином, а глицерин и свободные жирные кислоты поступают в жировые клетки и превращаются в триглицериды. Остатки хиломикронов крови захватываются гепатоцитами, подвергаются эндоцитозу и разрушаются в лизосомах. В печени формируются липопротеиды для транспорта синтезированных в ней липидных молекул. Это липопротеиды очень низкой и липопротеиды низкой плотности, которые транспортируют из печени к другим тканям триглицериды, холестерин. Липопротеиды низкой плотности захватываются из крови клетками тканей с помощью липопротеидных рецепторов, эндоцитируются, высвобождают для нужд клеток холестерин и разрушаются в лизосомах. В случае избыточного накопления в крови липопротеидов низкой плотности, они захватываются макрофагами и другими лейкоцитами. Эти клетки, накапливая метаболически низкоактивные эфиры холестерина, становятся одними из компонентов атеросклеротических бляшек сосудов. Липопротеиды высокой плотности транспортируют избыточный холестерин и его эфиры из тканей в печень, где они превращаются в желчные кислоты, которые выводятся из организма. Кроме того, липопротеиды высокой плотности используются для синтеза стероидных гормонов в надпочечниках. Как простые, так и сложные липидные молекулы могут синтезироваться в организме, за исключением ненасыщенных линолевой, линоленовой и арахидоновой жирных кислот, которые должны поступать с пищей. Эти незаменимые кислоты входят в состав молекул фосфолипидов. Из арахидоновой кислоты образуются простагландины, простациклины, тромбоксаны, лейкотриены. Отсутствие или недостаточное поступление в организм незаменимых жирных кислот приводит к задержке роста, нарушению функции почек, заболеваниям кожи, бесплодию. Биологическая ценность пищевых липидов определяется наличием в них незаменимых жирных кислот и их усвояемостью. Сливочное масло и свиной жир усваиваются на 93 – 98%, говяжий – на 80 – 94%, подсолнечное масло – на 86 -90%, маргарин – на 94 -98%.Обмен углеводов
Углеводы являются основным источником энергии, а также выполняют в организме пластические функции, в ходе окисления глюкозы образуются промежуточные продукты – пентозы, которые входят в состав нуклеотидов и нуклеиновых кислот. Глюкоза необходима для синтеза некоторых аминокислот, синтеза и окисления липидов, полисахаридов. Организм человека получает углеводы главным образом в виде растительного полисахарида крахмала и в небольшом количестве в виде животного полисахарида гликогена. В желудочно-кишечном тракте осуществляется их расщепление до уровня моносахаридов (глюкозы, фруктозы, лактозы, галактозы). Моносахариды, основным из которых является глюкоза, всасываются в кровь и через воротную вену поступают в печень. Здесь фруктоза и галактоза превращаются в глюкозу. Внутриклеточная концентрация глюкозы в гепатоцитах близка к ее концентрации в крови. При избыточном поступлении в печень глюкозы она фосфорилируется и превращается в резервную форму ее хранения – гликоген. Количество гликогена может составлять у взрослого человека 150 – 200 г. В случае ограничения потребления пищи, при снижении уровня глюкозы в крови происходит расщепление гликогена и поступление глюкозы в кровь. В течение первых 12 часов и более после приема пищи поддержа-ние концентрации глюкозы крови обеспечивается за счет распада гликогена в печени. После истощения запасов гликогена усиливается синтез ферментов, обеспечивающих реакции глюконеогенеза – синтеза глюкозы из лактата или аминокислот. В среднем за сутки человек потребляет 400 – 500 г углеводов, из которых обычно 350 – 400 г составляет крахмал, а 50- 100 г – моно- и дисахариды. Избыток углеводов депонируется в виде жира.Обмен воды и минеральных веществ
Содержание воды в организме взрослого человека составляет в среднем 73,2±3% от массы тела. Водный баланс в организме поддерживается за счет равенства объемов потерь воды и ее поступления в организм. Суточная потребность в воде колеблется от 21 до 43 мл/кг (в среднем 2400 мл) и удовлетворяется за счет поступления воды при питье («1200 мл), с пищей («900 мл) и воды, образующейся в организме в ходе обменных процессов (эндогенной воды («300 мл). Такое же количество воды выводится в составе мочи («1400 мл), кала («100 мл), посредством испарения с поверхности кожи и дыхательных путей («900 мл). Потребность организма в воде зависит от характера питания. При питании преимущественно углеводной и жирной пищей и при небольшом поступлении NaCl потребности в воде меньше. Пища, богатая белками, а также повышенный прием соли обусловливают большую потребность в воде, которая необходима для экскреции осмотически активных веществ (мочевины и минеральных ионов). Недостаточное поступление в организм воды или ее избыточная потеря приводят к дегидратации, что сопровождается сгущением крови, ухудшением ее реологических свойств и нарушением гемодинамики. Недостаток в организме воды в объеме 20% от массы тела ведет к летальному исходу. Избыточное поступление воды в организм или снижение ее объемов, выводимых из организма, приводит к водной интоксикации. В результате повышенной чувствительности нервных клеток и нервных центров к уменьшению осмолярности водная интоксикация может сопровождаться мышечными судорогами. Обмен воды и минеральных ионов в организме тесно взаимосвязаны, что обусловлено необходимостью поддержания осмотического давления на относительно постоянном уровне во внеклеточной среде и в клетках. Осуществление ряда физиологических процессов (возбуждения, синоптической передачи, сокращения мышцы)невозможно без поддержания в клетке и во внеклеточной среде определенной концентрации Na+, К+, Са2+ и других минеральных ионов. Все они должны поступать в организм с пищей.Питание
Исходным материалом для создания живой ткани и ее постоянного обновления, а также единственным источником энергии для человека и животных является пища. Поэтому рациональное питание является важнейшим фактором, обеспечивающим здоровье человека. Питание – это процесс поступления, переваривания, всасывания и усвоения в организме пищевых веществ (нутриентов). Для поддержания процессов жизнедеятельности питание должно обеспечивать все пластические и энергетические потребности организма. С пищей организм получает вещества, необходимые для биосинтеза, обновления биологических структур. Энергия поступающих в организм питательных веществ преобразуется и используется для синтеза компонентов клеточных мембран и органелл клетки, для выполнения механической, химической, осмотической и электрической работы. Биологическая и энергетическая ценность пищевых продуктов определяется содержанием в них питательных веществ: белков, жиров, углеводов, витаминов, минеральных солей, органических кислот, воды, ароматических и вкусовых веществ. Важное значение имеют такие свойства питательных веществ, как их перевариваемость и усвояемость. Потребность организма в пластических веществах может быть удовлетворена тем минимальным уровнем их потребления с пищей, который будет уравновешивать потери структурных белков, липидов и углеводов при поддержании энергетического баланса. Эти потребности индивидуальны и зависят от таких факторов, как возраст человека, состояние здоровья, интенсивность и вид труда.Теоретические основы питания
Каждому человеку необходим собственный набор компонентов рациона, отвечающий индивидуальным особенностям его обмена веществ. Согласно теории сбалансированного питания (А. А. Покровский) – полноценное питание характеризуется оптимальным соответствием количества и соотношений всех компонентов пищи физиологическим потребностям организма. Принимаемая пища должна с учетом ее усвояемости восполнять энергетические затраты человека, которые определяются как сумма основного обмена, специфического динамического действия пищи и расхода энергии на выполняемую работу. При регулярном превышении суточной калорийности пищи над затратами энергии происходит увеличение количества депонированного жира. Например, ежедневное употребление сверх нормы одной сдобной булочки (300 ккал) в течение года может привести к отложению 5,4- 10,8 кг жира. В рационе должны быть сбалансированы белки, жиры и углеводы. Среднее соотношение их энергетической ценности должно составлять – 15:30:55%, что обеспечивает энергетические и пластические потребности организма. Должны быть сбалансированы белки с незаменимыми и заменимыми аминокислотами, жиры с разной насыщенностью жирных кислот, углеводы с разным числом мономеров и наличием балластных веществ (целлюлоза, пектин и др.). Согласно теории адекватного питания (А. М. Уголев), важно соответствие набора пищевых веществ ферментному составу пищеварительной системы. В ней подчеркивается трехэтапность пищеварения и необходимость индивидуальной адекватности питания этим этапам. Например, при недостаточности лактазы молоко является неадекватным видом пищи. В этой теории считается, что первичный поток нутриентов формируется в результате переваривания и всасывания пищи, но кроме него есть поток вторичных пищевых веществ, который образуется в результате деятельности микроорганизмов кишечника. Из компонентов пищи с участием микроорганизмов образуются вещества, которые обладают не только энергетической и пластической ценностью, но и способностью влиять на многие физиологические процессы (иммунные, защитные, поведенческие).Принципы составления пищевых рационов
Питание должно точно соответствовать потребностям организма в пластических веществах и энергии, минеральных солях, витаминах и воде, обеспечивать нормальную жизнедеятельность, хорошее самочувствие, высокую работоспособность, сопротивляемость инфекциям, рост и развитие организма.При составлении пищевого рациона (т. е. количества и состава продуктов питания, необходимых человеку в сутки) следует соблюдать ряд принципов. 1. Калорийность пищевого рациона должна соответствовать энергетическим затратам организма, которые определяются видом трудовой деятельности. 2. Учитывается калорическая ценность питательных веществ, для этого используются специальные таблицы, в которых указано процентное содержание в продуктах белков, жиров и углеводов и калорийность 100 г продукта. 3. Используется закон изодинамии питательных веществ, т. е. взаимозаменяемость белков, жиров и углеводов, исходя из их энергетической ценности. Например, 1 г жира (9,3 ккал) можно заменить 2,3 г белка или углеводов. Однако такая замена возможна только на короткое время, так как питательные вещества выполняют не только энергетическую, но и пластическую функцию. 4. В пищевом рационе должно содержаться оптимальное для данной группы работников количество белков, жиров и углеводов, например, для работников 1-й группы в суточном рационе должно быть 80 120 г белка, 80-100 г жира, 400-600 г углеводов. 5. Соотношение в пищевом рационе количества белков, жиров и углеводов должно быть 1:1,2:4. 6. Пищевой рацион должен полностью удовлетворять потребность организма в витаминах, минеральных солях и воде, а также содержать все незаменимые аминокислоты (полноценные белки). 7. Не менее одной трети суточной нормы белков и жиров должно поступать в организм в виде продуктов животного происхождения. 8. Необходимо учитывать правильное распределение калорийности рациона по отдельным приемам пищи. Первый завтрак должен содержать примерно 25 – 30% всего суточного рациона, второй завтрак – 10 -15%, обед 40 -45% и ужин – 15 – 20%.
Фармакологические средства, влияющие на процессы обмена веществ
К числу препаратов, влияющих на обмен веществ относятся прежде всего гормоны, их аналоги и антигормональные препараты. Гормоны гипофиза: кортикотропин (влияет на белковый и углеводный обмен), тиротропин (стимулирует функцию щитовидной железы), соматотропин (оказывает анаболическое действие), адипозин (активирует липолитические ферменты, гонадотропины). Препараты, стимулирующие и тормозящие функцию щитовидной железы, небольшие дозы тироксина оказывают анаболический эффект, большие – приводят к усиленному распаду белка. Мерказолил – синтетическое антитиреоидное вещество, вызывает уменьшение синтеза тироксина, понижает основной обмен. Тестостерон и его аналоги, помимо специфического действия, оказывают стимулирующее действие на белковый анаболизм. Использованию этих соединений в качестве лечебных анаболических веществ препятствует их выраженное андрогенное действие. Анаболические стероиды (метандростенолон, феноболин, силаболин), синтетические препараты, близкие по химическому строению к тестостерону, но обладающие более избирательным анаболическим действием (андрогенные свойства у них менее выражены), оказывают положительное влияние на азотистый обмен, способствуют фиксации кальция в костях, увеличивают массу мышц. Существенную роль в обмене веществ играют витамины и их аналоги (витамин А, витамин В1). При патологических процессах, требующих улучшения углеводного обмена, применяется кокарбоксилаза, которая является простетической группой (коферментом) ферментов, участвующих в процессах углеводного обмена. Углеводный обмен улучшает никотиновая кислота (витамин РР), которая является простетической группой ферментов, осуществляющих окислительно-восстановительные процессы. Пиридоксин (витамин В6) входит в состав ферментов, осуществляющих декарбоксилирование и переаминирование аминокислот, участвует в обмене триптофана, метионина, цистеина, глутаминовой и других аминокислот. Цианокобаламин (витамин В12) является фактором роста, необходимым для нормального кроветворения и созревания эритроцитов, участвует в образовании холина, метионина, креатина, нуклеиновых кислот. Этот витамин в организме животных не образуется, его синтез в природе осуществляется микроорганизмами, живущими в кишечнике. Липоевая кислота является коферментом, участвующим в окислительном декарбоксилировании пировиноградной кислоты и а-кетокислот, и играет важную роль в энергетическом обмене. В регуляции окислительно-восстановительных процесов, углеводного обмена, в регенерации тканей и в образовании стероидных гормонов участвует аскорбиновая кислота (витамин С). Эргокальциферол (витамин D2) регулирует обмен фосфора и кальция, содействует всасыванию этих веществ кишечником и отложению их в растущих костях. Витамин Е и соединения, близкие к нему по химической природе и биологическому действию (токоферолы), участвуют в биосинтезе гема и белков, применяются при мышечных дистрофиях. Для парентерального питания используют ряд препаратов, являющихся растворами аминокислот и простейших пептидов (гидролизин, аминокровин, фибриносол и др.). Метаболические процессы стимулируют производные пиримидина и тиазолина. Оротовая кислота является одним из предшественников пиримидиновых нуклеотидов, входящих в состав нуклеиновых кислот, которые участвуют в синтезе белковых молекул, применяется как общий стимулятор обменных процессов.Глава 11. Терморегуляция
Температура окружающей среды оказывает большое влияние на физиологическую активность живых организмов. В разных регионах Земли температура колеблется от -50" во время арктической зимы до +60°С летом в некоторых пустынях. Температурный диапазон, в котором способны функционировать живые клетки, составляет около 50°. Живые клетки замерзают при нескольких градусах ниже 0°С. Кристаллы льда, которые образуются при замерзании тканей, разрушают клеточные структуры. Однако некоторые животные способны восстанавливать свою жизнедеятельность после размораживания. При температурах выше 45°С происходит денатурация белков, т. е. в этих условиях функционирование организма невозможно. Температура способна влиять на метаболизм живой ткани, так как скорость биохимических реакций зависит от температуры. Зависимость скорости химической реакции от температуры описывается уравнением Аррениуса. При изучении влияния температуры на скорость реакции можно путем сравнения этой скорости при двух разных температурах определить температурный коэффициент. Разница температур, равная 10°С, стала стандартным диапазоном, по которому определяют температурную чувствительность биологических систем. В этом случае температурный коэффициент, обозначаемый О10. рассчитывают из уравнения Вант-Гоффа. Согласно правилу Вант-Гоффа скорость химических реакций возрастает при повышении температуры на 10°С примерно в 2–3 раза. В животном мире существует несколько основных способов реагирования на внешнюю температуру. У пойкилотермных (холоднокровных) животных, к которым относятся большинство беспозвоночных и низших позвоночных, температура тела зависит от температуры окружающей среды. Интенсивность энергетических процессов и уровень активности пойкилотермных организмов определяются температурой внешней среды (рис. 27). У пойкилотермиых животных температура тела близка к температуре воздуха. Гомойотермные сохраняют температуру тела на сравнительно постоянном уровне в широком диапазоне температур воздуха
В процессе эволюции у млекопитающих и птиц выработалась способность сохранять одинаковую температуру внутренних частей тела, несмотря на ее изменения в окружающей среде (терморегуляция), что обеспечивает относительное постоянство метаболических процессов и делает организм менее зависимым от внешних изменений. Такие организмы называются гомойотермными (теплокровными), их отличают от пойкилотермиых организмов, близких по массе, значительно более высокий уровень энергетического обмена и относительно независимый от температуры окружающей среды уровень активности. Интенсивность обмена энергии на единицу массы тела у гомойотермных животных даже после разрушения центров терморегуляции как минимум в 3 раза превышает интенсивность обмена у пойкилотермиых (при одинаковой температуре).
Поскольку гомойотермные организмы могут поддерживать постоянную температуру, а следовательно, постоянный уровень активности независимо от окружающей температуры, они имеют превосходство над пойкилотермными животными. Вместе с тем, пойкилотермия дает преимущество в том случае, когда пищевые ресурсы ограничены или подвержены сезонным изменениям.
Есть животные, которые обладают способностью переходить на некоторое время из гомойотермного состояния в пойкилотермное и наоборот. Такой переход наблюдается у животных, впадающих в зимнюю спячку (сурки, суслики, сони и др.), отчего они получили название гетеротермных. Гетеротермия – это особое состояние, при котором гомойотермные животные на время выключают терморегуляцию и температура их тела снижается до пределов, отличных приблизительно на ГС от окружающей среды. Гетеротермия является свойством, приобретенным в процессе эволюции позже, чем гомойотермия, и имеет важное значение для приспособления организма к неблагоприятным условиям (например, к недостатку пищи, воды).
Животных можно также классифицировать по тем источникам тепла, которые они используют для поддержания температуры тела. Эктотермные, например рептилии, используют для этого наружное тепло; эндотермные, и в частности человек, используют тепло метаболического происхождения.
У пойкилотермиых животных температура тела близка к температуре воздуха. Гомойотермные сохраняют температуру тела на сравнительно постоянном уровне в широком диапазоне температур воздуха
В процессе эволюции у млекопитающих и птиц выработалась способность сохранять одинаковую температуру внутренних частей тела, несмотря на ее изменения в окружающей среде (терморегуляция), что обеспечивает относительное постоянство метаболических процессов и делает организм менее зависимым от внешних изменений. Такие организмы называются гомойотермными (теплокровными), их отличают от пойкилотермиых организмов, близких по массе, значительно более высокий уровень энергетического обмена и относительно независимый от температуры окружающей среды уровень активности. Интенсивность обмена энергии на единицу массы тела у гомойотермных животных даже после разрушения центров терморегуляции как минимум в 3 раза превышает интенсивность обмена у пойкилотермиых (при одинаковой температуре).
Поскольку гомойотермные организмы могут поддерживать постоянную температуру, а следовательно, постоянный уровень активности независимо от окружающей температуры, они имеют превосходство над пойкилотермными животными. Вместе с тем, пойкилотермия дает преимущество в том случае, когда пищевые ресурсы ограничены или подвержены сезонным изменениям.
Есть животные, которые обладают способностью переходить на некоторое время из гомойотермного состояния в пойкилотермное и наоборот. Такой переход наблюдается у животных, впадающих в зимнюю спячку (сурки, суслики, сони и др.), отчего они получили название гетеротермных. Гетеротермия – это особое состояние, при котором гомойотермные животные на время выключают терморегуляцию и температура их тела снижается до пределов, отличных приблизительно на ГС от окружающей среды. Гетеротермия является свойством, приобретенным в процессе эволюции позже, чем гомойотермия, и имеет важное значение для приспособления организма к неблагоприятным условиям (например, к недостатку пищи, воды).
Животных можно также классифицировать по тем источникам тепла, которые они используют для поддержания температуры тела. Эктотермные, например рептилии, используют для этого наружное тепло; эндотермные, и в частности человек, используют тепло метаболического происхождения.
Температура тела и тепловой баланс
Возможность процессов жизнедеятельности ограничена узким пределом температуры внутренней среды, в котором могут происходить основные ферментативные реакции. Для человека снижение температуры тела ниже 25° и ее увеличение выше 43°, как правило, смертельно, особенно чувствительны к изменениям температуры нервные клетки. Температура тела зависит от двух факторов: интенсивности образования тепла (теплопродукции) и величины потерь тепла (теплоотдачи). Главным условием поддержания постоянной тем-пературы тела гомойотермных животных, в том числе и человека, является достижение устойчивого баланса теплопродукции и теп-лоотдачи. Такой баланс описывается уравнением M±EH±Et±EK-EK±S=О, где М – метаболическая теплопродукция; Ея – излучение; ЕТ – теплопроведение; Ек – конвекция; Ет – испарение; S – накопление тепла; плюс означает приток, минус – теплоотдачу. Тепло может быть получено или отдано путем излучения, теплопроведения и конвекции в зависимости от условий внешней среды. Тепло всегда образуется в качестве побочного продукта биохимических реакций, протекающих в организме, поэтому метаболизм всегда имеет положительный знак, а испарение – отрицательный. Противоположная реакция – конденсация практически не влияет на тепловой баланс у человека. Вся высвобождающаяся в организме при биологическом окислении питательных веществ энергия в конечном счете превращается в тепло. Чем интенсивнее протекание обменных процессов, тем больше теплообразование в организме. Скорость биологического окисления возрастает при увеличении температуры. Взаимозависимость обменных процессов и теплообразования не приводит к самоускорению величины обмена и температуры, так как прирост температуры тела сопровождается увеличением отдачи тепла. Оптимальное соотношение теплопродукции и теплоотдачи обеспечивается совокупностью физиологических процессов, называемых терморегуляцией. Различают химическую и физическую терморегуляцию.Химическая терморегуляция
Этот вид регуляции температуры осуществляется за счет изменения уровня обмена веществ, что ведет к повышению или понижению образования тепла в организме. Суммарная теплопродукция в организме складывается из первичной теплоты, выделяющейся в ходе постоянно протекающих во всех тканях реакций обмена веществ, и вторичной теплоты, образующейся при расходовании энергии макроэргических соединений на выполнение определенной работы. Интенсивность метаболических процессов неодинакова в различных органах и тканях, поэтому их вклад в общую теплопродукцию неравнозначен. Наибольшее количество тепла образуется в мышцах при их напряжении и сокращении. Образование тепла в мышцах при этих условиях получило название сократительного термогенеза. Сократительный термогенез является основным механизмом дополнительного теплообразования у взрослого человека. У новорожденных, а также у мелких млекопитающих имеется механизм ускоренного теплообразования за счет возрастания скорости окисления жирных кислот бурого жира, который расположен в межлопаточной области, вдоль крупных сосудов грудной и брюшной полостей, в затылочной области шеи. Такой оттенок ей придают многочисленные, в сравнении с белой жировой тканью, окончания симпатических нервных волокон и митохондрии, содержащиеся в клетках этой ткани. Масса бурой жировой ткани достигает у взрослого 0,1% массы тела. У детей содержание бурого жира больше, чем у взрослых. В митохондриях жировых клеток имеется полипептид, способный разобщать идущие здесь процессы окисления и образования АТФ. Результатом этого является образование в этой ткани значительно большего количества тепла, чем в белой жировой ткани. Этот механизм получил название несократительного термогенеза.Физическая терморегуляция
Под физической терморегуляцией понимают совокупность физиологических процессов, ведущих к изменению уровня теплоотдачи. При повышении температуры окружающей среды теплоотдача увеличивается, а при понижении – уменьшается. Различают следующие механизмы отдачи тепла в окружающую среду: излучение, теплопроведение, конвекцию и испарение. Излучение – это отдача тепла в виде электромагнитных волн инфракрасного диапазона (а = 5 – 20 мкм). Все предметы с температурой выше абсолютного нуля (-273°С) отдают энергию путем излучения. Электромагнитная радиация свободно проходит через вакуум, атмосферный воздух также можно считать прозрачным для электромагнитных волн. Количество тепла, рассеиваемого организмом в окружающую среду излучением, пропорционально площади поверхности изучения (площадь поверхности тех частей тела, которые соприкасаются с воздухом) и разности средних значений температур кожи и окружающей среды. При температуре окружающей среды 20°С и относительной влажности воздуха 40 – 60% организм взрослого человека рассеивает путем излучения около 40 – 50% всего отдаваемого тепла. Излучение с поверхности тела возрастает при повышении температуры кожи и уменьшается при ее понижении. Если температуры поверхности кожи и окружающей среды выравниваются, отдача тепла излучением прекращается. Если температура окружающей среды превышает температуру кожи, тело человека согревается, поглощая инфракрасные лучи, выделяемые средой. Теплопроведение (кондукция) – отдача тепла при непосредственном соприкосновении тела с другими физическими объектами. Сухой воздух, жировая ткань характеризуются низкой теплопроводностью и являются теплоизоляторами. Влажный, насыщенный водяными парами воздух, вода имеют высокую теплопроводность. Поэтому пребывание при низкой температуре в среде с высокой влажностью сопровождается усилением теплопотерь организма. Влажная одежда теряет свои теплоизолирующие свойства. Конвекция – теплоотдача, осуществляемая путем переноса тепла движущимися частицами воздуха (воды). Конвекционный теплообмен, в отличие от теплопроведения, связан с обменом не только энергии, но и молекул. Это происходит потому, что вокруг всех предметов существует пограничный слой воздуха или жидкости, толщина которого зависит от окружающих условий. Когда тело окружено неподвижным воздухом, от кожи отходит теплый воздух, который, переходя в окружающий воздух, переносит как энергию, так и молекулы. Такой процесс называется свободной конвекцией. Если окружающий воздух движется, то толщина пограничного слоя зависит от скорости движения воздуха. Пограничный слой, равный при неподвижном воздухе нескольким миллиметрам, при ветре может уменьшиться до нескольких микронов. Теплообмен такого типа в значительной степени зависит от скорости движения воздуха и называется принудительной конвекцией. Для рассеяния тепла конвекцией требуется обтекание поверхности тела потоком воздуха с более низкой температурой. Непосредственно контактирующий с кожей слой воздуха нагревается, снижает свою плотность, поднимается и замещается более холодным и плотным воздухом. В условиях, когда температура воздуха равна 20°С, а относительная влажность – 40 – 60%, тело взрослого человека рассеивает в окружающую среду путем теплопроведения и конвекции около 25 – 30% тепла. Количество отдаваемого конвекцией тепла увеличивается при возрастании скорости движения воздушных потоков (ветер, вентиляция). Испарение – это отдача тепла в окружающую среду за счет испарения пота или влаги с поверхности кожи и слизистых дыхательных путей. При температуре внешней среды около 20°С испарение составляет около 36 г/ч. На испарение 1 г воды затрачивается 0,58 ккал тепловой энергии, т. е. путем испарения организм человека отдает в этих условиях около 20% всего рассеиваемого тепла. Повышение внешней температуры, выполнение физической работы усиливают потоотделение, и оно может возрасти до 500 – 2000 г/ч. Если внешняя температура превышает среднее значение температуры кожи, то организм не может отдавать во внешнюю среду тепло излучением, конвекцией и теплопроведением, поэтому единственным способом рассеяния тепла становится усиление испарения влаги с поверхности тела. Такое испарение возможно до тех пор, пока влажность воздуха окружающей среды остается меньше 100%. При интенсивном потоотделении, высокой влажности и малой скорости движения воздуха капельки пота, не успевая испариться, стекают с поверхности тела, теплоотдача путем испарения становится менее эффективной.Температура тела человека и ее измерение
Температура тела гомойотермных организмов является сложной функцией теплопродукции в разных тканях, переноса тепла в результате циркуляции крови и локальных температурных градиентов. Поскольку тепло отдается в окружающую среду главным образом через кожу, температура поверхностных тканей (оболочки), как правило, ниже температуры более глубоких тканей (ядра). В понятие «гомойотермное ядро» включают ткани человеческого тела, расположенные на глубине 1 см от поверхности и более. Температура поверхностных тканей неравномерна: она выше на участках тела, хорошо снабжаемых кровью или закрытых одеждой, т. е. зависит, с одной стороны, от интенсивности переноса к ней тепла кровью, а с другой – от охлаждающего или согревающего действия температуры внешней среды. В конечностях существует продольный (осевой) температурный градиент и радиальный (перпендикулярный поверхности) температурный градиент. В связи с неравномерностью геометрических форм человеческого тела пространственное распределение температуры тела описывается сложной трехмерной функцией. Например, когда легко одетый человек находится в помещении с температурой воздуха 20°С, температура глубокой мышечной части бедра составляет примерно 35°С, температура глубоких слоев икроножной мышцы 33°С, а в центре стопы лишь 27 – 28°С. Температура глубоких тканей тела распределена более равномерно и составляет около 36,7 -37,0°С (рис. 28). Температура ядра – одна из важнейших констант гомеостаза, определяющая скорость биохимических реакций, конформационные изменения биологически важных молекул, а следовательно, и уровень активности всех клеток организма. Однако и она не является постоянной ни в пространственном, ни во временном отношении. Даже в головном мозге существует радиальный температурный градиент более чем в ГС от центральной части до коры. Суточные колебания внутренней температуры в условиях относительного покоя находятся в пределах ГС. Максимального значения температура тела достигает в 18 – 20 часов и снижается до своего минимума во время ночного сна, к 4 -6 часам утра. Суточные изменения температуры ядра основаны на эндогенном ритме (биологические часы), который обычно синхронизирован с внешними датчиками времени. Во время путешествий с пересечением земных меридианов требуется 1 – 2 недели для того, чтобы температурный ритм пришел в соответствие с местным временем. На суточный ритм могут накладываться ритмы с более длительными периодами. Наиболее отчетливо проявляется температурный ритм, синхронизированный с менструальным циклом.
Колебания температуры тела, вызванные изменениями внешней температуры, выражены в значительно большей степени вблизи поверхности тела и в концевых частях конечностей, т. е. можно выделить «пойкилотермную» оболочку и «гомойотермную» сердцевину (ядро). При охлаждающем действии температуры внешней среды масса ядра уменьшается, а при согревании – возрастает. Наиболее близко среднее значение температуры ядра тела отражает температура крови в полостях сердца, аорте и других крупных сосудах. В качестве показателя температуры глубоких тканей тела обычно используют значения ректальной, подъязычной и подмышечной температуры, а также температуры в наружном слуховом проходе. Температуру мозга хорошо отражает температура барабанной перепонки. Для клинических целей предпочтительно измерение ректальной температуры, подъязычная температура обычно на 0,2 – 0,5°С ниже ректальной. Подмышечная температура также может служить показателем внутренней температуры, поскольку если рука плотно прижата к туловищу, температурные градиенты смещаются так, что граница внутреннего слоя доходит до подмышечной впадины, однако это требует длительного времени (в ряде случаев до 30 мин).
Температура ядра – одна из важнейших констант гомеостаза, определяющая скорость биохимических реакций, конформационные изменения биологически важных молекул, а следовательно, и уровень активности всех клеток организма. Однако и она не является постоянной ни в пространственном, ни во временном отношении. Даже в головном мозге существует радиальный температурный градиент более чем в ГС от центральной части до коры. Суточные колебания внутренней температуры в условиях относительного покоя находятся в пределах ГС. Максимального значения температура тела достигает в 18 – 20 часов и снижается до своего минимума во время ночного сна, к 4 -6 часам утра. Суточные изменения температуры ядра основаны на эндогенном ритме (биологические часы), который обычно синхронизирован с внешними датчиками времени. Во время путешествий с пересечением земных меридианов требуется 1 – 2 недели для того, чтобы температурный ритм пришел в соответствие с местным временем. На суточный ритм могут накладываться ритмы с более длительными периодами. Наиболее отчетливо проявляется температурный ритм, синхронизированный с менструальным циклом.
Колебания температуры тела, вызванные изменениями внешней температуры, выражены в значительно большей степени вблизи поверхности тела и в концевых частях конечностей, т. е. можно выделить «пойкилотермную» оболочку и «гомойотермную» сердцевину (ядро). При охлаждающем действии температуры внешней среды масса ядра уменьшается, а при согревании – возрастает. Наиболее близко среднее значение температуры ядра тела отражает температура крови в полостях сердца, аорте и других крупных сосудах. В качестве показателя температуры глубоких тканей тела обычно используют значения ректальной, подъязычной и подмышечной температуры, а также температуры в наружном слуховом проходе. Температуру мозга хорошо отражает температура барабанной перепонки. Для клинических целей предпочтительно измерение ректальной температуры, подъязычная температура обычно на 0,2 – 0,5°С ниже ректальной. Подмышечная температура также может служить показателем внутренней температуры, поскольку если рука плотно прижата к туловищу, температурные градиенты смещаются так, что граница внутреннего слоя доходит до подмышечной впадины, однако это требует длительного времени (в ряде случаев до 30 мин).
Система терморегуляции
Терморегуляция – это совокупность физиологических процессов, деятельность которых направлена на поддержание относительного постоянства температуры ядра в условиях изменения температуры среды с помощью регуляции теплоотдачи и теплопродукции. Терморегуляция направлена на предупреждение нарушений теплового баланса организма или на его восстановление, если такие изменения уже произошли. Система терморегуляции состоит из ряда элементов со взаимосвязанными функциями. Информация о температуре приходит от периферических и центральных терморецепторов (датчиков) по афферентным нервам к центру терморегуляции в гипоталамусе. Этот центр обрабатывает поступившую информацию и посылает команды эффекторам (исполнительным звеньям), т. е. активирует различные механизмы, которые обеспечивают изменение теплопродукции и теплоотдачи. По своей работе система терморегуляции аналогична системе автоматизированного контроля с отрицательной обратной связью, которая противодействует изменениям температуры, вызванным внешними и внутренними возмущениями. Температура ядра поддерживается на определенном уровне, и величина реакции эффекторов пропорциональна отклонению истинной температуры от этого уровня.Рефлекторные и гуморальные механизмы терморегуляции
Терморецепторы
Функции терморецепторов выполняют специализированные нервные клетки, имеющие особо высокую чувствительность к температурным воздействиям. Они расположены в различных частях тела: коже, скелетных мышцах, кровеносных сосудах, во внутренних органах (в желудке, кишечнике, матке, мочевом пузыре), в дыхательных путях, в спинном мозге, ретикулярной формации, среднем мозге, гипоталамусе, коре больших полушарий и в других отделах ЦНС. Много термочувствительных нейронов в медиальной преоптической области переднего гипоталамуса. Можно выделить три группы терморецепторов: экстерорецепторы (расположены в коже), интерорецепторы (сосуды, внутренние органы), центральные терморецепторы (ЦНС). Наиболее изучены терморецепторы кожи. Больше всего их на коже лица и шеи. Кожные терморецепторы бывают двух типов – холодовые и тепловые. Оба типа особенно чувствительны к степени изменения температуры. Холодовые рецепторы резко повышают частоту импульсации в ответ на охлаждение и снижают ее, когда температура увеличивается. Тепловые рецепторы реагируют на изменение температуры противоположным образом. На поверхности тела количественно преобладают холодочувствительные терморецепторы. Холодовые рецепторы располагаются на глубине 0,17 мм от поверхности кожи, их около 250 тысяч. Тепловые рецепторы находятся глубже – 0,3 мм от поверхности, их примерно 30 тысяч. При любой совместимой с жизнью температуре от периферических рецепторов в ЦНС поступает стационарная информация. Разряды тепловых рецепторов наблюдаются в диапазоне температур от 20 до 50°, а холодовых – от 10 до 41°С. При температуре ниже 10° холодовые рецепторы и нервные волокна гомойотермных животных блокируются. При температуре выше 45° холодовые рецепторы могут вновь активироваться, что объясняет феномен парадоксального ощущения холода, наблюдаемый при сильном нагревании. Усиление активности холодовых и тепловых рецепторов наблюдается вплоть до 50°, при более высоких температурах терморецепторы повреждаются. При температуре 47 – 48°С наряду с терморецепторами начинают возбуждаться и болевые рецепторы. Этим объясняют необычную остроту парадоксального ощущения холода. Возбуждение рецепторов зависит как от абсолютных значений температуры кожи в месте раздражения, так и от скорости и степени ее изменения. Одни рецепторы реагируют на перепад температуры в 0,1°, другие – в 1°, а третьи возбуждаются лишь при достижении разницы в 10°. Для холодовых рецепторов оптимум чувствительности (генерация импульсации максимальной частоты) лежит в пределах 25 – 30°, для тепловых в пределах – 38 – 43°С. В этих областях минимальные изменения температуры вызывают наибольшую реакцию рецепторов.Центры терморегуляции
Информация от кожных рецепторов идет по чувствительным нервным волокнам типа А-дельта (от холодовых рецепторов) и С, поэтому в ЦНС она доходит с разной скоростью. Афферентный поток нервных импульсов от терморецепторов поступает через задние корешки спинного мозга к вставочным нейронам задних рогов, по спиноталамическому тракту этот поток достигает передних ядер таламуса, откуда часть информации после переключения проводится в соматосенсорную кору больших полушарий, а часть – в гипоталамические центры терморегуляции. Часть афферентного потока импульсов от терморецепторов кожи и внутренних органов поступает по более древним (спиноталамическому и спиноретикулярному) трактам, восходящим в ретикулярную формацию, неспецифические ядра таламуса, медиальную преоптическую область гипоталамуса и в ассоциативные зоны коры головного мозга. Кора больших полушарий, участвуя в переработке температурной информации, обеспечивает условно-рефлекторную регуляцию теплопродукции и теплоотдачи. Сильные терморегуляторные реакции вызывают природные условные раздражители, сопровождающие на протяжении всей жизни организма его охлаждение или нагревание (вид снега, льда, яркое солнце и т. д.). Высшие отделы ЦНС (кора и лимбическая система) обеспечивают возникновение субъективных температурных ощущений (холодно, прохладно, тепло, жарко), мотивационных возбуждений и поведения, направленного на поиск более комфортной среды. На теплопродукцию и теплоотдачу организма влияют многие нервные структуры. Интеграция различной сенсорной информации, связанной с тепловым балансом, и регуляция температуры тела осуществляются главным центром терморегуляции, расположенным в гипоталамусе. Разрушение этого участка гипоталамуса или нарушение его нервных связей (перерезка на уровне среднего мозга) ведет к утрате способности регулировать температуру тела. В терморегуляторном центре обнаружены различные по функциям группы нервных клеток – термочувствительные нейроны; клетки, определяющие уровень поддерживаемой в организме температуры тела; в переднем гипоталамусе расположены нейроны, управляющие процессами теплоотдачи, а в заднем гипоталамусе – процессами теплопродукции. После разрушения центров переднего гипоталамуса физиологическая активность в условиях холода сохраняется, но в условиях жары температура тела быстро повышается. Разрушение центров заднего гипоталамуса нарушает способность к усилению энергетического обмена в холодной среде, и температура тела в этих условиях падает. Термочувствительные нервные клетки способны различать разницу температуры в 0,0 ГС крови, протекающей через мозг. Данные о температуре передаются в группу нервных клеток гипоталамуса, задающих в организме уровень регулируемой температуры тела – «установочную точку» терморегуляции. На основе анализа и сравнения значений средней температуры тела и заданной величины температуры механизмы «установочной точки» через эффекторные нейроны гипоталамуса воздействуют на процессы теплоотдачи или теплопродукции, чтобы привести в соответствие фактическую и заданную температуру. Посредством центра терморегуляции устанавливается равновесие между теплопродукцией и теплоотдачей. Имеются данные о том, что соотношение в гипоталамусе концентраций ионов натрия и кальция определяет «заданный» уровень температуры. Изменение концентрации этих ионов приводит к изменению уровня температуры тела. В терморегуляции принимают участие и гуморальные факторы – прежде всего гормоны щитовидной железы (тироксин и др.) и надпочечников (адреналин и др.). Снижение температуры вызывает увеличение концентрации этих гормонов в крови. Эти гормоны усиливают окислительные процессы, что сопровождается увеличением теплообразования. Адреналин суживает периферические сосуды, что приводит к снижению теплоотдачи.Участие эффекторов в регуляции температуры
Процессы, которые обеспечивают температурный гомеостаз, можно разделить на следующие группы: 1. поведенческие механизмы (перемещение в среде с целью поиска комфортных температурных условий); 2. вегетативные механизмы (сосудистые реакции, изменение интенсивности метаболизма; 3. адаптивные механизмы, или акклиматизация.Обычно гомойотермные организмы одновременно используют все эти способы. В термонейтральных условиях внешней среды гомойотермные животные могут регулировать температуру тела, изменяя лишь величину теплоотдачи. Подобная терморегуляция включает в себя вазомоторные реакции, изменение позы (уменьшение или увеличение величины, участвующей в теплообмене поверхности тела), пиломоторные реакции (изменение теплоизолирующей эффективности шерстного покрова, у человека они сохранились в рудиментарном виде). В этих условиях баланс теплопродукции и теплоотдачи достигается преимущественно с помощью сосудодвигательных реакций. Подкожная жировая клетчатка плохо проводит тепло, поэтому переход тепла от внутренних органов к поверхности тела происходит медленно, и регуляция интенсивности теплоотдачи в основном осуществляется за счет перераспределения крови между кожными покровами и внутренними органами. В печени, мозге, почках температура выше, чем в других тканях, так как обменные процессы в них протекают с большой скоростью и образуется много тепла. Обладая высокой теплоемкостью, кровь переносит тепло к тканям с низким уровнем теплообразования, что обеспечивает выравнивание температуры в различных частях тела (рис. 29).
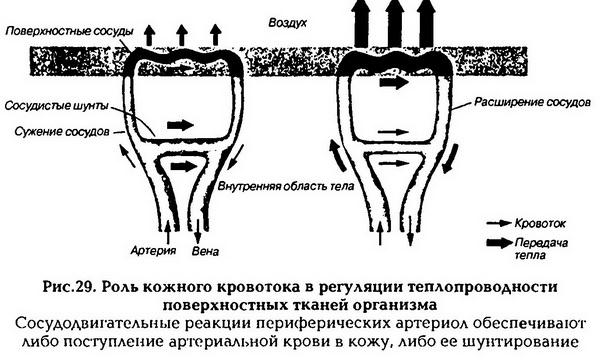 Конвекция тепла из внутренних областей тела к оболочке за счет изменения кровотока является важным способом регуляции теплоотдачи. Если в центре терморегуляции величины средней интегральной температуры и установленной температуры не совпадают, включаются механизмы, которые, изменяя кровоток в сосудах поверхности тела, увеличивают или уменьшают величину теплоотдачи организма, что достигается посредством симпатических влияний на просвет сосудов. При отклонении средней температуры тела на небольшую величину от установочной температуры имеющиеся различия легко компенсируются за счет изменения интенсивности отдачи тепла без существенного изменения теплопродукции.
Конвекция тепла из внутренних областей тела к оболочке за счет изменения кровотока является важным способом регуляции теплоотдачи. Если в центре терморегуляции величины средней интегральной температуры и установленной температуры не совпадают, включаются механизмы, которые, изменяя кровоток в сосудах поверхности тела, увеличивают или уменьшают величину теплоотдачи организма, что достигается посредством симпатических влияний на просвет сосудов. При отклонении средней температуры тела на небольшую величину от установочной температуры имеющиеся различия легко компенсируются за счет изменения интенсивности отдачи тепла без существенного изменения теплопродукции.
Терморегуляция при изменениях температуры внешней среды
Холодовое воздействие
В ответ на охлаждение происходит возбуждение холодовых рецепторов кожи, импульсация от них поступает в центры гипоталамуса. От центра терморегуляции идут сигналы к эффекторам, в результате прежде всего уменьшается потоотделение, изменяется поза, происходит снижение притока крови на периферию посредством сужения сосудов. При воздействии холода сосуды кожи, главным образом артериолы, суживаются, поэтому большая часть крови поступает в сосуды внутренних областей тела. В поверхностных слоях кожи циркулирует меньшее количество крови, кожа охлаждается, поэтому уменьшается излучение и проведение тепла в окружающую среду. У человека по мере прохождения крови по крупным артериям рук и ног ее температура значительно снижается. Прохладная венозная кровь, возвращаясь внутрь тела по сосудам, расположенным близ артерий, получает большую долю тепла, отдаваемого артериальной кровью (противоточный теплообмен), что способствует возвращению части тепла к внутренним областям тела. При температуре воздуха, близкой к нулю, такая система не выгодна, так как в результате интенсивного обмена тепла между артериальной и венозной кровью температура конечностей может упасть ниже точки замерзания (отморожение). При более интенсивном холодовом воздействии, когда, несмотря на сужение поверхностных сосудов и минимальное потоотделение, уровень средней температуры становится ниже, чем величина установочной температуры, активизируются процессы теплопродукции.Это может происходить за счет механизмов теп-лопродукции: 1. сократительного термогенеза – продукции тепла в результате сокращения скелетных мышц (произвольная активность локомоторного аппарата; терморегуляционный тонус; холодовая мышечная дрожь); 2. несократительного (недрожательного) термогенеза – продукции тепла за счет активации гликолиза, гликогенолиза и липолиза в скелетных мышцах, печени, в буром жире.
При охлаждении происходит увеличение притока афферентных нервных импульсов от холодовых рецепторов кожи в гипоталамус. В результате его нейроны возбуждаются и посылают через ядра среднего и продолговатого мозга поток эфферентных нервных импульсов к мотонейронам спинного мозга, которые усиливают ритмическую импульсацию, идущую к скелетным мышцам шеи, туловища и конечностей. Первоначально это проявляется в росте тонического напряжения мышцы, сокращений она при этом не совершает. При сравнительно слабом охлаждении в мышцах при их видимом покое возникают одиночные сокращения отдельных волокон, что позволяет повысить общую теплопродукцию на 20 – 40%. В терморегуляционный тонус последовательно вовлекаются мышцы подбородка, шеи, верхнего плечевого пояса, туловища, сгибатели конечностей. Этим объясняется принятие определенной позы, уменьшающей площадь поверхности тела, контактирующей с внешней средой. При дальнейшем охлаждении, когда начинается снижение внутренней температуры организма, возникают непроизвольные периодические сокращения скелетной мускулатуры (холодовая дрожь). В этом случае совершается минимальная механическая работа, и почти вся метаболическая энергия в мышце освобождается в виде тепла. Теплопродукция организма человека при холодовой мышечной дрожи увеличивается в 2 – 3 раза и более. Одновременно через симпатический отдел вегетативной нервной системы и железы внутренней секреции происходит стимуляция обмена веществ, т. е. несократительного термогенеза. При действии холода нарастает выработка тропных гормонов гипофиза, происходит выброс катехоламинов из надпочечников и тироксина из щитовидной железы. Эти гормоны активируют ферменты, катализирующие гликогенолиз в скелетных мышцах и печени, а также липолиз в жировой ткани. В кровоток выделяются и в последующем окисляются с образованием большого количества тепла свободные жирные кислоты и глюкозофосфаты. Под влиянием гормонов происходит разобщение процессов окисления и фосфорилирования, поэтому большая часть энергии превращается в тепло. Норадреналин и адреналин вызывают быстрое, но непродолжительное повышение теплопродукции. Более продолжительное усиление обменных процессов достигается под влиянием гормонов щитовидной железы – тироксина и трийодтиронина. За счет сократительного и несократительного термогенеза теплообразование может возрастать в 3–5 раз по сравнению с теплообразованием в условиях относительного покоя.
Тепловое воздействие
При повышении температуры окружающей среды, прямом действии теплового излучения, увеличении теплопродукции организма (мышечная работа) поддержание температурного гомеостаза осуществляется главным образом за счет регуляции теплоотдачи. Ответная реакция организма на действие высоких температур выражается прежде всего в расширении поверхностных кровеносных сосудов, повышении температуры кожи, усилении потоотделения, возникновении тепловой одышки, изменении поведения и позы, способствующих интенсивной теплоотдаче, происходит также незначительное снижение уровня обмена веществ. Повышение температуры среды воспринимается тепловыми рецепторами, импульсация от них поступает в центры гипоталамуса. В ответ происходит рефлекторное расширение сосудов кожи (вследствие снижения симпатического вазоконстрикторного тонуса), в результате кожный кровоток резко усиливается и кожа приобретает красный цвет, ее температура повышается иизбыток тепла рассеивается от поверхности тела за счет теплоизлучения, теплопроведения и конвекции. Кровь возвращается к внутренним областям тела по венам, лежащим под самой поверхностью кожи, минуя противоточный теплообменник, благодаря чему снижается количество тепла, которое она получает от артериальной крови. Близость этих вен к кожной поверхности увеличивает охлаждение венозной крови, возвращающейся к внутренним областям тела. У человека максимальное расширение сосудов кожи от состояния максимального сужения уменьшает общую величину теплоизоляции кожного покрова в среднем в б раз. Не все участки поверхности кожи равноценно участвуют в теплоотдаче. Особое значение имеют кисти рук, от них может быть отведено до 60% теплопродукции основного обмена, хотя их площадь составляет лишь около 6% от общей поверхности тела. Если уровень температуры тела, несмотря на расширение поверхностных сосудов, продолжает увеличиваться, в действие вступает другая реакция физической терморегуляции – происходит резкое усиление потоотделения. Процесс просачивания воды через эпителий и последующего ее испарения называется неощутимой перспирацией. За счет этого процесса поглощается примерно 20% теплопродукции основного обмена. Неощутимая перспирация не регулируется и мало зависит от температуры окружающей среды. Поэтому при угрозе перегревания симпатическая нервная система стимулирует работу потовых желез. Возбуждаются эфферентные нейроны центра теплоотдачи, которые активируют симпатические нейроны и постганглионарные волокна, идущие к потовым железам и являющиеся холинергическими, ацетилхолин повышает активность потовых желез за счет взаимодействия с их М-холинорецепторами. В условиях очень высокой температуры отдача тепла путем испарения пота становится единственным способом поддержания теплового баланса. В насыщенном водяными парами теплом воздухе испарение жидкости с поверхности кожи ухудшается, теплоотдача затрудняется и температурный гомеостаз может нарушиться.Адаптация к длительным изменениям температуры
Процессы акклиматизации основаны на определенных изменениях в органах и функциональных системах, которые развиваются только под влиянием продолжительных (несколько недель, месяцев) температурных воздействий. Тепловая адаптация играет решающую роль для жизни в условиях тропиков или пустынь. Ее основной характеристикой является значительное увеличение интенсивности потоотделения (примерно в три раза), в течение коротких интервалов времени потоотделение может достигать 4 л в 1 час. В ходе адаптации содержание электролитов в поте заметно снижается, что уменьшает опасность их чрезмерной потери. Усиливается способность ощущать жажду при данном уровне потерь воды с потом, что необходимо для поддержания водного баланса. У лиц, длительно проживающих в жарком климате, по сравнению с неадаптированными реакция выделения пота и расширения сосудов кожи начинается при температуре примерно на 0,5°С более низкой. В условиях продолжительного действия холода у людей развивается ряд приспособительных реакций. Их вид зависит от характера воздействий. Может возникнуть толерантная адаптация, при которой порог развития дрожи и интенсификации обменных процессов смещается в сторону более низких значений температуры. Например, аборигены Австралии могут провести целую ночь почти раздетые при температуре, близкой к нулю, без развития дрожи. Если воздействие холода более длительно или температура окружающей среды ниже нуля, такая форма адаптации становится непригодной. У эскимосов и других жителей Севера выработался другой механизм (метаболическая адаптация): у них интенсивность основного обмена стала на 25 – 50% выше. Однако для большинства людей характерна не столько физиологическая, сколько поведенческая адаптация к холоду, т. е. использование теплой одежды и обогреваемых жилищ.Гипотермия и гипертермия. Лихорадка
Нарушения терморегуляции могут возникать при повреждении центральных и периферических аппаратов температурной чувствительности (кровоизлияния, опухоли в области гипоталамуса, некоторые инфекции), а также после травматических перерывов проводящих путей. Они могут приводить к развитию состояний, для которых характерно отклонение от нормы температуры тела, что сопровождается разнообразными нарушениями жизнедеятельности. Значительные отклонения температуры тела от нормы могут возникнуть и при чрезмерно сильных изменениях температуры окружающей среды. Если, несмотря на активацию обмена веществ, величина теплопродукции организма становится меньше величины теплоотдачи, возникает понижение температуры тела, получившее название переохлаждения, или гипотермии. Развитию гипотермии способствуют факторы, увеличивающие теплоотдачу, например, холодный воздух, движущийся с высокой скоростью, повышенная влажность. Переохлаждение развивается в три стадии. Во время I стадии, компенсации, при снижении температуры среды обитания уменьшается теплоотдача и увеличивается теплопродукция, но этих механизмов недостаточно для сохранения нормальной температуры тела. Во II стадии, переходной, вследствие нарушения механизмов терморегуляции периферические сосуды расширяются, поэтому теплоотдача увеличивается и температура тела начинает быстро понижаться. В III стадии, декомпенсации, теплоотдача еще более возрастает, а теплопродукция снижается, вследствие чего организм становится пойкилотермным и принимает температуру окружающей среды. В этот период снижается активность ЦНС и возникает сон, происходит угнетение дыхания и кровообращения. Искусственную гипотермию используют при проведении некоторых операций для повышения резистентности организма к недостатку кислорода и уменьшения дозы, необходимых для операции наркотических средств. Противоположное состояние организма, сопровождающееся повышением температуры тела, – гипертермия возникает, когда интенсивность теплопродукции превышает способность организма отдавать тепло. При подъеме температуры тела в результате потери жидкости с потом уменьшается объем циркулирующей крови и повышается ее осмотическое давление. Организм в этих условиях стремится сохранить водный гомеостаз, даже если это идет в ущерб терморегуляторным реакциям, поэтому отдача тепла за счет потоотделения уменьшается, и температура тела устанавливается на более высоком уровне. Развивается чувство жажды, уменьшается диурез. Гипертермия наиболее легко развивается в условиях действия на организм внешней температуры, превышающей 37°С при 100% влажности воздуха, когда испарение пота или влаги с поверхности тела становится невозможным. В случае продолжительной гипертермии может возникнуть «тепловой удар». Это состояние организма характеризуется покраснением кожи в результате расширения периферических сосудов, отсутствием потоотделения, признаками нарушения функций ЦНС (нарушение ориентации, бред, судороги). В более легких случаях гипертермии может проявиться тепловой обморок, когда в результате резкого расширения периферических сосудов про-исходит падение артериального давления. В процессе эволюции выработана особая ответная реакция организма на действие пирогенных факторов – лихорадка (пирексия, жар, горячка). Она является защитным механизмом, направленным против вирусов, микроорганизмов и чужеродных веществ. По степени подъема температуры различают: субфебрильную лихорадку (повышение температуры до 38°), умеренную (38–39°) и чрезмерную (выше 41°). Лихорадка – это состояние организма, при котором центр терморегуляции стимулирует повышение температуры тела. Это достигается перестраиванием механизма «установочной точки» на более высокую, чем в норме, температуру регуляции. Группа нейронов, осуществляющих анализ текущей средней температуры тела и ее сравнение с новым установленным значением, воспринимает нормальную температуру ядра тела как низкую. Включаются механизмы, активизирующие теплопродукцию (повышение терморегуляционного тонуса мышц, мышечная дрожь) и снижающие интенсивность теплоотдачи (сужение сосудов поверхности тела, принятие позы, уменьшающей площадь соприкосновения поверхности тела с внешней средой). Хотя субъективно в это время человек ощущает озноб, на самом деле температура тела повышается и вскоре достигает нового, установленного уровня регуляции. С этого момента начинается уравновешивание процессов выработки и отдачи тепла. В результате дрожь, как один из наиболее эффективных способов теплопродукции, исчезает, расширяются поверхностные сосуды, повышается температура кожи и поверхностных тканей. С момента, когда в организме достигается баланс интенсивностей теплопродукции и теплоотдачи, возникает ощущение тепла и исчезает озноб. Переход «установочной точки» на более высокий уровень происходит в результате действия на соответствующую группу нейронов преоптической области гипоталамуса эндогенных пирогенов – веществ, вызывающих подъем температуры тела. К ним относят: полисахариды дрожжей, липотейхоевую кислоту грамположительных микробов, белковые экзотоксины микробов, различные аллергены, лектины, содержащиеся в растительных продуктах, продукты активации комплемента, комплексы антиген-антитело, продукты распада собственных тканей после их поступления в кровь. Все они сами по себе не способны вызывать лихорадку, поэтому их называют экзогенными пирогенами. Попав в кровь, они активируют высвобождение из лейкоцитов эндогенного пирогена (лейкоцитарного пирогена) – интерлейкина. Выработка эндогенных пирогенов происходит в нейтрофилах, эозинофилах, моноцитах, гистиоцитах, клетках Купфера. Эндогенными пирогенами являются пептиды: интерлейкины в формах а и р, фактор некроза опухолей, а-интерферон и другие.Влияние фармакологических препаратов на температуру тела
Для человека снижение температуры тела ниже 25°С и ее увеличение выше 43°С, как правило, смертельно. Особенно чувствительны к изменениям температуры нервные клетки. Как было показано выше, температура оказывает глубокое влияние на жизненные процессы организма. Однако правило Вант-Гоффа вполне оправдывается только для химических реакций in vivo. Для сложных химических процессов в клетках и тканях оно имеет относительное значение. Одним из важных факторов, ограничивающих его значение, является влияние нервной системы на интенсивность обмена веществ. Выключение центральной нервной системы (например, при наркозе или алкогольном опьянении) приводит к большей зависимости интенсивности обмена веществ от температуры внешней среды. Иногда в послеоперационном периоде наблюдается озноб (вследствие расширения сосудов и теплопотери во время операции). У детей с врожденной патологией костной и мышечной ткани во время наркоза (особенно фторотанового) велика опасность возникновения злокачественной гипертермии (причина ее пока не ясна), сопровождающейся судорогами и имеющей в большинстве случаев летальный исход. Уже после применения небольших доз этанола происходит угнетение сосудодвигательного центра, приводящее к расширению сосудов кожи, увеличению теплоотдачи и к появлению субъективного ощущения тепла. Такое расширение сосудов кожи иногда используют при обморожениях, резком охлаждении организма, но человек при этом должен находиться в теплом помещении, иначе повышенная теплоотдача приведет к еще большему охлаждению и гибели. Существует две группы препаратов, способных влиять на терморегуляцию: средства, устраняющие чувство жара и снижающие повышенную температуру до нормальной (жаропонижающие средства), и препараты, способные понизить нормальную температуру, т. е. обладающие гипотермическим действием.К первой группе относятся ненаркотические анальгетики (анальгетики-антипиретики), по химическому строению их можно разделить: 1. на салицилаты (аспирин, салициламид, метилсалицилин); 2. производные пиразолона (антипирин, амидопирин, анальгин, бутадион); 3. производные парааминофенола (парацетамол, фенацитин).
Они применяются при лихорадочных состояниях для снижения температуры, способны снижать возбуждение центров терморегуляции. Жаропонижающий эффект этих средств заключается в снижении лихорадочной, но не нормальной температуры тела. Лихорадка является следствием повышения концентрации в цереброспинальной жидкости простагландина Е,, что обусловлено активностью эндогенных или экзогенных пирогенов, В результате нарушается нормальное соотношение между ионами натрия и кальция в нейронах терморегулирующих структур головного мозга, изменяется их активность, что сопровождается возрастанием теплопродукции и уменьшением теплоотдачи. Эти препараты, тормозя образование простагландина Е, восстанавливают нормальную активность нейронов центров терморегуляции.
Нормализация температуры тела происходит прежде всего за счет увеличения теплоотдачи, что обеспечивается тремя основными механизмами: 1. расширением сосудов оболочки 2. повышением потоотделения (стимуляция функции потовых желез) 3. увеличением легочной вентиляции (повышение частоты дыхания и дыхательного объема).
Температуру тела способна снижать и другая группа анальгетиков – нестероидные противовоспалительные препараты (вольтарен, ибупрофен, индометацин), но они в клинике с этой целью не используются, а применяются только как противовоспалительные средства. Механизм их жаропонижающего действия тот же, что и у анальгетиков-антипиретиков (он один для всей группы не-наркотических анальгетиков). Препараты отличаются лишь выраженностью эффекта. К средствам, способным понизить нормальную температуру тела (гипотермические средства), относятся нейролептики и прежде всего производные фенотиазина (аминазин, френолон, трифтазин). Их гипотермическое действие обусловлено тем, что они уменьшают способность организма адаптироваться к снижению температуры окружающей среды, т. е. сам препарат не способен снизить температуру, для этого необходимо действие внешних охлаждающих факторов. Этот эффект возникает в результате угнетения адренои серотонинорецепторов в гипоталамических центрах, расширения периферических сосудов и увеличения теплоотдачи, а также вследствие понижения активности дыхательных ферментов тканей и уменьшения образования тепла. В психиатрических клиниках нейролептики могут применяться в больших дозах и пациенты могут сохранять нормальную температуру в комфортных условиях, но если они выходят на улицу, то это может привести к заметному переохлаждению в холодное время года, а при жаре возможно развитие гипертермии, хотя этот эффект возникает значительно реже. Иногда нейролептики используются для создания искусственной гипотермии при проведении хирургических операций: больного помещают в специальную ванну, заполненную холодной водой, и снижают температуру его тела. Вызванное холодом замедление метаболических процессов предоставляет врачу дополнительное время для действий, а также позволяет использовать для наркоза минимальные дозы наркотических препаратов. В экспериментах на животных было показано, что, используя g-оксибутират натрия (ГОМК), можно создать глубокую гипотермию с сохранением сердечной деятельности при температуре ниже 10ºС, а также гипотермию с сохранением бодрствования (до 10–20°С), при которой животное способно поддерживать нормальную позу, сохранять рефлекторную деятельность, при этом на ЭЭГ регистрируется биоэлектрическая активность, характерная для периода бодрствования. Применение ГОМК в сочетании с гидрохиноном и глицерином позволяет достичь состояния длительной гипотермии (4 дня на уровне 20 – 25°С).
Глава 12. Выделение. Физиология почек
В процессе жизнедеятельности в организме человека образуются значительные количества продуктов обмена, которые уже не используются клетками и должны быть удалены из организма. Кроме того, организм должен быть освобожден от токсичных и чужеродных веществ, от избытка воды, солей, лекарственных препаратов. Иногда процессам выделения предшествует обезвреживание токсических веществ, например в печени. Так, такие вещества, как фенол, индол, скатол, соединяясь с глюкуроновой и серной кислотами, превращаются в менее вредные вещества. Органы, выполняющие выделительные функции, называются выделительными, или экскреторными. К ним относят почки, легкие, кожу, печень и желудочно-кишечный тракт. Главное назначение органов выделения – это поддержание постоянства внутренней среды организма. Экскреторные органы функционально взаимосвязаны между собой. Сдвиг функционального состояния одного из этих органов меняет активность другого. Например, при избыточном выведении жидкости через кожу при высокой температуре снижается объем диуреза. Нарушение процессов выделения неизбежно ведет к появлению патологических сдвигов гомеостаза вплоть до гибели организма. Легкие и верхние дыхательные пути удаляют из организма углекислый газ и воду. Кроме того, через легкие выделяется большинство ароматических веществ, как, например, пары эфира и хлороформа при наркозе, сивушные масла при алкогольном опьянении. При нарушении выделительной функции почек через слизистую оболочку верхних дыхательных путей начинает выделяться мочевина, которая разлагается, определяя соответствующий запах аммиака изо рта. Слизистая оболочка верхних дыхательных путей способна выделять йод из крови. Печень и желудочно-кишечный тракт выводят с желчью из организма ряд конечных продуктов обмена гемоглобина и других порфиринов в виде желчных пигментов, конечные продукты обмена холестерина в виде желчных кислот. В составе желчи из организма экскретируются также лекарственные препараты (антибиотики), бромсульфалеин, фенолрот, маннит, инулин и др. Желудочно-кишечный тракт выделяет продукты распада пищевых веществ, воду, вещества, поступившие с пищеварительными соками и желчью, соли тяжелых металлов, некоторые лекарственные препараты и ядовитые вещества (морфий, хинин, салицилаты, ртуть, йод), а также красители, используемые для диагностики заболеваний желудка (метиленовый синий, или конгорот). Кожа осуществляет выделительную функцию за счет деятельности потовых и в меньшей степени сальных желез. Потовые железы удаляют воду, мочевину, мочевую кислоту, креатинин, молочную кислоту, соли щелочных металлов, особенно натрия, органические вещества, летучие жирные кислоты, микроэлементы, пепсиноген, амилазу и щелочную фосфатазу. Роль потовых желез в удалении продуктов белкового обмена возрастает при заболеваниях почек, особенно при острой почечной недостаточности. С секретом сальных желез из организма выделяются свободные жирные и неомыляемые кислоты, продукты обмена половых гормонов.Функции почек
Почки являются основным органом выделения. Они выполняют в организме много функций.Одни из них прямо или косвенно связаны с процессами выделения, другие – не имеют такой связи. 1. Выделительная, или экскреторная, функция. Почки удаляют из организма избыток воды, неорганических и органических веществ, продукты азотистого обмена и чужеродные вещества: мочевину, мочевую кислоту, креатинин, аммиак, лекарственные препараты. 2. Регуляция водного баланса и соответственно объема крови, вне- и внутриклеточной жидкости (волюморегуляция) за счет изменения объема выводимой с мочой воды. 3. Регуляция постоянства осмотического давления жидкостей внутренней среды путем изменения количества выводимых осмотически активных веществ: солей, мочевины, глюкозы (осморегуляция). 4. Регуляция ионного состава жидкостей внутренней среды и ионного баланса организма путем избирательного изменения экскреции ионов с мочой (ионная регуляция). 5. Pei-уляция кислотно-основного состояния путем экскреции водородных ионов, нелетучих кислот и оснований. 6. Образование и выделение в кровоток физиологически активных веществ: ренина, эритропоэтина, активной формы витамина D, простагландинов, брадикининов, урокиназы (инкреторная функция). 7. Регуляция уровня артериального давления путем внутренней секреции ренина, веществ депрессорного действия, экскреции натрия и воды, изменения объема циркулирующей крови. 8. Регуляция эритропоэза путем внутренней секреции гуморального регулятора эритрона – эритропоэтина. 9. Регуляция гемостаза путем образования гуморальных регуляторов свертывания крови и фибринолиза – урокиназы, тромбопластина, тромбоксана, а также участия в обмене физиологического антикоагулянта гепарина. 10. Участие в обмене белков, липидов и углеводов (метаболическая функция). 11. Защитная функция: удаление из внутренней среды организма чужеродных, часто токсических веществ.
Следует учитывать, что при различных патологических состояниях выделение лекарств через почки иногда существенно нарушается, что может приводить к значительным изменениям переносимости фармакологических препаратов, вызывая серьезные побочные эффекты вплоть до отравлений.
Строение нефрона
Основной структурно-функциональной единицей почки является нефрон, в котором происходит образование мочи. В зрелой почке человека содержится около 1 – 1,3 мл нефронов. Нефрон состоит из нескольких последовательно соединенных отделов (рис.30). Начинается нефрон с почечного (мальпигиева) тельца, которое содержит клубочек кровеносных капилляров. Снаружи клубочки покрыты двухслойной капсулой Шумлянского – Боумена. Внутренняя поверхность капсулы выстлана эпителиальными клетками. Наружный, или париетальный, листок капсулы состоит из базальной мембраны, покрытой кубическими эпителиальными клетками, переходящими в эпителий канальцев. Между двумя листками капсулы, расположенными в виде чаши, имеется щель или полость капсулы, переходящая в просвет проксимального отдела канальцев. Проксимальный отдел канальцев начинается извитой частью, которая переходит в прямую часть канальца. Клетки проксимального отдела имеют щеточную каемку из микроворсинок, обращенных в просвет канальца.
Затем следует тонкая нисходящая часть петли Генле, стенка которой покрыта плоскими эпителиальными клетками. Нисходящий отдел петли опускается в мозговое вещество почки, поворачивает на 180° и переходит в восходящую часть петли нефрона.
Дистальный отдел канальцев состоит из восходящей части петли Генле и может иметь тонкую и всегда включает толстую восходящую часть. Этот отдел поднимается до уровня клубочка своего же нефрона, где начинается дистальный извитой каналец.
Этот отдел канальца располагается в коре почки и обязательно соприкасается с полюсом клубочка между приносящей и выносящей артериолами в области плотного пятна.
Дистальные извитые канальцы через короткий связующий отдел впадают в коре почек в собирательные трубочки. Собирательные трубочки опускаются из коркового вещества почки в глубь мозгового вещества, сливаются в выводные протоки и открываются в полости почечной лоханки. Почечные лоханки открываются в мочеточники, которые впадают в мочевой пузырь.
Проксимальный отдел канальцев начинается извитой частью, которая переходит в прямую часть канальца. Клетки проксимального отдела имеют щеточную каемку из микроворсинок, обращенных в просвет канальца.
Затем следует тонкая нисходящая часть петли Генле, стенка которой покрыта плоскими эпителиальными клетками. Нисходящий отдел петли опускается в мозговое вещество почки, поворачивает на 180° и переходит в восходящую часть петли нефрона.
Дистальный отдел канальцев состоит из восходящей части петли Генле и может иметь тонкую и всегда включает толстую восходящую часть. Этот отдел поднимается до уровня клубочка своего же нефрона, где начинается дистальный извитой каналец.
Этот отдел канальца располагается в коре почки и обязательно соприкасается с полюсом клубочка между приносящей и выносящей артериолами в области плотного пятна.
Дистальные извитые канальцы через короткий связующий отдел впадают в коре почек в собирательные трубочки. Собирательные трубочки опускаются из коркового вещества почки в глубь мозгового вещества, сливаются в выводные протоки и открываются в полости почечной лоханки. Почечные лоханки открываются в мочеточники, которые впадают в мочевой пузырь.
По особенностям локализации клубочков в коре почек, строения канальцев и особенностям кровоснабжения различают 3 типа нефронов: 1. суперфициальные (поверхностные) 2. интракортикальные 3. юкстамедуллярные.
Кровоснабжение почек
Отличительной особенностью кровоснабжения почек является то, что кровь используется не только для трофики органа, но и для образования мочи. Почки получают кровь из коротких почечных артерий, которые отходят от брюшного отдела аорты. В почке артерия делится на большое количество мелких сосудов-артериол, приносящих кровь к клубочку. Приносящая (афферентная) артериола входит в клубочек и распадается на капилляры, которые, сливаясь, образуют выносящую (эфферентную) артериолу. Диаметр приносящей артериолы почти в 2 раза больше, чем выносящей, что создает условия для поддержания необходимого артериального давления (70 мм рт.ст.) в клубочке. Мышечная стенка у приносящей артериолы выражена лучше, чем у выносящей. Это дает возможность регуляции просвета приносящей артериолы. Выносящая артериола вновь распадается на сеть капилляров вокруг проксимальных и дистальных канальцев. Артериальные капилляры переходят в венозные, которые, сливаясь в вены, отдают кровь в нижнюю полую вену. Капилляры клубочков выполняют только функцию мочеобразования. Особенностью кровоснабжения юкстамедуллярного нефрона является то, что эфферентная артериола не распадается на околоканальцевую капиллярную сеть, а образует прямые сосуды, которые вместе с петлей Генле спускаются в мозговое вещество почки и участвуют в осмотическом концентрировании мочи. Через сосуды почки в 1 мин проходит около 1/4 объема крови, выбрасываемого сердцем в аорту. Почечный кровоток условно делят на корковый и мозговой. Максимальная скорость кровотока приходится на корковое вещество (область, содержащую клубочки и проксимальные канальцы) и составляет 4 – 5 мл/мин на 1 г ткани, что является самым высоким уровнем органного кровотока. Благодаря особенностям кровоснабжения почки давление крови в капиллярах сосудистого клубочка выше, чем в капиллярах других областей тела, что необходимо для поддержания нормального уровня клубочковой фильтрации. Процесс мочеобразования требует создания постоянных условий кровотока. Это обеспечивается механизмами ауторегуляции. При повышении давления в приносящей артериоле ее гладкие мышцы сокращаются, уменьшается количество поступающей крови в капилляры и происходит снижение в них давления. При падении системного давления приносящие артериолы, напротив, расширяются. Клубочковые капилляры также чувствительны к ангиотензину II, простагландинам, брадикининам, вазопрессину. Благодаря указанным механизмам кровоток в почках остается постоянным при изменении системного артериального давления в пределах 100- 150ммрт. ст. Однако при ряде стрессовых ситуаций (кровопотеря, эмоциональный стресс и т. д.) кровоток в почках может уменьшаться.Юкстагломерулярный аппарат
Юкстагломерулярный (ЮГА), или околоклубочковый, аппарат представляет собой совокупность клеток, синтезирующих ренин и другие биологически активные вещества. Морфологически он образует как бы треугольник, две стороны которого составляют подходящая к клубочку афферентная и выходящая эфферентная артериолы, а основание – специализированный участок стенки извитой части дистального канальца – плотное пятно (macula densa). В состав ЮГА входят гранулярные клетки (юкстагломерулярные), расположенные на внутренней поверхности афферентной артериолы, клетки плотного пятна и специальные клетки (юкставаскулярные), расположенные между приносящей и выносящей артериолами и плотным пятном.Механизмы мочеобразования
Мочеобразование осуществляется за счет трех последовательных процессов: 1. клубочковой фильтрации (ультрафильтрации) воды и низкомолекулярных компонентов из плазмы крови в капсулу почечного клубочка с образованием первичной мочи; 2. канальцевой реабсорбции – процесса обратного всасывания профильтровавшихся веществ и воды из первичной мочи в кровь; 3. канальцевой секреции – процесса переноса из крови в просвет канальцев ионов и органических веществ.Клубочковая фильтрация
Фильтрация воды и низкомолекулярных компонентов из плазмы крови в полость капсулы происходит через клубочковый, или гломерулярный, фильтр. Гломерулярный фильтр имеет 3 слоя: эндотелиальные клетки капилляров, базальную мембрану и эпителий висцерального листка капсулы, или подоциты. Эндотелий капилляров имеет поры диаметром 50–100 нм, что ограничивает прохождение форменных элементов крови (эритроцитов, лейкоцитов, тромбоцитов). Основным барьером для фильтрации является базальная мембрана. Поры в базальной мембране составляют 3 – 7,5 нм. Эти поры изнутри содержат отрицательно заряженные молекулы (анионные локусы), что препятствует проникновению отрицательно заряженных частиц, в том числе белков. Третий слой фильтра образован отростками подоцитов, между которыми имеются щелевые диафрагмы, которые ограничивают прохождение альбуминов и других молекул с большой молекулярной массой. Эта часть фильтра также несет отрицательный заряд. Легко фильтроваться могут вещества с молекулярной массой не более 5500, абсолютным пределом для прохождения частиц через фильтр в норме является молекулярная масса 80 000. Таким образом, состав первичной мочи обусловлен свойствами гломерулярного фильтра. В норме вместе с водой фильтруются все низкомолекулярные вещества, за исключением большей части белков и форменных элементов крови. В остальном состав ультрафильтрата близок к плазме крови. При нефропатиях, нефритах поры теряют отрицательный заряд, что приводит к прохождению через них многих белков. Такие вещества, как гепарин, способствуют восстановлению анионных локусов, а антибиотики, наоборот, уменьшают их наличие. Основным фактором, способствующим процессу фильтрации, является давление крови (гидростатическое) в капиллярах клубочков. К силам, препятствующим фильтрации, относится онкотическое давление белков плазмы крови и давление жидкости в полости капсулы клубочка, т. е. первичной мочи. Следовательно, эффективное фильтрационное давление представляет собой разность между гидростатическим давлением крови в капиллярах и суммой онкотического давления плазмы крови и внутрипочечного давления. Таким образом, фильтрационное давление составляет: 70 (30 + 20) = 20 мм рт.ст. Количественной характеристикой процесса фильтрации является скорость клубочковой фильтрации, которая определяется путем сравнения концентрации определенного вещества в плазме крови и моче. Для этого используются вещества, которые являются физиологически инертными, нетоксичными, не связывающиеся с белками в плазме крови, не реабсорбирующиеся в почечных канальцах и выделяющиеся с мочой только путем фильтрации. Таким веществом является полимер фруктозы инулин. В организме человека инулин не образуется, поэтому для измерения скорости клубочковой фильтрации его вводят внутривенно. Измеренная с помощью инулина скорость клубочковой фильтрации называется также коэффициентом очищения от инулина, или клиренсом инулина. Клиренс показывает, какой объем плазмы (в мл) очистился целиком от данного вещества за 1 мин. Сравнивая клиренсы других веществ с клиренсом инулина, можно определить процессы, участвующие в выделении этих веществ с мочой. Если клиренс вещества равен клиренсу инулина, следовательно это вещество только фильтруется. Если клиренс вещества больше клиренса инулина, значит это вещество выделяется не только за счет фильтрации, но и секреции. Если клиренс вещества меньше клиренса инулина, то вещество после фильтрации реабсорбируется. В клинике для определения скорости клубочковой фильтрации обычно используют эндогенный метаболит креатинин, концентрация которого в крови довольно стабильна. Креатинин удаляется из крови в основном путем клубочковой фильтрации, но в очень малых количествах он секретируется, поэтому его клиренс – менее точный показатель, чем клиренс инулина. Тем не менее он широко используется в клинике, так как для его измерения не требуется внутривенное введение. В норме у мужчин скорость клубочковой фильтрации составляет 125 мл/мин, а у женщин – 110 мл/мин.Канальцевая реабсорбция
Первичная моча превращается в конечную благодаря процессам, которые происходят в почечных канальцах и собирательных трубочках. В почке человека за сутки образуется 150- 180 л фильтрата, или первичной мочи, а выделяется 1,0 – 1,5 л мочи. Остальная жидкость всасывается в канальцах и собирательных трубочках. Канальцевая реабсорбция – это процесс обратного всасывания воды и веществ из содержащейся в просвете канальцев мочи в лимфу и кровь. Основной смысл реабсорбции состоит в том, чтобы сохранить организму все жизненно важные вещества в необходимых количествах. Обратное всасывание происходит во всех отделах нефрона. Основная масса молекул реабсорбируется в проксимальном отделе нефрона. Здесь практически полностью реабсорбируются аминокислоты, глюкоза, витамины, белки, микроэлементы, значительное количество ионов Na+, Сl-, НСО3- и многие другие вещества. В петле Генле, дистальном отделе канальца и собирательных трубочках всасываются электролиты и вода. Ранее считали, что реабсорбция в проксимальной части канальца является обязательной и нерегулируемой. В настоящее время доказано, что она регулируется как нервными, так и гуморальными факторами. Обратное всасывание различных веществ в канальцах может происходить пассивно и активно. Пассивный транспорт происходит без затраты энергии по электрохимическому, концентрационному или осмотическому градиентам. С помощью пассивного транспорта осуществляется реабсорбция воды, хлора, мочевины. Активным транспортом называют перенос веществ против электрохимического и концентрационного градиентов. Причем различают первично-активный и вторично-активный транспорт. Первично-активный транспорт происходит с затратой энергии клетки. Примером служит перенос ионов Na+ с помощью фермента Na+,К+–АТФазы, использующей энергию АТФ. При вторично-активном транспорте перенос вещества осуществляется за счет энергии транспорта другого вещества. Механизмом вторично-активного транспорта реабсорбируются глюкоза и аминокислоты.Глюкоза.
Она поступает из просвета канальца в клетки проксимального канальца с помощью специального переносчика, который должен обязательно присоединить ион Na+. Перемещение этого комплекса внутрь клетки осуществляется пассивно по электрохимическому и концентрационному градиентам для ионов Na+. Низкая концентрация натрия в клетке, создающая градиент его концентрации между наружной и внутриклеточной средой, обеспечивается работой натрий-калиевого насоса базальной мембраны. В клетке этот комплекс распадается на составные компоненты. Внутри почечного эпителия создается высокая концентрация глюкозы, поэтому в дальнейшем по градиенту концентрации глюкоза переходит в интерстициальную ткань. Этот процесс осуществляется с участием переносчика за счет облегченной диффузии. Далее глюкоза уходит в кровоток. В норме при обычной концентрации глюкозы в крови и, соответственно, в первичной моче вся глюкоза реабсорбируется. При избытке глюкозы в крови, а значит, в первичной моче может произойти максимальная загрузка канальцевых систем транспорта, т. е. всех молекул-переносчиков. В этом случае глюкоза больше не сможет реабсорбироваться и появится в конечной моче (глюкозурия). Эта ситуация характеризуется понятием «максимальный канальцевый транспорт» (Тм). Величине максимального канальцевого транспорта соответствует старое понятие «почечный порог выведения». Для глюкозы эта величина составляет 10 ммоль/л. Вещества, реабсорбция которых не зависит от их концентрации в плазме крови, называются непороговыми. К ним относятся вещества, которые или вообще не реабсорбируются, (инулин, маннитол) или мало реабсорбируются и выделяются с мочой пропорционально накоплению их в крови (сульфаты).Аминокислоты.
Реабсорбция аминокислот происходит также по механизму сопряженного с Na+ транспорта. Профильтровавшиеся в клубочках аминокислоты на 90% реабсорбируются клетками проксимального канальца почки. Этот процесс осуществляется с помощью вторично-активного транспорта, т. е. энергия идет на работу натриевого насоса. Выделяют не менее 4 транспортных систем для переноса различных аминокислот (нейтральных, двуосновных, дикарбоксильных и иминокислот). Эти же системы транспорта действуют и в кишечнике для всасывания аминокислот. Описаны генетические дефекты, когда определенные аминокислоты не реабсорбируются и не всасываются в кишечнике.Белок.
В норме небольшое количество белка попадает в фильтрат и реабсорбируется. Процесс реабсорбции белка осуществляется с помощью пиноцитоза. Эпителий почечного канальца активно захватывает белок. Войдя в клетку, белок подвергается гидролизу со стороны ферментов лизосом и превращается в аминокислоты. Не все белки подвергаются гидролизу, часть их переходит в кровь в неизмененном виде. Этот процесс активный и требует энергии. За сутки с конечной мочой уходит не более 20 – 75 мг белка. Появление белка в моче носит название протеинурии. Протеинурия может быть и в физиологических условиях, например, после тяжелой мышечной работы. В основном протеинурия имеет место в патологии при нефритах, нефропатиях, при миеломной болезни.Мочевина.
Она играет важную роль в механизмах концентрирования мочи, свободно фильтруется в клубочках. В проксимальном канальце часть мочевины пассивно реабсорбируется за счет градиента концентрации, который возникает вследствие концентрирования мочи. Остальная часть мочевины доходит до собирательных трубочек. В собирательных трубочках под влиянием АДГ происходит реабсорбция воды и концентрация мочевины повышается. АДГ усиливает проницаемость стенки и для мочевины, и она переходит в мозговое вещество почки, создавая здесь примерно 50% осмотического давления. Из интерстиция по концентрационному градиенту мочевина диффундирует в петлю Генле и вновь поступает в дистальные канальцы и собирательные трубочки. Таким образом совершается внутрипочечный круговорот мочевины. В случае водного диуреза всасывание воды в дистальном отделе нефрона прекращается, а мочевины выводится больше. Таким образом ее экскреция зависит от диуреза.Слабые органические кислоты и основания.
Реабсорбция слабых кислот и оснований зависит от того, в какой форме они находятся – в ионизированной или неионизированной. Слабые основания и кислоты в ионизированном состоянии не реабсорбируются и выводятся с мочой. Степень ионизации оснований увеличивается в кислой среде, поэтому они с большей скоростью экскретируются с кислой мочой, слабые кислоты, напротив, быстрее выводятся с щелочной мочой. Это имеет большое значение, так как многие лекарственные вещества являются слабыми основаниями или слабыми кислотами. Поэтому при отравлении ацетилсалициловой кислотой или фенобарбиталом (слабыми кислотами) необходимо вводить щелочные растворы (NaHCО3), для того чтобы перевести эти кислоты в ионизированное состояние, тем самым способствуя их быстрому выведению из организма. Для быстрой экскреции слабых оснований необходимо вводить в кровь кислые продукты для закисления мочи.Вода и электролиты.
Вода реабсорбируется во всех отделах нефрона. В проксимальных извитых канальцах реабсорбируется около 2/3 всей воды. Около 15% реабсорбируется в петле Генле и 15% – в дистальных извитых канальцах и собирательных трубочках. Вода реабсорбируется пассивно за счет транспорта осмотически активных веществ: глюкозы, аминокислот, белков, ионов натрия, калия, кальция, хлора. При снижении реабсорбции осмотически активных веществ уменьшается и реабсорбция воды. Наличие глюкозы в конечной моче ведет к увеличению диуреза (лолиурии). Основным ионом, обеспечивающим пассивное всасывание воды, является натрий. Натрий, как указывалось выше, также необходим для транспорта глюкозы и аминокислот. Кроме того, он играет важную роль в создании осмотически активной среды в интерстиции мозгового слоя почки, благодаря чему происходит концентрирование мочи. Реабсорбция натрия совершается во всех отделах нефрона. Около 65% ионов натрия реабсорбируется в проксимальных канальцах, 25% – в петле нефрона, 9% – в дистальном извитом канальце и 1% – в собирательных трубочках. Поступление натрия из первичной мочи через апикальную мембрану внутрь клетки канальцевого эпителия происходит пассивно по электрохимическому и концентрационному градиентам. Выведение натрия из клетки через базолатеральные мембраны осуществляется активно с помощью Na+,К+–АТФазы. Так как энергия клеточного метаболизма расходуется на перенос натрия, транспорт его является первично-активным. Транспорт натрия в клетку может происходить за счет разных механизмов. Один из них – это обмен Na+ на Н+ (противоточный транспорт, или антипорт). В этом случае ион натрия переносится внутрь клетки, а ион водорода – наружу. Другой путь переноса натрия в клетку осуществляется с участием аминокислот, глюкозы. Это так называемый котранспорт, или симпорт. Частично реабсорбция натрия связана с секрецией калия. Сердечные гликозиды (строфантин К, оубаин) способны угнетать фермент Na+,К+–АТФазу, обеспечивающую перенос натрия из клетки в кровь и транспорт калия из крови в клетку. Большое значение в механизмах реабсорбции воды и ионов натрия, а также концентрирования мочи имеет работа так называемой поворотно-противоточной множительной системы. Поворотно-противоточная система представлена параллельно рас-положенными коленами петли Генле и собирательной трубочкой, по которым жидкость движется в разных направлениях (противоточно). Эпителий нисходящего отдела петли пропускает воду, а эпителий восходящего колена непроницаем для воды, но способен активно переносить ионы натрия в тканевую жидкость, а через нее обратно в кровь. В проксимальном отделе происходит всасывание натрия и воды в эквивалентных количествах и моча здесь изотонична плазме крови. В нисходящем отделе петли нефрона реабсорбируется вода и моча становится более концентрированной (гипертонической). Отдача воды происходит пассивно за счет того, что в восходящем отделе одновременно осуществляется активная реабсорбция ионов натрия. Поступая в тканевую жидкость, ионы натрия повышают в ней осмотическое давление, тем самым способствуя притягиванию в тканевую жидкость воды из нисходящего отдела. В то же время повышение концентрации мочи в петле нефрона за счет реабсорбции воды облегчает переход натрия из мочи в тканевуюжидкость. Так как в восходящем отделе петли Генле реабсорбируется натрий, моча становится гипотоничной. Поступая далее в собирательные трубочки, представляющие собой третье колено противоточной системы, моча может сильно концентрироваться, если действует АДГ, повышающий проницаемость стенок для воды. В данном случае по мере продвижения по собирательным трубочкам в глубь мозгового вещества все больше и больше воды выходит в межтканевую жидкость, осмотическое давление которой повышено вследствие содержания в ней большого количества Na+ и мочевины, и моча становится все более концентрированной. При поступлении больших количеств воды в организм почки, наоборот, выделяют большие объемы гипотонической мочи.Канальцевая секреция
Канальцевая секреция – это транспорт веществ из крови в просвет канальцев (мочу). Канальцевая секреция позволяет быстро экскретировать некоторые ионы, например калия, органические кислоты (мочевая кислота) и основания (холин, гуанидин), включая ряд чужеродных организму веществ, таких как антибиотики (пенициллин), рентгеноконтрастные вещества (диодраст), красители (феноловый красный), парааминогиппуровую кислоту ПАГ. Канальцевая секреция представляет собой преимущественно активный процесс, происходящий с затратами энергии для транспорта веществ против концентрационного или электрохимического градиентов. В эпителии канальцев существуют разные системы транспорта (переносчики) для секреции органических кислот и органических оснований. Это доказывается тем, что при угнетении секреции органических кислот пробенецидом секреция оснований не нарушается. Транспортные секретирующие механизмы обладают свойством адаптации, т. е. при длительном поступлении вещества в кровоток количество транспортных систем за счет белкового синтеза постепенно увеличивается. Данный факт необходимо учитывать, например, при лечении пенициллином. Так как очищение крови от него постепенно возрастает, требуется увеличение дозировки для поддержания необходимой терапевтической концентрации. Так как при невысоких концентрациях в крови ПАГ или диодраста они полностью удаляются из крови при однократном про-хождении через почку путем секреции клетками проксимальных канальцев, это позволило, определяя клиренс этих веществ, получить значение объема плазмы крови, которое протекает по сосудам коркового вещества почки, т. е. эффективного почечного плазмотока. Зная гематокрит, можно рассчитать и величину коркового кровотока в почке. Кроме того, канальцевый эпителий синтезирует и секретирует вещества, образующиеся в самих клетках эпителия, например, аммиак (путем дезаминирования некоторых аминокислот), гиппуровую кислоту (из бензойной кислоты и гликокола), которые выделяются с мочой, а также ренин, простагландины, глюкозу почек, поступающие в кровь. Таким образом, состав конечной мочи зависит от процессов фильтрации, реабсорбции и секреции.Количество, состав и свойства мочи
За сутки человек выделяет в среднем около 1,5 л мочи. После обильного питья, потребления белковой пищи диурез возрастает. При потреблении небольшого количества воды, при усиленном потоотделении диурез снижается. Интенсивность мочеобразования колеблется в течение суток. Ночью мочеобразование меньше, чем днем. Моча представляет собой прозрачную жидкость светло-желтого цвета, с относительной плотностью 1005–1025, которая зависит от количества принятой жидкости. Реакция мочи здорового человека обычно слабокислая. Однако рН ее колеблется от 5,0 до 7,0 в зависимости от характера питания. При питании преимущественно белковой пищей реакция мочи становится кислой, растительной – нейтральной или даже щелочной. В моче здорового человека белок отсутствует или определяются его следы. В моче содержатся мочевина, мочевая кислота, аммиак, пуриновые основания, креатинин; в небольшом количестве – производные продуктов гниения белков в кишечнике (индол, скатол, фенол). Среди органических соединений небелкового происхождения в моче встречаются соли щавелевой кислоты, молочной кислоты, кетоновые тела. Глюкозы в моче в обычных условиях не должно быть. Эритроциты появляются в моче (гематурия) при заболеваниях почек и мочевыводящих органов. В моче содержатся пигменты (уробилин, урохром), которые и определяют цвет мочи. С мочой выделяются электролиты (Na+, К+, CI-, Са2+, Мg2+, сульфаты и др.). В моче содержатся гормоны и их метаболиты, ферменты, витамины.Регуляция объема внутрисосудистой и внеклеточной жидкости
При увеличении притока крови в левое предсердие возбуждаются волюморецепторы, расположенные здесь. Импульсы по афферентным волокнам блуждающего нерва идут в ЦНС, угнетая секрецию АДГ, что приводит к увеличению диуреза. Одновременно снижается деятельность сердца и в малый круг кровообращения поступает меньше крови. Растяжение стенки предсердия приводит к стимуляции выработки клетками предсердия натрийуретического гормона, который усиливает выделение ионов натрия и воды почкой. Все это приводит к нормализации объема циркулирующей крови (ОЦК). В регуляции ОЦК принимает участие и ренин-ангиотензин-альдостероновая система. При снижении ОЦК уменьшается ар-териальное давление, что приводит к увеличению секреции ренина. Ренин, в свою очередь увеличивает образование в крови ангиотензина II, который стимулирует секрецию альдостерона. Альдостерон вызывает повышение реабсорбции натрия в канальцах, а за ним – воды. В результате ОЦК увеличивается.Регуляция осмотического давления крови
Почки играют важную роль в осморегуляции. При обезвоживании организма в плазме крови увеличивается концентрация осмотически активных веществ, что приводит к повышению ее осмотического давления. В результате возбуждения осморецепторов, которые расположены в области супраоптического ядра гипоталамуса, а также в сердце, печени, селезенке, почках и других органах усиливается выброс АДГ из нейрогипофиза. АДГ повышает реабсорбцию воды, что приводит к задержке воды в организме, выделению осмотически концентрированной мочи. Секреция АДГ изменяется не только при раздражении осморецепторов, но и специфических натриорецепторов. При избыточном содержании воды в организме, напротив, уменьшается концентрация растворенных осмотически активных веществ в крови, снижается ее осмотическое давление. Активность осморецепторов в данной ситуации уменьшается, что вызывает снижение продукции АДГ, увеличение выделения воды почкой и снижение осмолярности мочи.Регуляция ионного состава крови
Почки, регулируя реабсорбцию и секрецию различных ионов в почечных канальцах, поддерживают их необходимую концентрацию в крови. Реабсорбция натрия регулируется альдостероном и натрийуретическим гормоном, вырабатывающимся в предсердии. Альдостерон усиливает реабсорбцию натрия в дистальных отделах канальцев и собирательных трубочках. Секреция альдостерона увеличивается при снижении концентрации ионов натрия в плазме крови и при уменьшении объема циркулирующей крови. Натрийуретический гормон угнетает реабсорбцию натрия и усиливает его выведение. Выработка натрийуретического гормона возрастает при увеличении объема циркулирующей крови и объема внеклеточной жидкости в организме. Концентрация калия в крови поддерживается за счет регуляции его секреции. Альдостерон усиливает секрецию калия в дистальном отделе канальцев и собирательных трубочках. Инсулин уменьшает выделение калия, увеличивая его концентрацию в крови, при алкалозе выделение калия увеличивается. При ацидозе – уменьшается. Паратгормон паращитовидных желез увеличивает реабсорбцию кальция в почечных канальцах и высвобождение кальция из костей, что приводит к повышению его концентрации в крови. Гормон щитовидной железы тиреокальцитонин увеличивает выделение кальция почками и способствует переходу кальция в кости, что снижает концентрацию кальция в крови. В почках образуется активная форма витамина D, который участвует в регуляции обмена кальция. В регуляции уровня хлоридов в плазме крови участвует альдостерон. При увеличении реабсорбции натрия возрастает и реабсорбция хлора. Выделение хлора может происходить и независимо от натрия.Регуляция кислотно-основного состояния
Почки принимают участие в поддержании кислотно-основного равновесия крови, экскретируя кислые продукты обмена. Активная реакция мочи у человека может колебаться в достаточно широких пределах – от 4,5 до 8,0, что способствует поддержанию рН плазмы крови на уровне 7,36. В просвете канальцев содержится бикарбонат натрия. В клетках почечных канальцев находится фермент карбоангидраза, под влиянием которой из углекислого газа и воды образуется угольная кислота. Угольная кислота диссоциирует на ион водорода и анион HCO3-. Ион Н+ секретируется из клетки в просвет канальца и вытесняет натрий из бикарбоната, превращая его в угольную кислоту, а затем в Н2О и СО2. Внутри клетки НСО3- взаимодействует с реабсорбированным из фильтрата Na+. СО2, легко диффундирующий через мембраны по градиенту концентрации, поступает в клетку и вместе с СО2, образующимся в результате метаболизма клетки, вступает в реакцию образования угольной кислоты. Секретируемые ионы водорода в просвете канальца связываются также с двузамещенным фосфатом (Na2HPО4), вытесняя из него натрий и превращая в однозамещенный – NaH2PО4. В результате дезаминирования аминокислот в почках происходит образование аммиака и выход его в просвет канальца. Ионы водорода связываются в просвете канальца с аммиаком и образуют ион аммония NH4+. Таким образом происходит детоксикация аммиака. Секреция иона Н+ в обмен на ион Na+ приводит к восстановлению резерва оснований в плазме крови и выделению избытка ионов водорода. При интенсивной мышечной работе, питании мясом моча становится кислой, при потреблении растительной пищи – щелочной.Инкреторная функция почек
Инкреторная функция почки заключается в синтезе и выведении в кровоток физиологически активных веществ, которые действуют на другие органы и ткани или обладают преимущественно местным действием, регулируя почечный кровоток и метаболизм почки. Ренин образуется в гранулярных клетках юкстагломерулярного аппарата. Ренин является протеолитическим ферментом, который приводит к расщеплению α2-глобулина – ангиотензиногена плазмы крови и превращению его в ангиотензин I. Под влиянием ангиотензинпревращающего фермента ангиотензин I превращается в активное сосудосуживающее вещество ангиотензин II. Ангиотензин II, суживая сосуды, повышает артериальное давление, стимулирует секрецию альдостерона, увеличивает реабсорбцию натрия, способствует формированию чувства жажды и питьевого поведения. Ангиотензин II вместе с альдостероном и ренином составляют одну из важнейших регуляторных систем – ренин-ангиотензин-альдостероновую систему. Ренин-ангиотензин-альдостероновая система участвует в регуляции системного и почечного кровообращения, объема циркулирующей крови, водно-электролитного баланса организма. Если давление в приносящей артериоле возрастает, то продукция ренина снижается и наоборот. Продукция ренина также регулируется плотным пятном. При большом количестве NaCl в дистальном отделе нефрона тормозится секреция ренина. Возбуждение β-адренорецепторов гранулярных клеток приводит к усилению секреции ренина, α-адренорецепторов – торможению. Простагландины типа ПГИ-2, арахидоновая кислота стимулируют продукцию ренина, ингибиторы синтеза простагландинов, например салицилаты, уменьшают продукцию ренина. В почке образуются эритропоэтины, которые стимулируют образование эритроцитов в костном мозге. Почки извлекают из плазмы крови прогормон витамин D3, образующийся в печени, и превращают его в физиологически активный гормон – витамин D3. Этот стероидный гормон стимулирует образование кальцийсвязывающего белка в клетках кишечника, регулируя реабсорбцию кальция в почечных канальцах, и способствует его освобождению из костей. Почки принимают участие в регуляции фибринолитической активности крови, синтезируя активатор плазминогена – урокиназу. В мозговом веществе почки синтезируются простагландины, которые участвуют в регуляции почечного и общего кровотока, увеличивают выделение натрия с мочой, уменьшают чувствительность клеток канальцев к АДГ. В почке образуются кинины. Почечный кинин брадикинин является сильным вазодилататором, участвующим в регуляции почечного кровотока и выделения натрия.Регуляция артериального давления
Регуляция артериального давления почкой осуществляется несколькими механизмами. Во-первых, как уже указывалось выше, в почке синтезируется ренин. Через ренин-ангиотензин-альдостероновую систему происходит регуляция сосудистого тонуса и объема циркулирующей крови. В почках синтезируются вещества и депрессорного действия: депрессорный нейтральный липид мозгового вещества, простагландины. Почка участвует в поддержании водно-электролитного обмена, объема внутрисосудистой, вне- и внутриклеточной жидкости, что является важным для уровня артериального давления. Лекарственные вещества, повышающие выведение натрия и воды с мочой (диуретики), применяются в качестве гипотензивных средств. Кроме того, почка экскретирует большинство гормонов и других физиологически активных веществ, которые являются гуморальными регуляторами артериального давления, поддерживая их необходимый уровень в крови.Метаболическая функция почек
Метаболическая функция почек заключается в поддержании во внутренней среде организма постоянства определенного уровня и состава компонентов белкового, углеводного и липидного обмена. Почки расщепляют фильтрующиеся в почечных клубочках низкомолекулярные белки, пептиды, гормоны до аминокислот и возвращают их в кровь. Почка обладает способностью к глюконеогенезу. При длительном голодании половина поступающей в кровь глюкозы образуется почками. Участие почки в обмене липидов заключается в том, что свободные жирные кислоты в ее клетках включаются в состав триацилглицеринов и фосфолипидов и в виде этих соединений поступают в кровь.Нейрогуморальная регуляция деятельности почек
Нервная регуляция
Нервная система регулирует гемодинамику почки, работу юкстагломерулярного аппарата, а также фильтрацию, реабсорбцию и секрецию. Раздражение симпатических нервов, иннервирующих почку, которые являются преимущественно ветвями чревных нервов, приводит к сужению ее кровеносных сосудов. При сужении приносящих артериол уменьшаются фильтрационное давление и фильтрация. Сужение выносящих артериол сопровождается повышением фильтрационного давления и ростом фильтрации. Стимуляция симпатических эфферентных волокон приводит к увеличению реабсорбции натрия, воды. Раздражение парасимпатических волокон, идущих в составе блуждающих нервов, вызывает усиление реабсорбции глюкозы и секреции органических кислот. При болевых раздражениях диурез рефлекторно уменьшается вплоть до полного его прекращения (болевая анурия). Механизм этого явления заключается в сужении почечных сосудов в результате возбуждения симпатической нервной системы, усилении секреции катехоламинов надпочечниками и увеличении продукции антидиуретического гормона (вазопрессина). Уменьшение и увеличение диуреза может быть вызвано условно-рефлекторным путем, что свидетельствует о выраженном влиянии высших отделов ЦНС на работу почек. ЦНС регулирует работу почек или непосредственно через вегетативные нервы, или через нейроны гипоталамуса, изменяя секрецию гормонов. В этом проявляется единство нервной и гуморальной регуляции.Гуморальная
Ведущая роль в регуляции деятельности почек принадлежит гуморальной системе. На работу почек оказывают влияние многие гормоны, главными из которых являются антидиуретический гормон (АДГ), или вазопрессин, и альдостерон. Антидиуретический гормон (АДГ), или вазопрессин, способствует реабсорбции воды в дистальных отделах нефрона путем увеличения проницаемости для воды стенок дистальных извитых канальцев и собирательных трубочек. Механизм действия АДГ заключается в активации фермента аденилатциклазы, который участвует в образовании цАМФ из АТФ. цАМФ активирует цАМФ-зависимые протеинкиназы, которые участвуют в фосфорилировании мембранных белков, что приводит к повышению проницаемости для воды мембраны и увеличению ее поверхности. Кроме того, АДГ активирует фермент гиалуронидазу, которая деполимеризует гиалуроновую кислоту межклеточного вещества, что обеспечивает пассивный межклеточный транспорт воды по осмотическому градиенту. При избытке АДГ может наступить полное прекращение мочеобразования. Уменьшение секреции АДГ вызывает развитие тяжелого заболевания несахарного диабета (несахарного мочеиз-нурения). При этом заболевании выделяется большое количество светлой мочи с незначительной относительной плотностью (до 25 л в сутки). АДГ имеет важное значение, как уже отмечалось выше, в поддержании осмотического давления крови, волюморегуляции. Альдостерон увеличивает реабсорбцию ионов натрия и секрецию ионов калия и водорода клетками почечных канальцев. Одновременно возрастает реабсорбия воды, которая всасывается пассивно по осмотическому градиенту, создаваемому ионами Na +, что приводит к уменьшению диуреза. Гормон уменьшает реабсорбцию кальция и магния в проксимальных отделах канальцев. Натрийуретический гормон (атриальный пептид) усиливает выведение ионов натрия с мочой. Паратгормон стимулирует реабсорбцию кальция и тормозит реабсорбцию фосфатов, что приводит к повышению концентрации ионов кальция в плазме крови и усилению выведения фосфатов с мочой. Кроме того, этот гормон угнетает реабсорбцию ионов натрия и HCO3- в проксимальных канальцах и активирует реабсорбцию магния в восходящем колене петли Генле. Кальцитонин тормозит реабсорбцию кальция и фосфата. Адреналин в малых дозах суживает просвет выносящих артериол, в результате чего повышается гидростатическое давление, увеличиваются фильтрация и диурез. В больших дозах он вызывает сужение как выносящих, так и приносящих артериол, что приводит к уменьшению диуреза вплоть до анурии. Инсулин. Недостаток этого гормона приводит к гипергликемии, глюкозурии, увеличению осмотического давления мочи и увеличению диуреза. Тироксин усиливает обменные процессы, в результате чего в моче возрастает количество осмотически активных веществ, в частности азотистых, что приводит к увеличению диуреза. Простагландины угнетают реабсорбцию натрия, стимулируют кровоток в мозговом веществе почки, увеличивают диурез. Соматотропин и андрогены увеличивают секрецию некоторых веществ, например парааминогиппуровой кислоты. Ренин-ангиотензин-альдостероновая система участвует в регуляции почечного и системного кровообращения, объема циркулирующей крови, электролитного баланса организма.Мочевыведение, мочеиспускание и их регуляция
Образовавшаяся моча из собирательных трубочек поступает в почечные лоханки. По мере заполнения лоханки мочой до определенного предела, который контролируется барорецепторами, происходит рефлекторное сокращение мускулатуры лоханки, раскрытие мочеточника и поступление мочи в мочевой пузырь. Поступающая в мочевой пузырь моча постепенно приводит к растяжению его стенок. При наполнении до 250 мл раздражаются механорецепторы мочевого пузыря и импульсы передаются по афферентным волокнам тазового нерва в крестцовый отдел спинного мозга, где расположен центр непроизвольного мочеиспускания. Импульсы из центра по парасимпатическим волокнам достигают мочевого пузыря и мочеиспускательного канала и вызывают сокращение гладкой мышцы стенки мочевого пузыря (детрузора) и расслабление сфинтера пузыря и сфинктера мочеиспускательного канала, что приводит к опорожнению мочевого пузыря. Ведущим механизмом раздражения рецепторов мочевого пузыря является его растяжение, а не рост давления. Важное значение имеет скорость наполнения мочевого пузыря. При быстром его наполнении импульсация резко увеличивается. Спинальный центр находится под регулирующим влиянием вышележащих отделов: кора больших полушарий и средний мозг тормозят его, а передние отделы варолиева моста и задний отдел гипоталамуса стимулируют. Устойчивый корковый контроль мочеиспускания развивается на втором году жизни.Фармакологические влияния на выделительную систему
Лекарственные вещества, вызывающие увеличение выведения из организма мочи и уменьшение содержания жидкости в тканях, называются мочегонными средствами, или диуретиками. Эти вещества применяются при отеках различного происхождения (особенно при хронической недостаточности кровообращения, циррозе печени), при острой анурии или олигурии, при повышении артериального давления, глаукоме и других заболеваниях. Мочегонные препараты имеют разные механизмы действия и оказывают диуретический эффект, влияя на разные участки нефрона. Так, например, тиазидовые диуретики (производные бензотиазина) уменьшают реабсорбцию ионов натрия и хлора в проксимальной и частично в дистальной части извитых канальцев почек, что сопровождается уменьшением реабсорбции воды. Одновременно в меньшей степени угнетается реабсорбция калия и бикарбонатов. Такие диуретики называются салуретиками. С выведением солей и воды из организма и уменьшением объема циркулирующей крови связан их гипотензивный эффект. К салуретикам относится и мощный диуретик фуросемид. Он резко угнетает реабсорбцию натрия и хлора в проксимальном, дистальном канальцах и в восходящем отделе петли Генле. Фуросемид также усиливает выделение ионов калия. Так как эти препараты усиливают выведение ионов калия, хлора, возможны нарушения электролитного и кислотно-основного равновесия, что необходимо учитывать, особенно при длительном назначении этих веществ. Другие диуретики угнетают фермент карбоангидразу (диакарб). В результате этого происходит уменьшение образования угольной кислоты и снижение реабсорбции ионов натрия и бикарбоната эпителием проксимальных канальцев. Угнетая карбоангидразу ресничного тела, эти вещества уменьшают секрецию водянистой влаги глаза, что дает возможность применять их для снижения внутриглазного давления при глаукоме. Имеются диуретики, которые увеличивают выделение только ионов натрия, а выделение ионов калия даже уменьшается. Это так называемые калийсберегающие диуретики. Они действуют в области дистальных канальцев в местах, где обмениваются ионы натрия и калия. Эти вещества (триамтерен, амилорид) снижают проницаемость клеточных мембран эпителия дистальных канальцев для ионов натрия. Секреция ионов калия в дистальных канальцах понижается. Для увеличения диуреза при отеке мозга, легких применяют лекарственные препараты, обладающие осмотической активностью. Эффект обусловлен повышением осмотического давления плазмы и понижением реабсорбции воды. К таким веществам, например, относится маннит, который фильтруется, но не реабсорбируется, поэтому с ним выделяется и вода. Эти вещества применяются также при острых отравлениях барбитуратами, салицилатами, чтобы вызвать форсированный диурез. Изучение проницаемости клубочкового фильтра имеет большой практический интерес при создании так называемых плазмозаменителей – лекарственных веществ, применяемых для замещения плазмы при острых кровопотерях. Плазмозаменители, содержащие онкотически активные вещества, задерживаются в кровотоке дольше, чем физиологический раствор. В то же время молекулярная масса этих веществ не должна превышать 70 ООО, так как они затем должны выводиться из организма почками. Знание мембранных механизмов, обеспечивающих образование мочи, необходимо как для более рационального применения имеющихся лекарственных веществ, так и для целенаправленного поиска новых более эффективных фармакологических препаратов.Глава 13. Физиология анализаторов
Организм и внешний мир – это единое целое. Восприятие окружающей нас среды происходит с помощью органов чувств или анализаторов. Еще Аристотелем были описаны пять основных чувств: зрение, слух, вкус, обоняние и осязание. Термин «анализатор» (разложение, расчленение) был введен И. П. Павловым в 1909 г. для обозначения совокупности образований, активность которых обеспечивает разложение и анализ в нервной системе раздражителей, воздействующих на организм. «Анализаторы – это такие аппараты, которые разлагают внешний мир на элементы и затем трансформируют раздражение в ощущение» (И. П. Павлов, 1911–1913).Общие представления об анализаторах
Анализатор – это не просто ухо или глаз. Он представляет собой совокупность нервных структур, включающих в себя периферический, воспринимающий аппарат (рецепторы), трансформирующий энергию раздражения в специфический процесс возбуждения; проводниковую часть, представленную периферическими нервами и проводниковыми центрами, она осуществляет передачу возникшего возбуждения в кору головного мозга; центральную часть – нервные центры, расположенные в коре головного мозга, анализирующие поступившую информацию и формирующие соответствующее ощущение, после которого вырабатывается определенная тактика поведения организма. С помощью анализаторов мы объективно воспринимаем внешний мир таким, какой он есть. Это материалистическое понимание вопроса. Напротив, идеалистическая концепция теории познания мира выдвинута немецким физиологом И. Мюллером, который сформулировал закон специфической энергии. Последняя, по мнению И. Мюллера, заложена и формируется в наших органах чувств и эту энергию мы же и воспринимаем в виде определенных ощущений. Но эта теория неверна, так как она базируется на действии неадекватного для данного анализатора раздражения. Например, удар по глазу приводит к ощущению света – «искры из глаз посыпались». Наши органы чувств способны воспринимать лишь адекватные и самые минимальные раздражители, которые уже дают соответствующее ощущение. Так, для зрительного анализатора адекватным раздражителем являются световые лучи, а для возбуждения фоторецепторов сетчатки глаза достаточно нескольких квантов света. Интенсивность стимула характеризуется порогом ощущения (восприятия). Абсолютный порог ощущения – это минимальная интенсивность стимула, которая создает соответствующее чувство. Дифференциальный порог – это минимальное различие интенсивностей, которое воспринимается субъектом. Это означает, что анализаторы способны дать количественную оценку прироста ощущения в сторону его увеличения или уменьшения. Так, человек может отличить яркий свет от менее яркого, дать оценку звуку по его высоте, тону и громкости. Существует закон Вебера (1831 г.) и Фехнера (I860 г.), доказывающий зависимость между абсолютным порогом стимула или ощущения и дифференциальным порогом интенсивности стимула. Согласно этому закону: JD/J =К, где JD – прирост раздражения, J – исходный раздражитель, К – постоянная величина. Это означает, что ощущаемый прирост раздражения (порог различения) должен превышать раздражение, действующее ранее (предыдущее), на некоторую определенную постоянную величину, т. е. сила ощущения повышается всегда на одну и ту же величину. Например, если на кожу руки положить гирьку массой 100 г, то для получения ощущения дополнительного груза нужно добавить 3 г, если лежит гирька массой 200 г, то едва ощутимая добавка составит б г. Для гирьки в 300 г нужно добавить 9 г и т. д. Этот закон применим в основном для тактильного и вкусового раздражителей и в меньшей степени – для светового и звукового. Периферическая часть анализатора представлена либо специальными рецепторами (сосочки языка, обонятельные волосковые клетки), либо сложно устроенным органом (глаз, ухо).Классификация рецепторов
В основу классификации рецепторов положены следующие принципы: 1. Среда, в которой рецепторы воспринимают информацию (экстеро-, интеро-, проприо- и другие рецепторы). 2. Природа адекватного раздражителя (механо-, термо-, фото- и другие рецепторы). 3. Характер ощущения после контакта с рецепторами (тепловые, холодовые, болевые и др.). 4. Способность воспринимать раздражитель, находящийся на расстоянии от рецептора – дистантный (обонятельный, зрительный) или при непосредственном контакте с ним – контактный (вкусовой, тактильный). 5. По количеству воспринимаемых модальностей (раздражителей) рецепторы могут быть мономодальными (например, световой) и полимодальными (механический и температурный). 6. Морфологические особенности и механизмы возникновения возбуждения. Различают первичночувствующие (обонятельные, тактильные) и вторичночувствующие рецепторы (зрения, слуха, вкуса).Первичночувствующие рецепторы – это биполярные сенсорные нервные клетки, снабженные ресничками, которые наподобие антенн ведут «поиск» адекватного раздражителя. Контакт с раздражителем приводит к возникновению рецешпорного потенциала, который электротонически распространяется к аксону сенсорного нейрона, где формируется ПД, распространяющийся по нервному волокну. К вторичночувствующим рецепторам относятся те рецепторы, у которых между сенсорными нейронами и раздражителем существует еще дополнительная рецептирующая клетка не нервного происхождения, например, палочки и колбочки, волосковые клетки слухового анализатора. После контакта с раздражителем в рецептирующей клетке возникает рецепторный потенциал, который с помощью синаптической передачи между рецептирующей клеткой и нервным волокном сенсорного нейрона способствует возникновению в нем генераторного потенциала. Последний на аксоне нейрона преобразуется в ПД, который электротонически распространяется по нервному волокну.
Свойства рецепторов
Рецепторы обладают целым рядом свойств, из которых можно выделить следующие: 1. Специфичность рецепторов, т. е. способность воспринимать только тот адекватный им вид раздражителя, к которому он приспособлен в процессе эволюции. Так, слуховые рецепторы приспособлены к восприятию звука, зрительные – света. 2. Высокая избирательная чувствительность по отношению к адекватному раздражителю, что позволяет рецептору выбрать определенный тип воздействия среди множества других. Так, ощущение запаха можно получить при содержании одной молекулы вещества в 1 м3 воздуха, контактирующего со слизистой оболочкой носа. 3. Способность к кодированию или преобразованию одной формы информации в другую, т. е. возбуждение или нервный импульс. 4. Функциональная мобильность. Так, у людей, живущих в условиях холодного климата, больше холодовых рецепторов, чем тепловых, а в условиях теплого климата – наоборот.Кодирование информации в рецепторах
Этот процесс происходит по следующим показателям: качеству, амплитуде (силе), времени и в пространстве. Кодирование качества осуществляется, во-первых, за счет избирательной чувствительности рецептора к адекватному с низким порогом возбуждения раздражителю, т. е. рецептор «узнает» свой стимул (глаз-свет, ухо-звук). Во-вторых, существует цепь модально-специфичных нейронов, соединенных синапсами в определенную жесткую цепь, передающую информацию только от своего рецептивного поля. Это принцип «меченой линии», или топической организации. Этому принципу противопоставляется теория «структуры ответа», согласно которой качество стимула и его кодирование осуществляются «паттернами», или пространственно-временным распределением импульсов, т. е. группой импульсов с определенной частотой и длительностью межимпульсных интервалов. Так, зрительные раздражители распознаются «мечеными линиями», а вкусовые – паттернами. Интенсивность или сила стимула кодируется увеличением частоты ПД, которая, в свою очередь, зависит от величины рецепторного потенциала. Пространственное кодирование осуществляется за счет того, что каждое рецептивное поле имеет свое представительство в определенных структурах центральной нервной системы. Кроме того, имеет место явление перекрытия рецептивных полей, что обеспечивает надежность в работе системы и позволяет слабым раздражителям вступать в контакт с наиболее чувствительными рецепторами и вовлекать в возбуждение менее чувствительные. Кодирование во времени происходит за счет изменения частоты импульсов и продолжительности межимпульсных интервалов. Процесс кодирования, т. е. преобразования соответствующих раздражителей в РП, а затем в нервный импульс или ПД, происходит уже на уровне рецепторов. Перекодирование – переключение сигнала внутри системы осуществляется в следующем отделе анализатора – проводниковом, представленном афферентными и эфферентными путями и подкорковыми центрами. Основная функция этого отдела – анализ и передача информации, формирование рефлексов, а также межанализаторные взаимодействия. Передача информации в проводниковой части анализатора проходит или по строго специфическим проекционным путям с небольшим количеством переключений в спинном, продолговатом мозге, зрительных буграх и в соответствующей проекционной зоне коры больших полушарий, или по неспецифическим с большим количеством коллатералей, синапсов и с участием ретикулярной формации, гипоталамуса, лимбической системы, а также двигательных центров коры больших полушарий, Последние структуры обеспечивают вегетативный, эмоциональный и двигательный компоненты сенсорного ответа. Центральный, корковый отдел анализатора находится на уровне коры больших полушарий. После перекодирования в проводящих путях и подкорковых центрах здесь происходит анализ поступившей сенсорной информации путем отбора и выделения биологически значимой для организма, а также взаимодействие различных анализаторов. В корковом отделе осуществляется декодирование сигнала или считывание сенсорного входа, в результате происходит формирование центробежных регулирующих влияний на эфферентные структуры, отвечающие за ответную реакцию. Так, за счет существования связей сенсорных ядер с двигательными и ассоциативными отделами мозга нервные импульсы сенсорных нейронов вызывают в нейронах двигательной системы или процесс возбуждения, или торможения. В результате происходит или движение – действие, или прекращение движения – бездействие. Взаимодействие анализаторов обеспечивается всеми уровнями центральной нервной системы, начиная со спинного мозга, ретикулярной формации и заканчиваясь таламокортикальными. На корковом уровне эта связь реализуется за счет ассоциативных и моторных зон коры больших полушарий. Пирамидные клетки последних собирают слуховую, зрительную и тактильную информацию. Это лежит, например, в основе обучения глухих или слепых чтению по зрительным, или тактильным, ощущениям.Частная физиология анализаторов
Зрительный анализатор
Зрительный анализатор – это совокупность структур, обеспечивающих восприятие энергии электромагнитных излучений с длиной волны от 400 до 700 ммк. Он является важнейшим из всех анализаторов, благодаря которому человек получает от 80 до 90% всей информации об окружающем мире. Глаз – это периферическая часть зрительного анализатора. Он состоит из глазного яблока, стенки которого образуют три оболочки. Наружная представляет собой фиброзную оболочку. Ее передняя прозрачная часть называется роговицей, имеющей сферическую поверхность. Остальная ее часть – склера является внешним скелетом глаза, обеспечивающим ему определенную форму. Через эпителий и эндотелий роговицы хорошо всасываются ионы Na+, К +, CI в строму и выделяют ее обратно в слезную жидкость и водянистую влагу передней камеры глаза, поддерживая необходимое осмотическое давление. Роговица обладает большой гидрофильностью, поэтому хорошо проницаема для лекарственных средств, вводимых в конъюктивальный мешок. Средняя, или сосудистая, оболочка предназначена для питания глаза. В основном она состоит из кровеносных сосудов и имеет три части: собственно сосудистую оболочку (chorioidea), ресничное, или цилиарное, тело (corpus ciliare) и радужную оболочку (iris). Склера связана с цилиарным телом с помощью цилиарной, или ресничной, мышцы, которую называют еще аккомодационной, так как она участвует в аккомодации глаза. Эта мышца иннервируется парасимпатическим глазодвигательным нервом. К отросткам цилиарного тела прикрепляются волокна цинновой связки, которые подвешивают внутри глаза хрусталик. Цилиарное тело с кровеносными сосудами – это структуры, продуцирующие внутриглазную жидкость. Радужка содержит пигментные клетки, определяющие цвет глаза и отверстие – зрачок (pupilla), играющий роль диафрагмы для проникающих в глаз лучей света. В радужке имеются две мышцы: кольцевидный сфинктер, суживающий зрачок (muse, sphincter pupillae) и расширяющий зрачок (muse, dilatator pupillae), первый из них иннервируется глазодвигательным нервом, второй – симпатическим. Мышцы радужки регулируют диаметр зрачка (зрачковый рефлекс) в зависимости от освещенности. Так, при очень ярком свете диаметр зрачка минимальный (1,8 мм), при средней освещенности – 2,4 мм, а в темноте – максимальный (7,5 мм). Третья, внутренняя оболочка глазного яблока представлена сетчаткой (retina), состоящей из 10 слоев высокодифференцированных нервных элементов, куда входят палочки (110- 125 млн) и колбочки (6 – 7 млн) – фоторецепторы сетчатки. В центральной ямке содержатся только колбочки – это область лучшего восприятия света и здесь наибольшая острота зрения. Место выхода зрительного нерва – слепое пятно, оно не содержит фоторецепторов и поэтому нечувствительно к свету. Палочки ответственны за сумеречное зрение, в них содержится зрительный пигмент – родопсин (зрительный пурпур), спектр поглощения которого находится в области 500 нм. В колбочках, воспринимающих синий, зеленый и красный цвета, содержатся три типа зрительных пигментов, максимумы спектров поглощения которых находятся в синей (420 нм), зеленой (531 нм) и красной (558 нм) частях спектра. Кроме йодопсина, отвечающего за лучи желтой части спектра, в колбочках имеются такие светочувствительные пигменты, как хлоролаб, поглощающий лучи, соответствующие зеленой части спектра, и эритролаб – красной части спектра, предпологается существование и других пигментов. Кнутри от слоя палочек и колбочек находится слой биполярных нервных клеток, к которым примыкает слой ганглиозных клеток. Полость глазного яблока содержит водянистую влагу, хрусталик с его подвешивающим аппаратом и стекловидным телом. Пространство, ограниченное задней поверхностью роговицы, передней поверхностью радужки и хрусталика, называется передней камерой глаза, заполненой прозрачной водянистой влагой. Угол передней камеры играет важную роль в процессах циркуляции внутриглазной жидкости и выступает в качестве «фильтра», через который уходит из глаза камерная жидкость. Пространство, ограниченное задней поверхностью радужки, периферической частью хрусталика и внутренней поверхностью ресничного тела, называется задней камерой глаза, также заполненной водянистой влагой. Камерная влага является источником питания тканей, не содержащих сосуды (роговица, хрусталик и стекловидное тело). От количества водянистой влаги зависит внутриглазное давление, равное 20 мм рт.ст. Повышение его может привести к нарушению кровообращения в глазном яблоке. Водянистая влага – это ультрафильтрат безбелковой плазмы, проходящей через эндотелиальную стенку капилляров ресничного тела. Ее образование зависит от кровенаполнения сосудов глаза. Водянистая влага оттекает через зрачок в переднюю камеру глаза и в ее передний угол (фильтрующая зона), а затем через венозный синус склеры поступает в передние ресничные вены. При затруднении оттока влаги повышается внутриглазное давление (глаукома). Для снижения внутриглазного давления в конъюктивальный мешок закапывают М-холиномиметики (пилокарпин), которые вызывают сужение зрачка, расширение пространства угла передней камеры (радужно-роговичного) и усиление оттока влаги через венозный синус склеры. Поэтому при подозрении на глаукому необходимо избегать препаратов, расширяющих зрачок, например, М-холинолитика – атропина. Хрусталик (lens) представляет собой прозрачное эластическое тело в форме двояковыпуклой чечевицы, подвешенное при помощи связочного аппарата – цинновой связки. Особенность хрусталика состоит в его способности при ослаблении натяжения волокон цинновой связки менять свою форму, становиться более выпуклым за счет чего и осуществляется акт аккомодации. Стекловидное тело представляет собой прозрачный гель, со-стоящий из внеклеточной жидкости с коллагеном и гиалуроновой кислотой в коллоидном растворе и не содержащий ни нервов, ни кровеносных сосудов. Глаз не может одинаково четко видеть предметы, отстоящие от него на разном расстоянии, и чтобы приспособить глаз к ясному видению разноудаленных предметов, необходим процесс аккомодации. Если человек смотрит вдаль, цинновы связки натянуты, а цилиарные мышцы расслаблены, при этом хрусталик уплощен – это покой аккомодации. При рассматривании близко расположенных от глаз предметов цилиарные мышцы сокращены, цинновы связки расслаблены, хрусталик становится более выпуклым – это напряжение аккомодации. Цилиарные мышцы иннервируются парасимпатическими волокнами глазодвигательного нерва. Введение вглаз М-холинолитика – атропина блокирует передачу возбуждения к цилиарной мышце и нарушает аккомодацию при рассматривании близко расположенных предметов. И наоборот, введение М-холиномиметиков – пилокарпина и эзерина способствует сокращению цилиарной мышцы и процессу аккомодации.Оптическая система глаза
Оптический аппарат глаза состоит из прозрачной роговицы, передней и задней камер, заполненных водянистой влагой, радужной оболочки, окружающей зрачок, хрусталика с прозрачной сумкой и стекловидного тела. В целом – это система линз, формирующая на сетчатке перевернутое и уменьшенное изображение рассматриваемых предметов. Преломляющая сила оптической системы выражается в диоптриях. Диоптрия – это преломляющая сила линзы с фокусным расстоянием 100 см. В состоянии покоя аккомодации преломляющая сила равна 58 – 60 диоптриям и называется рефракцией.Аномалии рефракции
При нормальной рефракции параллельные лучи от далеко расположенных предметов собираются на сетчатке в центральной ямке, такой глаз называется эмметропическим. К нарушениям рефракции относится миопия, или близорукость, когда параллельные лучи фокусируются не на сетчатке, а впереди нее (рис. 31). Это возникает при чрезмерно большой длине глазного яблока или преломляющей силе глаза. Близкие предметы близорукий видит хорошо, а удаленные – расплывчато. Коррекция ми-опии – использование рассеивающих двояковогнутых линз. Гиперметропия, или дальнозоркость – это такое нарушение рефракции, когда параллельные лучи от далеко расположенных предметов из-за малой длины глазного яблока или слабой преломляющей способности глаза фокусируются за сетчаткой. Для коррекции гиперметропии используются двояковыпуклые, собирающие линзы.
Ход лучей в эмметропическом (Л), миопическом (б); гиперметропическом (В) глазах; ГиД – коррекция близорукости и дальнозоркости с помощью линз
Существует старческая дальнозоркость, или пресбиопия, связанная с потерей хрусталиком эластичности, который плохо изменяет свою кривизну при натяжении цинновых связок. Поэтому точка ясного видения находится не на расстоянии 10 см от глаза, а отодвигается от него и близко расположенные предметы видны расплывчато. Для коррекции пресбиопии пользуются двояковыпуклыми линзами.
Гиперметропия, или дальнозоркость – это такое нарушение рефракции, когда параллельные лучи от далеко расположенных предметов из-за малой длины глазного яблока или слабой преломляющей способности глаза фокусируются за сетчаткой. Для коррекции гиперметропии используются двояковыпуклые, собирающие линзы.
Ход лучей в эмметропическом (Л), миопическом (б); гиперметропическом (В) глазах; ГиД – коррекция близорукости и дальнозоркости с помощью линз
Существует старческая дальнозоркость, или пресбиопия, связанная с потерей хрусталиком эластичности, который плохо изменяет свою кривизну при натяжении цинновых связок. Поэтому точка ясного видения находится не на расстоянии 10 см от глаза, а отодвигается от него и близко расположенные предметы видны расплывчато. Для коррекции пресбиопии пользуются двояковыпуклыми линзами.
Световоспринимающий, или рецепторный аппарат глаза
Он представлен сетчаткой. Фоторецепторные клетки – палочки и колбочки состоят из двух сегментов – наружного, чувствительного к действию света и содержащего зрительный пигмент, и внутреннего, в котором находятся ядро и митохондрии, отвечающие за энергетический процесс в клетке. Особенность топографии палочек и колбочек состоит в том, что они обращены своими наружными светочувствительными сегментами к слою пигментных клеток, т. е. в сторону, противоположную свету. Палочки более чувствительны к свету, чем колбочки. Так, палочку может возбудить всего один квант света, а колбочку – больше сотни квантов. При ярком дневном свете максимальной чувствительностью обладают колбочки, которые сконцентрированы в области желтого пятна или центральной ямки. При слабом освещении в сумерках наиболее чувствительна к свету периферия сетчатки, где находятся в основном палочки. При действии кванта света в рецепторах сетчатки происходит цепь фотохимических реакций, связанных с распадом зрительных пигментов родопсина и йодопсина и их ресинтез в темноте. Родопсин – пигмент палочек – высокомолекулярное соединение, состоящее из ретиналя – альдегида витамина А и белка опсина. При поглощении кванта света молекулой родопсина 11цис-ретиналь выпрямляется и превращается в транс-ретиналь. Это происходит в течение 1"|2сек. Белковая часть молекулы обесцвечивается и переходит в состояние метародопсина II, который взаимодействует с примембранным белком гуанозинтрифосфатсвязанным белком трансдуцином. Последний запускает реакцию обмена гуанозиндифосфата (ГДФ) на гуанозинтрифосфат (ГТФ), что приводит к усилению светового сигнала. ГТФ вместе с трансдуцином активирует молекулу примембранного белка – фермента фосфодиэстеразы (ФДЭ), который разрушает молекулу циклического гуанозинмонофосфата (цГМФ), вызывая еще большее усиление светового сигнала. Падает содержание цГМФ и закрываются каналы для Na+ и Са2+, что приводит к гиперполяризации мембраны фоторецептора и возникновению рецепторного потенциала. Возникновение гиперполяризации на мембране фоторецептора отличает его от других рецепторов, например слуховых, вестибулярных, где возбуждение связано с деполяризацией мембраны. Гиперполяризационный рецепторный потенциал возникает на мембране наружного сегмента, далее распространяется вдоль клетки до ее пресинаптического окончания и приводит к уменьшению скорости выделения медиатора-глутамата. Для того чтобы рецепторная клетка могла ответить на следующий световой сигнал, необходим ресинтез родопсина, который происходит в темноте (темновая адаптация) из цис-изомера витамина А,, поэтому при недостатке в организме витамина А, развивается недостаточность сумеречного зрения («куриная слепота»). Фоторецепторы сетчатки связаны с биполярной клеткой с помощью синапса. При действии света уменьшение глутамата в пресинаптическом окончании фоторецептора приводит к гипер-поляризации постсинаптической мембраны биполярной нервной клетки, которая также синаптически связана с ганглиозными клетками. В этих синапсах выделяется ацетилхолин, вызывающий деполяризацию постсинаптической мембраны ганглиозной клетки. В аксональном холмике этой клетки возникает потенциал действия. Аксоны ганглиозных клеток образуют волокна зрительного нерва, по которым в мозг устремляются электрические импульсы. Различают три основных типа ганглиозных клеток, отвечающих на включение света (оn-ответ); на выключение света (Off-ответ) и на то и другое (on/off-ответ) учащением фоновых разрядов. В центральной ямке каждая колбочка связана с одной биполярной клеткой, которая, в свою очередь – с одной ганглиозной. Это обеспечивает высокое пространственное разрешение, но резко уменьшает световую чувствительность. К периферии от центральной ямки с одной биполярной клеткой контактирует множество палочек и несколько колбочек, а с ганглиозной – множество биполярных, образующих рецептивное поле ганглиозной клетки. Это повышает световую чувствительность, но ухудшает пространственное разрешение. В слое биполярных клеток располагаются два типа тормозных нейронов – горизонтальные и амакриновые клетки, ограничивающие распространение возбуждения в сетчатке. Суммарный электрический потенциал всех элементов сетчатки называется электроретинограммой (ЭРГ). Она может быть за-регистрирована как от целого глаза, так и непосредственно от сетчатки. По ЭРГ можно судить об интенсивности цвета, размере и длительности действия светового сигнала. Она широко используется в клинике для диагностики и контроля лечения заболеваний сетчатки.Проводящие пути зрительного анализатора
Первый нейрон зрительного анализатора – это биполярная клетка, второй нейрон – ганглиозная. Зрительный нерв состоит из аксонов ганглиозных клеток. В области основания черепа часть волокон зрительного нерва переходит на противоположную сторону. Остальные волокна вместе с перекрещенными аксонами второго зрительного нерва образуют зрительный тракт, волокна которого идут в подкорковые центры: латеральные коленчатые тела, верхние бугры четверохолмия, подушку зрительного бугра, супрахиазматическое ядро гипоталамуса и ядра глазодвигательного нерва. В этих подкорковых структурах находятся остальные нейроны зрительных путей. Аксоны клеток латерального коленчатого тела в составе зрительной радиации направляются в затылочную долю, к центральной части зрительного анализатора, локализованной в клетках первичной зрительной зоны (поле 17), которая связана с вторичными зрительными зонами (поля 18 и 19) коры больших полушарий. Уже на уровне сетчатки, благодаря сложной организации и специализации нейронов происходит определение таких сложных качеств светового сигнала, как освещенность, цвет, форма, движение сигнала. В подкорковых структурах анализатора зрительная информация подвергается дальнейшей, более сложной переработке, вычленению и выявлению новых качеств стимула за счет наличия более сложных рецептивных полей, колонок – вертикальных скоплений нейронов, предназначенных для расчленения информации на отдельные составляющие. На этом уровне уже начинается взаимодействие обоих глаз. Благодаря нейронам зрительной коры происходит основной анализ зрительной информации с обязательным участием колонок; здесь имеются возбуждающие и тормозные зоны. Бинокулярное зрение обеспечивается за счет деятельности коркового конца зрительного анализатора, в одной точке представлены симметричные поля зрения справа и слева.Цветовое зрение
Цветовое зрение – это способность зрительного анализатора реагировать на изменения светового диапазона между коротковолновым – фиолетовым цветом (длина волны от 400 нм) и длинноволновым – красным цветом (длина волны 700 нм) с формированием ощущения цвета. Все остальные цвета: синий, желтый, зеленый, оранжевый имеют промежуточные значения длины волны. Если смешать лучи всех цветов, то получим белый цвет. Существуют две теории цветового зрения. Первая – трехкомпонентная теория цветоощущения Г. Гельмгольца пользуется наибольшим признанием. Согласно этой теории в сетчатке имеются три вида колбочек, отдельно воспринимающих красный, зеленый и сине-фиолетовый цвета. Различные сочетания возбуждения колбочек приводят к ощущению промежуточных цветов. Равномерное возбуждение всех трех видов колбочек дает ощущение белого цвета. Черный цвет ощущается в том случае, если колбочки не возбуждаются. Согласно второй контрастной теории Э. Геринга, основанной на существовании в колбочках трех светочувствительных веществ (бело-черное, красно-зеленое, желто-синее), под влиянием одних световых лучей происходит распад этих веществ и возникает ощущение белого, красного, желтого цветов. Другие световые лучи синтезируют эти вещества и в результате получается ощущение черного, зеленого и синего цветов. Впервые частичная цветовая слепота была описана Д. Дальтоном, который сам ею страдал (дальтонизм). В основном дальтонизмом страдают мужчины (8%) и только 0,5% – женщины. Ее возникновение связано с отсутствием определенных генов в половой непарной у мужчин х-хромосоме.Различают три типа нарушений цветового зрения: 1. Протанопия, или дальтонизм – слепота на красный и зеленый цвета, оттенки красного и зеленого цвета не различаются, сине-голубые лучи кажутся бесцветными. 2. Дейтеранопия – слепота на красный и зеленый цвета. Нет отличий зеленого цвета от темно-красного и голубого. 3. Тританопия – редко встречающаяся аномалия, не различаются синий и фиолетовый цвета. 4. Ахромазия – полная цветовая слепота при поражении колбочкового аппарата сетчатки. Все цвета воспринимаются как оттенки серого.
Восприятие пространства
Острота зрения – это наименьшее расстояние между двумя точками, которые глаз способен видеть раздельно. Нормальный глаз способен различать две светящиеся точки под углом зрения в 1', острота зрения такого глаза, или визус, (visus) равна 1,0. Острота зрения определяется с помощью буквенных или различного рода фигурных стандартных таблиц. При фиксированном на каком-либо предмете взгляде он воспринимается центральным зрением. Предметы, изображения которых попадают не на центральную ямку, а на остальные участки сетчатки, воспринимаются периферическим зрением. Пространство, которое человек может видеть фиксированным взглядом, называется полем зрения. Оно определяется с помощью прибора периметра (метод периметрии). Различают отдельно поле зрения для левого и правого глаза и общее поле зрения для двух глаз. Оно неодинаково в различных меридианах, книзу и кнаружи оно больше, чем кнутри и кверху. Самое большое поле зрения для белого цвета, самое узкое – для зеленого, желтого, больше – для синего и красного. Ощущение глубины пространства обеспечивается бинокулярным зрением. У человека с нормальным зрением при рассматривании предмета двумя глазами изображение попадает на симметричные (идентичные) точки сетчатки, а корковый отдел анализатора объединяет его в единое целое, давая одно изображение. Если изображение попадает на неидентичные, или диспаратные, точки двух сетчаток, то изображение раздваивается. При надавливании на глаз сбоку начинает двоиться в глазах, так как нарушилось соответствие сетчаток.Слуховой анализатор
Слуховой анализатор воспринимает звуковые сигналы, представляющие собой колебания воздуха с разной частотой и силой, трансформирует механическую энергию этих колебаний в нервное возбуждение, которое субъективно воспринимается как звуковое ощущение.Периферическая часть слухового анализатора или орган слуха состоит из трех основных отделов: 1. Звукоулавливающий аппарат (наружное ухо). 2. Звукопередающий аппарат (среднее ухо). 3. Звуковоспринимающий аппарат (внутреннее ухо).
Наружное ухо состоит из ушной раковины, наружного слухового прохода и барабанной перепонки. Ушная раковина, подобно локатору, улавливает звуковые колебания, концентрирует их и направляет в наружный слуховой проход. Эта функция особенно хорошо развита у некоторых видов животных (собак, кошек, летучих мышей), у которых благодаря рефлекторному управлению ушной раковиной происходит определение местонахождения источника звука. Наружный слуховой проход проводит звуковые колебания к барабанной перепонке и играет роль резонатора, собственная частота колебаний которого составляет 3000 Гц. При действии на ухо звуковых колебаний, близких по своим значениям к 3000 Гц, давление на барабанную перепонку увеличивается. Наружное ухо выполняет защитную функцию, охраняя отдельные структуры уха от механических и температурных воздействий, обеспечивает постоянную температуру и влажность, необходимую для сохранения упругих свойств барабанной перепонки. На границе между наружным и средним ухом находится барабанная перепонка – это малоподвижная и слаборастяжимая мембрана, площадь которой составляет 66 – 69,5 мм2. Она имеет форму конуса с вершиной, направленной в полость среднего уха. Основная функция барабанной перепонки – передача звуковых колебаний в среднее ухо. Колебания барабанной перепонки передаются в среднее ухо, в котором содержится цепь соединенных между собой косточек: молоточка, наковальни и стремечка. Рукоятка молоточка прикреплена к барабанной перепонке, основание стремечка – к овальному окну. Благодаря передаточной функции слуховых косточек давление звука в области круглого окна улитки увеличивается в 20 раз. В среднем ухе находятся две мышцы: мышца, натягивающая барабанную перепонку и прикрепленная к ручке молоточка, и стапедиальная, прикрепленная к стремечку. За счет сокращения этих мышц происходит уменьшение амплитуды колебаний барабанной перепонки и снижение коэффициента передачи уровня звукового давления на область внутреннего уха. Эти мышцы выполняют защитную функцию при действии звуковых колебаний больше 90 дБ и действующих длительное время. При резких внезапных звуках (удар в колокол) этот механизм не срабатывает. Сокращения стапедиальной мышцы происходят при жевании, глотании, зевании, во время речи и пения, при этом низкочастотные звуки подавляются, а высокочастотные проходят к внутреннему уху. В полости среднего уха давление приближается к атмосферному, это необходимо для нормальных колебаний барабанной перепонки. Уравновешиванию давления (при глотании) способствует специальное образование – евстахиева труба, которая соединяет носоглотку с полостью среднего уха. Внутреннее ухо соединено со средним с помощью овального окна, в котором неподвижно укреплено основание стремечка. Внутреннее ухо состоит из костного и лежащего в нем перепончатого лабиринтов, в котором находятся вестибулярный (преддверие и полукружные каналы) и слуховой аппараты. К последнему относится улитка. Улитка имеет длину 3,5 мм, что составляет 2,5 завитка. Она разделена двумя мембранами: основной и мембраной Рейснера на три хода или лестницы: барабанную, среднюю и вестибулярную (рис.32). Вестибулярная и барабанная лестницы у верхушки улитки соединены между собой через геликотрему. Обе эти лестницы заполнены перилимфой, сходной по химическому составу со спинномозговой жидкостью и содержащей много ионов натрия (около 140 ммоль/л).
 Средняя лестница изолирована и заполнена эндолимфой, богатой ионами К+ (около 155 ммоль/л) и напоминающей по своему составу внутриклеточную жидкость. Это обусловливает положительный заряд эндолимфы по отношению к перилимфе.
Основание барабанной лестницы сообщается со средним ухом с помощью еще одного отверстия – круглого окна, закрытого тонкой мембраной.
На основной мембране средней лестницы расположен кортиев орган – собственно звуковоспринимающий аппарат, содержащий рецепторы – внутренние и наружные волосковые клетки, несущие только стереоцилии. Внутренних волосковых клеток у человека около 3500, они располагаются в один ряд, и имеются три ряда наружных волосковых клеток, их приблизительно 12 000. Слуховые рецепторы – вторичночувствующие.
Над кортиевым органом находится текториальная (покровная) мембрана – желеобразная масса, соединенная с кортиевым органом и с внутренней стенкой улитки. Стереоцилии наружных и, вероятно, внутренних волосковых клеток контактируют с текториальной мембраной. При движении основной мембраны покровная мембрана сгибает волоски рецепторных клеток, воздействуя в большей степени на наружные волосковые клетки, чем на внутренние. В результате деформации волосков возникает возбуждение волосковых клеток.
На наружной стороне средней лестницы располагается сосудистая полоска – область с высокой метаболической активностью и хорошим кровоснабжением. Ее функция состоит в обеспечении улитки энергией и регуляции состава эндолимфы. Калиевый насос принимает активное участие в поддержании ионного состава эндолимфы и ее положительного потенциала. Некоторые диуретики блокируют не только ионные насосы почечных канальцев, но и влияют на ионные насосы сосудистой полоски, оказывая ототоксическое побочное действие, и могут приводить к глухоте.
Основная мембрана состоит из эластических волокон. Вблизи овального окна у основания улитки она составляет всего 0,04 мм, по направлению к вершине она расширяется и у геликотремы равна уже 0,5 мм. Основная мембрана слабо натянута, что создает условия для колебательных движений в зависимости от воздействия на нее звуковых волн различной частоты. Волокна, расположенные у основания улитки, реагируют как струны-резонаторы на звуки высокой частоты, а у вершины – на низкие частоты.
Средняя лестница изолирована и заполнена эндолимфой, богатой ионами К+ (около 155 ммоль/л) и напоминающей по своему составу внутриклеточную жидкость. Это обусловливает положительный заряд эндолимфы по отношению к перилимфе.
Основание барабанной лестницы сообщается со средним ухом с помощью еще одного отверстия – круглого окна, закрытого тонкой мембраной.
На основной мембране средней лестницы расположен кортиев орган – собственно звуковоспринимающий аппарат, содержащий рецепторы – внутренние и наружные волосковые клетки, несущие только стереоцилии. Внутренних волосковых клеток у человека около 3500, они располагаются в один ряд, и имеются три ряда наружных волосковых клеток, их приблизительно 12 000. Слуховые рецепторы – вторичночувствующие.
Над кортиевым органом находится текториальная (покровная) мембрана – желеобразная масса, соединенная с кортиевым органом и с внутренней стенкой улитки. Стереоцилии наружных и, вероятно, внутренних волосковых клеток контактируют с текториальной мембраной. При движении основной мембраны покровная мембрана сгибает волоски рецепторных клеток, воздействуя в большей степени на наружные волосковые клетки, чем на внутренние. В результате деформации волосков возникает возбуждение волосковых клеток.
На наружной стороне средней лестницы располагается сосудистая полоска – область с высокой метаболической активностью и хорошим кровоснабжением. Ее функция состоит в обеспечении улитки энергией и регуляции состава эндолимфы. Калиевый насос принимает активное участие в поддержании ионного состава эндолимфы и ее положительного потенциала. Некоторые диуретики блокируют не только ионные насосы почечных канальцев, но и влияют на ионные насосы сосудистой полоски, оказывая ототоксическое побочное действие, и могут приводить к глухоте.
Основная мембрана состоит из эластических волокон. Вблизи овального окна у основания улитки она составляет всего 0,04 мм, по направлению к вершине она расширяется и у геликотремы равна уже 0,5 мм. Основная мембрана слабо натянута, что создает условия для колебательных движений в зависимости от воздействия на нее звуковых волн различной частоты. Волокна, расположенные у основания улитки, реагируют как струны-резонаторы на звуки высокой частоты, а у вершины – на низкие частоты.
Механизм передачи звуковых колебаний
Звуковые колебания, воздействуя на систему слуховых косточек среднего уха, приводят к колебательным движениям мембраны овального окна, которая, прогибаясь, вызывает волнообразные перемещения перилимфы в вестибулярной и через геликотрему – в барабанной лестницах. Колебания перилимфы доходят до круглого окна и приводят к смещению его мембраны по направлению к среднему уху. Движения перилимфы верхней и нижней лестниц (каналов) передаются на вестибулярную мембрану, а затем на полость среднего канала, приводя в движение эндолимфу и базилярную мембрану (рис. 33). Если на ухо действуют низкочастотные звуки (до 1000 Гц), то, по мнению Г. Бекеши, происходит смещение базилярной мембраны на всем ее протяжении, от основания до верхушки улитки, так как собственная частота совпадает с низкой частотой звукового стимула. При действии высокочастотных колебаний происходит перемещение укороченного по длине колеблющегося столба жидкости ближе к овальному окну и наиболее жесткому и упругому участку базилярной мембраны. Вследствие смещений последней волоски рецептивных клеток контактируют с текториальной мембраной. При этом реснички волосковых клеток деформируются. В результате энергия звуковых колебаний трансформируется в электрический разряд (нервный импульс) волосковых клеток.
Помимо воздушной проводимости существует и костная (костями черепа). Ощущение звука возникает и тогда, когда вибрирующий предмет, например камертон, прикладывают к сосцевидному отростку височной кости, тогда звуковые колебания распространяются непосредственно через череп. Определение костной проводимости звука позволяет выявить патологию внутреннего уха.
Проводящие пути и центры слухового анализатора Нервный импульс возникает в волосковых клетках, передается биполярным нервным клеткам, расположенным в спиральном ганглии улитки (первый нейрон). Центральные отростки клеток спирального ганглия образуют слуховой, или кохлеарный, нерв (VIII пара черепно-мозговых нервов). Кохлеарный нерв проходит в продолговатый мозг и заканчивается на клетках кохлеарных ядер (второй нейрон). Нервные волокна от кохлеарных ядер в составе боковой петли доходят до верхней оливы (третий нейрон). Одна часть волокон латеральной петли достигает среднего мозга – ядер нижних бугров четверохолмия, другая – медиального коленчатого тела зрительных бугров, где происходит переключение и находится четвертый нейрон. Далее волокна в составе слуховой радиации заканчиваются в коре верхней части височной доли большого мозга (поля 41 и 42 по Бродману), т. е. в центральной части слухового анализатора.
Функция отдельных частей проводящей системы слухового анализатора состоит в следующем. В спиральном ганглии методом разрушения и перерезок было показано пространственно раздельное представительство низких и высоких частот. Так, частичная перерезка волокон слухового нерва приводит к потере слуха на высоких частотах. При полной перерезке слухового нерва происходит потеря слуха на низких частотах.
Нижние бугры четверохолмия отвечают за ориентировочный рефлекс (поворот головы в сторону источника звука). Слуховая кора принимает участие в переработке звуковой информации в процессе дифференцировки звуков, она отвечает за бинауральный слух.
Если на ухо действуют низкочастотные звуки (до 1000 Гц), то, по мнению Г. Бекеши, происходит смещение базилярной мембраны на всем ее протяжении, от основания до верхушки улитки, так как собственная частота совпадает с низкой частотой звукового стимула. При действии высокочастотных колебаний происходит перемещение укороченного по длине колеблющегося столба жидкости ближе к овальному окну и наиболее жесткому и упругому участку базилярной мембраны. Вследствие смещений последней волоски рецептивных клеток контактируют с текториальной мембраной. При этом реснички волосковых клеток деформируются. В результате энергия звуковых колебаний трансформируется в электрический разряд (нервный импульс) волосковых клеток.
Помимо воздушной проводимости существует и костная (костями черепа). Ощущение звука возникает и тогда, когда вибрирующий предмет, например камертон, прикладывают к сосцевидному отростку височной кости, тогда звуковые колебания распространяются непосредственно через череп. Определение костной проводимости звука позволяет выявить патологию внутреннего уха.
Проводящие пути и центры слухового анализатора Нервный импульс возникает в волосковых клетках, передается биполярным нервным клеткам, расположенным в спиральном ганглии улитки (первый нейрон). Центральные отростки клеток спирального ганглия образуют слуховой, или кохлеарный, нерв (VIII пара черепно-мозговых нервов). Кохлеарный нерв проходит в продолговатый мозг и заканчивается на клетках кохлеарных ядер (второй нейрон). Нервные волокна от кохлеарных ядер в составе боковой петли доходят до верхней оливы (третий нейрон). Одна часть волокон латеральной петли достигает среднего мозга – ядер нижних бугров четверохолмия, другая – медиального коленчатого тела зрительных бугров, где происходит переключение и находится четвертый нейрон. Далее волокна в составе слуховой радиации заканчиваются в коре верхней части височной доли большого мозга (поля 41 и 42 по Бродману), т. е. в центральной части слухового анализатора.
Функция отдельных частей проводящей системы слухового анализатора состоит в следующем. В спиральном ганглии методом разрушения и перерезок было показано пространственно раздельное представительство низких и высоких частот. Так, частичная перерезка волокон слухового нерва приводит к потере слуха на высоких частотах. При полной перерезке слухового нерва происходит потеря слуха на низких частотах.
Нижние бугры четверохолмия отвечают за ориентировочный рефлекс (поворот головы в сторону источника звука). Слуховая кора принимает участие в переработке звуковой информации в процессе дифференцировки звуков, она отвечает за бинауральный слух.
Электрические явления в улитке
При отведении электрических потенциалов от разных частей улитки различают пять электрических феноменов: 1. Мембранный потенциал волосковых клеток, равный -80 мв. Регистрируется при введении в нее микроэлектрода. 2. Эндокохлеарный потенциал – регистрируется при прохождении микроэлектрода через каналы улитки. Эндолимфа, содержащая много ионов калия, имеет положительный заряд по отношению к перилимфе верхнего и нижнего каналов, он ранен +80 мв. Эндокохлеарный потенциал создается за счет функционирования сосудистой полоски и обусловлен определенным уровнем окислительно-восстановительных реакций. Он является источником энергии для процесса преобразования воздействующего раздражителя в нервный импульс. Разрушение сосудистой полоски и гипоксия приводят к исчезновению эндокохлеарного потенциала. 3. Микрофонный потенциал, или эффект, возникает в улитке при действии звука, является физическим явлением и полностью отражает форму звуковых волн. Он регистрируется при помещении электродов в барабанной лестнице вблизи от кортиева органа или на круглом окне. Этот потенциал аналогичен выходному напряжению микрофона, и если его подать на усилитель и пропустить через громкоговоритель, то получим воспроизведение речи. Происхождение микрофонного эффекта не совсем ясно, его связывают с механохимическими преобразованиями в волосковых клетках кортиева органа, повреждение которого приводит к исчезновению микрофонного эффекта. 4. Суммационный потенциал: при действии звуков большой силы и частоты происходит стойкое изменение нулевой линии на записи электрических колебаний или сдвиг исходной разности потенциалов – это суммационный потенциал, который, в отличие от микрофонного, воспроизводит не форму звуковой волны, а ее огибающую. 5. Потенциалы действия слухового нерва регистрируются при отведении от волокон слухового нерва. Их частота зависит от высоты действующего на ухо гона, но до определенных пределов. Если частота звуковых колебаний не превышает 1000 в секунду, то в слуховом нерве возникают импульсы такой же частоты. При действии на ухо высокочастотных колебаний частота импульсов в слуховом нерве ниже, чем частота звуковых колебаний. Потенциал действия слухового нерва является результатом синаптической передачи возбуждения в нервных элементах кортиева органа с участием медиатора (возможно, глутамата).Механизм восприятия звуков различной частоты
Существуют две теории восприятия звуков. Согласно резонансной теории слуха Г. Д. Гельмгольца (1885 г.), базилярная мембрана состоит из отдельных волокон (струн резонатора), настроенных на звуки определенной частоты. Так, звуки высокой частоты воспринимаются короткими волокнами базилярной мембраны, расположенными ближе к основанию улитки, низкой частоты – длинными волокнами вершины улитки. Теория места основана на различной способности волосковых клеток, расположенных в разных местах базилярной мембраны, воспринимать звуки различной частоты. Повреждение отдельных участков базилярной мембраны с волосковыми клетками приводит к повышению порога восприятия звуков определенной частоты. Слуховая адаптация Понижение слуховой чувствительности, развивающееся в процессе длительного действия звука большой интенсивности или после его прекращения, называют слуховой адаптацией. Она обусловлена изменениями как в периферических, так и центральных отделах слухового анализатора. Ухо, адаптированное к тишине, обладает более низким порогом слуховой чувствительности. При длительном действии звуков большой интенсивности (громкая музыка, работа в шумных цехах) порог слуховой чувствительности повышается. Пространственный слух Способность человека и животного локализовать источник звука в пространстве называется пространственным слухом. Слуховая ориентация осуществляется двумя путями: определением местоположения самого звучащего объекта (первичная локализация) и с помощью эхолокации, т. е. восприятием отраженных от различных объектов звуковых волн. Эхолокация помогает ориентироваться в пространстве некоторым животным (дельфинам, летучим мышам), а также людям, потерявшим зрение. Пространственное восприятие звука возможно при наличии бинаурального слуха, т. е. способности определить местонахождение источника звука одновременно правым и левым ухом. Пределы слышимости, острота слуха Человеческое ухо различает звуки по высоте или частоте звуковых колебаний от 20 до 16 000 Гц, по громкости (силе звуковых колебаний, его амплитуде) и по тембру (окраске звука). Частоты выше 16 000 Гц называются ультразвуковыми, а ниже 20 Гц – инфразвуковыми. Для речи, хорошо воспринимаемой человеческим ухом, характерен диапазон от 200 до 3000 Гц – это речевая зона. С возрастом чувствительность к высоким частотам снижается (старческая тугоухость). Частота звука определяет абсолютный порог слышимости или минимальную силу слышимого звука. В области 1000 -4000 Гц слух человека максимально чувствителен. Звуки выше 16 000 – 20 000 Гц вызывают неприятные ощущения давления и боли в ухе. Это верхний предел слышимости. Единицей громкости звука является бел – это десятичный логарифм отношения действующей интенсивности звука I к его пороговой интенсивности Jg. В практике обычно используют в качестве единицы громкости децибел (дБ), т. е. 0,1 бела. Максимальный порог громкости, вызывающий болевые ощущения, равен 130–140 дБ. Определяется порог слышимости с помощью метода аудиометрии.Вестибулярный анализатор
Вестибулярный анализатор наряду со зрительным и соматосенсорным играет ведущую роль в ориентации человека в пространстве, является органом равновесия. Он воспринимает информацию о положении, линейных и угловых перемещениях тела и головы. Периферический отдел (вестибулярный аппарат) находится в костном лабиринте пирамиды височной кости и состоит из трех полукружных каналов и преддверия. Полукружные каналы расположены в трех взаимно перпендикулярных плоскостях: верхний – во фронтальной, задний – в сагиттальной и наружный – в горизонтальной. На одном конце каждого канала имеется колбообразное расширение – ампула. Преддверие состоит из двух отделов: мешочка (саккулус) и маточки (утрикулус). Утрикулус, саккулус и полукружные каналы состоят из тонких перепонок, образующих замкнутые трубки, – это перепончатый лабиринт, внутри которого находится эндолимфа, связанная с эндолимфой улитки. Между перепончатым и костным лабиринтом, в который заключены улитка и вестибулярный аппарат, находится перилимфа. В каждом мешочке имеются небольшие возвышения – макулы (пятна), в которых находится отолитовый аппарат – скопление рецепторных клеток, которые покрыты желеобразной массой, состоящей из мукополисахаридов. Благодаря наличию в ней кристаллов кальция она получила название отолитовой мембраны. В полукружных каналах желеобразная масса не содержит отолиты и называется купулой. Все вестибулорецепторы относятся к вторичночувствующим и делятся на два типа: клетки первого типа имеют колбообразную форму, второго типа – цилиндрическую. На своей свободной поверхности клетки имеют волоски, из них тонкие (60–80 на каждой клетке) называются стереоцилиями, а один толстый и длинный находится на периферии пучка и называется киноцилием. При изменении положения головы и тела в пространстве происходит перемещение желеобразной массы, которая отклоняет реснички, погруженные в нее. Их перемещение служит адекватным стимулом для возбуждения рецепторов. Смещение волосков в сторону киноцилия вызывает возбуждающий эффект, в противоположную – тормозный. Отолитовый аппарат предверия воспринимает прямолинейное движение, ускорение или замедление, наклоны головы и тела в сторону, а также тряску и качку. Раздражителем рецепторного аппарата полукружных каналов являются вращательные движения вокруг своей оси, их угловое ускорение или замедление.Проводящие пути и центры вестибулярного анализатора
На рецепторных клетках берут начало и заканчиваются афферентные и эфферентные нервные волокна. Первый нейрон проводникового отдела – это биполярные клетки, расположенные в вестибулярном ганглии. Периферические отростки этих клеток контактируют с рецепторными клетками, а центральные в составе вестибулярного нерва (VIII пара черепно-мозговых нервов) направляются в вестибулярные ядра продолговатого мозга (второй нейрон). Отсюда импульсы поступают к таламическим ядрам (третий нейрон), мозжечку, ядрам глазодвигательных мышц, к вестибулярным ядрам противоположной стороны, к мотонейронам шейного отдела спинного мозга, через вестибулоспинальный тракт – к мотонейронам мышц-разгибателей, к ретикулярной формации, гипоталамусу. За счет вышеперечисленных связей осуществляется автоматический контроль равновесия тела (без участия сознания). За сознательный анализ положения тела в пространстве отвечают таламокортикальные проекции, которые заканчиваются в задней постцентральной извилине коры больших полушарий центрального отдела вестибулярного анализатора. Через вестибуло-мозжечково-таламический тракт в моторную кору кпереди от центральной извилины поступает информация о поддержании тонических реакций, связанных с оценкой позы тела.Чувствительность вестибулярного анализатора
Она неодинакова для различных видов движений. При прямолинейном движении порог различения ускорения равен 2 – 20 см/с, для углового ускорения порог различения вращения равен 2 – 3 градусам/с. Порог различения наклона головы в сторону составляет около 1 градуса, вперед-назад – около 1,5 -2 градусов. При вибрации, качке, тряске происходит снижение чувствительности вестибулярного аппарата. Сильные и длительные нагрузки на вестибулярный аппарат вызывают у некоторых людей патологический симптомокомплекс, названный «болезнью движения, или морской болезнью». При этом возникают вестибуловегетативпые реакции: изменения сердечного ритма, тонуса сосудов, усиление моторики желудочно-кишечного тракта, саливация, тошнота, рвота. Проявления морской болезни могут быть уменьшены применением некоторых лекарственных препаратов. Важным показателем состояния вестибулярной системы является вестибулоглазодвигательный рефлекс (глазной нистагм), который проявляется в ритмическом медленном движении глаз в сторону, противоположную вращению, и быстром, скачкообразном движении глаз в обратном направлении. Нистагм появляется после вращения, он дает возможность обзора пространства в условиях перемещения тела.Обонятельный анализатор
С помощью обонятельного анализатора осуществляется восприятие и анализ пахучих веществ, химических раздражителей внешней среды, а также принимаемой пищи. Благодаря функциям обонятельного анализатора человек ориентируется в окружающем пространстве, апробирует пищу на съедобность, уходит от опасности, отвергает вредные для него вещества, животные обеспечивают половую ориентацию. Периферический отдел обонятельного анализатора расположен в задней части верхнего носового хода и представлен обонятельным эпителием, в состав которого входят обонятельные рецепторные клетки, количество которых у человека достигает 10 млн (у собаки – овчарки – около 200 млн), опорные и базальные клетки. Обонятельный эпителий покрыт сверху слоем слизи. Обонятельные рецепторные клетки – первичночувствующие. От верхней части клетки отходит дендрит, снабженный ресничками, погруженными в слой слизи. Движения ресничек обеспечивают процесс захвата молекулы пахучего вещества и контакта с ним (стереохимия пахучих веществ). Механизм обонятельной рецепции заключается в том, что молекула пахучего вещества взаимодействует со специализированными белками, встроенными в мембрану рецептора. Если форма молекулы воспринимаемого вещества соответствует форме рецепторного белка в мембране (как ключ к замку), тогда возможен контакт с этим веществом. Затем изменяется конфигурация молекулы белка, открываются натриевые каналы и возникает деполяризация мембраны рецепторной клетки. В результате генерируется рецепторный потенциал микроворсипок, а затем потенциал действия нервного волокна.Проводящие пути и центры обонятельного анализатора
Аксоны рецепторных клеток, объединившись в пучок, идут к обонятельной луковице, где находятся вторые нейроны. Волокна клеток обонятельной луковицы образуют обонятельный тракт, имеющий треугольное расширение и состоящий из нескольких пучков. Обонятельная луковица генерирует ритмические импульсы, частота которых изменяется при вдувании в нос различных пахучих веществ. Пучки обонятельного тракта проходят в различные структуры мозга: миндалину, гипоталамус (отвечает за эмоциональный компонент обонятельных ощущений), ретикулярную формацию, орбито-фронтальную кору, препериформную кору и периформную долю, в обонятельную луковицу противоположной стороны. Центральный отдел обонятельного анализатора находится в передней части грушевидной доли в области извилины морского коня (гиппокампа). Пахучие вещества воспринимаются также свободными окончаниями волокон тройничного нерва (V пара черепно-мозговых нервов), расположенными в слизистой носа. Так, вещества с резким запахом (аммиак) воспринимаются окончаниями тройничного нерва и могут вызвать остановку дыхания или защитные рефлексы (чихание). Эти рефлексы замыкаются на уровне продолговатого мозга. Человек способен различать многообразие запахов. Существует классификация (Ж. Эймур, 1962) запахов, служащая практическим целям.Она выделяет семь основных, или первичных, запахов: 1. камфароподобный 2. цветочный 3. мускусный 4. мятный 5. эфирный 6. гнилостный 7. острый.
Ко второй группе относятся смешанные вещества, которые раздражают не только обонятельные клетки, но и окончания тройничного нерва. Это запах камфары, эфира, хлороформа и др. Адаптация к действию пахучего вещества происходит довольно медленно в течение 10 секунд или минут и зависит от продолжительности действия вещества, его концентрации и скорости потока воздуха (принюхивание). Острота обоняния определяется порогом обонятельной чувствительности – это минимальное количество пахучего вещества, которое ощущается как соответствующий запах. Определение порогов обонятельной чувствительности проводится с помощью ольфактометрии. На остроту обоняния влияют влажность и температура воздуха, состояние периферического отдела анализатора. Набухлость слизистой носа при насморке вызывает понижение остроты обоняния – гипоосмию или полную потерю обонятельной чувствительности – аносмию, которая наблюдается или при атрофии рецепторного аппарата, или при нарушении коркового отдела анализатора, с которым может быть связана и гиперосмия – повышение чувства обоняния, а также паросмия – неправильное восприятие запахов, обонятельные галлюцинации при отсутствии пахучих веществ – обонятельная агнозия. С возрастом отмечено снижение обонятельной чувствительности.
Вкусовой анализатор
Вкус относится к контактным видам чувствительности и является мультимодальным ощущением, так как химические раздражители воспринимаются в комплексе с термическими, механическими и обонятельными. Различают четыре «первичных» вкусовых ощущения: сладкое, кислое, соленое, горькое. Кончик языка воспринимает в основном сладкий вкус, корень – горький, средняя часть – кислый, боковые части языка – соленый и кислый. Самые низкие пороги вкусовой чувствительности – для горького вкуса и определяются по концентрации действующих на рецепторы веществ. Длительное действие какого-либо вещества на вкусовые рецепторы приводит к адаптации к данному виду вкуса. Так, если человек часто употребляет кислую и соленую пищу (острую), то пороги на эти виды вкуса увеличиваются. Адаптация к сладкому и соленому развивается быстрее, чем к горькому и кислому. Рецепторы вкуса – вкусовые клетки расположены во вкусовых почках или луковицах. Последние локализуются во вкусовых сосочках языка и в виде отдельных включений – на задней стенке глотки, мягком небе, миндалинах, гортани, надгортаннике.Они делятся на три типа: 1. грибовидные (на всей поверхности языка) 2. желобоватые – поперек стенки языка, у его корня 3. листовидные – вдоль задних краев языка.
У человека насчитывают 2000 вкусовых почек, каждая из которых содержит 40 – 60 рецепторных клеток. Механизм вкусовой рецепции заключается в следующем. Вкусовое вещество, расщепленное слюной до молекул, попадает в поры вкусовых луковиц, вступает во взаимодействие с гликокаликсом и адсорбируется на клеточной мембране микроворсинки, вступая в контакт с рецепторным белком. Предполагается, что в области микроворсинки имеются стереоспецифические участки рецептора, воспринимающие только свои молекулы вещества. В результате происходит деполяризация мембраны и генерация рецепторного потенциала. Образовавшийся в рецепторной клетке медиатор (ацетилхолин, серотонин и др.) в рецепторно-афферентном синапсе приводит к возникновению ВПСП, а затем ПД, который передается по волокнам барабанной струны – веточки лицевого (VII пара), языкоглоточного (IX пара) и верхнегортанного (X пара) черепно-мозговых нервов в продолговатый мозг, в ядро солитарного нерва в виде паттерной нервной активности, определяющей разные вкусовые ощущения. Из продолговатого мозга нервные волокна в составе медиальной петли направляются к вентральным ядрам зрительного бугра и далее в кору больших полушарий – латеральную часть постцентральной извилины и гиппокамп. Вкусовая чувствительность может изменяться в зависимости от состояния организма (при голодании, беременности). Алкоголь и никотин увеличивают пороги вкусовой чувствительности. Полная потеря вкусового восприятия называется агевзией, пониженная – гипогевзией, повышение вкусовой чувствительности – гипергевзия, извращение вкуса – парагевзия.
Соматовисцеральная сенсорная система
В соматовисцеральную систему входят: кожный анализатор, объединяющий тактильную, температурную и болевую чувствительность, проприоцептивный анализатор, или мышечное чувство, следящее за изменением положения и движения суставов и мышц, а также висцеральный анализатор, позволяющий получить информацию о состоянии внутренних органов.Кожный анализатор
С помощью кожного анализатора осуществляется связь организма с внешним миром.Тактильная чувствительность.
При раздражении тактильных рецепторов кожи возникает чувство прикосновения, щекотания, давления, вибрации. Рецепторы, воспринимающие прикосновение, – это тельца Мейснера, расположенные в глубоком сосочковом слое кожи, а также свободные окончания нервных волокон, локализованных вдоль мелких сосудов, и тонкие нервные волокна, оплетающие волосяную сумку (на участках кожи с волосяным покровом). Тельца Мейснера относятся к быстроадаптирующимся рецепторам. Самое большое количество таких рецепторов располагается на открытых участках тела, принимающих участие в познании внешнего мира: кончики пальцев рук, ладонныеповерхности кисти, кончик языка, подошвы ног, кайма нижней губы. За чувство давления отвечают диски Меркеля – рецепторные образования, расположенные небольшими группами в глубоких слоях кожи и слизистой. Они реагируют на прогибание эпидермиса под действием механического стимула и медленно адаптируются при длительном действии раздражителя. Рецепторами, реагирующими на вибрацию, являются тельца Фатера-Пачини. Они находятся на участках кожи, не покрытой волосами: в слизистой оболочке, в жировой ткани подкожных слоев, в суставных сумках и сухожилиях и относятся к очень быстро адаптирующимся рецепторам. Тельца Фатера-Пачини – это детекторы коротких механических воздействий. Ощущение вибрации возникает при многократном раздражении капсулы тельца Фатера-Пачини. Последняя деформируется и действует на нервное окончание, расположенное в сердцевине тельца Фатера-Пачини. При этом в нервном окончании возникает генераторный потенциал. Тельце Фатера-Пачини реагирует на довольно высокочастотное раздражение – 40- 1000 Гц с максимальной чувствительностью 300 Гц. Выше 500 Гц ощущение давления или уменьшается, или полностью исчезает. Для появления ощущения вибрации необходимо вовлечение в процесс нескольких телец Фатера-Пачини. В этом случае потенциалы действия нервных волокон этих рецепторов дадут ощущение вибрации. За чувство щекотания отвечают свободные неинкапсулированные нервные окончания, расположенные в поверхностных слоях кожи. Они информируют как о наличии стимула, так и о его передвижениях по коже.Проводящие пути тактильного анализатора
Большинство механорецепторов кожи посылают импульсы в спинной мозг по волокнам типа А, а рецепторы щекотки – по Сволокнам. Пройдя через задние корешки в задние столбы, импульсы переключаются на интернейроны спинного мозга (второй нейрон, первый находится в спинальном ганглии) той же стороны. Далее по восходящим путям в составе задних столбов они достигают ядер Голля и Бурдаха, находящихся в продолговатом мозге (третий нейрон). Затем через медиальную петлю импульсы поступают в вентробазальные ядра (специфические) зрительного бугра (четвертый нейрон) и далее в первую и вторую соматосенсорные зоны коры противоположного полушария (задняя центральная извилина).Пороги тактильных ощущений
Тактильное ощущение можно получить в наиболее чувствительных тактильных точках, расположенных на кончиках пальцев, губах, кончике носа. Порог тактильного ощущения – это минимальная сила тактильного раздражения, при которой возникает первое тактильное ощущение. Для его определения используют специальный набор волосков (прибор Фрея). С помощью эстезиометрии определяют пространственный порог различения – это минимальное расстояние между двумя точками (рецепторами), на котором два одновременно приложенных раздражителя воспринимаются как раздельные. Так, на кончике пальцев, языка и губе он равен 1 – 3 мм, что свидетельствует о высокой чувствительности этих областей тела. На менее чувствительных поверхностях кожи – на спине, плечах, бедрах пространственное различение составляет 50- 100 мм.Температурная чувствительность
Различают два вида кожных рецепторов: холодовые и тепловые. К Холодовым рецепторам относят колбы Краузе, тепловым – тельца Руффини. Холодовые рецепторы располагаются под эпидермисом на глубине 0,17 мм от поверхности кожи, всего их около 250 тыс. Тепловые рецепторы залегают глубже – на расстоянии 0,3 мм от поверхности кожи в верхнем и нижнем слоях собственно кожи и слизистой. Их меньше, чем холодовых – около 30 тыс. На 1 см2 тыльной поверхности кисти руки у жителей, живущих в средней полосе России, приходится 11 – 13 холодовых и 1 – 2 тепловых рецептора. У холодовых рецепторов постоянная импульсация наблюдается в диапазоне от 41 до 10°С, а оптимальная чувствительность – в пределах от 15 до 30°С. Тепловые рецепторы реагируют постоянной частотой ПД в диапазоне от 20 до 50°С с оптимальной чувствительностью в пределах 34 – 42°С. Это статическая реакция рецепторов. Изменения температуры на 0,2°С вызывают изменения импульсации рецепторов в сторону ее уменьшения или увеличения. Такая реакция терморецепторов называется динамической. В диапазоне от 30 до 36°С происходит полное исчезновение ощущений холода или тепла – это зона комфорта, или нейтральная зона. Если повысить или понизить температуру выше или ниже этой зоны, то появляется ощущение тепла или холода. При небольших отклонениях температуры и длительном действии температурного фактора определенной величины развивается медленная частичная адаптация. Большие отклонения температуры внешней среды замедляют развитие адаптации. Импульсы от холодовых рецепторов поступают в спинной мозг по миелинизированным волокнам типа А-дельта, а от тепловых – по немиелинизированным волокнам типа С. Там находятся вторые нейроны, от которых начинается спиноталамический тракт, перекрещивающийся в каждом сегменте спинного мозга и заканчивающийся в вентробазальных ядрах зрительного бугра. Часть температурной информации поступает в сенсомоторную зону коры больших полушарий, а часть – в гипоталамические центры терморегуляции. В коре и лимбической системе формируется ощущение тепла, холода или температурного комфорта. Ощущение температурного комфорта можно получить, если в условиях высокой температуры окружающей среды поместить тело в прохладную воду, например при летнем купании. Можно получить парадоксальное ощущение холода, если «молчащие» при температуре 40°С холодовые рецепторы быстро нагревать до температуры выше 45°С.Висцеральный анализатор
Висцеральная чувствительность, или интероцепция, отвечает за восприятие раздражений внутренней среды организма и обеспечивает рефлекторную регуляцию и координацию работы внутренних органов. Рецепторы интероцептивного анализатора по функциональному назначению делят на механорецепторы, хеморецепторы, осморецепторы и терморецепторы. К механорецепторам относятся рецепторы, реагирующие на механические раздражения – растяжение и деформацию стенок внутренних органов (мочевого пузыря, желудка, сердца), барорецепторы кровеносных сосудов, принимающие участие в регуляции уровня кровяного давления. Хеморецепторы – это все тканевые рецепторы, воспринимающие различные химические раздражители; рецепторы аортальной и синокаротидной рефлексогенных зон, ответственные за изменения химического состава омывающей их крови, слизистых оболочек пищеварительного тракта и органов дыхания; рецепторы серозных оболочек, гипоталамуса, продолговатого мозга. Для осморецепторов адекватным стимулом являются изменения осмотического давления внутренней среды и концентрации осмотически активных веществ в крови и внеклеточной жидкости. Осморецепторы располагаются в интерстициальной ткани вблизи капилляров, их много в гипоталамусе. Так, недостаточное потребление пищи или воды вызывает раздражение глюкозных рецепторов или осморецепторов. В результате возникает ощущение голода или жажды. Терморецепторы воспринимают изменения температуры внутренней среды организма и локализованы в основном в верхних отделах пищеварительного тракта, органах дыхания, гипоталамусе. Интероцепторы представлены в организме свободными нервными окончаниями и специализированными инкапсулированными рецепторами, например тельцами Фатера -Пачини. Афференты от висцеральных рецепторов проходят в общих стволах с волокнами вегетативной нервной системы, в составе языкоглоточного, блуждающего, чревного и тазового нервов. Первые нейроны расположены в чувствительных ганглиях, вторые – в спинном и продолговатом мозге, третьи – в заднемедиальном ядре зрительного бугра. Корковый отдел висцерального анализатора находится в С, и С2 соматосенсорной и орбитальной областях коры больших полушарий.Проприоцептивный анализатор
Так называемое «мышечное чувство» формируется при изменении напряжения мышц, их оболочек, суставов, связок, сухожилий. Различают три типа проприоцепции: чувство позы или ощущение положения конечностей и ориентация их частей относительно друг друга чувство движения, когда проприоцепторы воспринимают как направление, так и скорость движения при изменениях угла сгибания в суставе. При этом человек осознает все виды движений в суставе; чувство силы, оцениваемое самим человеком и необходимое для поднятия груза или его перемещения в пространстве. Проприорецепторы находятся в мышцах, связках, сухожилиях, суставных сумках, фасциях. Это первичночувствующие рецепторы: мышечные веретена, тельца Гольджи, Фатера-Пачини, свободные нервные окончания. Мышечные веретена – это высокоспециализированные инкапсулированные мышечные волокна, снабженные афферетными и эфферентными нервными волокнами. В состав веретена входят интрафузальные мышечные волокна. В центре каждого волокна располагается ядерная сумка, содержащая первичные рецепторы или спиралевидные окончания чувствительных нервов. По обе стороны от ядерной сумки в миотрубке находятся вторичные рецепторы. На интрафузальном мышечном волокне заканчиваются эфферентные нервные волокна, относящиеся к типу гамма-волокон. Последние являются аксонами гамма-мотонейронов, расположенных в спинном мозге. Возбуждение гамма-мотонейронов приводит к сокращению интрафузальных мышечных волокон и уменьшению длины мышечного веретена. Сокращение скелетной мышцы поддерживается за счет активации гамма-эфферентов, а интрафузальное мышечное волокно постоянно следит за состоянием экстрафузальных мышечных волокон и всей скелетной мышцы, даже если она сокращена. Это позволяет держать скелетные мышцы в состоянии постоянного тонуса и сохранять определенную позу тела. Тельца Гольджи находятся в сухожилиях и представляют собой гроздевидные чувствительные окончания. При мышечном сокращении они испытывают действие натяжения и контролируют силу мышечного сокращения или напряжения. Первые нейроны проводникового отдела проприоцептивного анализатора располагаются в спинальных ганглиях. Аксоны нервных клеток в составе пучков Голля (нежного) и Бурдаха (клиновидного) через задние столбы достигают соответствующих ядер продолговатого мозга, где располагаются вторые нейроны. Далее после перекреста в составе медиальной петли доходят до третьих нейронов, расположенных в вентральном заднелатеральном и заднемедиальном ядрах зрительного бугра, откуда информация поступает в соматосенсорную область коры и область сильвиевой борозды (С,-С,2). Благодаря вышеописанному специфическому пути осознается положение мышцы. Импульсы от проприорецепторов идут и по неспецифическому пути. Направляясь к таламусу, информация поступает в ретикулярную формацию, от нее – к неспецифическим ядрам зрительного бугра, а затем диффузно ко всем участкам коры больших полушарий.Болевая чувствительность
Боль можно назвать шестым чувством, кроме основных пяти: зрения, слуха, вкуса, обоняния и осязания, благодаря которым организм получает необходимую информацию об окружающем мире. Боль дополняет каждое из пяти основных чувств, но в то же время остается самостоятельной и независимой от них. Ее главная особенность состоит в том, что она сообщает о внешних и внутренних повреждениях, хотя и является неприятным, тягостным, мучительным чувством. «Боль, – по выражению древних греков, – это сторожевой пес здоровья», постоянный союзник и помощник врача. Именно боль учит человека осторожности и сигнализирует о болезни. По мнению Ч. Шеррингтона, боль «в корне целесообразна», но до тех пор, пока она предупреждает о нарушении целостности организма. Как только информация учтена, а боль превращается в страдание, ее необходимо выключить. Согласно формулировке Международного комитета экспертов «боль – это неприятное сенсорное и эмоциональное переживание, связанное с истинным или потенциальным повреждением ткани». По определению П. К. Анохина, «боль – это интегративная функция организма, которая мобилизует различные функциональные системы организма для его защиты от вредоносных факторов». Проблема боли имеет три основных аспекта. Избавление человека от болей – это проблема врачей, фармацевтов, научных работников, т. е. медицинская проблема. Боль изменяет психику человека, его поведение в обществе, приводит к его дезорганизации, это – социальная проблема. И, наконец, боль – причина нетрудоспособности, а это уже экономическая проблема. Боль называют ноцицепцией (повреждением), а болевые рефлексы – ноцицептивными. Последние отличаются от других рефлексов, во-первых, тем, что они вызывают двигательную активность, направленную на устранение вредоносного фактора. Вовторых, ноцицептивные рефлексы всегда сопровождаются отрицательными эмоциями. B-трегьих, они доминируют в деятельности организма над всеми и остальными рефлексами.Типы боли
Боль делят на соматическую и висцеральную. Соматическая боль может быть поверхностной, если она возникает в коже, или глубокой – если в мышцах, костях, суставах или соединительной ткани. Поверхностная боль бывает эпикритической, или ранней, острой, быстрой, локализованной, предупреждающей и быстроадаптирующейся (например, укол иглой под ногтем), а также протопатической, которая следует за ранней. Это поздняя, тупая, нелокализованная, длительная, напоминающая и неадаптирующаяся боль. Глубокая соматическая боль – тупая, трудно локализованная, иррадиирующая в окружающие ткани. Висцеральная боль возникает во внутренних органах, например, боли в сердце при нарушении коронарного кровообращения, почечная колика при растяжении почечной лоханки. Зуд – это малоизученный тип кожного ощущения, который может переходить в боль при действии ряда вызывающих зуд стимулов высокой интенсивности. Блокада ноцицептивных путей приводит к исчезновению зуда, кроме того, болевые точки совпадают с точками зуда. Это ощущение можно вызвать внутрикожной инъекцией гистамина, который относят к алгогенам, т. е. веществам, вызывающим боль. Выделяют две основные причины болевых ощущений. Первая – это нарушение целостности покровных оболочек (кожи), при этом чаще всего возникает соматическая боль. Вторая причина – изменение уровня кислородного обеспечения, гипоксия тканей и как следствие – накопление Н+ ионов, которое улавливается рецепторами того органа, в котором нарушено кровообращение (например, боли в сердце при ишемии миокарда).Защитные реакции организма в ответ на боль
Болевые раздражители вызывают ряд рефлекторных соматических и вегетативных реакций. 1. Повышение мышечной активности и тонуса мускулатуры, а также принятие мер по устранению повреждения. 2. Активация симпатоадреналовой системы, трофики и кисло-родного обеспечения тканей. 3. Увеличение минутного объема дыхания, частоты дыхания. 4. Увеличение частоты сердечных сокращений, повышение артериального давления, расширение зрачков. 5. При повреждении кожи – увеличение содержания про-тромбина, тромбоцитов, лейкоцитов. Выработка антител, восста-новление целостности кожных покровов.Ноцицепторы
Относительно болевых рецепторов существуют две теории. Согласно «теории специфичности» М. Фрея боль воспринимают специализированные рецепторы – ноцицепторы, с очень высоким порогом, отвечающие лишь на повреждающие или грозящие поврежднением стимулы и несущие информацию по своим специализированным проводящим путям. Другая «теория интенсивности» отрицает наличие специализированных ноцицепторов, а болевое ощущение может быть вызвано надпороговым температурным или тактильным раздражителями. К ноцицепторам относят свободные немиелинизированные нервные окончания, образующие сплетения вокруг органов, в коже и мышцах. На 1 см2 поверхности кожи приходится 100 – 200 болевых рецепторов. По механизму возбуждения они делятся на механоноцицепторы и хемоноцицепторы. Механоноцицепторы связаны преимущественно с афферентными тонкими миелинизированными волокнами типа А-дельта со скоростью проведения импульсов от 2,5 до 20 м/с. Деполяризация мембраны механоноцицепторов происходит в результате ее механического смещения. Хемоноцицепторы деполяризуются при воздействии химических веществ (алгогенов). Они реагируют на изменения кровообращения в тканях и посылают информацию по тонким немиелинизированным нервным волокнам типа С со скоростью проведения возбуждения до 2 м/с. Волокна типа А-дельта проводят быструю, острую предупреждающую боль, а волокна типа С – медленную, тупую, напоминающую.Проводящие пути болевой чувствительности
Первый нейрон находится в чувствительных ганглиях, аксоны этих нейронов вступают в спинной мозг через задние корешки спинного мозга и подходят к вставочным нейронам (второй нейрон) и желатинозной субстанции. Далее импульсы проводятся двумя путями: специфическим (лемнисковым) и неспецифическим (экстралемнисковым). Специфический путь проходит в составе перекрещенного в каждом сегменте спиноталамического тракта до специфических ядер таламуса (третий нейрон) и заканчивается в соматосенсорной области коры (зоны С,-С2). Неспецифический путь – спиноретикулярный – от вставочного нейрона спинного мозга идет в ядре ретикулярной формации продолговатого мозга (третий нейрон) и в неспецифическом ядре таламуса (четвертый нейрон) и оттуда во все отделы коры больших полушарий. В проведении болевых ощущений участвуют также спиномезенцефалический и спиноцервикальный тракты. По коллатералям от проводящих путей болевая информация поступает в лимбическую систему, гипоталамус, обусловливая вегетативный и эмоциональный компоненты боли. Кора больших полушарий – зона С, отвечает за тонкий дискриминационный анализ болевого раздражения, а зона С2 – за осознание болевого ощущения и выработку программы действия. Лобная кора формирует мотивацию избавления от боли. Операция удаления лобной коры приводит к безразличному отношению к боли. Теменные доли коры отвечают за психогенную окраску боли. Механизм появления болевых ощущений объясняется гипотезой «ворот», предложенной в 1965 г. Р. Мелзаком, согласно которой на уровне спинного мозга, скорее всего в области желатинозной субстанции, а также, вероятно, в таламусе имеется скопление тормозных нейронов, препятствующих прохождению ноцицептивных импульсов по спиноталамическому тракту. Если поток этих импульсов превышает некоторый критический уровень, то человек ощущает боль.Гуморальная регуляция боли
Медиаторы: ацетилхолин, адреналин, норадреналин, серотонин активируют хемоноцицепторы. Ацетилхолин вызывает жгучую боль при подкожном введении или при накалывании на слизистую оболочку. Эта боль длится, как правило, 15 – 45 мин и может быть устранена М-холиноблокатором – атропином. Адреналин и норадреналин были обнаружены в большом количестве в моче больных инфарктом миокарда. Серотонин относят к модуляторам боли. Алгогенами является ряд биологически активных веществ: гистамин, который называют медиатором боли, брадикинин, выделяющийся в нервных окончаниях сердечной мышцы у больных с ишемией миокарда, каллидин, простагландины, субстанция Р – вызывает жгучую боль, находится в яде змей, пчел, скорпионов, была найдена в большом количестве в задних корешках спинного мозга. Ее также относят к медиаторам боли. Вызывают боль при подкожном введении вазопрессин, окситоцин, соматостатин, глутамат, а также ионы К+ и водорода.Отраженная боль
Ноцицептивная стимуляция внутреннего органа вызывает болевое ощущение не только в нем самом, но и в поверхностных и удаленных от данного органа частях тела. Это отраженная боль. Она возникает в результате конвергенции на одном и том же инернейроне спинного мозга афферентных волокон от определенного участка кожи и внутреннего органа, в котором имеет место ноцицептивное воздействие. Кроме того, ноцицептивные афференты в пределах одного и того же сегмента спинного мозга образуют коллатерали, при этом одно и то же волокно иннервирует и внутренний орган, и определенный участок кожи, а боль будет проявляться в соответствующем дерматоме (зоны Захарьина-Геда). Так, например, боли в сердце отражаются в левую лопатку и левое плечо. Действуя на активные точки в пределах зоны на поверхности кожи, можно снять боли в органе. На этом основан метод акупунктуры (иглоукалывания).Фантомная боль
Боль в утраченной конечности, появляющаяся после ее ампутации, называется фантомной болью. Эта боль возникает чаще всего у тех больных, которые ее испытывали еще до ампутации. Причина ее возникновения – создание очага патологического возбуждения в таламических ядрах, отвечающих за боль, и в коре больших полушарий. Запускают эту боль, вероятно, или медиатор боли, накопившийся в культе перерезанного нерва, или рубец, вызывающий раздражение конца нерва в культе. Примером фантомных болей могут быть также боли, возникающие в лунке удаленного зуба.Антиноцицептивная система
В 1973 г. с помощью радиоактивного морфия и его агонистов в головном и спинном мозге нашли участки связывания опиатов, т. е. веществ, оказывающих аналгезирующее (обезболивающее) действие, подобное опию. Были выявлены места «узнавания» опиатов или опиатные рецепторы. Найдены были вещества – лиганды, вступающие в контакт с этими рецепторами. Ими оказались олигопептиды: эндорфины – альфа, бета и гамма, лейцин или лей-энкефалин, метионин – или мет-энкефалин и динорфин. Самое большое количество опиатов было обнаружено в полосатом теле, среднем мозге, гипоталамусе, гипофизе, таламусе, центральном сером веществе, ядре шва, ретикулярной формации, желатинозной субстанции спинного мозга, в первой и второй сенсомоторпых зонах коры, в желудочно-кишечном тракте. В этих структурах были найдены опиатные рецепторы разных видов: мю, сигма), дельта, эпсилон, каппа. Каждый из опиатов взаимодействует преимущественно со своим рецептором. Так, морфий (алкалоид опия, сока мака) вступает в контакт с мю-рецепторами, энкефалин – с дельта-рецепторами, бета-эндорфин – сэпсклоп-роцепторами, динорфин – с каппа-рецепторами. Механизм действия этих веществ можно представить в виде следующей схемы. Боль запускает выработку гипоталамусом эндорфинов, последние стимулируют синтез эндорфинов гипофизом, которые затем попадают в спинномозговую жидкость и кровь, доставляющую их к пораженному органу и тканям, где они и оказывают обезболивающий эффект. Так, при шоке после обширной травмы тканей выделяется большое количество опиоидов, которые блокируют все виды чувствительности. Действие опиоидов подобно действию морфия. Аналгезирующий эффект морфия связан с уменьшением содержания брадикинина, субстанции Р и простагландинов. Морфий усиливает пресинаптическое торможение на уровне спинного мозга, вызывает гиперполяризацию в задних корешках и увеличивает уровень ГАМК.Аналгезирующие средства
Болевые ощущения можно снять, воздействуя на различные звенья болевого анализатора: ноцицепторы, проводящие пути и центры. На ноцицепторы действуют преимущественно наркотические анальгетики (морфин, кодеин, промедол, фентамин и др.), обезболивающий эффект которых обусловлен их способностью связываться с опиатными рецепторами и стабилизацией природных опиатов: энкефалинов и эндорфинов путем инактивации ферментов энкефалиназ, разрушающих опиаты. При субарахноидальном введении их аналгезирующее действие связывают с непосредственным влиянием этих веществ на структуры спинного мозга, участвующие в проведении болевых импульсов. Обезболивающий эффект этих препаратов может быть снят их антагонистом налоксоном. Инактивация ноцицепторов может быть получена путем локального разбрызгивания или смазывания поверхности слизистых оболочек местными анестетиками (новокаин, лидокаин и др.), которые используются также при инфильтрационной анестезии, блокирующей проведение болевых импульсов по нерву. К обезболивающим препаратам, оказывающим тормозное влияние наталамические центры, проводящие болевые импульсы к коре больших полушарий, относятся ненаркотические анальгетики: производные салициловой кислоты (ацетилсалициловая кислота, натрия салицилат); производные пиразолона (антипирин, анальгин, амидопирин и др.); производные парааминофенола (фенацетин, парацетамол и др.). Кроме центрального действия ненаркотические анальгетики ингибируют синтез простагландинов, относящихся к алгогенам.Глава 14. Высшая нервная деятельность
Приспособление животных и человека к изменяющимся условиям существования во внешней среде обеспечивается деятельностью нервной системы и реализуется через рефлекторную деятельность. В процессе эволюции возникли наследственно закрепленные реакции (безусловные рефлексы), которые объединяют и согласовывают функции различных органов, осуществляют адаптацию организма. У человека и высших животных в процессе индивидуальной жизни возникают качественно новые рефлекторные реакции, которые И. П. Павлов назвал условными рефлексами, считая их самой совершенной формой приспособления. В то время как относительно простые формы нервной деятельности определяют рефлекторную регуляцию гомеостаза и вегетативных функций организма, высшая нервная деятельность (ВНД) обеспечивает сложные индивидуальные формы поведения в изменяющихся условиях жизни. ВНД реализуется за счет доминирующего влияния коры на все нижележащие структуры центральной нервной системы. Основными процессами, динамично сменяющими друг друга в ЦНС, являются процессы возбуждения и торможения. В зависимости от их соотношения, силы и локализации строятся управляющие влияния коры. Функциональной единицей ВНД является условный рефлекс. Высшая нервная деятельность – это совокупность безусловных и условных рефлексов, а также высших психических функций, которые обеспечивают адекватное поведение в изменяющихся природных и социальных условиях. Впервые предположение о рефлекторном характере деятельности высших отделов мозга было высказано И. М. Сеченовым, что позволило распространить рефлекторный принцип и на психическую деятельность человека. Идеи И. М. Сеченова получили экспериментальное подтверждение в трудах И. П. Павлова, который разработал метод объективной оценки функций высших отделов мозга – метод условных рефлексов. И. П. Павлов показал, что все рефлекторные реакции можно разделить на две группы: безусловные и условные.Безусловные рефлексы 1. Врожденные, наследственно передающиеся реакции, большинство из них начинают функционировать сразу же после рождения. 2. Являются видовыми, т. е. свойственны всем представителям данного вида. 3. Постоянны и сохраняются в течение всей жизни. 4. Осуществляются за счет низших отделов ЦНС (подкорковые ядра, ствол мозга, спинной мозг). 5. Возникают в ответ на адекватные раздражения, действующие на определенное рецептивное поле.
Условные рефлексы 1. Реакции, приобретенные в процессе индивидуальной жизни. 2. Индивидуальные. 3. Непостоянны – могут возникать и исчезать. 4. Являются преимущественно функцией коры больших полушарий. 5. Возникают на любые раздражители, действущие на разные рецептивные поля.
Безусловные рефлексы могут быть простыми и сложными. Сложные врожденные безусловно-рефлекторные реакции называются инстинктами. Их характерной особенностью является цепной характер реакций. Условный рефлекс – это сложная многокомпонентная реакция, которая вырабатывается на базе безусловных рефлексов с использованием предшествующего индифферентного раздражителя. Он имеет сигнальный характер, и организм встречает воздействие безусловного раздражителя подготовленным. Например, в предстартовый период происходит перераспределение крови, усиление дыхания и кровообращения, и когда мышечная нагрузка начинается, организм уже к ней подготовлен.
Правила выработки условных рефлексов
Для выработки условного рефлекса необходимо: 1. наличие двух раздражителей, один из которых безусловный (пища, болевой раздражитель и др.), вызывающий безусловно-рефлекторную реакцию, а другой – условный (сигнальный), сигнализирующий о предстоящем безусловном раздражении (свет, звук, вид пищи и т. д.); 2. многократное сочетание условного и безусловного раздражителей (хотя возможно образование условного рефлекса при их однократном сочетании); 3. условный раздражитель должен предшествовать действию безусловного; 4. в качестве условного раздражителя может быть использован любой раздражитель внешней или внутренней среды, который должен быть по возможности индифферентным, не вызывать оборонительной реакции, не обладать чрезмерной силой и способен привлекать внимание; 5. безусловный раздражитель должен быть достаточно сильным, в противном случае временная связь не сформируется; 6. возбуждение от безусловного раздражителя должно быть более сильным, чем от условного; 7. необходимо устранить посторонние раздражители, так как они могут вызывать торможение условного рефлекса; 8. животное, у которого вырабатывается условный рефлекс, должно быть здоровым;? 9. при выработке условного рефлекса должна быть выражена мотивация, например, при выработке пищевого слюноотделительного рефлекса животное должно быть голодным, у сытого – этот рефлекс не вырабатывается (рис. 34). Условные рефлексы легче вырабатывать на экологически близкие данному животному воздействия. В связи с этим условные рефлексы делятся на натуральные и искусственные. Натуральные условные рефлексы вырабатываются на агенты, которые в естественных условиях действуют вместе с раздражителем, вызывающим безусловный рефлекс (например, вид пищи, ее запах и т. д.). Все остальные условные рефлексы искусственные, т. е. вырабатываются на агенты, в норме не связанные с действием безусловного раздражителя, например, пищевой слюноотделительный рефлекс на звонок.
Физиологической основой для возникновения условных рефлексов служит образование функциональных временных связей в высших отделах ЦНС. Временная связь – это совокупность нейрофизиологических, биохимических и ультраструктурных изменений в мозге, возникающих в процессе совместного действия условного и безусловного раздражителей. И. П. Павлов высказал предположение, что при выработке условного рефлекса происходит формирование временной нервной связи между двумя группами клеток коры – корковыми представительствами условного и безусловного рефлексов. Возбуждение от центра условного рефлекса может передаваться к центру безусловного рефлекса от нейрона к нейрону. Следовательно, первый путь образования временной связи между корковыми представительствами условного и безусловного рефлексов является внутрикортикальным. Однако при разрушении коркового представительства условного рефлекса выработанный условный рефлекс сохраняется. По-видимому, образование временной связи идет между подкорковым центром условного рефлекса и корковым центром безусловного рефлекса. При разрушении коркового представительства безусловного рефлекса условный рефлекс также сохраняется. Следовательно, выработка временной связи может идти между корковым центром условного рефлекса и подкорковым центром безусловного рефлекса. Разобщение корковых центров условного и безусловного рефлексов путем пересечения коры мозга не препятствует образованию условного рефлекса. Это свидетельствует о том, что временная связь может образоваться между корковым центром условного рефлекса, подкорковым центром безусловного рефлекса и корковым центром безусловного рефлекса.
Имеются различные мнения по вопросу о механизмах образования временной связи. Возможно, образование временной связи происходит по принципу доминанты. Очаг возбуждение от безусловного раздражителя всегда сильнее, чем от условного, так как безусловный раздражитель всегда биологически более значим для животного. Этот очаг возбуждения является доминантным, следовательно притягивает к себе возбуждение от очага условного раздражения. Если возбуждение прошло по каким-либо нервным цепям, то в следующий раз оно по этим путям пройдет значительно легче (явление «проторения пути»), В основе этого лежат: суммация возбуждений, длительное повышение возбудимости синаптических образований, увеличение количества медиатора в синапсах, увеличение образования новых синапсов. Все это создает структурные предпосылки к облегчению движения возбуждения по определенным нейронным цепям.
Другим представлением о механизме формирования временной связи является конвергентная теория. В ее основе лежит способность нейронов отвечать на раздражения разных модальностей. По представлениям П. К. Анохина, условный и безусловный раздражители вызывают распространенную активацию корковых нейронов благодаря включению ретикулярной формации. В результате восходящие сигналы (условного и безусловного раздражителей) перекрываются, т. е. происходит встреча этих возбуждений на одних и тех же корковых нейронах. В результате конвергенции возбуждений возникают и стабилизируются временные связи между корковыми представительствами условного и безусловного раздражителей.
Условные рефлексы легче вырабатывать на экологически близкие данному животному воздействия. В связи с этим условные рефлексы делятся на натуральные и искусственные. Натуральные условные рефлексы вырабатываются на агенты, которые в естественных условиях действуют вместе с раздражителем, вызывающим безусловный рефлекс (например, вид пищи, ее запах и т. д.). Все остальные условные рефлексы искусственные, т. е. вырабатываются на агенты, в норме не связанные с действием безусловного раздражителя, например, пищевой слюноотделительный рефлекс на звонок.
Физиологической основой для возникновения условных рефлексов служит образование функциональных временных связей в высших отделах ЦНС. Временная связь – это совокупность нейрофизиологических, биохимических и ультраструктурных изменений в мозге, возникающих в процессе совместного действия условного и безусловного раздражителей. И. П. Павлов высказал предположение, что при выработке условного рефлекса происходит формирование временной нервной связи между двумя группами клеток коры – корковыми представительствами условного и безусловного рефлексов. Возбуждение от центра условного рефлекса может передаваться к центру безусловного рефлекса от нейрона к нейрону. Следовательно, первый путь образования временной связи между корковыми представительствами условного и безусловного рефлексов является внутрикортикальным. Однако при разрушении коркового представительства условного рефлекса выработанный условный рефлекс сохраняется. По-видимому, образование временной связи идет между подкорковым центром условного рефлекса и корковым центром безусловного рефлекса. При разрушении коркового представительства безусловного рефлекса условный рефлекс также сохраняется. Следовательно, выработка временной связи может идти между корковым центром условного рефлекса и подкорковым центром безусловного рефлекса. Разобщение корковых центров условного и безусловного рефлексов путем пересечения коры мозга не препятствует образованию условного рефлекса. Это свидетельствует о том, что временная связь может образоваться между корковым центром условного рефлекса, подкорковым центром безусловного рефлекса и корковым центром безусловного рефлекса.
Имеются различные мнения по вопросу о механизмах образования временной связи. Возможно, образование временной связи происходит по принципу доминанты. Очаг возбуждение от безусловного раздражителя всегда сильнее, чем от условного, так как безусловный раздражитель всегда биологически более значим для животного. Этот очаг возбуждения является доминантным, следовательно притягивает к себе возбуждение от очага условного раздражения. Если возбуждение прошло по каким-либо нервным цепям, то в следующий раз оно по этим путям пройдет значительно легче (явление «проторения пути»), В основе этого лежат: суммация возбуждений, длительное повышение возбудимости синаптических образований, увеличение количества медиатора в синапсах, увеличение образования новых синапсов. Все это создает структурные предпосылки к облегчению движения возбуждения по определенным нейронным цепям.
Другим представлением о механизме формирования временной связи является конвергентная теория. В ее основе лежит способность нейронов отвечать на раздражения разных модальностей. По представлениям П. К. Анохина, условный и безусловный раздражители вызывают распространенную активацию корковых нейронов благодаря включению ретикулярной формации. В результате восходящие сигналы (условного и безусловного раздражителей) перекрываются, т. е. происходит встреча этих возбуждений на одних и тех же корковых нейронах. В результате конвергенции возбуждений возникают и стабилизируются временные связи между корковыми представительствами условного и безусловного раздражителей.
Условные рефлексы второго, третьего и более высоких порядков
Если выработать прочный условный пищевой рефлекс, например, на свет, то такой рефлекс является условным рефлексом первого порядка. На его базе можно выработать условный рефлекс второго порядка, для этого дополнительно применяют новый, предшествующий сигнал, например звук, подкрепляя его условным раздражителем первого порядка (светом). В результате нескольких сочетаний звука и света звуковой раздражитель также начинает вызывать слюноотделение. Таким образом возникает новая более сложная опосредованная временная связь. Следует подчеркнуть, что подкреплением для условного рефлекса второго порядка является именно условный раздражитель первого порядка, а не безусловный раздражитель (пища), так как если и свет и звук подкреплять пищей, то возникнут два отдельных условных рефлекса первого порядка. При достаточно прочном условном рефлексе второго порядка можно выработать условный рефлекс третьего порядка. Для этого используется новый раздражитель, например, прикосновение к коже. В этом случае прикосновение подкрепляется только условным раздражителем второго порядка (звуком), звук возбуждает зрительный центр, а последний – пищевой центр. Возникает еще более сложная временная связь. Рефлексы более высокого порядка (4, 5, 6 и т. д.) вырабатываются только у приматов и человека.Динамический стереотип
Отдельные условные рефлексы в определенной ситуации могут связываться между собой в комплексы. Если осуществлять ряд условных рефлексов в строго определенном порядке с примерно одинаковыми временными интервалами и весь этот комплекс сочетаний многократно повторять, то в мозге сформируется единая система, имеющая специфическую последовательность рефлекторных реакций, т. е. ранее разрозненные рефлексы связываются в единый комплекс. Нейроны головного мозга, обладая большой функциональной подвижностью, тем не менее могут стойко удерживать систему ответных реакций на повторяющиеся условные раздражения. Возникает динамический стереотип, который выражается в том, что на систему различных условных сигналов, действующих всегда один за другим через определенное время, вырабатывается постоянная и прочная система ответных реакций. В дальнейшем, если применять только первый раздражитель, то в ответ будут развиваться все остальные реакции. Динамический стереотип – характерная особенность психической деятельности человека. Многие наши навыки, например, способность писать, играть на музыкальных инструментах, танцевать и т. д. в сущности являются автоматическими цепями двигательных актов. В процессе жизни человека обычно вырабатываются и более сложные стереотипы поступков: поведение после пробуждения или перед сном, режим труда, отдыха, питания. Возникают относительно устойчивые формы поведения в обществе, во взаимоотношениях с другими людьми, в оценке текущих событий и реагирования на них. Такие стереотипы имеют большое значение в жизни человека, так как позволяют выполнять многие виды деятельности с меньшим напряжением нервной системы. Биологический смысл динамических стереотипов сводится к тому, чтобы освободить корковые центры от решения стандартных задач, для того чтобы обеспечить выполнение более сложных, требующих эвристического мышления.Торможение условных рефлексов
Для обеспечения приспособления и адекватного поведения необходимы не только способность к выработке новых условных рефлексов и их длительное сохранение, но и возможность к устранению тех условно-рефлекторных реакций, необходимость в которых отсутствует. Исчезновение условных рефлексов обеспечивается процессами торможения. По И. П. Павлову, различают следующие формы коркового торможения: безусловное, условное и запредельное торможение.Безусловное торможение
Этот вид торможения условных рефлексов возникает сразу в ответ на действие постороннего раздражителя, т. е. является врожденной, безусловной формой торможения. Безусловное торможение может быть внешним и запредельным. Внешнее торможение возникает под влиянием нового раздражителя, создающего доминантный очаг возбуждения, формирующего ориентировочный рефлекс. Биологическое значение внешнего торможения состоит в том, что, затормаживая текущую условно-рефлекторную деятельность, оно позволяет переключить организм на определение значимости и степени опасности нового воздействия. Посторонний раздражитель, оказывающий тормозящее влияние па течение условных рефлексов, называется внешним тормозом. При многократном повторении постороннего раздражителя вызываемый ориентировочный рефлекс постепенно уменьшается, а затем исчезает и уже не вызывает торможения условных рефлексов. Такой внешний тормозящий раздражитель называется гаснущим тормозом. Если же посторонний раздражитель содержит биологически важную информацию, то он всякий раз вызывает торможение условных рефлексов. Такой постоянный раздражитель называется постоянным тормозом. Биологическое значение внешнего торможения – обеспечение условий для более важного в данный момент ориентировочного рефлекса, вызванного экстренным раздражителем, и создание условий для его срочной оценки.Условное торможение (внутреннее)
Оно возникает, если условный раздражитель перестает подкрепляться безусловным. Его называют внутренним, потому что оно формируется в структурных компонентах условного рефлекса. Условное торможение требует для выработки определенного времени. К этому виду торможения относятся: угасательное, дифференцировочное, условный тормоз и запаздывающее. Угасательное торможение развивается в тех случаях, когда условный раздражитель перестает подкрепляться безусловным, при этом условная реакция постепенно исчезает. При первом предъявлении условного раздражителя без последующего подкрепления условная реакция проявляется как обычно. Последующие предъявления условного раздражителя без подкрепления начинают вызывать ориентировочную реакцию, которая затем угасает. Постепенно исчезает и условно-рефлекторная реакция. Дифференцировочное торможение вырабатывается на раздражители, близкие по характеристике к условному раздражителю. Этот вид торможения лежит в основе различения раздражителей. С помощью этого торможения из сходных раздражителей выделяется тот, который будет подкрепляться безусловным раздражителем, т. е. биологически важный для организма. Например, на звук метронома с частотой 120 ударов в 1 мин у собаки выделяется слюна. Если теперь этому животному в качестве раздражителя предъявить звук метронома с частотой 60 ударов, но не подкреплять его, то в первых опытах этот раздражитель тоже вызывает отделение слюны. Но через некоторое время возникает дифференцировка этих двух раздражителей и на звук с частотой 60 ударов слюна выделяться перестает. Условный тормоз – это разновидность дифференцировочного торможения. Возникает в том случае, если положительный условный раздражитель подкрепляется безусловным, а комбинация из условного и индифферентного раздражителей не подкрепляется. Например, условный раздражитель свет подкрепляется безусловным раздражителем, а комбинация свет и звонок не подкрепляется. Первоначально эта комбинация вызывает такой же условный ответ, но в дальнейшем она утрачивает свое сигнальное значение и на нее условная реакция возникать не будет, в то время как на изолированный условный раздражитель (свет) она сохраняется. Звонок же приобретает значение тормозного сигнала. Его подключение к любому другому условному раздражителю затормаживает проявление условного рефлекса. Запаздывающее торможение характеризуется тем, что условная реакция на условный раздражитель возникает до действия безусловного раздражителя. При увеличении интервала между началом действия условного раздражителя и моментом подкрепления (до 2–3 мин) условная реакция все более и более запаздывает и начинает возникать непосредственно перед предъявлением подкрепления. Отставание условной реакции от начала действия условного раздражителя свидетельствует о выработке запаздывающего торможения, так как период торможения соответствует периоду запаздывания подкрепления. Условное торможение дает возможность организму избавиться от большого количества лишних биологически нецелесообразных реакций. Внутреннее торможение (по П. К. Анохину) является результатом борьбы двух потоков возбуждений при их выходе на эффекторы. При угасательном торможении, например, пищевого слюноотделительного условного рефлекса – это поток возбуждений соответствующей пищевой реакции и поток возбуждений, характерный для биологически отрицательной реакции, возникающий при отсутствии подкрепления. Более сильное, доминирующее возбуждение реакции неудовлетворения тормозит менее сильное, пищевое возбуждение.Запредельное торможение
Этот вид торможения отличается от внешнего и внутреннего по механизму возникновения и физиологическому значению. Оно возникает при чрезмерном увеличении силы или продолжительности действия условного раздражителя, вследствие того, что сила раздражителя превышает работоспособность корковых клеток. Это торможение имеет охранительное значение, так как препятствует истощению нервных клеток. По своему механизму оно напоминает явление «пессимума», которое было описано Н. Е. Введенским. Запредельное торможение может вызываться действием не только очень сильного раздражителя, но и действием небольшого по силе, но длительного и однообразного по характеру раздражения. Это раздражение, постоянно действуя на одни и те же корковые элементы, приводит их к истощению, а следовательно, сопровождается возникновением охранительного торможения. Запредельное торможение легче развивается при снижении работоспособности, например, после тяжелого инфекционного заболевания, стресса, чаще развивается у пожилых людей.Иррадиация, концентрация и индукция возбуждения и торможения
В начале образования положительного условного рефлекса происходит распространение возбуждения из непосредственного пункта раздражения в коре мозга на другие отделы. Такое распространение И. П. Павлов назвал иррадиацией возбудительного процесса. При иррадиации в процесс возбуждения вовлекаются соседние нервные клетки по отношению к группе клеток, непосредственно возбужденных пришедшими сигналами. Распространение происходит по ассоциативным нервным волокнам коры, которые соединяют рядом расположенные клетки. В иррадиации возбуждения могут участвовать также подкорковые образования и ретикулярная формация. По мере замедления условного рефлекса возбуждение сосредоточивается все в более ограниченной зоне коры, к которой адресовано раздражение. Это явление носит название концентрации возбудительного процесса. В случае выработки дифференцировочного торможения, оно и ограничивает иррадиацию возбуждения. И. П. Павлов считал, что торможение также способно к иррадиации и концентрации. Торможение, возникшее в анализаторе при использовании отрицательного условного раздражителя, иррадиирует по коре головного мозга, но в 4–5 раз медленнее (от 20 сек до 5 мин), чем возбуждение. Еще медленнее происходит концентрация торможения. По мере повторения и закрепления отрицательного условного рефлекса время концентрации торможения укорачивается и торможение сосредоточивается в ограниченной зоне коры. При исследовании взаимоотношений возбуждения и торможения в коре мозга было установлено, что в течение нескольких секунд после воздействия тормозного раздражителя эффект положительных условных раздражителей усиливается. И наоборот, после применения положительных условных раздражителей усиливается действие тормозящих раздражений. Первое явление названо И. П. Павловым отрицательной индукцией, второе – положительной индукцией. При положительной индукции в клетках, смежных с теми, где только что вызывалось торможение, после прекращения действия тормозного сигнала возникает состояние повышенной возбудимости. Вследствие этого импульсы, поступающие к нейронам при действии положительного раздражителя, вызывают повышенный эффект. При отрицательной индукции в клетках коры, окружающих возбужденные нейроны, возникает процесс торможения. Отрицательная индукция ограничивает иррадиацию процесса возбуждения в коре мозга. Отрицательной индукцией можно объяснить торможение условных рефлексов более сильными посторонними раздражениями (внешнее безусловное торможение). Такое сильное раздражение вызывает в коре мозга интенсивное возбуждение нейронов, вокруг которых появляется широкая зона торможения нейронов, захватывающая клетки, возбужденные условным раздражителем. Явления отрицательной и положительной индукции в коре головного мозга подвижны, постоянно сменяют друг друга. В разных пунктах коры мозга одновременно могут возникать очаги возбуждения и торможения, положительной и отрицательной индукции.Аналитическая и синтетическая деятельность коры головного мозга
Деятельность коры головного мозга обеспечивает постоянный анализ и синтез сигналов, поступающих из окружающей и внутренней среды организма. Анализ и синтез неразрывно связаны между собой и не могут происходить изолированно. Синтетическая деятельность коры головного мозга проявляется объединением возбуждений, возникающих в различных зонах коры мозга. Важнейшим механизмом этого объединения является образование временной условно-рефлекторной связи. У человека синтетическая деятельность коры не ограничивается лишь формированием временных связей между корковыми представительствами безусловных рефлексов и центрами органов чувств. Существенное значение имеет образование временных связей между центрами, участвующими в восприятии комплексных и последовательных раздражений. Аналитическая деятельность коры головного мозга заключается в дифференцировании по характеру и интенсивности массы раздражений, доходящих в форме сигналов до мозговой коры, что достигается с помощью внутреннего торможения, позволяющего точно дифференцировать раздражители по их биологической значимости. Анализ внешних и внугренних воздействий в организме начинается с момента их действия на рецепторы. По пути к корковым нейронам афферентные сигналы проходят ряд образований центральной нервной системы, где происходит их элементарный анализ. Высший же анализ осуществляется в коре головного мозга.Свойства нервных процессов
Под свойствами нервных процессов понимают такие характеристики возбуждения и торможения, как сила, уравновешенность и подвижность этих процессов.Сила нервных процессов.
При измерении силы процесса возбуждения обычно пользуются кривой зависимости величины условной реакции от силы раздражителя. Условная реакция перестает увеличиваться при определенной интенсивности условного сигнала. Эта граница и характеризует силу процесса возбуждения. Показателем силы тормозного процесса является стойкость тормозных условных рефлексов, а также скорость и прочность выработки дифференцировочного и запаздывающего вида торможения.Уравновешенность нервных процессов.
Для определения уравновешенности нервных процессов сравниваются силы процессов возбуждения и торможения у данного животного. Если оба процесса взаимно компенсируют друг друга, то они уравновешены, а если нет, то, например, при выработке дифференцировок может наблюдаться срыв тормозного процесса, если он оказывается слабым. Если же доминирует тормозной процесс в силу недостаточности возбуждения, то в трудных условиях дифференцировка сохраняется, но резко уменьшается величина реакции на положительный условный сигнал.Подвижность нервных процессов.
О ней можно судить по скорости переделки положительных условных рефлексов в тормозные и обратно. Часто для определения подвижности нервных процессов применяется переделка динамического стереотипа. Если переход от положительной реакции к тормозной и от тормозной к положительной осуществляется быстро, то это свидетельствует о высокой подвижности нервных процессов.Типы высшей нервной деятельности
В лаборатории И. П. Павлова было замечено, что поведение собак в естественной обстановке и во время выработки условных рефлексов различное. Некоторые животные очень подвижны, возбудимы и любопытны, другие медлительны и трусливы. Между этими крайними типами имеется ряд промежуточных. На основании свойств нервных процессов И. П. Павлову удалось разделить животных на определенные группы, причем эта классификация совпала с умозрительной классификацией типов людей (темпераментов), данной еще Гиппократом. В основу классификации типов ВНД были положены свойства нервных процессов: сила, уравновешенность и подвижность. По критерию силы нервных процессов выделяют сильный и слабый типы. У слабого типа процессы возбуждения и торможения слабые, поэтому подвижность и уравновешенность нервных процессов не могут быть охарактеризованы достаточно точно. Сильный тип нервной системы подразделяется на уравновешенный и неуравновешенный. Выделяется группа, которая характеризуется неуравновешенными процессами возбуждения и торможения с преобладанием возбуждения над торможением (безудержный тип), когда основным свойством является неуравновешенность. Для уравновешенного типа, у которого процессы возбуждения и торможения сбалансированы, приобретает значение быстрота смены процессов возбуждения и торможения. В зависимости от этого показателя различают подвижный и инертный типы ВНД.Эксперименты, проведенные в лабораториях И. П. Павлова, позволили создать следующую классификацию типов ВНД: 1. Слабый (меланхолик). 2. Сильный, неуравновешенный с преобладанием процессов возбуждения (холерик). 3. Сильный, уравновешенный, подвижный (сангвиник). 4. Сильный, уравновешенный, инертный (флегматик).
Экспериментальные неврозы
В лаборатории И. П. Павлова удалось вызвать экспериментальные неврозы (функциональные расстройства деятельности ЦНС), используя перенапряжение нервных процессов, что достигалось путем изменения характера, силы и продолжительности условных раздражений.Неврозы могут возникать: 1. при перенапряжении процесса возбуждения вследствие применения длительного интенсивного раздражителя; 2. при перенапряжении тормозного процесса путем, например, удлинения периода действия дифференцировочных раздражений или выработки тонких дифференцировок на очень близкие фигуры, тоны и др.; 3. при перенапряжении подвижности нервных процессов, например, путем переделки положительного раздражителя в тормозной при очень быстрой смене раздражителей или при одновременной переделке тормозного условного рефлекса в положительный.
При неврозах возникает срыв высшей нервной деятельности. Он может выражаться в резком преобладании или возбудительного, или тормозного процесса. При преобладании возбуждения подавлены тормозные условные рефлексы, появляется двигательное возбуждение. При преобладании тормозного процесса ослабляются положительные условные рефлексы, возникает сонливость, ограничивается двигательная активность. Неврозы особенно легко воспроизводятся у животных с крайними типами нервной системы: слабым и неуравновешенным. Сущность невроза заключается в понижении работоспособности нервных клеток. Нередко при неврозах развиваются переходные (фазовые) состояния: уравнительная, парадоксальная, ультрапарадоксальная фазы. Фазовые состояния отражают нарушения закона силовых отношений, характерного для нормальной нервной деятельности. В норме наблюдается количественная и качественная адекватность рефлекторных реакций действующему раздражителю, т. е. на раздражитель слабой, средней или большой силы возникает соответственно слабая, средняя или сильная реакция. При неврозе уравнительное фазовое состояние проявляется одинаковыми по выраженности реакциями на раздражители разной силы, парадоксальное – развитием сильной реакции на слабое воздействие и слабые реакции на сильные воздействия, ультрапарадоксальпое – возникновением реакции на тормозной условный сигнал и выпадением реакции на положительный условный сигнал. При неврозах развивается инертность нервных процессов или их быстрая истощаемость. Функциональные неврозы могут приводить к патологическим изменениям в различных органах. Так, например, возникают поражения кожи типа экземы, выпадение волос, нарушение деятельности пищеварительного тракта, печени, почек, эндокринных желез и даже возникновение злокачественных новообразований. Обостряются заболевания, которые были до невроза.
Первая и вторая сигнальные системы
Типы ВНД, о которых говорилось выше, являются общими для животных и человека. Можно выделить особые, присущие только человеку типологические черты. По мнению И. П. Павлова, в их основе лежит степень развития первой и второй сигнальных систем. Первая сигнальная система – это зрительные, слуховые и другие чувственные сигналы, из которых строятся образы внешнего мира. Восприятие непосредственных сигналов предметов и явлений окружающего мира и сигналов из внутренней среды организма, приходящих от зрительных, слуховых, тактильных и других рецепторов, составляет первую сигнальную систему, которая имеется у животных и человека. Отдельные элементы более сложной сигнальной системы начинают появляться у общественных видов животных (высокоорганизованных млекопитающих и птиц), которые используют звуки (сигнальные коды) для предупреждения об опасности, о том, что данная территория занята и т. д. Но лишь у человека в процессе трудовой деятельности и социальной жизни развивается вторая сигнальная система – словесная, в которой слово в качестве условного раздражителя, знака, не имеющего реального физического содержания, но являющегося символом предметов и явлений материального мира, становится сильным стимулом. Эта система сигнализации состоит в восприятии слов – слышимых, произносимых (вслух или про себя) и видимых (при чтении и письме). Одно и то же явление, предмет на разных языках обозначается словами, имеющими разное звучание и написание, из этих словесных (вербальных) сигналов создаются абстрактные понятия. Способность понимать, а потом и произносить слова возникает у ребенка в результате ассоциации определенных звуков (слов) со зрительными, тактильными и другими впечатлениями о внешних объектах. Субъективный образ возникает в мозге на основе нейронных механизмов при декодировании информации и сравнении ее с реально существующими материальными объектами. С возникновением и развитием второй сигнальной системы появляется возможность осуществления абстрактной формы отражения – образование понятий и представлений. Раздражители второй сигнальной системы отражают окружающую действительность с помощью обобщающих, абстрагирующих понятий, выражаемых словами. Человек может опе-рировать не только образами, но и связанными с ними мыслями, осмысленными образами, содержащими смысловую (семантическую) информацию. С помощью слова осуществляется переход от чувственного образа первой сигнальной системы к понятию, представлению второй сигнальной системы. Способность оперировать абстрактными понятиями, выражаемыми словами служит основой мыслительной деятельности. Язык – это средство выражения мысли и форма существования мысли. Язык закрепляет в предложениях результаты работы мышления, делает возможным обмен мыслями. Речь дает возможность создавать научные понятия, формулировать законы. Речь может участвовать в регуляции деятельности различных органов с помощью слова. Словесные раздражители являются физиологически активными факторами, они изменяют функцию внутренних органов, интенсивность обменных процессов, воздействуют на мышечную и сенсорные системы. Вовремя сказанное доброе слово может повышать работоспособность, способствовать хорошему настроению. Неосторожно произнесенное в присутствии больного слово может значительно ухудшить его состояние.Физиологические основы речи.
Для декодирования речи, воспринимаемой в акустической форме, важнейшим условием является удержание в речевой памяти всех ее элементов, а в оптической форме – участие сложных поисковых движений глаз. Процессы декодирования речи осуществляются височно-теменно-затылочными отделами левого полушария (у правшей). При поражении этих отделов коры происходит нарушение понимания логико-грамматических конструкций и счетных операций. Вторая сигнальная система допускает неоднозначные отношения между явлением, предметом и его обозначением (словом), ч то позволило человеку действовать разумно в условиях вероятностного событийного окружения (информационной неопределенности). Это во многом способствовало развитию способностей к интуитивному мышлению. Возникла принципиально новая форма мыслительной деятельности – построение умозаключений па основе использования многозначной (вероятностной) логики. Постоянное использование языка привело к тому, что человеческий мозг, как правило, оперирует неточными понятиями, качественными оценками легче, чем количественными категориями, числами. Учитывая соотношения первой и второй сигнальной систем в том или ином индивидууме, И. П. Павлов выделил специфические человеческие типы ВНД в зависимости от преобладания первой или второй сигнальной системы в восприятии действительности. Людей с преобладанием функций корковых проекций, ответственных за первосигнальные раздражители, И. П. Павлов относил к художественному типу (у представителей этого типа преобладает образный тип мышления). Это люди, для которых характерна яркость зрительных и слуховых восприятий событий окружающего мира (художники и музыканты). Если же более сильной оказывается вторая сигнальная система, то таких людей относят к мыслительному типу. У представителей этого типа преобладает логический тип мышления, способность к построению абстрактных понятий (ученые, философы). В тех случаях, когда первая и вторая сигнальные системы создают нервные процессы одинаковой силы, то такие люди относятся к среднему (смешанному типу), к которому относится большинство людей. Но есть еще один крайне редкий типологический вариант, к которому относятся очень редкие люди, имеющие особо сильное развитие и первой, и второй сигнальных систем. Эти люди способны как к художественному, так и к научному творчеству, к числу таких гениальных личностей И. П. Павлов относил Леонардо да Винчи.Высшие психические функции
Психика – это специфическое свойство головного мозга, заключающееся в отражении предметов и явлений существующего вне нас и независимо от нас материального мира. Ощущения и восприятия являются необходимым начальным этапом наших знаний о самом себе и о внешнем мире. Ощущение – это процесс отражения в ЦНС отдельных свойств предметов и явлений объективной реальности, непосредственно воздействующей на органы чувств. Всякое ощущение имеет качество, силу, длительность. Качественные особенности тех или иных ощущений называются их модальностью. Ощущения дают материал для более сложных форм отражения действительности в сознании (восприятия, мышления), т. е. являются источником всех знаний об окружающей нас действительности. Восприятие – процесс приема и преобразования информации, обеспечивающей организму ориентировку в окружающем мире. Это активный процесс выделения из массы разнородных объектов внешнего мира тех, которые более всего необходимы в данный момент. Ощущения и восприятия человека носят сознательный, осмысленный характер. Важную роль в этом играют мышление и речь. Мышление позволяет получить знания о таких объектах, свойствах и отношениях реального мира, которые не могут быть непосредственно чувственно восприняты. Мышление – процесс опосредованного, обобщенного отражения действительности с ее связями, отношениями и закономерностями. С помощью мышления познается содержание и смысл воспринимаемого, а также внутренние особенности предметов и явлений. С помощью мышления человек может понять настоящее, будущее и прошедшее, строить гипотезы и обеспечивать их проверку. Наиболее высокая форма обобщения – понятие. В понятии отражено то, что не может быть непосредственно воспринято при помощи органов чувств, оно отражает в предмете лишь существенное. Отличительной особенностью человеческого мышления является его неразрывная связь с речью, языком. Внимание – это сосредоточенность психической деятельности на определенном объекте. С помощью внимания обеспечивается отбор необходимой информации. Нейрофизиологические механизмы внимания связаны с проявлениями ориентировочного рефлекса, с локальными процессами активации коры головного мозга, а также с эмоциональными состояниями и биологическими потребностями организма. Избирательное внимание возможно лишь при состоянии повышенного, но не чрезмерно высокого бодрствования, которое на ЭЭГ характеризуется высокочастотными десинхронизированными колебаниями низкой амплитуды с редким появлением групп синхронизированных альфаволи. Диффузным формам внимания соответствуют состояния расслабленного бодрствования с четко выраженными синхронизированными альфа-ритмами. Рассеянное внимание часто возникает в состоянии сильного возбуждения, при этом на ЭЭГ регистрируется десинхронизированная высокочастотная низкоамплитудная электрическая активность. Анатомическим субстратом регуляции различных форм внимания является ретикулярная формация ствола мозга, диффузная таламическая система, субталамус и гипоталамус. Неспецифическая таламическая система рассматривается как фильтрующий механизм, обладающий способностью переключать внимание с одних раздражителей на другие. Ассоциативные зоны коры являются центральным звеном в системе механизмов, регулирующих отбор информации, избирательные формы восприятия, внимания и сознания.Память
Память – одно из основных свойств ЦНС, выражающееся в способности на короткое или длительное время сохранять информацию (отпечатки, следы) о событиях внешнего мира и реакциях организма. Память складывается из трех взаимосвязанных этапов: запоминания, хранения и воспроизведения информации. Процесс запечатления в ЦНС поступающей информации может быть двух видов: произвольный и непроизвольный. Произвольное запечатление оказывается более эффективным. Стимулы, имеющие большое биологическое и социальное значение, фиксируются значительно эффективнее независимо от их физической силы. Сохранение следов является центральным звеном в системе памяти. В процессе накопления и хранения приобретенной информации в ЦНС происходит ее сложная переработка. Различают следующие виды памяти: наследуемую (генетическую) и ненаследуемую (индивидуальную), образную (которая воспроизводит образ объекта), эмоциональную (когда ситуация вызывает эмоции, характерные для происходивших ранее событий), словеснологическую (свойственную только человеку). По времени сохранения информации различают: непосредственный отпечаток сенсорной информации (сенсорная память), кратковременную и долговременную память. Непосредственный отпечаток сенсорной информации обеспечивает удержание следов в сенсорной памяти не более 500 мс. Сенсорная память человека не зависит от его воли и не может сознательно контролироваться, но зависит от функционального состояния организма. Время сохранения образа внешнего мира неодинаково для различных органов чувств (длительно сохраняются зрительные образы). Непосредственный отпечаток сенсорной информации является начальным этапом переработки поступивших сигналов. Количество информации, содержащейся в нем, избыточно и высший аппарат анализа информации определяет и использует лишь наиболее существенную ее часть. Кратковременная память обеспечивает удержание ограниченной части поступившей информации, позволяет воспроизводить какую-то ее часть и тем самым некоторое время использовать определенное количество информации. Долговременная память позволяет сохранять информацию неограниченное время и имеет практически неограниченный объем, сохраняет огромное количество информации без искажения. Информация при необходимости может легко воспроизводиться. Воспроизведение заключается в извлечении информации из памяти. Воспроизведение, как и запоминание, может быть произвольным и непроизвольным. Произвольное воспроизведение, заключающееся в воспроизведении из долговременной памяти ранее приобретенной информации, имеет избирательный характер и представляет собой активный процесс, требующий включения внимания, а иногда и значительных умственных усилий. Под забыванием понимают невозможность воспроизведения приобретенной информации, которая, тем не менее, при определенных обстоятельствах может воспроизводиться. Существуют несколько теорий, рассматривающих физиологические механизмы кратковременной памяти. Согласно теории реверберации импульсов субстратом, хранящим поступающую информацию, является нейронная ловушка, образующаяся из цепи нейронов, что обеспечивает длительную циркуляцию возбуждения по таким кольцевым связям. Если импульсация будет повторно поступать к тем же нейронам, то возникает закрепление следов этих процессов в памяти. Отсутствие повторной импульсации или приход тормозного импульса к одному из нейронов цепочки приводит к прекращению реверберации, т. е. к забыванию. Электротоническая теория памяти основана на том, что кратковременная память может быть объяснена специфическими явлениями, развивающимися при прохождении нервных импульсов через синапсы и развитии в них электротонических потенциалов, которые регистрируются в течение нескольких минут и даже часов и способны облегчить прохождение импульсов через определенные синапсы. Сильное раздражение нейронов часто приводит к явлению посттетанической потенциации, которая выражается в нарастании возбудимости этого нейрона и развитии длительной импульсной активности после прекращения раздражения. Физиологические механизмы долговременной памяти не могут базироваться на циркуляции импульсов или изменениях электрофизиологических характеристик отдельных нейронов. При различных воздействиях на организм (гипоксия, наркоз, охлаждение, электрошок) разрушаются кольцевые реверберационные связи и снижается возбудимость нейронов. Но при этом огромное количество информации сохраняется в долговременной памяти в неизменном виде. Согласно анатомической теории запоминание и хранение информации осуществляется за счет образования новых терминальных волокон, изменения их размеров, развития шипикового аппарата на дендритах нейронов. Глиальная теория основывается на изменениях глиальных клеток, которые окружают нейроны и могут синтезировать особые вещества, облегчающие синаптическую передачу или повышающие возбудимость соответствующих нейронов. Согласно биохимической теории, происходит активирование ферментативных процессов при образовании медиаторов или перестройке мембраны нейронов. Активация нейрональных процессов сопровождается интенсификацией белкового обмена. Для хранения и воспроизведения информации необходимы специфические белки, торможение синтеза белка приводит к нарушению или прекращению формирования долговременной памяти. В механизмах долговременной памяти участвуют молекулы ДНК и РНК нейронов головного мозга.Мотивации
Источником активности животного и человека являются потребности. Мотивации – это побуждения к деятельности, связанные с удовлетворением определенных потребностей. Их делят на три основные группы: биологические мотивации, которые свойственны человеку и животным; социальные мотивации, свойственные человеку и частично животным; духовные – свойственные только человеку и связанные с интеллектуальными потребностями. Основной причиной возникновения биологических мотиваций является отклонение основных констант внутренней среды организма, т. е. биологические мотивации формируются на основе биологических потребностей – голода, жажды, полового чувства и др. Так, например, при снижении в крови уровня питательных веществ, возбуждаются хеморецепторы, информация от которых поступает в латеральные ядра гипоталамуса (центр голода). Эти ядра могут раздражаться и непосредственно кровью, в которой снижено содержание питательных веществ. Возбуждение от них передается в кору головного мозга – возникает чувство голода. Возбуждение постепенно захватывает все большие и большие участки коры, что обеспечивает формирование пищевого поведения.Эмоции
С помощью эмоций определяется личностное отношение человека к окружающему миру и к самому себе. Эмоциональные состояния реализуются в определенных поведенческих реакциях. Эмоции возникают на этапе оценки вероятности удовлетворения или неудовлетворения возникших потребностей, а также при удовлетворении этих потребностей. Биологическое значение эмоций состоит в выполнении ими сигнальной и регуляторной функций. Сигнальная функция эмоций заключается в том, что они сигнализируют о полезности или вредности данного воздействия, успешности или неуспешности выполняемого действия. Приспособительная роль этого механизма заключается в немедленной реакции на внезапное воздействие внешнего раздражения, поскольку эмоциональное состояние мгновенно приводит к быстрой мобилизации всех систем организма. Возникновение эмоциональных переживаний дает общую качественную характеристику воздействующему фактору, опережая его более полное, детальное восприятие. Регуляторная функция эмоций проявляется в формировании активности, направленной на усиление или прекращение действия раздражителей. Неудовлетворенные потребности обычно сопровождаются отрицательными эмоциями. Удовлетворение потребности, как правило, сопровождается приятным эмоциональным переживанием и ведет к прекращению дальнейшей поисковой деятельности. Эмоции делят также на низшие и высшие. Низшие связаны с органическими потребностями и подразделяются на два вида: гомеостатические, направленные на поддержание гомеостаза, и инстинктивные, связанные с половым инстинктом, инстинктом сохранения рода и другими поведенческими реакциями. Высшие эмоции возникают только у человека в связи с удовлетворением социальных и идеальных потребностей (интеллектуальных, моральных, эстетических и др.). Эти более сложные эмоции развивались на базе сознания и оказывают контролирующее и тормозящее влияние на низшие эмоции. В соответствии с теорией И. Пейпеца возникновение эмоций связано с лимбической системой. В гиппокампе возникает возбуждение, оттуда импульсы идут в мамиллярные (mamilllaris) тела, затем в передние ядра гипоталамуса и в поясную извилину и распространяются на другие области коры. Эмоции возникают либо сначала в коре, откуда импульсы поступают в «круг» через гиппокамп, либо через гипоталамус и тогда кору поясной извилины следует рассматривать как воспринимающую область для эмоциональных ощущений. В настоящее время принято считать, что нервным субстратом эмоций является лимбико-гипоталамический комплекс. Включение гипоталамуса в эту систему обусловлено тем, что множественные связи гипоталамуса с различными структурами головного мозга создают физиологическую и анатомическую основу для возникновения эмоций. Новая кора на основе взаимодействия с другими структурами, особенно гипоталамусом, лимбической и ретикулярной системами, играет важную роль в субъективной оценке эмоциональных состояний. Сущность биологической теории эмоций (П. К. Анохин) заключается в том, что положительные эмоции при удовлетворении какой-либо потребности возникают только в том случае, если па-раметры реально полученного результата совпадают с параметрами предполагаемого результата, запрограммированного в акцепторе результатов действия. В таком случае возникает чувство удовлетворения, положительные эмоции. Если параметры полученного результата не совпадают с запрограммированными, это сопровождается отрицательными эмоциями, что приводит к формированию новой комбинации возбуждений, необходимых для организации нового поведенческого акта, который обеспечит получение результата, параметры которого совпадают с запрограммированными в акцепторе результатов действия.Сознание
Это высшая форма отражения действительности. С помощью сознания целенаправленно регулируются формы контакта человека с окружающим миром. Сознание представляет собой субъективные переживания действительности, протекающие на фоне существующего у индивида опыта и сознаваемые им как определенная субъективная реальность. Соотнесение накопленных знаний с реальной действительностью и включение их в индивидуальный опыт – есть процесс осознания действительности. Сознание включает все формы психической деятельности человека: ощущения, восприятия, представления, мышление, внимание, чувства и волю.Соотношение сознания и подсознания
Раздражитель, воздействуя на рецепторы, приводит к появлению афферентных сигналов, которые формируют в проекционных областях коры электрические ответы, которые можно зарегистрировать и у спящего организма. Следовательно, его распространение осуществляется без участия сознания. После оценки мозгом поступившей информации ответная реакция может протекать по-разному. Если поступивший сигнал не несет какой-либо существенной информации, то подсознание тормозит ответные реакции. В таком случае сигнал вызывает лишь первичный биоэлектрический ответ и вторичную биоэлектрическую активность. Если при первичной оценке сигнала (протекающей на уровне подсознания) обнаружено, что он по своему характеру требует стандартного ответа, то возникает автоматизированная ответная реакция. Такой ответ организма не требует подключения сознания и осуществляется на уровне подсознания. Если поступившая информация является важной и для ответной реакции требуется включения всей ЦНС, то еще на уровне подсознания в коре большого мозга формируется команда, вызывающая через ретикулярную формацию общую активацию мозга. Возникает десинхронизация ЭЭГ. В этом случае сигнал осознается, и ответная реакция на него протекает уже с участием сознания. Если в реакцию вовлекается относительно небольшое количество нейронов коры и подкорки, то такие реакции протекают как подсознательные. Если в ответную реакцию вовлекается вся гигантская система нейронных ансамблей коры и подкорки, то она осуществляется с участием сознания. Подсознание оценивает любой, приходящий в мозг, сигнал не только во сне, но и при бодрствовании, являясь своеобразным первичным фильтром для всей поступающей в мозг информации. Вся ВНД человека постоянно протекает на двух уровнях – подсознания и сознания. Сознание может отключаться от окружающей обстановки, оперировать абстрактными категориями, но связь организма и среды продолжает осуществляться на уровне подсознания. На уровне подсознания протекает и условно-рефлекторная регуляция внутренних органов здорового человека.Физиология сна
Сон – физиологическое состояние, которое характеризуется потерей активных психических связей субъекта с окружающим его миром. Сон является жизненно необходимым для высших животных и человека. Длительное время считали, что сон представляет собой отдых, необходимый для восстановления энергии клеток мозга после активного бодрствования. Однако оказалось, что активность мозга во время сна часто выше, чем во время бодрствования. Было установлено, что активность нейронов ряда структур мозга во время сна существенно возрастает, т. е. сон – это активный физиологический процесс. Рефлекторные реакции во время сна снижены. Спящий человек не реагирует на многие внешние воздействия, если они не имеют чрезмерной силы. Сон характеризуется фазовыми изменениями ВНД, которые особенно отчетливо проявляются при переходе от бодрствования ко сну (уравнительная, парадоксальная, ультрапарадоксальная и наркотическая фазы). В наркотическую фазу животные перестают отвечать условно-рефлекторной реакцией на любые условные раздражители. Сон сопровождается рядом характерных изменений вегетативных показателей и биоэлектрической активности мозга. Для состояния бодрствования характерной является низкоамплитудная высокочастотная ЭЭГ активность (бета-ритм). При закрывании глаз эта активность сменяется альфа-ритмом, происходит засыпание человека. В этот период пробуждение происходит достаточно легко. Через некоторое время начинают возникать «веретена». Примерно через 30 мин стадия «веретен» сменяется стадией высокоамплитудных медленных тета-волн. Пробуждение в эту стадию затруднено, она сопровождается рядом изменений вегетативных показателей: уменьшается частота сердечных сокращений, снижается кровяное давление, температура тела и др. Стадия тета-волн сменяется стадией высокоамплитудных сверхмедленных дельта-волн. Дельтасон – это период глубокого сна. Частота сердечных сокращений, артериальное давление, температура тела в эту фазу достигают минимальных значений. Медленноволновая стадия сна длится 1 – 1,5 часа и сменяется появлением на ЭЭГ низкоамплитудной высокочастотной активности, характерной для состояния бодрствования (бета-ритм), которая получила название парадоксального, или быстроволнового, сна. Таким образом, весь период сна делится на два состояния, которые сменяют друг друга 6 -7 раз в течение ночи: медленноволновой (ортодоксальный) сон и быстроволновой (парадоксальный) сон. Если разбудить человека в фазу парадоксального сна, то он сообщает о сновидениях. Человек, проснувшись в фазу медленного сна, обычно не помнит сновидений. Если человека во время сна избирательно лишать только парадоксальной фазы сна, например, будить его, как только он переходит в эту фазу, то это приводит к существенным нарушениям психической деятельности.Теории сна.
Гуморальная теория в качестве причины сна рассматривает вещества, появляющиеся в крови при длительном бодрствовании. Доказательством этой теории служит эксперимент, при котором бодрствующей собаке переливали кровь животного, лишенного сна в течение суток. Животное-реципиент немедленно засыпало. В настоящее время удалось идентифицировать некоторые гипногенные вещества, например пептид, вызывающий дельта-сон. Но гуморальные факторы не могут рассматриваться как абсолютная причина возникновения сна. Об этом свидетельствуют наблюдения за поведением двух пар неразделившихся близнецов. У них разделение нервной системы произошло полностью, а системы кровообращения имели множество анастомозов. Эти близнецы могли спать в разное время: одна девочка, например, могла спать, а другая бодрствовала.Подкорковая и корковая теории сна.
При различных опухолевых или инфекционных поражениях подкорковых, особенно стволовых, образований мозга, у больных отмечаются различные нарушения сна – от бессонницы до длительного летаргического сна, что указывает на наличие подкорковых центров сна. При раздражении задних структур субталамуса и гипоталамуса животные засыпали, а после прекращения раздражения они просыпались, что указывает на наличие в этих структурах центров сна. В лаборатории И. П. Павлова было установлено, что при длительной выработке тонкого дифференцировочного торможения животные часто засыпали. Поэтому ученый рассматривал сон как следствие процессов внутреннего торможения, как углубленное, разлитое, распространившееся на оба полушария и ближайшую подкорку торможение (корковая теория сна). Однако ряд фактов не могли объяснить ни корковая, ни подкорковая теории сна. Наблюдения за больными, у которых отсутствовали почти все виды чувствительности, показали, что такие больные впадают в состояние сна как только прерывается поток информации от действующих органов чувств. Например, у одного больного из всех органов чувств был сохранен только один глаз, закрытие которого погружало больного в состояние сна. Многие вопросы организации процессов сна получили объяснение с открытием восходящих активирующих влияний ретикулярной формации ствола мозга на кору больших полушарий. Экспериментально было доказано, что сон возникает во всех случаях устранения восходящих активирующих влияний ретикулярной формации на кору мозга. Были установлены нисходящие влияния коры мозга на подкорковые образования. В бодрствующем состоянии при наличии восходящих активирующих влияний ретикулярной формации на кору мозга нейроны лобной коры тормозят активность нейронов центра сна заднего гипоталамуса. В состоянии сна, когда снижаются восходящие активирующие влияния ретикулярной формации на кору мозга, тормозные влияния лобной коры на гипоталамические центры сна снижаются. Между лимбико-гипоталамическими и ретикулярными структурами мозга имеются реципрокные отношения. При возбуждении лимбико-гипоталамических структур мозга наблюдается торможение структур ретикулярной формации ствола мозга и наоборот. При бодрствовании за счет потоков афферентации от органов чувств активируются структуры ретикулярной формации, которые оказывают восходящее активирующее влияние на кору больших полушарий. При этом нейроны лобных отделов коры оказывают нисходящие тормозные влияния на центры сна заднего гипоталамуса, что устраняет блокирующие влияния гипоталамических центров сна на ретикулярную формацию среднего мозга. При уменьшении потока сенсорной информации снижаются восходящие активирующие влияния ретикулярной формации на кору мозга. В результате чего устраняются тормозные влияния лобной коры на нейроны центра сна заднего гипоталамуса, которые начинают еще активнее тормозить ретикулярную формацию ствола мозга. В условиях блокады всех восходящих активирующих влияний подкорковых образований на кору мозга наблюдается медленноволновая стадия сна. Гипоталамические центры за счет связей с лимбическими структурами мозга могут оказывать восходящие активирующие влияния на кору мозга при отсутствии влияний ретикулярной формации ствола мозга. Эти механизмы составляют корково-подкорковую теорию сна (П. К. Анохин), которая позволила объяснить все виды сна и его расстройства. Она исходит из того, что состояние сна связано с важнейшим механизмом – снижением восходящих активирующих влияний ретикулярной формации на кору мозга. Сон бескорковых животных и новорожденных детей обьясняется слабой выраженностью нисходящих влияний лобной коры на гипоталамические центры сна, которые при этих условиях находятся в активном состоянии и оказывают тормозное действие на нейроны ретикулярной формации ствола мозга. Сон новорожденного периодически прерывается только возбуждением центра голода, расположенного в латеральных ядрах гипоталамуса, который тормозит активность центра сна. При этом создаются условия для поступления восходящих активирующих влияний ретикулярной формации в кору. Эта теория объясняет многие расстройства сна. Бессонница, например, часто возникает как следствие перевозбуждения коры под влиянием курения, напряженной творческой работы перед сном. При этом усиливаются нисходящие тормозные влияния нейронов лобной коры на гипоталамические центры сна и подавляется механизм их блокирующего действия на ретикулярную формацию ствола мозга. Длительный сон может наблюдаться при раздражении центров заднего гипоталамуса сосудистым или опухолевым патологическим процессом. Возбужденные клетки центра сна непрерывно оказывают блокирующее влияние на нейроны ретикулярной формации ствола мозга. Иногда во время сна наблюдается так называемое частичное бодрствование, которое объясняется наличием определенных каналов реверберации возбуждений между подкорковыми структурами и корой больших полушарий во время сна на фоне снижения восходящих активирующих влияний ретикулярной формации на кору мозга. Например, кормящая мать может крепко спать и не реагировать на сильные звуки, но она быстро просыпается даже при небольшом шевелении ребенка. В случае патологических изменений в том или ином органе усиленная импульсация от него может определять характер сновидений и быть своего рода предвестником заболевания, субъективные признаки которого еще не воспринимаются в состоянии бодрствования. Фармакологический сон неадекватен по своим механизмам естественному сну. Снотворные препараты ограничивают активность разных структур мозга – ретикулярной формации, гипоталамической области, коры головного мозга. Это приводит к нарушению естественных механизмов формирования стадий сна, нарушению процесса консолидации памяти, переработки и усвоения информации.Функциональная система поведения
Степень сложности и характер компонентов поведенческих актов могут быть различными, но их принципиальная организация одинакова. Современная физиология рассматривает все поведенческие акты с позиций теории функциональных систем П. К. Анохина (рис. 35).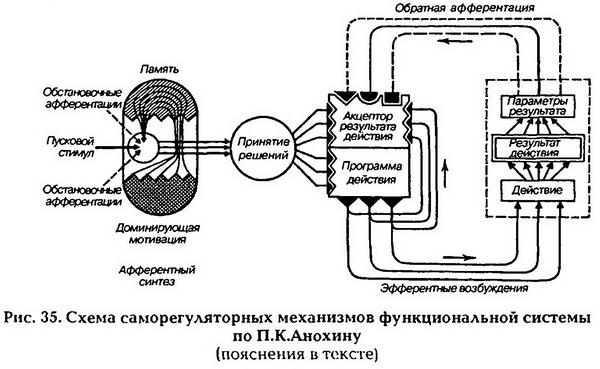 Согласно этой теории при осуществлении условного рефлекса раздражитель действует на фоне предпусковой интеграции, которая формируется на базе различных видов афферентных возбуждений. Обстановочная афферентация – сумма афферентных возбуждений, возникающих в конкретных условиях и сигнализирующих об обстановке, в которой находится организм. Обстановочная афферентация действует на организм, в котором имеется тот или иной уровень мотивационного возбуждения (мотивация). Доминирующая мотивация формируется на основе ведущей потребности, при участии мотивационных центров гипоталамуса. На стадии афферентного синтеза доминирующая мотивация активирует память. Значение памяти на стадии афферентного синтеза состоит в том, что она извлекает информацию, связанную с удовлетворением доминирующей мотивации. Эти три вида возбуждений: мотивационное, память и обстановочная афферентация создают предпусковую интеграцию, на фоне которой действует четвертый вид афферентации – пусковая афферентация (пусковой стимул, условный сигнал). Эти четыре вида возбуждений взаимодействуют и обеспечивают формирование первого этапа функциональной системы поведения – афферентного синтеза. Основным условием формирования афферентного синтеза является встреча всех четырех видов афферентаций, которые обрабатываются одновременно благодаря конвергенции всех видов возбуждений. Этап афферентного синтеза обеспечивает постановку цели, достижению которой будет посвящена вся реализация функциональной системы.
Принятие решения (постановка цели) является вторым этапом и осуществляется только на основе полного афферентного синтеза. Благодаря принятию решения принимается форма поведения, соответствующая внутренней потребности, прежнему опыту и окружающей обстановке, которая позволяет осуществлять именно то действие, которое должно привести к запрограммированному результату.
Третьим этапом является формирование программы действия. На этом этапе обеспечиваются пути реализации конкретной цели, формируются эфферентные команды к различным исполнительным органам. Одновременно в нейронных структурах создается специальный аппарат – акцептор результата действия, который прогнозирует все параметры будущего результата.
Формирование акцептора результатов действия является четвертым этапом создания функциональной системы. Он должен обеспечить механизмы, позволяющие не только прогнозировать параметры необходимого результата, но и сравнить их с параметрами реально полученного результата. Информация о них приходит к акцептору благодаря обратной афферентации, которая позволяет исправить ошибку или довести несовершенные поведенческие акты до совершенных. Акцептор результатов действия – это идеальный образ (эталон) будущих результатов действия. В этот нервный комплекс приходят возбуждения не только афферентной, но и эфферентной природы. Коллатеральные ответвления пирамидного тракта через цепь промежуточных нейронов отводят часть эфферентных команд, идущих к эффекторам. Эти возбуждения конвергируют на те же промежуточные нейроны сенсомоторной области коры, куда поступают афферентные возбуждения, передающие информацию о параметрах реального результата. Если результаты не соответствуют прогнозу, то возникает реакция рассогласования, активирующая ориентировочно-исследовательскую реакцию, которая увеличивает ассоциативные возможности мозга, обеспечивая активный поиск дополнительной информации. На ее основе формируется новый более полный афферентный синтез, принимается более адекватное решение, что, в свою очередь, приводит к формированию более совершенной программы действия, которая позволяет получить необходимый результат. Нейроны, участвующие в формировании функциональной системы, расположены во всех структурах ЦНС, на всех ее уровнях. При достижении желаемого полезного результата в акцепторе результатов действия формируется реакция согласования, поступает афферентация, сигнализирующая об удовлетворении мотивации. На этом функциональная система перестает существовать.
Процессы согласования или рассогласования, возникающие при сличении параметров реально полученного результата с за-программированным в акцепторе результатов действия, сопровождаются либо чувством удовлетворения, либо неудовлетворения, т. е. положительными и отрицательными эмоциями.
Согласно этой теории при осуществлении условного рефлекса раздражитель действует на фоне предпусковой интеграции, которая формируется на базе различных видов афферентных возбуждений. Обстановочная афферентация – сумма афферентных возбуждений, возникающих в конкретных условиях и сигнализирующих об обстановке, в которой находится организм. Обстановочная афферентация действует на организм, в котором имеется тот или иной уровень мотивационного возбуждения (мотивация). Доминирующая мотивация формируется на основе ведущей потребности, при участии мотивационных центров гипоталамуса. На стадии афферентного синтеза доминирующая мотивация активирует память. Значение памяти на стадии афферентного синтеза состоит в том, что она извлекает информацию, связанную с удовлетворением доминирующей мотивации. Эти три вида возбуждений: мотивационное, память и обстановочная афферентация создают предпусковую интеграцию, на фоне которой действует четвертый вид афферентации – пусковая афферентация (пусковой стимул, условный сигнал). Эти четыре вида возбуждений взаимодействуют и обеспечивают формирование первого этапа функциональной системы поведения – афферентного синтеза. Основным условием формирования афферентного синтеза является встреча всех четырех видов афферентаций, которые обрабатываются одновременно благодаря конвергенции всех видов возбуждений. Этап афферентного синтеза обеспечивает постановку цели, достижению которой будет посвящена вся реализация функциональной системы.
Принятие решения (постановка цели) является вторым этапом и осуществляется только на основе полного афферентного синтеза. Благодаря принятию решения принимается форма поведения, соответствующая внутренней потребности, прежнему опыту и окружающей обстановке, которая позволяет осуществлять именно то действие, которое должно привести к запрограммированному результату.
Третьим этапом является формирование программы действия. На этом этапе обеспечиваются пути реализации конкретной цели, формируются эфферентные команды к различным исполнительным органам. Одновременно в нейронных структурах создается специальный аппарат – акцептор результата действия, который прогнозирует все параметры будущего результата.
Формирование акцептора результатов действия является четвертым этапом создания функциональной системы. Он должен обеспечить механизмы, позволяющие не только прогнозировать параметры необходимого результата, но и сравнить их с параметрами реально полученного результата. Информация о них приходит к акцептору благодаря обратной афферентации, которая позволяет исправить ошибку или довести несовершенные поведенческие акты до совершенных. Акцептор результатов действия – это идеальный образ (эталон) будущих результатов действия. В этот нервный комплекс приходят возбуждения не только афферентной, но и эфферентной природы. Коллатеральные ответвления пирамидного тракта через цепь промежуточных нейронов отводят часть эфферентных команд, идущих к эффекторам. Эти возбуждения конвергируют на те же промежуточные нейроны сенсомоторной области коры, куда поступают афферентные возбуждения, передающие информацию о параметрах реального результата. Если результаты не соответствуют прогнозу, то возникает реакция рассогласования, активирующая ориентировочно-исследовательскую реакцию, которая увеличивает ассоциативные возможности мозга, обеспечивая активный поиск дополнительной информации. На ее основе формируется новый более полный афферентный синтез, принимается более адекватное решение, что, в свою очередь, приводит к формированию более совершенной программы действия, которая позволяет получить необходимый результат. Нейроны, участвующие в формировании функциональной системы, расположены во всех структурах ЦНС, на всех ее уровнях. При достижении желаемого полезного результата в акцепторе результатов действия формируется реакция согласования, поступает афферентация, сигнализирующая об удовлетворении мотивации. На этом функциональная система перестает существовать.
Процессы согласования или рассогласования, возникающие при сличении параметров реально полученного результата с за-программированным в акцепторе результатов действия, сопровождаются либо чувством удовлетворения, либо неудовлетворения, т. е. положительными и отрицательными эмоциями.
Фармакологические средства, влияющие на психическую деятельность
Воздействуя на медиаторные системы различных отделов мозга психотропными препаратами, можно вызвать не только усиление или угнетение возбудительного и тормозного процессов, но и изменения со стороны психики, умственной работоспособности и эмоционального поведения больного.В группу психотропных препаратов входят: 1. нейролептики (антипсихотические средства); 2. транквилизаторы, 3. седативные средства; 4. антидепрессанты; 5. препараты лития; 6. ноотропные средства; 7. психостимуляторы.
Нейролептики оказывают успокаивающее действие с уменьшением реакции на внешние стимулы, ослаблением психомоторного возбуждения и напряженности. Они подавляют чувство страха, бред, галлюцинации. Механизм действия нейролептиков основан на их угнетающем действии на ретикулярную формацию и ее активирующем влиянии на кору больших полушарий, а также на взаимодействии нейролептиков с медиаторными системами мозга: адрен-, серотонин-, холин-, ГАМКи особенно с дофаминергическими. Антипсихотическая активность нейролептиков (аминазина, левомепромазина) обусловлена их угнетающим влиянием на но-радренергические рецепторы, на дофаминовые рецепторы черной субстанции, полосатого тела, лимбической системы мозга (фторфеназин, галоперидол и др.). Транквилизаторы (от лат. tranquillo-are – делать спокойным, безразличным) применяются в основном при неврозах для устранения эмоциональной напряженности, тревоги и страха. Кроме антифобического они обладают гипнотическим, миорелаксантным и противосудорожным действием. Транквилизаторы уменьшают возбудимость подкорковых структур мозга (лимбической системы, таламуса, гипоталамуса) и тормозят взаимодействие между этими структурами и корой больших полушарий. Кроме того, эти препараты тормозят полисинаптические спинальные рефлексы и вызывают миорелаксацию. В лечебной практике нашли применение такие препараты этой группы, как элениум (хлозепид), диазепам (реланиум), феназепам, амизил, мебикар и др. Седативные средства оказывают менее выраженный успокаивающий и антифобический эффект, чем транквилизаторы, не вызывают миорелаксации. Они оказывают регулирующее влияние на процессы возбуждения и торможения в мозге и применяются в амбулаторной практике для лечения легких невротических состояний. К ним относятся прежде всего препараты растительного происхождения (из корня валерианы, пустырника). Антидепрессанты – это препараты, оказывающие положительное влияние на настроение и общее психическое состояние больного. При депрессивных состояниях наблюдается снижение активности норадренергической и серотонинергической синаптической передачи. Поэтому действие антидепрессантов основано на их ингибировании моноаминоксидазы (МАО) – фермента, вызывающего инактивацию моноаминов (норадреналина, дофамина, серотонина). Подавление активности МАО приводит к накоплению моноаминов и улучшению синаптической передачи в структурах мозга. К таким препаратам относятся: ниаламид, пиразидол, бефол и др. Кроме того, существуют антидепрессанты – ингибиторы обратного нейронального захвата избирательно или норадреналина, или серотонина, или дофамина (азафен). Препараты лития (лития карбонат, лития оксибутират) получили широкое применение для лечения эндогенных аффективных заболеваний, для купирования острого маниакального возбуждения у психических больных. В больших дозах литий понижает содержание в мозге серотонина и повышает чувствительность нейронов гиппокампа и других областей мозга к действию дофамина, влияя на нейрохимические процессы в нервной ткани. Ноотропные средства (пирацетам, аминалон, натрия оксибутират, фенибут и др.) – это группа препаратов, оказывающих специфическое активирующее влияние на интегративную деятельность мозга, улучшает память, обучение и познавательную деятельность, облегчает передачу информации между полушариями головного мозга, повышает устойчивость мозга к гипоксии. В связи с тем, что основной представитель препаратов этой группы – пирацетам является синтетическим аналогом тормозного медиатора ГАМК, надо полагать, что пирацетам способен усиливать тормозные процессы в мозге. Кроме того, этот препарат усиливает синтез дофамина и повышает уровень норадреналина, некоторые ноотропы увеличивают содержание ацетилхолина и серотонина в нервной ткани. Особенностью ноотропов является их стимулирующее влияние на метаболические и биоэнергетические процессы в нервных клетках. Ноотропы используются для стабилизации нарушенных функций мозга при психических заболеваниях, у пожилых людей и детей для лечения сосудистых и метаболических нарушений мозга. В группу психостимуляторов центральной нервной системы помимо аналептиков и препаратов, действующих на спинной мозг, входят психомоторные стимуляторы (кофеин, фенамин и др.), активирующие биоэлектрическую активность мозга, повышающие физическую и умственную работоспособность, уменьшающие усталость и сонливость. Механизм действия этих препаратов связывают с их способностью стимулировать синтез циклического АМФ, который участвует во всех метаболических процессах.


Последние комментарии
3 часов 52 минут назад
3 часов 55 минут назад
2 дней 10 часов назад
2 дней 14 часов назад
2 дней 16 часов назад
2 дней 17 часов назад