Наркотики [Нина Владимировна Веселовская] (fb2) читать онлайн
- Наркотики 1.31 Мб, 176с. скачать: (fb2) - (исправленную) читать: (полностью) - (постранично) - Нина Владимировна Веселовская - Алексей Евгеньевич Коваленко
[Настройки текста] [Cбросить фильтры]
[Оглавление]
Глава 1. Опиаты
Термин опиаты объединяет вещества, извлекаемые из опия, среди которых наиболее важны морфин, кодеин, папаверин, широко применяемые в качестве лекарственных средств, и тебаин, используемый в основном в медицинской промышленности для получения лекарств, а также синтезированные производные морфина, которые относят к полусинтетическим опиатам и среди которых наиболее известен за свои наркотические свойства героин. Вещества, отличающиеся по структуре от структуры морфина, но действующие по сходному механизму (через опиоидные рецепторы) относят к опиоидам.Уже с древних времен (шумерами и египтянами, а позднее в Греции и Риме) опий использовали в качестве обезболивающего, а также средства, способного вызывать эйфорию и расслабление при оральном приеме и особенно при курении, распространившемся в IX веке в Китае и Индии. К началу XIX века в США и Европе опий в виде различных лекарственных препаратов повсеместно продавался легально, а выделенный из опия в 1803 г. морфин становится основным обезболивающим средством при тяжелых ранениях в случае войн, катастроф и при несчастных случаях. В 1874 г. был синтезирован героин, который некоторое время также использовали в качестве мощного лекарственного средства. Параллельно шло немедицинское «освоение» опия, морфина и героина и переход от орального приема и курения к инъекциям. Уже к концу XIX и началу XX века тяжелейшие последствия употребления опиатов как медицинские, так и социальные стали очевидны. Законодательное преследование нелегального изготовления и распространения опиатов началось в США в 1914 г. так называемым Актом Гаррисона введением контроля и закончилось полным запретом на использование героина уже в 1924 г. С тех пор борьба с нелегальным изготовлением и распространением героина ведется во всех цивилизованных странах. Международный контроль и систему борьбы с наркотиками в самом широком смысле возглавляет Всемирная организация здравоохранения под эгидой ООН.
В настоящее время в РФ опий и героин, как один из наиболее мощных («тяжелых») наркотиков, вызывающих сильную зависимость уже после нескольких инъекций, запрещен к производству, распространению и употреблению и внесен в Список №1 Постоянного Комитета по наркотикам. Другие опиаты (морфин, кодеин и др.) относят к разрешенным лекарственным средствам, используемым под определенным контролем при соответствующих медицинских показаниях.
Опий
Источником опия является опийный мак Papaver somniferum, который в районе Средиземноморья выращивался еще в 300 г. до н.э. В настоящее время основными производителями мака являются Индия (основной легальный производитель), Австралия, Китай, Корея, Япония страны Среднего Востока (Афганистан, Пакистан, Иран), Юго–Восточная Азия (Лаос, Бирма, Таиланд), Мексика. Новые производители: страны Балканского региона и среднеазиатские страны СНГ. Из всего объема выращиваемого опия только четверть используется для медицинских целей.Опий – натуральный продукт, получающийся при надрезании незрелых головок мака. Млечный сок, вытекающий из надрезов, собирается вручную и высушивается на воздухе, образуя опийную смолу, или опий–сырец.
Опий – сложная смесь сахаров, белков, липидов, смол, восков, пигментов, воды и т.д. В его состав входят более 50 активных алкалоидов, составляющих 10–20% общей массы. Их относительные количества зависят от условий произрастания, климата, сорта и возраста растений и т.п.
Состав индийского опия.
| Компоненты | Содержание в опии,% |
|---|---|
| Морфин | 9,7 |
| Другие алкалоиды | 13,3 |
| Жиры | 21 |
| Белки и углеводы | 15 |
| Меконовая кислота | 11 |
| Молочная и серосодержащие кислоты | 8 |
| Вода | 14 |
| Неустановленные примеси | 8 |
Основные алкалоиды опия.
| Алкалоиды | Содержание в опии,% |
|---|---|
| Морфин | 4–21 (42) |
| Кодеин | 0,7–3(12) |
| Носкапин (наркотин) | 2–8 (21) |
| Тебаин | 0,2–1 (6,5) |
| Папаверин | 0,5–1,3(18) |
Кроме основных, в опии содержатся «минорные» алкалоиды, называемые так из–за их незначительного содержания. Среди них наиболее известные: нарцеин (0,2%), неопин, протопин, порфироксин, криптопин, псевдоморфин, лауданозин.
Характеристическими компонентами опия являются меконовая кислота, содержание которой может доходить до 15%, и лактон меконин, не обладающий психоактивными свойствами, который может также образоваться вместе с гидрокотарнином при восстановлении наркотина.
Виды опия. ■ Опий сырец в свежем виде – липкая, смолоподобная пластичная масса, темно–коричневого цвета, с характерным лакричным запахом. По мере старения пластичность исчезает, масса становится твердой и хрупкой. ■ Обработанный (экстракционный) опий – продукт, получаемый из опия–сырца путем различной обработки, обычно водной экстракцией с последующим фильтрованием и выпариванием воды. ■ Медицинский опий – тонкий порошок светло–коричневого цвета с содержанием морфина 9,5–10,6%. Включает добавки «разбавителей»: лактозу, крахмал и другие компоненты. Имеет характерный запах опия. ■ Пантопон (омнопон) – светло–коричневый порошок легко растворимый в воде, содержит 48–50% морфина. ■ Опиумные шлаки – продукт, остающийся в трубке после курения опия, еще содержит значительные количества морфина. Смешивается с сырцом или обработанным опием для дальнейшего использования. Выделение основных алкалоидов из опия осуществляют пря экстракции водой при температуре 50–55ºС, при этом в водный экстракт практически полностью переходят морфин, кодеин и тебаин, большая часть папаверина и около трети всего количества наркотина. Помимо алкалоидов, водой извлекается меконовая кислота, присутствие которой может служить признаком использования опийного экстракта. Дальнейшая обработка экстракта позволяет в конечном итоге разделить основные алкалоиды и выделить их в чистом виде.
 Рис. 1. Основные опиаты: 1. Морфин. 2. Кодеин. 3. Тебаин. 4. Орипавин. 5. Диацетилморфин. 6. 6–Моноацетилморфин.
Рис. 1. Основные опиаты: 1. Морфин. 2. Кодеин. 3. Тебаин. 4. Орипавин. 5. Диацетилморфин. 6. 6–Моноацетилморфин.
Трава мака также используется для получения алкалоидов и концентрированных экстрактов. Содержание алкалоидов в сухих маковых головках, корнях и стеблях (соломе) мака колеблется в широких пределах в зависимости от сорта. Так, в масличном (голубом) маке содержится до 0,5% морфина. В коробочках и корнях мака Papaver bracteatum найдено до 3,75% тебаина. Кроме алкалоидов, в траве мака определены тритерпеновый спирт, циклолауденол, меконин, β–цитостерин, органические кислоты: хелидоновая, оксицинхониновая, кофейная, ванилиновая, кумаровая, меконовая и др. компоненты.
Морфин (morph, white, stuff, miss, emma, monkey)
Морфин извлекается из опия и поступает на нелегальный рынок в виде препарата различной степени чистоты и содержания активного компонента. Качество изменяется от очень высокого до очень низкого в зависимости от применяемой технологии и квалификации лаборатории. Известны различные виды: морфин–сырец, очищенный морфин и морфин медицинский, различающиеся как по содержанию активного компонента, так и по наличию примесей и добавок. В частности, морфин–сырец, извлекаемый из опия и часто используемый для получения героина в подпольных лабораториях, в зависимости от методики экстракции и очистки может получаться очень чистым или, напротив, содержать в качестве примесей другие алкалоиды опия: кодеин, дающий в процессе приготовления героина примесь ацетил кодеина, наркотин, а также неалкалоидные компоненты, в частности, меконовую кислоту. Рис. 2. Алкалоиды и другие компоненты опия: 1. Папаверин. 2. Наркотин (носкапин). 3. Меконовая кислота. 4. Меконин
Рис. 2. Алкалоиды и другие компоненты опия: 1. Папаверин. 2. Наркотин (носкапин). 3. Меконовая кислота. 4. Меконин
Героин (smack, junk, horse, stuff)
■ Героин наиболее опасный наркотик. Производится в подпольных лабораториях из морфина (или любого морфин–содержащего сырья: морфина–сырца, экстракционного опия, экстракта маковой соломы) по реакции ацетилирования с образованием активного действующего компонента – диацетилморфина (ДАМ). ■ Чистый героин – белый порошок с горьким вкусом. Нелегальный героин может отличаться по цвету и агрегатному состоянию. Цвет порошка от белого до темно–коричневого определяется количеством примесей, полученных в процессе производства, или в большинстве случаев присутствием пищевых красителей, какао или карамелизованного сахара. Агрегатное состояние зависит от происхождения (вида) героина: тонкий порошок, гранулы, порошок с небольшими сыпучими агрегатами. Состав зависит от качества сырья для ацетилирования, содержания морфина, соблюдения условий реакции, условий хранения и транспортировки, фальсифицирующими добавками. Героин может содержать до 30–40 компонентов. Это: ■ Вещества из сырья (экстракты маковой соломы и опия, морфин различной степени очистки) – алкалоиды, не подвергающиеся ацетилированию и ацетилированные алкалоиды, среди которых основной – ацетилкодеин. Из компонентов, не являющихся алкалоидами, в «героине–сырце», или «грязном героине» (crud heroin) часто присутствует компонент опия меконин, который также может образоваться при восстановительном разложении наркотина. ■ Продукты неполного ацетилирования – 3–моноацетилморфин, 6–моноацетилморфин. ■ Продукты гидролиза (при плохих условиях хранения и транспортировки) – 6–моноацетилморфин. ■ Добавки – амфетамин, метадон, эфедрин, кокаин, кофеин, хинин, стрихнин, сахара и т.п.Общий состав героина
| Диацетилморфин | От 20 до 80–90% |
| Ацетилкодеин | 2–5% |
| 6–моноацетилморфин | 1–15% |
| Носкапин | 0–10% |
| Папаверин | 0–4% |
| Морфин | 0,04–0,35% |
| Кодеин | 0,01–0,08% |
Героин Юго–западной Азии
Тип 1
Очень тонкий порошок от бежевого до темно–коричневого цвета с небольшими включениями мягких агрегатов, рассыпающихся при легком нажатии. Внешний вид и химический сослав героика этого типа весьма разнообразны. В типичном случае это тонкий светло–коричневый порошок с характерным запахом опия. Все алкалоиды присутствуют в форме оснований.Состав (%):
| Диацетилморфин | 60 |
| Ацетилкодеин | 5 |
| 6–Моноацетилморфин | 3 |
| Наркотин | 10 |
| Папаверин | 4. |
Тип 2
Тонкий сухой порошок от белого до кремового цвета с менее сильным, чем для типа 1, запахом. Это высокочистый продукт, неотличимый в ряде случаев от фармацевтического героина. Все алкалоиды присутствуют в форме гидрохлоридов.Состав (%):
| Диацетилморфин | 80–90 |
| Ацетилкодеин | 3 |
| 6–моноацетилморфин | 2 |
| Наркотин | не обнаружен |
| Папаверин | не обнаружен. |
Средне–восточный героин
Тип 1
Тонкий порошок практически без агрегатов от бежевого до очень светлого коричневого цвета. Часто содержит добавки, например, прокаин. Все алкалоиды присутствуют в форме гидрохлоридов.Состав (%):
| Диацетилморфин | Более 70 (редко около 50) |
| Ацетил кодеин | 3 |
| 6–Моноацетилморфин | 2 |
| Наркотин | не обнаружен |
| Папаверин | не обнаружен. |
Тип 2
Тонкий порошок различных оттенков белого цвета. Высокочистый героин. Все алкалоиды присутствуют в форме гидрохлоридов.| Диацетилморфин | 70–80 |
| Ацетилкодеин | 2–3 |
| 6–Моноацетилморфин | 2 |
| Наркотин | следы |
| Папаверин | Следы |
Героин Юго–Восточной Азии
Тип 1. Героин для курения «Chinese N.3»
В основном состоит из твердых, не рассыпающихся при нажатии гранул диаметром 1–5 мм, и небольшого количества порошка. Цвет гранул обычно серый, но встречается также героин с темно–коричневыми и, реже, с розовыми или красными (Penang Pink) гранулами. Алкалоиды присутствуют в форме оснований или гидрохлоридов, причем, если обе формы присутствуют вместе, то это может быть следствием нестехиометрического добавления соляной кислоты.Состав (%):
| Диацетилморфин | 20 |
| Кофеин | 40 (В Penang Pink вместо кофеина добавлен барбитал) |
| Ацетилкодеин | следы |
| 6–моноацетилморфин | до 5 (в результате гидролиза) |
| Наркотин | следы |
| Папаверин | следы. |
Тип 2. Героин для инъекций «Chinese N.4»
Тонкий белый порошок без агрегатов со слабым запахом. Фактически целиком состоит из диацетилморфина. Содержание 6–МАМ обычно ниже 3%, а ацетилкодеина – выше, чем в высокочистом героине Юго–Западной Азии. Алкалоиды присутствуют в форме гидрохлоридов.Повышенное содержание 6–МАМ в различных образцах героина, связанное с гидролизом ДАМ в условиях производства, может быть следствием добавления избытка соляной кислоты. Высокое содержание морфина в героине объясняется неполным ацетилированием, а не результатом гидролиза моноацетилморфина.
Черная героиновая смола mexican brown, black tar, mud
Героин, который производится непосредственно из опиумного мака, на сленге называемый «черная смола», «грязь», «Мексиканский коричневый», обычно представляет собой вязкую, пластичную, похожую на вар или деготь массу темно–коричневого или черного цвета. Также встречаются образцы твердые, похожие на уголь. Наиболее часто используется для инъекций.Спидболл
Спидболл – это смесь кокаин–основания (крэка) и героина, предназначенная для курения. (Более подробное описание см. в разделе, посвященном кокаину).Профили примесей опия, морфина–сырца и героина
Хроматограммы, отражающие состав основных и примесных компонентов в продуктах, так называемые примесные профили, позволяют по некоторым характеристическим компонентам получить представление о способах производства продукта и даже о месте его изготовления. Примесные профили опия и морфина–сырца схожи, поскольку последний получают из опия в процессах растворения, экстракции и осаждения. Основными компонентами обоих продуктов являются: морфин, наркотин, папаверин, кодеин и тебаин. В морфине–сырце уровни папаверина и наркотина гораздо ниже, так как они в значительной мере отделяются в процессе экстракции алкалоидов из опия, по той же причине в морфине–сырце содержится гораздо меньшее количество примесей. Примеси опия представляют собой в основном неалкалоидные компоненты, среди которых много длинноцепочечных кислот. Это пальмитиновая, стеариновая, олеиновая, линолевая, бегеновая, лигноцериновая кислоты. Другие компоненты опия: папавералдин, меконин, тебаол и др. Характеристические компоненты морфина–сырца: насыщенные кислоты, тебаол, меконин. Ацетилирование морфина–сырца уксусным ангидридом с целью получения героина сильно изменяет примесный профиль. Из основных компонентов, помимо диацетилморфина, в заметных количествах остаются неацетилированные алкалоиды: папаверин, наркотин и следы тебаина, а также появляются новые ацетилированные алкалоиды: ацетилкодеин (второй по интенсивности после диацетилморфина) и 6–моноацетилморфин в вариабельных количествах. Примесный профиль ацетилированного морфина–сырца содержит более 100 пиков на хроматограмме. Среди них идентифицированы: ацетилтебаол, 4–ацетокси–3,6–диметокси–5–[2–(N–метилацетамидо)]–этилфенантрен, N–ацетилнорлауданозин, N–ацетилнорнаркотин, N–ацетилангидронарцеин. Также обнаружены продукты разложения термически неустойчивого тебаина.Способы употребления опиатов
■ оральный (прием внутрь) ■ интраназальный (вдыхание и втягивание через нос) ■ курение ■ инъекции (внутривенные, подкожные, внутримышечные).Опий обычно курят. Чаще всего героин используют в виде раствора для подкожных и внутривенных инъекций, а порошковую форму курят и вдыхают или втягивают носом. По данным, на долю внутривенного введения приходится около 80% общего числа случаев употребления героина, а доля интраназального употребления составляет около 15%.
Физиологическое действие опиатов на системы организма
| ЦНС | Аналгезия |
| Эйфория | |
| Подавление кашлевого центра | |
| Подавление нервного возбуждения | |
| Дыхание | Угнетение дыхания |
| Замедление ритма дыхания | |
| ЖКТ | Уменьшение перистальтики |
| Уменьшение секреции желчи | |
| Уменьшение панкреатической и кишечной секреции | |
| Колики | |
| Запоры | |
| Мышцы | Расслабление |
| Уменьшение физической активности |
Последствия регулярного приема опиатов
Опасность длительного употребления опиатов в быстром развитии пристрастия, психической и физической зависимости.Психическая зависимость – развивается в течение 3–4 мес для опия, 2 мес для морфина и гораздо быстрее для героина.
Физическая зависимость очень сильная, развивается за 10–20 дней приема опия и за 2 дня ежедневного использования героина.
Толерантность развивается также быстро: от 500 мг морфина ежедневно в начале первого месяца до более 1000 мг в день к концу четвертого (контролированный прием морфина хроническим наркоманом в течение четырех месяцев). Дозы героина, принимаемые ежедневно наркоманом с резко выраженной толерантностью, могут составлять до 2 г в день.
Разовые дозы (мг): ■ Морфин 10–30 (при толерантности 250 мг в день и выше) ■ Кодеин 10–50 ■ Героин 5–10 мг вызывают состояние опьянения, обычная доза 10–40 мг, «уличная» доза до 100 мг (для наркоманов с сильной толерантностью до 2 г/день).
Летальные дозы (мг):
| Морфин | 200 |
| Кодеин | 800 |
| Героин | 60–200 |
Симптомы и диагностика
Диагностика опийного опьянения наиболее простая. Эйфория, настроение приподнятое, благодушное, состояние расслабленности, покоя, удовлетворения, безмятежности. Агрессия и грубость не проявляются. Начальное расслабленное состояние сменяется затем оживлением с выразительной мимикой и жестикуляцией без нарушения координации и речи. Наиболее характерным диагностическим признаком потребления опиатов является резкое сужение зрачков в момент приема («булавочная головка») и бледность кожных покровов. Также обычно проявляются затрудненность дыхания и снижение температуры тела.Симптомы морфинизма ■ сужены зрачки ■ резкое истощение ■ желтушность кожи ■ рубцы и пигментные пятна на локтевых сгибах и бедрах после частых инъекций.
Симптомы острого отравления при передозировке ■ цианоз. ■ суженные в точку зрачки. ■ гипотония. ■ спазм желудочно–кишечного и желчного путей. ■ снижение температуры тела, влажная и липкая кожа ■ угнетение дыхания. ■ нитевидный пульс. ■ потеря сознания. ■ кома. ■ смерть от паралича дыхания через 2–4 ч при подкожном или пероральном введении сверхдозы и мгновенно – при внутривенном.
Отравление кодеином может сопровождаться конвульсиями. Смертные случаи от передозировки героина часто сопровождаются сопутствующим приемом алкоголя или депрессантов.
Через 6–18 (5–12) ч после последнего приема отмечаются начальные симптомы абстинентного синдрома: психическая зависимость («наркотический голод»), плохое настроение, эмоциональное напряжение, раздражение. Помимо этих признаков, появляются признаки, за которые ответственна вегетативная нервная система: расширение зрачков, слезящиеся глаза, чиханье, насморк, слюнотечение, озноб, потливость, «гусиная кожа»; зевота.
Второй этап (1–2 сут) характеризуется появлением дополнительных признаков: напряжение мышц спины, рук и ног. Ранее описанные симптомы усиливаются и на второй день достигают максимального уровня. Появляются чувство тревоги, напряжение, физическая слабость, тахикардия, аритмия, учащенное дыхание, увеличение температуры до субфебрильной (37,1–37,2°С), тошнота, рвота, понос, тремор.
К концу второго дня кризиса и в интервале 48–72 ч усиливаются боли в мышцах спины, появляются выламывающие боли мышц рук и ног, сведение жевательных мышц. Далее присоединяются нестерпимые боли в животе, пояснице, области сердца, сведение икр, зуд и жжение.
Психические расстройства выражаются в депрессии, раздражительности, истерии, психопатических реакциях, отказа от пищи, склонности к гневу, агрессии, суициду.
Острая фаза длится 7–10 дней, затяжная абстиненция – до 6 мес и характеризуется гипотензией, брадикардией, бессонницей, отсутствием аппетита и пассивностью.
Действие спидболла на организм
Смесь героина и кокаина как в форме для внутривенного введения, так и в форме для курения, усиливает действие каждого наркотика на организм и психику. ■ ЦНС. Действие кокаиновой составляющей проявляется как действие стимулятора, вызывающего гиперактивность и раздражительность. ■ Действие героиновой составляющей вызывает состояние миролюбия и расслабленности. Настроение потребителя спидболла меняется быстро и непредсказуемо. ■ Легкие. Постоянное использование спидболла для курения вызывает болезни горла, эмфизему, бронхиты, различные респираторные заболевания. ■ Вес. Наркоманы часто теряют интерес к еде и сну. Многие страдают катастрофической потерей веса. ■ Мозг. Биохимическое состояние мозга изменяется, и привыкание наступает очень быстро.Фармакокинетика
Опий
После приема опия (1 г/день) в виде опиумных шлаков в моче определены свободные соединения (негидролизованная моча) (мкг/ мл): морфин – 0,64, кодеин – 0,37, норморфин и норкодеин по 0,15 и носкапин. Количества конъюгированных соединений (анализ гидролизованной мочи) превышают эти величины в 10 раз.Морфин
Фармакокинетические параметры: период полужизни в плазме T½ – 2–3 ч, объем распределения V(D)=3,3 л/кг, клиренс Cl (Пл)=15–20 мл/мин/кг, связывание с белками 20–30%.Концентрации морфина в плазме (мг/л).
| Терапевтическая: | 0,08–0,12 |
| Токсическая: | 0,15–0,5 |
| Летальная: | 0,05–4,0 |
При ВВ субклинических доз морфина 2 мг максимальная концентрация в плазме 200 нг/мл достигается через 3–4 мин, затем снижается до 6 нг/мл через 20 мин и до примерно 2 нг/мл в интервале 3–6 ч.
Кинетика элиминирования из плазмы свободного и связанного морфина различны. После введения 1 мг/кг морфина (инъекции в спинномозговой канал) максимальная концентрация свободного морфина в плазме 100 нг/мл в интервале 2–5 мин уменьшается до 60 нг/мл в течение 1–1,5 ч и до 15–10 нг/мл через 2–4 ч. Концентрация связанного (конъюгированного) морфина увеличивается при этом от 9 до 80 нг/мл в интервале 2–20 мин и затем остается неизменной по крайней мере до 4 ч.
Распределение
Распределяется морфин в основном в органы: почки, печень, легкие, селезенку и мозг. Процесс протекает очень быстро: через 6 мин после внутривенного введения в системе циркуляции остается только 7% введенной дозы морфина. Морфин амфотерен и умеренно растворим в липидах. Его концентрация в мозге в 2–5 раз выше, чем в крови. Повышенные концентрации морфина также найдены в легких, печени, мышцах, желчи и миокарде.Основные метаболиты.
| Морфин–3–О–глюкуронид (М3Г) | 65–75% |
| Морфин–3–О–сульфат | 5–10% |
| Морфин–6–О–глюкуронид (М6Г) | 0,3–33% |
| Морфин свободный (м) | 2–12% |
| Норморфин свободный (нм) | 1% |
| Норморфин глюкуронид (НМГ) | 3–4% |
Основной метаболит: морфин–3–глюкуронид является основной фармакологически неактивной формой выведения морфина. морфин–6–глюкуронид – фармакологически активен. Соотношение свободного и конъюгированного морфина в моче в период 1–2 ч после приема 1:3, а в интервале 9–72 ч 1:17. Соотношение морфин–3–глюкуронид: морфин–6–глюкуронид составляет примерно 7:1 в моче и 3:1 в сыворотке крови. Эти метаболиты имеют различные времена «полужизни» в плазме, T½ для М3Г составляет 16,8, а для М6Г – 6,0, что отражает различие в скорости элиминирования. Элиминирование М3Г протекает гораздо медленнее, чем М6Г.
 Рис. 3. Взаимные превращения опиатов при метаболизме.
Рис. 3. Взаимные превращения опиатов при метаболизме.
Кроме указанных выше, в следовых коладестрах образуются метаболиты: ■ N–оксид. ■ морфин–3,6–диглюкуронид.
Кодеин не является метаболитом морфина, но может присутствовать в биопробах как сопутствующий опийный алкалоид.
Выведение
За 8 ч выводится 80% введенной дозы морфина, за 24 ч – 64–90%, через 72–100 ч в моче определяют лишь следы морфина. Концентрация М, измеренная в 2000 образцах мочи наркоманов, составляет 0–750 нг/мл.После внутримышечного введения 20 мг морфина пик концентрации в моче свободного и конъюгированного морфина достигается через 4–9 ч. В начальный период времени в виде свободного морфина выводится 25–34% общего морфина, спустя 12 ч свободный морфин составляет только 5,9% общего морфина. За весь период выводится в виде свободного морфина 6,8% дозы и в виде конъюгированного морфина – 58,6% дозы. Время полувыведения T½ составляет соответственно для свободного и связанного морфина 3,6–6,6 и 7,9–8,2 ч. В табл. 1 приведены параметры, характеризующие выведение морфина после внутримышечного введения.
Таблица 1. Концентрация морфина в моче, нг/мл.
Пациент – хронический потребитель героина, доза 20 мг морфина ВМ
| Время отбора пробы, ч | Морфин свободный | Морфин общий |
|---|---|---|
| 1,2 | 2123 | 8006 |
| 4,2 | 5254 | 44843 |
| 8,8 | 1598 | 23010 |
| 11,6 | 228 | 4335 |
| 24 | 157 | 2579 |
| 36 | 100 | 1640 |
| 48 | 40 | 62760 |
| 60 | – | 112 |
| 72 | – | 54 |
| 84 | – | 0 |
Морфин–6–глюкуронид
Морфин–6–глюкуронид (М6Г) – активный метаболит морфина, превышает анальгетическую активность морфина в 4 раза. При дозе 1 мг М6Г вызываемое им анальгетическое действие длится более 7 ч. Концентрация М6Г в плазме превышает концентрацию морфина в 4–6 раз при оральном приеме.Накопление М6Г при терапии морфином при ослабленной ренальной функции у пациентов может привести к летальному исходу. В этом случае концентрация в плазме свободного морфина несколько, а М6Г значительно превышает обычные значения при терапии (нг/мл): морфин своб. – 76–102, М6Г – 4500–13000.
Содержание морфина в волосах
Содержание морфина в волосах лица спустя 11 дней после получения 20 мг морфина ВМ составило 1,3 нг/мг, а после дополнительного введения 10 мг спустя 7 дней после первой дозы – менее 1,0 нг/мг. Соответствующие максимальные концентрации морфина в плазме, слюне и моче для первой и второй инъекций составляют: 150,2 и 66,1 нг/мл (через 0,25–0,5 ч после введения), 37,8 и 10,8 нг/мл (через 0,5 ч), 2423,5 и 1058,8 нг/мл (через 1 ч).Содержание морфина в организме при фатальных случаях
При смертельном исходе в результате приема сверхдоз морфина концентрация исходного соединения в биожидкостях (мкг/мл) или органах (мкг/г):| кровь (n=10) | 0,2–2,3 |
| плазма (среднее из n=60) | 0,521 |
| моча (n=10) | 14–81 |
| печень | 0,4–18 |
Время детектирования морфина в моче
Среднее время детектирования общего морфина в моче при уровне порога значимости результата (ПЗР, cut–off), принятого между народными организациями для опиатов 300 нг/мл, составляет 45 ч, при величине 40 нг/мл – 80 ч. Для определения свободного морфина методом ГХ/МС с пределом детектирования 15 нг/мл – 50 ч.Поступление морфина и кодеина с едой
Морфин и кодеин могут определяться в моче после употребления в пищу различных продуктов, содержащих маковое семя в качестве приправы, или кондитерских изделий с маком. Эти случаи следует дифференцировать с нелегальным приемом опия или морфина. Так, предложено использовать в качестве доказательства употребления в пищу семян мака присутствие в моче алкалоида опия тебаина. Его концентрация в моче после употребления в пищу 11 г мака от 2 до 81 нг/мл, в то время как при введении «уличных» препаратов героина и приеме внутрь лекарственных препаратов кодеина или морфина тебаин в моче не был обнаружен.В среднем содержание морфина в маковых семенах – от 20 до 200 мкг/г, кодеина – от 2 до 80 мкг/г. Максимальные концентрации достигаются в интервале 2–5 ч после еды и медленно уменьшаются в период 24–48 ч до уровня предела детектирования. Иммунными методами опиаты могут детектироваться в моче вплоть до 60 ч после употребления в пищу изделий, содержащих мак. В табл. 2 приведены максимальные значения концентраций опиатов в моче, определяемые в этих случаях.
Таблица 2. Концентрация морфина и кодеина в моче после употребления маковых семян в качестве пищи.
| № | Содержание в маке, мкг/г | Доза мака, г | Максимальная концентрация в моче, нг/мл | ||
|---|---|---|---|---|---|
| Морфин | Кодеин | Морфин | Кодеин | ||
| 1 | 100 | – | 100 | 305 | . |
| 2 | 200 | – | 150 | 18000 | |
| 3 | 960 | 80 | 5 | 2797 | 214 |
| 4 | – | – | – | 1481 | 75 |
| 5 | 18,6 | 2,5 | 70 | 3300 | |
| 6 | 294 | 14 | 40 | 2635 | 45 |
| 7 | 106 | 3,8 | 200 | 860 | 358 |
| 8 | 108 | – | 15 | 2010 | 78 |
Героин, диацетилморфин
Фармакокинетические параметры диацетилморфина (ДАМ): полужизнь в плазме T½= 9 мин (по другим данным 3–7 мин).После ВВ максимальная концентрация ДАМ в плазме достигается за 1–2 мин и в последующие 10 мин быстро уменьшается благодаря метаболизму и депонированию в ткани. В последующие 12 ч в плазме сохраняются низкие уровни концентраций ДАМ. Вследствие меньшей полярности и высокой липидной и мембранной растворимости всасывание быстрее, чем морфина. По тем же причинам ДАМ легко преодолевает гематоэнцефалический барьер. Достигая мозга, героин превращается в морфин, отвечая таким образом за транспорт морфина к мозгу.
Диацетилморфин быстро метаболизируется в крови до 6–моноацетилморфина (6–МАМ), за 10–12 мин биотрансформация проходит полностью. Далее 6–МАМ быстро покидает кровяное русло и деацетилируется (в основном в печени и частично в мозге) медленно до морфина, так что превращение заканчивается в течение нескольких часов. Период полувыведения из плазмы T½ – 38 мин. Морфин конъюгируется, превращаясь, главным образом, в неактивный метаболит М3Г и в меньшей степени в активный М6Г.
Основные метаболиты ■ 6–Моноацетилморфин (6–МАМ). ■ Морфин (м) ■ Морфин–3–глюкуронид (М3Г) ■ Морфин–6–глюкуронид (М6Г).
Следовые метаболиты ■ норморфин ■ норморфин–глюкуронид ■ 6–ацетилморфин–глюкуронид ■ морфин–3,6–диглюкуронид ■ дигидроморфинон и др.
Соотношение свободного и конъюгированного морфина около 1:9. При внутривенном введении 200 мг героина максимальная концентрация в плазме через I мин составляет (нг/мл): ДАМ – 1490, 6–МАМ – 3410, за 2 мин эти значения уменьшаются до 814 (ДАМ) и 1887 (6–МАМ) нг/мл. Спустя 6 мин концентрация морфина максимальна и составляет 166 нг/мл. Конъюгаты морфина достигают максимального содержания спустя 15 мин после введения: преобладающий и долгоживущий метаболит М3Г – 3850 и активный М6Г – 399 нг/мл.
В течение 24–96 ч с мочой выводится около 80% дозы героина. В первые 8 ч выделяется 48% дозы, из которых 7% составляет морфин свободный. К 96 ч выводится 79% дозы. T½ элиминирования свободного 6–МАМ 1,3 ч, морфина свободного – 3,6–6,6 ч, морфина конъюгированного – 7,9–8,2 ч. Менее 3% дозы выводится желчью в двенадцатиперстную кишку. Благодаря бета–глюкуронидазной активности кишечной флоры и слизистых, в небольшой степени конъюгаты распадаются до свободного морфина, который реабсорбируется и участвует в энтерогепатитной рециркуляции. Выведение отдельных метаболитов за 24 ч в процентах дозы после приема 10 мг/кг героина, разделенных на 4 приема, приведено ниже (в скобках даны средние величины):
| Диацетилморфин (ДАМ) | 0,05–0,5% (0,1%) |
| Морфин–3–глюкуронид (М3Г) | 50–60% (38,2%) |
| Морфин (М) | 5–7% (4,2%) |
| 6–моноацетилморфин (6–МАМ) | 0,2–1,7% (1,3%) |
| Норморфин (нм) общий | 2,8–4% |
| 6–МАМ + 6–МАМ–3–глюкуронид | менее 5%. |
Пациент А, курение: доза 10,5 мг героина основания, внутривенное введение: доза 10 мг героина гидрохлорида, плазма не гидролизована.
| Время | Курение | Внутривенное введение | ||||
|---|---|---|---|---|---|---|
| Мин | Героин | 6–МАМ | Морфин | Героин | 6–МАМ | Морфин |
| 2 | 299 | 140 | 56 | 72 | 15,9 | 0 |
| 5 | 82 | 58 | 39,6 | 64 | 39,5 | 16,1 |
| 10 | 11,9 | 27,9 | 28,1 | 14 | 20,7 | 12,5 |
| 15 | 3,9 | 19,5 | 21,9 | 4,3 | 14,1 | 11,6 |
| 30 | 0 | 7,6 | 19,4 | 1,0 | 7.1 | 10,8 |
| 60 | 0 | 2,5 | 13,9 | 0 | 2,8 | 10,3 |
| 120 | 0 | 0 | 9,5 | 0 | 0 | 7,8 |
| 240 | 0 | 0 | 0 | 0 | 0 | 4,3 |
| 480 | 0 | 0 | 0 | 0 | 0 | 1,9 |
| 720 | 0 | 0 | 0 | 0 | 0 | 1,3 |
| 1440 | 0 | 0 | 0 | 0 | 0 | 0 |
При интраназальном и внутримышечном введении 6 или 12 мг героина шести добровольцам показано, что фармакинетические закономерности в основном подобны, хотя при внутримышечном введении (ВМ) концентрации свободного и связанного морфина, как и 6–МАМ, выше, чем при интраназальном (ИН). Максимальная концентрация в моче общего и свободного морфина и 6–МАМ достигается за 4–6 ч и составляет в среднем 2821 нг/мл (интервал 1628–3455) (ИН, 6 мг героина); 6371 нг/мл (интервал 3085–10 425) (ИН, 12 мг героина) и 3892 нг/мл (интервал 1869–6117) (ВМ, 6 мг героина). Средние значения концентрации свободного морфина и 6–МАМ (нг/мл): 364 и 34 (ИН, 6 мг героина); 1174 и 73 (ИН, 12 мг героина), 789 и 118 (ВМ, 6 мг героина). Общий морфин может быть определен в моче в период времени 24–36 ч, 6–МАМ – в течение 2–3 ч. Времена «полувыведения» T½, рассчитанные из этих данных, составляют для связанного морфина: 7,0–7,8, для свободного морфина 5,9–7,0. В виде связанного морфина выводится от 31,4 до 33,9% дозы, свободного морфина 2,4–7,7%, 6–МАМ 0,1–0,4%.
В крови и моче живых водителей автотранспорта, подозреваемых в употреблении героина (дозы и время приема не известны), концентрации метаболитов меняются в широких пределах (см. табл.4). В табл. 5 приведены значения концентраций метаболитов героина, выводимых с мочой.
Метаболит героина – 6–МАМ
Диацетилморфин (ДАМ)–липидорастворимое “пролекарство”, обеспечивающее доставку (за 10–15 сек после внутривенного введения) и накопление 6–МАМ и морфина в ткани мозга. 6–Моноацетилморфин – основной метаболит героина, посредством которого осуществляется анальгетическое и наркотическое действие героина (морфин – второй метаболит, выполняющий в организме ту же функцию).Таблица 4. Концентрация метаболитов в биожидкостях водителей автотранспорта, употреблявших героин, нг/мл. БЖ – биожидкость, К – кровь, М – моча.
| № | БЖ | М3Г | М6Г | М | К | К6Г | 6–МАМ |
|---|---|---|---|---|---|---|---|
| 1 | Кр | 32 | 15 | 4 | н.д. | н.д. | следы |
| 1 | Мч | 89 | 60 | 18 | н.д. | н.д. | 4 |
| 2 | Кр | 84 | 16 | 9 | н.д. | н.д. | н.д. |
| 2 | Мч | 2600 | 1280 | 290 | 48 | н.д. | 32 |
| 3 | Кр | 153 | 120 | 25 | 95 | 530 | 3 |
| 3 | Мч | 9900 | 2500 | 1600 | 450 | 2600 | 320 |
| 4 | Кр | 190 | 32 | 5 | н.д. | н.д. | н.д. |
| 4 | Мч | 463 | 146 | 19 | н.д. | 6 | н.д. |
| 5 | Кр | 397 | 117 | 153 | н.д. | 17 | н.д. |
Таблица 5. Концентрация метаболитов героина в моче, нг/мл. Разовая доза героина ВМ, 6 мг, пациент Q.
| Время отбора пробы, час | 6–МАМ | Морфин–общий | Морфин–свободный |
|---|---|---|---|
| 2,8 | 206 | 7322 | 1201 |
| 3,8 | 10,6 | 1433 | 149 |
| 6,6 | 1.6 | 1234 | 107 |
| 7,4 | 0 | 1062 | 84 |
| 9,4 | 0 | 311 | 28 |
| 24 | 0 | 229 | 28 |
| 36 | 0 | 110 | 0 |
| 48 | 0 | 66 | 15 |
| 60 | 0 | 0 | 0 |
Сделана попытка выработать статистический критерий на основе значений концентраций общего кодеина и общего морфина в моче для оценки вероятности присутствия 6–МАМ, т.е. использования героина. По результатам анализа 100 проб мочи живых лиц, употреблявших героин, составлены два массива данных. Первый объединяет пробы (71 образец), в которых присутствуют: общий морфин в интервале 1580–296 750 нг/мл, общий кодеин в интервале 144–71800 нг/мл и 6–МАМ в интервале 9–7700 нг/мл. Во второй массив входят остальные 29 образцов, в которых обнаружены только кодеин и морфин.
Предложен статистический критерий, при выполнении которого с высокой вероятностью можно ожидать появления в моче 6–МАМ: ■ концентрация общего морфина должна превышать 5000 нг/мл. ■ отношение концентрации общего кодеина к концентрации общего морфина должно быть ниже 0,125.
Данные табл. 5 подтверждают, что в небольшой (до 3 ч) период времени после употребления героина количество 6–МАМ в моче может быть значительно, однако затем его концентрация резко снижается, что затрудняет подтверждение факта употребления героина при анализе.
Активный метаболит героина – морфин–6–глюкуронид
Морфин–6–глюкуронид (М6Г) – активный метаболит героина, чье анальгетическое и токсическое действие проявляется и при клиническом применении морфина (см. ранее). В табл. 6 приведены значения концентрации М, М3Г и М6Г в сыворотке крови двадцати героиновых наркоманов и для десяти случаев смерти от передозировки героина. Содержание М6Г в фатальных случаях выше, чем для живых лиц, употребляющих героин. Это может быть связано с относительно коротким периодом времени между приемом наркотика и смертью (так называемая «быстрая смерть»), когда образование глюкуронидов превышает их выведение. Низкая величина отношения концентрации М6Г/М (менее двух) в фатальных случаях указывает, что при соответствующей концентрации морфина процесс перераспределения все еще продолжается и смерть можно отнести к категории «быстрой».Таблица 6. Содержание метаболитов героина в сыворотке крови живых лиц и погибших в результате передозировки героина, нг/мл
| Метаболиты | Живые лица, n=20 | Погибшие от передозировки, n=7 | ||
|---|---|---|---|---|
| интервальное значение | среднее | интервальное значение | среднее | |
| морфии (М) | 5–171 | 26 | 232–1700 | 665 |
| М6Г | 26–321 | 116 | 316–2300 | 780 |
| М3Г | 65–1300 | 411 | 481–5800 | 1862 |
| М6Г/М | 1,41–38,58 | 7,80 | 0,34–2,85 | 1.20 |
| М3Г/м | 5,35–101,00 | 19,89 | 1,11–7,76 | 2.52 |
| М6Г/М3Г | 0,11–1.63 | 0.42 | 0.23–0.78 | 0.49 |
Содержание героина и метаболитов в слюне и поте
Содержание ДАМ, 6–МАМ и морфина в слюне исследовано для двух добровольцев при разных путях введения: внутривенном (2,6–10,5 мг героина–основания) и при курении (3–20 мг героина–гидрохлорида). 6–МАМ и морфин обнаружены в слюне, начиная с 2 мин после введения в обоих случаях. Пик концентрации ДАМ достигается через 2–5 мин после ВВ и через 2 мин после начала курения. Значения максимальных концентраций ДАМ в слюне зависят от дозы и способа введения и составляют: для ВВ от 6 (10 мг героина) до 30 (12 мг) нг/мл; для курения от 3534 (2,6 мг героина) до 20 580 (5,2 мг) нг/мл. Значительное превышение концентрации ДАМ при курении связывают с сорбцией героина в ротовой полости. Кроме того, в этом случае уменьшение концентрации ДАМ до 15 нг/мл в течение 1 ч и до 1 нг/мл в течение следующих 2–24 ч происходит более медленно, чем это установлено для ВВ, когда в пределах 1 ч концентрация ДАМ падает примерно до 1 нг/мл.“Полужизнь” ДАМ в слюне выше, чем в крови, при курении в 14–60 раз, при ВВ в 2–208 раз.
Начиная с 2 мин в слюне определяется метаболит 6–МАМ, максимальная концентрация которого для курения: 640–3577 нг/мл (2 мин) и для ВВ: 18–141 нг/мл (2–10 мин), соответственно. Далее содержание 6–МАМ, резко падает и, начиная с 0,5–8 ч при курении и 1–4 ч при ВВ, он не детектируется.
Морфин содержится в слюне в гораздо более низких количествах, но, как и для ДАМ и 6–МАМ, после курения содержание выше: 6–142 нг/мл (в максимуме). Низкие концентрации морфина в слюне после ВВ: 5–15 нг/мл к тому же обнаруживаются только в интервале 10–120 мин, а при небольших дозах (3–5 мг героина) не обнаруживаются вовсе. По сравнению с уровнями ДАМ и 6–МАМ в плазме (см. табл. 3) их концентрации в слюне после курения героина значительно выше, что может быть использовано при выборе объекта исследования.
Время; в течение которого ДАМ может быть обнаружен в слюне: 60 мин (в плазме 15–30 мин), 6–МАМ: 0,5–8 ч (в плазме 2 ч) при обоих способах введения. Морфин детектируется в слюне в течение 10–12 ч (в плазме 2 ч), но только после курения.
Из других так называемых «нетрадиционных объектов» исследования может быть использован пот. Пот является удобной биологической матрицей для определения опиатов и других наркотиков из–за простоты сбора, гигиеничности и отсутствия инвазии. Его собирают с помощью различных сорбирующих материалов, которые крепятся к коже посредством пластыря. В коммерческой продаже существуют пластыри с разной площадью сорбирующего участка – коллектора пота, в частности, «Pharm–Chekf (Rhaernchem Laboratory, Menlo Park, CA). Обычно на какой–либо участок тела ставится несколько пластырей, которые затем снимаются поочередно через некоторый период времени для анализа. В поте героиновых наркоманов (20 человек), собранном с помощью пластырей в течение 5 дней, определены опиаты и другие наркотики (нг/пластырь): ДАМ 37–175,6–МАМ 60–2386, кодеин 36–4918, морфин 21–271. При приеме бупренорфина (доза от 0,4 до 6,0 мг) с потом выводится от 13 до 153,2 нг/ пластырь (для 20 пациентов). При получении 20 мг героина в интервале 0–24 ч выделяется 533 нг ДАМ и 5,7 нг 6–МАМ, 0–48 ч – 47,3 нг ДАМ и 7,4 нг 6–МАМ 0–72 ч – 17,3 нг ДАМ и 38,5 нг 6–МАМ, 0–120 ч – 22,2 нг ДАМ и 31,3 нг 6–МАМ Морфин в этих образцах не обнаружен. Но в поте 17 героиновых наркоманов детектируются ДАМ и оба метаболита: 6–МАМ и морфин в вариабельных количествах (нг на пластырь): ДАМ от 2 до 4, 0,6–МАМ от 2,1 до 441, морфин от 6 до 156,2 [Cone E.J. et al. J.AnalytToxic 1994, 18298–305]
Содержание героина и метаболитов в волосах
Интервальные значения концентраций ДАМ и метаболитов в волосах наркоманов (нг/мг): ДАМ (n=38) – 0,045–53,14; 6–МАМ (n=141) – 0,045–53,14; морфин (n=87) – 0,011–7,8. Для 20 наркоманов–хроников, длительное время употреблявших героин, определены следующие средние значения (нг/ мг волос): ДАМ 0,17 (определен только в 7 образцах из 20); 6–МАМ 90,0; морфин 0,26; кодеин 0,18 (определен только в 15 образцах из 20) Контролируемое изучение распределения героина в волосах с участием 20 добровольцев в условиях внутривенного введения 30–800 мг/день героина, разделенных на 2–3 приема, показало влияние индивидуальных различий на процесс накопления ДАМ и метаболитов в волосах. При общей дозе 14 620–71 540 мг героина в течение 100 дней роста волос в сегменте 4 см определены: ДАМ в диапазоне 0–4,53 нг/мг волос, 6–МАМ – от 0,38 до 10,11 нг/мг, морфин – от 0,71 до 5,20 нг/мг. При этом у трех пациентов из 20 основным компонентом опиатов в волосах являлся ДАМ, в 15 – 6–МАМ и только в двух – мор? фин. Корреляции между введенной дозой героина и суммарной концентрацией опиатов в волосах не установлено (коэффициент корреляции 0,346).Содержание опиатов в меконии новорожденных
Организм плода и новорожденных, чьи матери в процессе беременности или кормления употребляли наркотические средства, содержат их в вариабельных количествах. Сами наркотики и их метаболиты достигают плода, проникая через плацентарный барьер из организма матери, а также связываясь посредством белкового связывания с белками околоплодной жидкости. Для выяснения, подвергался ли плод воздействию наркотиков, в настоящее время предпочтительно используют в качестве объекта исследования не мочу, а меконий. Меконий – это первородный кал. новорожденного, выделяемый на 1–5–й день после рождения. Меконий начинает формироваться примерно е 16–й недели беременности. В его состав входят вода, соли, желчные кислоты, мукополисахариды, липиды, белки, элементы крови, энзимы, а также эпителиальные клетки. Соединения, подвергшиеся метаболизму в печени плода, далее выводятся в мочу и желчь. Из мочи они вновь возвращаются в околоплодную жидкость, участвуя в процессе рециркуляции» в то время как в составе желчи наркотики и метаболиты достигают мекония и там сохраняются. Таким образом, меконий аккумулирует соединения, действию которых подвергался организм плода в процессе вынашивания, и их концентрация в этом случае значительно превышает концентрацию в моче. При употреблении матерью героина или морфина в меконии ребенка обнаруживают свободный и конъюгированный морфин, а также кодеин.Содержание опиатов в организме умерших в результате передозировки героина
В случае смертельного исхода в результате введения сверхдозы героина интервальные (n=403) концентрации метаболитов в биожидкостях (нг/мл) и органах (мкг/г) имеют следующие значения:| кровь: | |
|---|---|
| морфин общий | 0–3300 |
| морфин общий | 50–4400 |
| кодеин свободный (примесь) | 10–221 |
| 6–МАМ | 0–83 |
| морфин–6–глюкуронид | 316–2300 |
| морфин–3–глюкуронид | 481–5800 |
| моча: | |
| ДАМ | 0–97 |
| 6–МАМ | 5,6–2756 |
| морфин общий | 100–120 000 |
| желчь: | |
| морфин общий | 5000–175 260 |
| кодеин | 250 |
| органы: | |
| морфин общий (почки | 0,7–1,51 |
| (печень) | 0,35–0,66 |
| (мозг) | 0,02–0,60 |
| (лимфоузлы | >1) 0,2–8,7 |
| СМЖ: | |
| морфин общий | 20–140 |
Количество 6–МАМ выше в тканях с меньшей гидролитической активностью (мозг, селезёнка, СМЖ), чем в тканях с высокой гидролитической активностью (печень, легкие, почки). Содержание 6–МАМ в стекловидном теле в 41 образце из 223 «положительных» по иммунному анализу: от 10 до 125 нг/мл. Помимо 6–МАМ, в стекловидном теле определены кодеин и морфин в различных соотношениях.
Для семи случаев смерти в результате передозировки героина усредненные концентрации метаболитов в крови (бедренная вена) (нг/мл): М3Г – 432, М6Г – 165, М – 245, К – 19, К6Г – 333, 6–МАМ – 33. Достаточно высокие уровни содержания кодеина связаны с метаболизмом ацетил кодеина, который в вариабельных количествах присутствует во многих образцах героина, производимого из морфина–сырца и опия, но особенно из маковой соломы. Для 21 жертвы передозировки героина приведены аналогичные величины содержания метаболитов в крови (нг/мл): М от 8 до 1539, М3Г от 111 до 941, М6Г от 32 до 332, 6–МАМ от 0 до 73. Те же соединения определены в спинномозговой жидкости (СМЖ) (11 образцов из 21), в моче (6 образцов) и стекловидном теле (12 образцов). В СМЖ концентрации М, М3Г и М6Г ниже, чем в крови. Еще ниже концентрации в стекловидном теле. Для 16 жертв передозировки героина или морфина (внутривенные инъекции) концентрация морфина в СМЖ 20–140 нг/мл, а в крови 17–920 нг/мл. Отношение концентрации морфина СМЖ/кровь изменяется в широком диапазоне от 0,18 до 1,82.
Таблица 7. Содержание диацетилморфина и метаболитов в организме человека, погибшего в результате передозировки героина. нг/мл или нг/г.
| Орган | ДАМ | 6–МАМ | Морфин |
|---|---|---|---|
| кровь | 0 | 16,2 | 81,7 |
| моча | 71 | 848 | 655 |
| СМЖ | 0 | 38,5 | 36,6 |
| печень | 0 | следы | 90,6 |
| почки | 0 | следы | 358,5 |
| легкие | 0 | 3,5 | 285,1 |
| мозг | 0 | 53,6 | 88,5 |
| селезенка | 0 | 124,9 | 244,8 |
| место инъекции | 130 | 3656,7 | 1088,3 |
| волосы головы | 0 | 0,10 | 0,07 |
Таблица 8. Опиаты в организме матери и плода после смерти от передозировки героина, мкг/г. н.д. – не детектированы при данном пределе обнаружения анализа.
| Образец | Морфин | 6–МАМ | ДАМ | Кодеин | ||||
|---|---|---|---|---|---|---|---|---|
| Мать | Плод | Мать | Плод | Мать | Плод | Мать | Плод | |
| кровь | 1,8 | 0,71 | 0,25 | 0,036 | н.д. | н.д. | 0,097 | 0,027 |
| желчь | 24 | 5,55 | н.д. | н.д. | н.д. | н.д. | 0,03 | 0,019 |
| почки | н.д. | 2,81 | н.д. | н.д. | н.д. | н.д. | н.д. | 0,12 |
| моча | 14 | н.д. | н.д. | н.д. | н.д. | н.д. | н.д. | н.д. |
| волосы 0–1 см | 8,1 | 3,97 | 3,28 | 11,77 | 4,18 | 2,5 | 1,25 | следы |
| мозжечок | 2,09 | 1,17 | 0,02 | 0,01 | Н.Д. | Н.Д. | 0,014 | 0,026 |
В табл. 9 приведены концентрации опиатов в крови шести лиц, погибших в результате передозировки героина. Высокое содержание кодеина в некоторых пробах указывает на высокий уровень ацетилкодеина в исходном героине и на возможность его получения из экстракционного опия или экстрактов травы мака.
Таблица 9. Содержание морфина, кодеина и 6–МАМ в крови погибших от передозировки героина. Нг/г.
| Субъект | Морфин | Кодеин | 6–МАМ |
|---|---|---|---|
| 1 | 250 | 151 | 3,5 |
| 2 | 1592 | 221 | 2,0 |
| 3 | 1452 | 142 | 3,0 |
| 4 | 243 | 10 | 4,6 |
| 5 | 463 | 48 | 1,6 |
| 6 | 835 | 50 | 6,1 |
| Среднее | 805 | 104 | 3,5 |
Таблица 10. Концентрация морфина и 6–МАМ в биожидкостях (нг/мл) и тканях (нг/г)(случай самоотравления в результате введения сверхдозы героина)н.д. – не детектирован при данном пределе обнаружения анализа.
| Образец | Мсвоб. | Мобщ. | 6–МАМ | %Мсвоб. |
|---|---|---|---|---|
| Кровь, лев. жел. сердца | 800 | 1170 | н.д. | 68,4 |
| Кровь, прав. жел. сердца | 464 | 534 | Н.Д. | 86,9 |
| Кровь правой бедр. вены | 1350 | 1570 | Н.Д. | 86,0 |
| Жидкость перикарда | 757 | 1500 | Н.Д. | 50,5 |
| СМЖ | 364 | 960 | н.д. | 37,8 |
| Моча | 435 | 1680 | 417 | 25,9 |
| Головной мозг | 336 | 340 | н.д. | 98,8 |
| Мышца сердца | 669 | 848 | и.я. | 78,9 |
| Легкие | 1140 | 2270 | н.д. | 50,2 |
| Печень | 1440 | 4200 | н.д. | 34,3 |
| Селезенка | 700 | 956 | н.д. | 73,2 |
| Правая почка | 1790 | 1900 | н.д. | 94,2 |
| Правая мышца бедра | 736 | 992 | н.д. | 74,2 |
| Содержимое желудка | 1200 | 5220 | 78 | 23,0 |
Специальными исследованиями 32 случаев в интервале 3–37 ч после момента смерти (Т1), вызванной передозировкой героина, было показано, что морфин в течение последующих 3–43 ч (Т2) не перераспределяется из тканей в кровяное русло центральной или периферической систем. Концентрация морфина в крови центральной системы (желудочковая кровь) в момент Т1: 0,008–0,836, в момент Т2: 0,010–0,732 мг/л, в крови периферической системы (бедренная кровь) в момент Т1: 0,006–1,28, в момент Т2: 0,007–1,61 мг/л.
В зависимости от интервала времени между введением наркотика и моментом смерти условно различают так называемую “быструю”, или “внезапную” (наступающую вслед за введением героина с небольшим интервалом) и «задержанную», или «отложенную» смерть. «Быстрая» смерть по сравнению с «задержанной» характеризуется следующими закономерностями: ■ средние концентрации метаболитов морфина свободного, морфина общего и 6–МАМ в крови выше. ■ средние концентрации тех же метаболитов в моче ниже. ■ отношение концентрации морфина свободного к общей концентрации морфина в крови выше. ■ более высокая вероятность детектировать 6–МАМ в крови. ■ меньшая вероятность обнаружить ДАМ в моче.
Для «быстрой» смерти доля морфина свободного от общего составляет в крови в среднем 76,1 % (интервал от 50 до 100%, п–44), для «задержанной» – 31 % (интервал от 20 до 40%, n=8), т.е. в случае “быстрой” смерти морфин в крови присутствует в основном в свободном, а в случае “задержанной” – в связанном виде.
В табл. 11 приведены концентрации опиатов в крови и моче для обеих категорий смертей, наступивших в результате передозировки героина спустя 15 мин и несколько часов соответственно.
Таблица 11. Концентрации героина и метаболитов, характеризующих различие «быстрой» (Б.С.) и «задержанной» (З.С.) смерти в результате передозировки героина. Нг/мл
| n | кровь | моча | |||||
|---|---|---|---|---|---|---|---|
| ДАМ | 6–МАМ | М | ДАМ | 6–МАМ | М | ||
| Б.С. | 1 | 0 | 2,3 | 87,5 | 0 | 145,6 | 184,6 |
| Б.С. | 2 | 0 | 5,8 | 138,5 | 0 | 110,9 | 43,0 |
| Б.С. | 3 | 0 | 1,4 | 95,9 | 0 | 5,6 | 332.7 |
| Б.С. | 4 | 0 | 5,9 | 619,0 | 8,5 | 356 | 1024 |
| Б.С. | 5 | 0 | 24,4 | 95,1 | 0 | 11,8 | 1061 |
| Б.С. | 6 | 0 | 82,9 | 1277,0 | 5,0 | 15,0 | 5,2 |
| Б.С. | 7 | 0 | 0 | 88,6 | 0 | 88,1 | 2795 |
| Б.С. | 8 | 0 | 28,1 | 481,9 | 6,3 | 43,8 | 6,5 |
| Б.С. | среднее | 0 | 18,9 | 360,4 | 2,5 | 196,2 | 681,5 |
| З.С. | 1 | 0 | 9,9 | 100,2 | 8,3 | 259 | 705 |
| З.С. | 2 | 0 | 29,8 | 117,6 | 14,5 | 96,4 | 30,4 |
| З.С. | 3 | 0 | 1.4 | 41,8 | 3,2 | 312 | 3412 |
| З.С. | 4 | 0 | 0 | 121,1 | 5,8 | 278 | 1570 |
| З.С. | 5 | 0 | 6,0 | 131,1 | 4,7 | 398 | 1301 |
| З.С. | 6 | 0 | 0 | 145,7 | 83,9 | 2756 | 9500 |
| З.С. | 7 | 0 | 0 | 71,6 | 90,3 | 1357 | 2380 |
| З.С. | среднее | 0 | 6,7 | 104,2 | 30,1 | 779,5 | 2699,8 |
Кодеин
Фармакокинетические параметры: период полуэлиминации 2–4 ч, объем распределения 3,5 л/кг, клиренс из плазмы 10–15 мл/мин/ кг, связывание с белками плазмы 7–25%.Концентрации кодеина в плазме (мг/л) :
| терапевтическая | (0,01–0,05) – (0,05–0,25) |
| токсическая | 0,3–0,5 |
| летальная | более 1,6. |
При увеличении дозы до 60 и 120 мг кодеина, принимаемой в клинических условиях наркоманами с длительным опытом употребления наркотиков (6–14 лет) в течение трех дней в неделю (попеременно с кокаином), максимальные концентрации кодеина в плазме через 1–2 ч после приема составили 17–271 (среднее 147) для низкой дозы и 184–739 (среднее 378) нг/мл для высокой. Снижение концентрации начинается через 4 ч и через 8 ч после приема она доходит до 1 нг/ мл. Кроме кодеина, определены метаболиты (в скобках приведена максимальная концентрация в нг/мл): норкодеин (57), морфин (11) и норморфин (12). Последние два метаболита присутствуют не во всех пробах плазмы. Через 24 ч элиминирование кодеина и метаболитов из плазмы заканчивается.
Мониторинг метаболитов кодеина в плазме в течение 24 ч был проведен после приема внутрь 25 и 50 мг кодеина тринадцатью участниками, никогда не принимавших каких–либо наркотиков. Определены кодеин, кодеин–6–глюкуронид (К6Г), морфин (М), морфин–6–глюкуронид (М6Г) и морфин–3–глюкуронид (М3Г). В табл. 12 приведены полученные данные. «Пиковые» концентрации всех соединений достигаются в одном временном интервале 1–2 ч. Наибольшее «пиковое» значение установлено для К6Г, а концентрация М3Г превышает значения для морфина и М6Г. Метаболиты К6Г, М3Г и М6Г имеют различные времена «полужизни» в плазме T½, т.е. различные скорости элиминирования. М3Г элиминируется гораздо медленнее, чем К6Г, а морфин – медленнее, чем кодеин. Во всем временном вплоть до 24 ч после приема кодеина доминирует К6Г, но, начиная с этого времени, количество М3Г превышает количество всех соединений в плазме.
Таблица 12. Некоторые параметры кодеина и метаболитов в плазме. Средние значения для N=13 (в скобках приведены интервальные значения)
| Параметр | Доза, мг | Кд | К6Г | М | М3Г | М6Г |
|---|---|---|---|---|---|---|
| Т (макс), ч | 25 | 1.3 (0,5–4) | 1,5 (0,65–4) | 1,2 (0,5–4) | 1,5 (0,6–4) | 1,4 (0,7–4) |
| 50 | 1,1 (0.5–2,2) | 1.4 (0,7–2,3) | 1,0 (0,5–2,2) | 1,3 (0,7–2,2) | 2,0 (0,9–6) | |
| С (макс)., наномоль в литре | 25 | 149 (42,6–250) | 2131 (1470–3513) | 4,2 (1,0–10,8) | 79,7 (18,3–150) | 14,5 (1,7–28,4) |
| 50 | 310 (121–501) | 4037 (1964–5757) | 7,6 (1,5–25,3) | 146 (22,9–333) | 27,3 (3,5–53,5) | |
| Т½, ч | 25 | 2,1 | 3,9 | 4,0 | 16,8 | 6,0 |
| 50 | 2,0 | 4,0 | 1,9 | 8,4 | 8,5 |
Метаболизм
Основные пути метаболизма в печени: конъюгирование, О–деметилирование до морфина и N–деметилирование до норкодеина.Основные метаболиты: минорные метаболиты кодеина:
| кодеин–6–глюкуронид (К6Г) – основная форма выведения | 35–46% |
| кодеин (К) общий | 40–70% |
| кодеин свободный | 5–17% |
| морфин (М) свободный | 1% |
| морфин–3–глюкуронид (М3Г) | 5–13% |
| морфин общий | 5–15% |
| норкодеин (НК) общий | 10–20% |
| норкодеин свободный | 4–8%, |
| норморфин (НМ) общий менее | 1% |
| гидрокодон, норгидрокодон, дигидрокодеин, в сумме составляют | 0,2–0,3% |
Выведение
За 24 ч выводится с мочой примерно 86% введенной дозы кодеина. После орального приема разовой дозы кодеина 60 мг в моче, собранной в период 0–6 ч, найдено (нг/мл): К6Г – 18 100, К – 4900, 38.Таблица 13. Интервальные содержания кодеина и морфина в моче после приема кодеина–фосфата.
| Пациент | Кодеин общий, нг/мл | Морфин общий, нг/мл | К/М |
|---|---|---|---|
| 1 | 30–9500 | 30–510 | 0–30,5 |
| 2 | 20–16400 | 20–920 | 0,9–42,3 |
| 3 | 30–5800 | 40–350 | 0,7–19,7 |
| 4 | 40–13400 | 40–1430 | 0–12,4 |
| 5 | 70–9400 | 20–310 | 3,1–31,2 |
| 6 | 20–22200 | 20–350 | 0,8–20,9 |
| 7 | 20–32 000 | 80–630 | 0,2–51,7 |
| 8 | 20–19 500 | 20–1250 | 0,7–20,5 |
| 9 | 20–19 700 | 40–360 | 0,5–54,3 |
| 10 | 20–37300 | 30–690 | 0–55,7 |
Таблица 14. Содержание кодеина и морфина в моче после приема кодеина нг/мл.
| Время, час | Субъект 1 | Субъект 2 | Субъект 3 | |||
|---|---|---|---|---|---|---|
| Кодеин | Морфин | Кодеин | Морфин | Кодеин | Морфин | |
| 1 | 8534 | 1405 | 8175 | 947 | 6499 | 1030 |
| 2 | 6764 | 1671 | 4603 | 923 | 8563 | 1441 |
| 3 | 4294 | 1206 | 5678 | 2156 | 3221 | 657 |
| 4 | 5088 | 1494 | 5169 | 1971 | 3056 | 667 |
| 12 | 4605 | 1562 | 5120 | 2183 | 4431 | 1035 |
| 24 | 370 | 404 | 713 | 571 | 666 | 504 |
| 36 | 69 | 265 | 283 | 509 | 311 | 459 |
| 48 | 16 | 150 | 77 | 201 | 10 | 31 |
| 72 | 5 | 58 | . | 17 | 3 | 36 |
| 96 | – | – | – | – | – | – |
В табл. 13 приведено содержание общего кодеина и общего морфина в моче после приема десятью добровольцами лекарственного средства кодеина–фосфата (1 таблетка, 22,6 мг кодеина основания). Анализ проводили для проб мочи от момента введения препарата до полного его выведения (до 42–72 ч). Отношение концентраций кодеина и морфина (К/М) представляет собой важный параметр, который используют для дифференцирования лекарственного приема кодеина от употребления опиатов с немедицинскими целями (см. далее).
В табл. 14 приведена концентрация В Моче кодеина и морфина для трех, человек, принявших внутрь разовую дозу кодеина 90 мг. Оба соединения детектируются в моче в течение 4 дней. В период др 12 ч после введения концентрация общего кодеина Превышала концентрацию общего морфина: отношение кодеин/морфин 1, но далее оно снижалось до 0,1 и морфин становился основным метаболитом.
Выведение кодеина с мочой в течение 96 ч в виде неизмененного соединениями метаболитов (морфина и норкодеина) после приема орально 25 и 50 мг кодеина тринадцатью здоровыми добровольцами изучено в клинических условиях. Было установлено, что с мочой выводится в среднем (% от принятой дозы): общий кодеин 65,8 и 57,5;; общий морфин 5,44 и 5,56; норкодеин 2,76 и 3,77 для низких и высоких доз соответственно. Отношение элиминированных количеств морфина и кодеина составляет от 2,3 до 23,3%;в среднем 9,8% для обеих доз. Времена полувыведения Т½: для кодеина 3,48 и 3,71, для морфина 6,90 и 8,27 при дозах 25 и 50 мг соответственно. Эти данные указывают на более медленное элиминирование морфина по сравнению с кодеином (так же, как для метаболитов М3Г и К6Г в плазме, см. выше). В результате, начиная с некоторого времени после приема кодеина, концентрация общего морфина в моче начинает превышать концентрацию общего кодеина (в некоторых опытах величина отношения М/К доходит до трех). Эта трансформация приходится примерно на 30 ч независимо от дозы яри общем времени детектирования по иммунному скринингу 20–39 ч для дозы 25 мг и 30–62 ч для дозы 50 мг. Выполнение двух условий: величина отношения морфин/кодеин превышает 2, а концентрация кодеина более 5000 нг/мл – рассматривается авторами как твердое доказательство приема чистого кодеина и дифференцирование от нелегального употребления морфина или героина. Однако в трёх случаях из исследованных тринадцати содержание кодеина всегда превышало содержание морфина, что сопровождалось низкими уровнями концентрации свободной) морфина и глюкуронидов морфина в плазме. Эти отклонения объясняются индивидуальными особенностями организма, а именно генетически обусловленным слабым метаболизмом в. отношении Q–деметилирования кодеина в морфин.
Содержание кодеина в волосах
После приема внутрь 120 мг кодеина–фосфата в волосах лица в интервале от 12 ч до 28 дней детектируется кодеин в среднем (n=2) 0,15 нг/мг волос. Ни один из метаболитов кодеина (морфин, норкодеин, норморфин, глюкурониды морфина и кодеина) не обнаружены. После внутримышечного введения двух доз кодеина 120 и 60 мг (с интервалом в неделю) содержание кодеина в волосах в интервале трех недель не выше 7 нг/мг. Соответствующие максимальные значения концентрации кодеина после первой и второй инъекций (нг/мл): в плазме 272,4 и 212,4; в слюне 307,6 и 183,9; в моче 325,1 и 1797,3. Из метаболитов найдены только следовые количества морфина в моче.Как указывалось ранее (см. раздел, посвященный героину), пот используется в качестве биологической матрицы для анализа многих наркотических веществ, в том числе опиатов. После приема внутрь 90 мг кодеина тремя участниками исследования количество выделившегося с потом кодеина определено в период времени от 1 до 6 дней, пик содержания приходится на 12–24 ч. Динамика выделения кодеина в пот (N=3): 1,8–2,9 (1 ч после дозы), 26,1–101,8 (48 ч), 24,9–127,2 (144 ч) нг/пластырь. Наблюдалось два концентрационных максимума: в пределах 12–24 и 72–98 ч. Морфин в поте не обнаружен.
Содержание кодеина в верхнем слое эпидермиса (ороговевшие частички кожи) после приема внутрь 60 и 120 мг соответственно составляет 0–4,8 и 0,3–5,6 нг/мг (N=5, хронические наркоманы).
Содержание кодеина и метаболитов в случае смерти в результате передозировки кодеина
В смертных случаях вследствие приема сверхдоз кодеина концентрации в биожидкостях (мкг/мл) или тканях (мкг/г) изменяются в следующих пределах (обобщенные данные по различным источникам)| Ткань | Вещество | Концентрация, мкг/мл |
|---|---|---|
| кровь | кодеин | 0,1–48 |
| морфин | 0,1–0,7 | |
| моча | кодеин | 3,2–370 |
| морфин | 0,1–70 | |
| желчь | кодеин | 0,22–89 |
| морфин | 0,1–119 | |
| почки | кодеин | 0,1–36,3 |
| морфин | 0,1–12.4 | |
| печень | кодеин | 0,1–45 |
| морфин | 0,1–64 |
Дифференцирование лекарственного потребления кодеина и нелегального приема опиатов
При употреблении кодеина в качестве лекарственного средства, как и при нелегальном приеме героина или морфина, в моче детектируется морфин, являющийся метаболитом как кодеина, так и диацетилморфина, или морфин вместе с кодеином, который может образоваться из ацетил кодеин а, присутствующего в героине–сырце. Кроме того, морфин и кодеин могут присутствовать в организме после употребления в пищу семян мака. Для дифференцирования лекарственного употребления чистого кодеина и нелегального приема опиатов предложены следующие подходы. ■ В случае приема терапевтических доз кодеина в интервале 0–20 ч в моче определяется метаболит норкодеин, при этом концентрация кодеина превышает концентрацию морфина. В интервале 20–40 ч концентрация морфина выше, чем концентрация кодеина, а норкодеин не детектируется (или в моче присутствует только основной метаболит морфин). ■ кодеин можно исключить как источник морфина, если выполняется два условия: • отношение концентраций общего кодеина и общего морфина в моче меньше чем 0,5 • концентрация морфина в моче превышает 200 нг/мл.Стабильность
Морфин свободный и Морфин конъюгированный стабильны в образцах мочи и крови в течение 10 дней хранения при температуре 4°С, 18–22°С и даже 37°С.Концентрация общего морфина в моче (n=42, от 116 до 12679 нг/ мл) и кодеина (n=48, от 118 до 18 380 нг/мл) при хранении в замороженном состоянии при –20°С была стабильна в течение года (Dugan S. at al. J.Anal. Toxic 1994, 18:391–396).
По данным, содержание общего морфина и кодеина в моче снижается на 10–40% в течение 11 мес при хранении охлажденными до 4–8 С или замороженными при –15 С, при этом концентрация свободных морфина и кодеина незначительно, но постоянно возрастает. В комнатных условиях (25–30 °С) за 11 мес концентрация общего морфина в моче может уменьшиться на 70–100%, а концентрация свободного морфина меняется непредсказуемо (в зависимости от pH, наличия бактерий, концентрации конъюгатов), значительно увеличиваясь в некоторых образцах в интервале 30–90 дней хранения.
При хранении образцов печени процесс гидролиза Морфин конъюгированный → Морфин свободный не идет при 4°С, и полностью проходит за, время 10–дневного хранения при 18–22°С и 37°С. Ответственным за гидролиз считают остаточную активность фермента печени (глюкуронидазы) или некоторых бактериальных энзимов. Спонтанный гидролиз, по–видимому, обеспечивает малый вклад в процесс, поскольку превращение не зависит от величины pH.
Морфин–глюкуронид стабилен в трупе при комнатной температуре в течение 8–9 ч после смерти (возможно в течение нескольких дней).
6–МАМ в моче стабилен при 4°С и в диапазоне 18–22°С в течение 10 дней. При 37°С его содержание слабо уменьшается в течение 5 дней хранения. В условиях глубокого охлаждения при –17°С количество 6–МАМ неизменно в течение более 2 лет.
Глава 2. Стимуляторы. Метамфетамин, амфетамин
Вещества, относящиеся к классу стимуляторов ЦНС, имеют свойства активизировать психическую деятельность, устранять физическую и психическую усталость. Во многих случаях это известные лекарственные средства, используемые в практике для лечения депрессивных состояний, нарколепсии (непреодолимого желания спать), для преодоления усталости, контролирования веса и снижения аппетита, а также лечения гиперкинезии у детей. Наиболее известные стимуляторы «черного рынка» наркотиков – кокаин, амфетамин, метамфетамин, эфедрон (последний особенно характерен для России периода до 1993–1994 г.).Стимуляторы – лекарственные средства
Среди лекарственных стимуляторов ЦНС (см. таблицу) наиболее распространены: ■ производные пурина – кофеин ■ производные фенилалкиламина – амфетамин, декстроамфетамин, метамфетамин (в РФ запрещен), бензфетамин, фентермин, пара–хлорфентермин, фенфлурамин, эфедрин, псевдоэфедрин, d–норпсевдоэфедрин, метилэфедрин, фепранон, метилфенидат, фенметразин, меклофеноксат, мезокарб и другие ■ препараты других химических групп – аминорекс, пемолин, бемитил, мазиндол, деанол и другие.Действие стимуляторов на организм
Общее действие стимуляторов на организм выражается в проявлении физической активности и бодрости, повышении умственной работоспособности, уменьшении аппетита, сонливости, усталости и улучшении настроения. Вместе с тем проявляются раздражительность, беспокойство, неадекватные реакции, бессонница. Характерным признаком является расширение зрачков. Характер, длительность И сила симптомов определяются эффективностью средства и дозой.Большие дозы стимуляторов могут вызывать повторяющееся скрежетание зубов, потерю веса, ложные тактильные ощущения, покалывания кожи лица.
Сверхдоза может привести к головокружению, тремору, спазмам кишечника, болям в груди, сильному сердцебиению, а также вызвать чувство тревоги, агрессивность, паническое состояние и паранойю.
Значительная передозировка ведет к сердечным приступам и остановке сердца.



 Прекращение приема стимуляторов после длительного применения может вызвать синдром отмены, что выражается в проявлении тревожного состояния и глубокой депрессии, длящейся несколько дней, апатии, усталости, долгих периодах сна. Появляются и нарастают признаки ухудшения восприятия и потери ориентации. В течение нескольких месяцев не проходит состояние тревоги и суицидальные тенденции.
Прекращение приема стимуляторов после длительного применения может вызвать синдром отмены, что выражается в проявлении тревожного состояния и глубокой депрессии, длящейся несколько дней, апатии, усталости, долгих периодах сна. Появляются и нарастают признаки ухудшения восприятия и потери ориентации. В течение нескольких месяцев не проходит состояние тревоги и суицидальные тенденции.
Особеннуюопасность стимуляторов представляет их свойство вызывать привыкание.
Действие стимуляторов на мозг
Стимуляторы действуют на нейротрансмиттеры – звенья, ответственные за передачу сигнала от клетки к клетке. Их влияние на деятельность мозга осуществляется по механизмам, различным для разных препаратов. В основе действия лежит стимулирование высвобождения катехоламинов (норадреналина, серотонина, дофамина) и торможение их обратного захвата.Амфетамин
Амфетамин (рацемат d,l–α–метилфенилэтиламин, торговые названия фенамин, бензедрин, а также d–изомер, торговые названия декстроамфетамин, декседрин) (далее, АМФ) – широко и давно применяется как в терапии, так и с немедицинскими целями. АМФ был синтезирован в 1887 г. как аналог эфедрина – растительного алкалоида, выделенного из травы Ephedra vulgaris (Ма Huang), и сразу получил широкое распространение как ингаляционное лекарственное средство для расширения бронхов, в частности, при лечении бронхиальной астмы. Психоактивные свойства АМФ стали известны лишь к 1927 г., и с тех пор началось его использование в качестве стимулятора ЦНС, для подавления аппетита, лечения гиперкинезии у детей и нарколепсии. Однако в результате почти тридцатилетнего наблюдения были сделаны выводы о формировании зависимости к АМФ, и, кроме того, стали очевидными тяжелые последствия длительного и регулярного использования препарата: увеличение вероятности мозговых кровоизлияний, повышение давления крови, аритмии, а также параноидальные психозы. Эта информация потребовала резкого ограничения и контроля лекарственного применения АМФ.Метамфетамин
Метамфетамин (рацемат d,l–N–α–диметил–фенэтиламин) (далее МАФ). Лекарственное средство, разрешенное в США, представляет собой d–изомер метамфетамина, торговые названия первитин, метедрин, дезоксин и др. Препарат используется с 1919 г. в качестве аналептика при алкогольной, барбитуровой или наркотической интоксикации (для преодоления состояния ступора), во время хирургических операций для поддержания кровяного давления при анестезии. В настоящее время основная сфера применения МАФ как лекарственного препарата в странах, где он зарегистрирован, – лечение детской гиперактивности с расстройством внимания. В РФ МАФ введен в Список 1 Постоянного Комитета по контролю наркотиков как вещество, оборот которого запрещен.Нелегальное использование стимуляторов
Из перечисленных лекарственных средств с немедицинскими целями наиболее широко используют фенилалкиламины, объединяемые в класс «амфетаминов», среди которых выделяются метамфетамин и амфетамин. Основное количество этих препаратов поступает в нелегальную продажу (на «черный рынок») из подпольных лабораторий, и некоторая часть из легального источника в виде фармацевтических препаратов. В 70–е годы на нелегальном рынке было отмечено появление фенметразина. Ранее в РФ интенсивно использовали эфедрон, кустарно изготовляемый из препаратов, содержащих эфедрин, известны также случаи употребления его аналога амфепрамона. Из стимуляторов других химических групп отмечалось распространение фенметразина (в 70–е годы в США), а также немедицинское использование метилфенидата и 4–метиламинорекса, которые запрещены к применению в РФ решением Постоянного комитета по контролю наркотиков РФ.АМФ в качестве стимулятора давно используется различными категориями людей в различных ситуациях, требующих длительной физической и умственной работоспособности: студентами в период экзаменов, водителями грузовиков в дальних поездках для ночного бодрствования, спортсменами и бизнесменами для снятия усталости и выработки устойчивости к длительным нагрузкам, женщинами для подавления аппетита и т.д. Известно, что во время Второй мировой войны солдаты обоих фронтов принимали АМФ как средство против усталости.
Однако одним из основных классов наркотиков амфетамины становятся, когда была обнаружена их способность вызывать мгновенный и мощный эйфорический эффект после внутривенного введения. С этого времени злоупотребление амфетаминами подобно эпидемии распространяется по странам Европы, Северной Америки и Азии. При этом в странах Европы запрещенное производство АМФ превышает МАФ, а в Северной Америке и Японии становится более популярен МАФ.
Подпольный синтез амфетаминов
Для распространения на «черном рынке» амфетамины синтезируют в подпольных лабораториях, хотя значительные количества могут поступать и из источников легального производства. Различные методики синтеза определяют наличие примесей в конечном продукте.Продукты, получаемые в подпольных лабораториях, как правило, представляют собой рацемические смеси: d,l–АМФ или d,l–МАФ. В качестве исходных продуктов могут быть применены фенил–2–пропанон (подлежит контролированию в РФ), эфедрин или псевдоэфедрин, фенилпропаноламин. Наличие этих соединений, а также красного фосфора, йодистоводородной кислоты, перманганата калия и других вспомогательных химических средств могут указывать на подпольное производство стимуляторов.
Есть указания на использование в качестве исходного продукта нелегального синтеза МАФ непосредственно растения эфедра, в котором содержатся различные алкалоиды, включая диастереомеры: 1–эфедрин и d–псевдоэфедрин, d–норпсевдоэфедрин и l–норэфедрин, l–метилэфедрин и d–метилпсевдоэфедрин. Наличие в препаратах нелегально изготовленного МАФ, кроме d–МАФ, еще и значительного количества d–АМФ и d–N,N–ди–мeтил–aмфeтaминa указывает на возможность осуществления такого способа.
Примеси, содержащиеся в нелегальных препаратах амфетамина и метамфетамина
Наличие определенных примесей позволяет отличить легально изготавливаемые лекарственные средства от синтезированных подпольно. Ниже перечислены вещества, которые могут указывать на нелегальное происхождение препарата и использованный метод синтеза. ■ фенил–2–пропанон ■ N–формил–амфетамин ■ N–метилформамид ■ N.N–диметил–амфетамин ■ N–формил–метамфетамин ■ N–ацетил–метамфетамин ■ 4–метил–5–фенил–пиримидин ■ N.N–ди (β–фенилизопропил) амин (ДФИА) ■ N–формил–ДФИА ■ N.N–ди (β–фенилизопропил) метиламин (ДФИМА) ■ N–формил–ДФИМА ■ высоко кипящие пиридины ■ дибензилкетон ■ α–бензилфенэтиламин ■ α–бензил–N–метил–фенэтиламин ■ пара–ОН–α–бензил–N–метил–фенэтиламин ■ N,α,α'–триметилдифенилэтиламин ■ продукт конденсации амфетамина и фенил–2–пропанона ■ бензилметилкетоксим ■ азиридины ■ эфедрин ■ хлорэфедрин ■ фенилуксусная кислота ■ неорганические соединения (цинк, йод, др.)Формы нелегальных амфетамина и метамфетамина
АМФ и МАФ получают в виде твердых солей: амфетамин сульфат или амфетамин фосфат и метамфетамин гидрохлорид, так как свободные основания представляют собой Жидкости с ограниченной устойчивостью. В нелегальную продажу они поступают в различной дозировке и формах: АМФ в основном в виде таблеток (иногда в виде капсул, сиропов и эликсиров); МАФ в виде порошка (в меньшей степени встречается таблетки, пилюли, капсулы), который вдыхают через нос или принимают внутрь (орально), стерильного раствора для внутривенный инъекций, а также кристаллической формы («ЛЁД») для курений (см. далее). Порошки продаются небольшими дозами в пластиковой или бумажной упаковке или в пластиковых пакетах.Как правило, чистота продукта, синтезированного в подпольной лаборатории, составляет 90–99%. Однако для продажи содержание основного компонента в порошках доводится до 40% и менее добавлением углеводов (глюкозы, лактозы, крахмала), сульфата магния, глутамата натрия, дешевых стимуляторов кофеина и эфедрина, а также прокаина, антипирина и др. В зависимости от условий производства: качества исходного сырья, условий синтеза, образования побочных продуктов, введенных добавок и проч., внешний вид амфетаминов может быть разным. Цвет АМФ варьирует от белого (подобно цвету лекарственного средства) до желтого, розового или коричневого. Часто препараты АМФ имеют характерный и неприятный запах, вследствие неполного удаления органических растворителей. МАФ продается в виде сыпучего или вязкого порошка от белого до темно–бежевого цвета, но возможны варианты коричневого или фиолетового цвета в зависимости от примесей.
«Лёд» – метамфетамин для курения ice, cristalls, batu
В 1985 г на нелегальном рынке наркотиков на Гавайях впервые было отмечено появление новой формы метамфетамина для курения, которая представляла собой кристаллический МАФ, по внешнему виду сходный с кусочками кристаллической соли и получивший поэтому «уличное» название «iсе» – «лед». Очень быстро «лёд» распространился по остальным странам мира, но вплоть до 1987 г. этот факт не был воспринят как всеобщая проблема, а рассматривался лишь как местное явление. Особая опасность курения «льда» проявилась тяжелыми последствиями, вплоть до смертельных исходов, из–за легкости получения слишком большой дозы и быстрого привыкания.Химически «лёд» – Это чистый 98–100% d–энантиомер гидрохлорида метамфетамина (см. далее).
В зависимости от условий синтеза получают «лёд» разного качества. О чистоте и эффективности средства судят по его окраске. Бесцветный и прозрачный «лёд» – это «водная, или гидратная» форма, он быстро сгорает, образуя молочно–белый остаток. Желтый «лед» – «жирная» форма, он медленнее сгорает, образуя коричневый или черный остаток. В отличие от марихуаны или крэка «лёд» не имеет запаха и не дает запаха при курении, и это одна из причин роста его популярности. Другой причиной популярности является то, что «лёд» дает долгий эффект, длящийся до 14 ч, в то время как, например, эффект крэка длится всего несколько минут.
Способы применения
Таблетки амфетамина принимают внутрь (орально). Порошкообразный амфетамин и метамфетамин вдыхают через нос или в виде раствора вводят внутривенно, «лёд» курят. При курении действие на мозг («hit», «удар») наступает гораздо быстрее, чем при вдыхании.Для амфетаминов характерна «циклическая» форма применения. После инъекции или «сеанса» курения ощущается короткий, но очень сильный эффект («приход»), всплеск ощущений, длящийся несколько минут. После спада эффекта, несмотря на то что концентрация стимулятора в крови все еще достаточно высока, вводится следующая доза, затем следующая и так далее («speed circle», «скоростной цикл», «скоростные бега»). Например, ритм цикла может быть таким: инъекции производятся каждые 50–60 мин в течение 2–3 дней, затем 6–10 ч длится период отказа от наркотика и угасания симптомов («отход») и длительный сон в течение 1–2 сут. Или принимается по 15 г/день в ритме по 1 г каждые 4 ч в течение 24 ч (и до 12 дней).
Такие режимы использования стимуляторов исчерпывают запасы энергии организма и приводит к истощению нервному, психическому и физическому .
«Лёд» курят через стеклянные трубки, которые по конструкции отличаются от трубок для крэка и марихуаны. Трубки для крэка состоят из 2 секций: в одной содержится препарат, в другой – охлаждающая жидкость. Эти секции разделены экраном. Трубки для «льда» имеют только одну секцию, в которой нагревается наркотик – метамфетамин. Обычно сверху имеется отверстие, ведущее в главную камеру, и вентиляционное отверстие. Одним из признаков, позволяющих идентифицировать потребителя «ЛЬДА», являются следы от ожогов на пальцах, получаемые наркоманами при закрывании этого отверстия в процессе курения.
Действие амфетаминов на организм
Симптомы действия амфетаминов на организм подобны симптомам, описанным для другого известного стимулятора: кокаина (крэка). Вначале амфетамины вызывают прилив сил и эйфорию, а также потерю аппетита, ускорение пульса, учащение дыхания и повышение температуры тела. Одним из внешних признаков употребления амфетаминов является расширение зрачков. Длительное применение ведет к быстрой потере веса, снижению иммунитета, разрушение легких, печени и почек, к ухудшению зрения, головокружению, потере координации и коллапсу. Прием больших доз («сверхдоза») сопровождается увеличением кровяного давления, появлением лихорадочного состояния и может привести к сердечным приступам и инфаркту.Характерными последствиями употребления метамфетамина являются проявления тяжелой депрессии, общий упадок сил, бессонница, беспокойство, напряжение и психозы. Токсические («амфетаминовые») психозы подобны параноидальной шизофрении, которая также может возникнуть в случае длительного употребления или «ударного» приема сверхдозы.
Психологическая зависимость развивается очень быстро: после 3–5 внутривенных инъекций и спустя 2–3 нед нерегулярного орального приема.
Физическая зависимость характеризуется признаками, составляющими синдром отмены.
Абстинентный синдром проявляется через 9 ч отмены препарата (до 4 сут) и может длиться 1–10 нед.
Толерантность к препарату развивается быстро. Разовая доза АМФ может доходить до 1 г, МАФ–до 0,8 г.
Физические и психические эффекты ЦНС – стимулирующее действие ■ эйфория, приподнятое настроение ■ повышенная работоспособность ■ активность, бодрость ■ гиперактивность ■ концентрация внимания ■ снижение утомляемости.
ЦНС – негативные эффекты ■ снижение аппетита ■ бессонница. ■ беспокойство ■ головокружение ■ внезапные изменения настроения, раздражительность ■ двигательная конвульсивность, судороги, тремор ■ спутанность сознания, делирий ■ паническое состояние ■ паранойя ■ психоз.
Сердечно–сосудистая система: ■ сердцебиение ■ аритмии ■ гипер– или гипотензия ■ сердечная недостаточность.
Дыхание ■ расширение бронхов.
ЖКТ ■ тошнота, рвота ■ диарея ■ анорексия ■ металлический привкус во рту ■ колики.
Почки ■ диурез.
Физиологические проявления употребления амфетаминов ■ расширение зрачков ■ головная боль ■ озноб ■ бледность или покраснение кожных покровов ■ потливость.
Эффекты передозировки и хронического употребления, симптомы зависимости ■ «амфетаминовый» психоз, параноидальный бред ■ галлюцинации тактильные, обонятельные, зрительные, слуховые ■ тахикардия ■ потеря аппетита, истощение ■ возбуждаемость, гиперактивность ■ непрекращающийся поток речи ■ дрожание рук ■ расширенные зрачки ■ сильное потение ■ сильное утомление, депрессия ■ мозговые кровоизлияния ■ судороги, кома.
Особенности хронического употребления амфетаминов ■ сохранение ясного сознания, памяти и ориентации ■ отсутствие формального расстройства мышления
Влияние употребления метамфетамина на поведение автоводителей.
Среди участников дорожно–транспортных происшествий, нередко заканчивающихся трагически, встречаются водители, находящиеся под воздействием стимуляторов, МАФ, в частности. Возникающие при этом ошибки управления автомобилем, приводящие к катастрофе: ■ превышение скорости ■ колебание траектории движения ■ выход за пределы трассы ■ высокая скорость столкновений.Поведение водителей, указывающее на воздействие МАФ, характеризуется чертами: ■ быстрая и путаная речь ■ учащенный пульс ■ возбуждение ■ расширенные зрачки ■ грубое и агрессивное поведение ■ паранойя.
Влияние эффекта отмены может также вызывать состояние, несовместимое с возможностью правильного управления автомобилем: ■ усталость ■ депрессия ■ сильная сонливость.
Оптические изомеры метамфетамина
АМФ и МАФ существуют в виде двух оптических изомеров: право– и левовращающих энантиомеров. Их фармакологические и фармакокинетические свойства различны.Правовращающий энантиомер метамфетамина: ■ (+)–метамфетамин ■ (D)–метамфетамин ■ (d)–метамфетамин ■ (S)–метамфетамин ■ dextro–метамфетамин
(+)–МАФ проявляет большую, чем (–)–энантиоме, активность как стимулятор ЦНС и как аноретик.
(+)–МАФ является лекарственным соединением в некоторых странах (США) и используется в медицинских целях для лечения нарколепсии и расстройства внимания.
(+)–МАФ в качестве нелегального средства синтезируется в подпольных лабораториях из (–)–эфедрина или (+)–псевдоэфедрина.
(+)–МАФ–гидрохлорид представляет собой*нелегальный препарат, известный на «черном рынке» под названием «ЛЕД».
Левовращающий энантиомер метамфетамина: ■ (–)–метамфетамин ■ (L)–метамфетамин ■ (1)–метамфетамин ■ (R)–метамфетамин ■ LEVO–метамфетамин
(–)–МАФ гораздо менее эффективен, чем (+)МАФ, в отношении свойств стимулятора ЦНС (по некоторым данным, примерно в 10 раз), и проявляет свойства симпатомиметика.
(–)–МАФ является основным активным компонентом (под названием (–)–дезоксиэфедрин) ингалятора викса (vicks nasal inhaler, США), легально используемого с медицинскими целями.
Рацемическая смесь метамфетамина
Смесь (+)– и (–)–энантиомеров МАФ в отношении 1:1 образуется при нелегальном синтезе МАФ из фенил–2–пропанона. (Нельзя исключить редкие случаи появления фармацевтического рацемата МАФ, если его синтезируют из рацемата исходного соединения.)Оптические изомеры метамфетамина
| Правый энантиомер | Левый энантиомер | Рацемат | |
|---|---|---|---|
| Обозначение | (+)–МАФ D–МАФ d–МАФ S–МАФ S(+)–MAФ | (–)–МАФ L–МАФ 1– МАФ R–МАФ R(–)–МАФ | (+,–)–МАФ (d,l)–МАФ |
| Легальное применение | Стимулятор ЦНС и аноретик. Применяют при лечении нарколепсии, дефицита внимания | Активность стимулятора ЦНС гораздо ниже, чем у (+)–МАФ. Применяют в ингаляторе Викса (США) для сужения периферических сосудов. | Возможно появление фармпрепаратов МАФ при синтезе из рацематов прекурсоров |
| Нелегальное применение | Синтезируется из (–)–эфедрина и (+)–псевдоэфедрина. Гидрохлорид применяют для курения («ЛЕД»), | Синтезируется из фенил–2–пропанола |
Оптические изомеры амфетамина
(+)–АМФ – в 4–10 раз более эффективен как стимулятор ЦНС. (–)–АМФ – проявляет более сильное действие на сердечно–сосудистую систему. Лекарственное средство представляет собой либо (+)–АМФ, либо рацемат АМФ.Фармакокинетические свойства
Способы введения. Таблетки, капсулы и пилюли принимают внутрь (орально), растворы используют для внутривенных инъекций, порошки вдыхают и втягивают через нос (интраназально), «ЛЁД» ((+)–МАФ–гидрохлорид) курят.АМФ в виде солей – сульфатов или фосфатов – обычно принимают орально или интраназально. Порошок МАФ–гидрохлорида используют для приготовления инъекционного раствора, реже встречаются таблетированные формы МАФ–гидрохлорида.
Дозы. Обычная оральная или интраназальная доза АМФ – 5–15 мг, для случайного потребления доза 30 мг АМФ может быть токсичной. Доза АМФ для внутривенного введения – 20–40 мг. Терапевтическая доза МАФ – 5–20 мг. Для толерантных потребителей дозы значительно выше: 100–2 000 мг в день АМФ, до 800 мг МАФ.
Начало действия. Через 30 сек при внутривенном введении, через 5–15 мин при интраназальном введении.
Длительность действия. АМФ – от 4 до 12 ч (по другим данным 2–3 ч).
Всасывание
В ЖКТ – полное и быстрое всасывание. Концентрация в плазме после приема орально дозы АМФ 2,5–15 мг достигает максимального значения 30–170 нг/мл через 2 ч и в последующие 48 ч уменьшается экспоненциально. После внутривенного введения разовой дозы 160 мг концентрация АМФ в плазме через 1 ч – 590 нг/мл, а через 24 ч – 60. Наиболее вероятный диапазон концентрации МАФ в крови 100–300 нг/мл, концентрации более 600 нг/мл встречаются сравнительно редко. При курении МАФ максимальная концентрация в крови устанавливается через 7 мин. после начала курения.Период полувыведения T½ из плазмы («полужизнь» в плазме) – 8–12 ч. В зависимости от диеты эта величина меняется: от 8 ч (7–14 ч) при кислой и до 22 ч (18–34 ч) при щелочной диете.
Табличные значения концентраций АМФ и МАФ в крови : ■ терапевтические концентрации АМФ: 50–150 нг/мл, МАФ: 20–60 нг/мл ■ токсические концентрации АМФ: 200–1000 нг/мл, МАФ: 200–1000 нг/мл ■ летальные концентрации АМФ: выше 1 мкг/мл, МАФ: 10–40 мкг/мл.
При циклическом введении амфетаминов (см. выше) концентрации могут значительно превышать приведенные табличные величины. Грубое и иррациональное поведение ассоциируется с концентрацией МАФ в крови 150–560 нг/мл, автоводители, привлекшие к себе внимание отклонениями в поведении, содержат в крови в среднем (N=29) 490 нг/мл. Для участников катастроф на трассах эта величина увеличивается до 2580 нг/мл.
Распределение
Амфетамины распределяются по всему организму. Хотя при физиологических значениях pH соединения ионизованы (рКа=9,77 для АМФ и 10,1 для МАФ), они легко преодолевают барьер кровь–мозг и после внутривенного введения достигают головного мозга за несколько секунд. При курении МАФ сначала конденсируется в легких, откуда проникает в кровяное русло. Рис. 1. Схема метаболизма амфетамина.
Рис. 1. Схема метаболизма амфетамина.
 Рис. 2. Схема метаболизма метамфетамина.
Рис. 2. Схема метаболизма метамфетамина.
Метаболизм
Основной процесс биотрансформации АМФ в организме человека – дезаминирование, в меньшей степени идут процессы гидроксилирования ароматического цикла, бета–гидроксилирование и N–окисление. Основной процесс биотрансформации МАФ – N–деметилирование. Гидроксилированные метаболиты далее конъюгируются с глюкуроновой и серной кислотами (рис. 1 и 2).Метаболиты амфетамина ■ фенилацетон ■ бензойная кислота ■ гиппуровая кислота ■ пара–гидрокси–амфетамин (в том числе конъюгаты) ■ норэфедрин ■ пара–гидрокси–норэфедрин (в том числе конъюгаты) ■ гидроксиламин (неустойчив, трансформируется в оксим и далее в фенилацетон). Пара–гидрокси–амфетамин и пара–гидроксинорэфедрин сохраняют биологическую активность.
Метаболиты метамфетамина ■ амфетамин ■ пара–гидрокси–метамфетамин (в том числе конъюгаты) ■ норэфедрин ■ пара–гидрокси–норэфедрин (в том числе конъюгаты) ■ пара–гидрокси–амфетамин ■ фенилацетон ■ бензойная кислота ■ гиппуровая кислота.
Пара–гидрокси–метамфетамин, пара–гидрокси–амфетамин и пара–гидрокси–норэфедрин – биологически активные метаболиты.
Стереоселективность метаболизма
Метаболизм различных энантиомеров АМФ и МАФ имеет значительные отличия. В общем случае (+)–изомеры подвергаются биотрансформации легче. Дезаминирование предпочтительнее протекает у (+)–изомера АМФ. N–деметилирование МАФ также легче осуществляется для (+)–МАФ, чем для (–)–МАФ. Кроме того, при N–деметилировании из (+)– и (–)–МАФ образуется соответственно (+)– и (–)–АМФ. В случае последовательного протекания двух процессов: пара–гидроксилирования ароматического цикла и N–деметилирования сначала осуществляется N–деметилирование.Выведение
АМФ и МАФ появляются в моче спустя 20 мин после приема оральной дозы АМФ экскретируется как неизмененное соединение в количестве 20–30% дозы и как сумма деаминированных (бензойная и гиппуровая кислоты) и гидроксилированных метаболитов (частично в виде конъюгатов) в количестве до 25% дозы. Скорость экскреции и доля неизмененного АМФ сильно зависит от рН мочи: T½ выведения меняется от 7 до 34 ч. При условиях метаболизма, продуцирующих «щелочную» мочу, например, при потреблении гидрокарбоната натрия (рН мочи превышает 6,6), за 24 ч выводится около 40–45% дозы, при этом 2% дозы составляют неизмененный АМФ и 6–13% дозы приходится на гидроксилированные метаболиты. В «кислой» моче (потребление хлорида аммония или аскорбиновой кислоты, рН мочи менее 6,6) за 24 ч может выводиться до 78% дозы, ц том числе 67–73% дозы как неизмененный АМФ и 3–8% как сумма гидроксилированных метаболитов. Выведение препаратов сильно ускоряется при потреблении 2,75 ммоль/кг хлорида аммония или 8 мг/кг аскорбиновой кислоты (рН мочи менее 5).При метаболитическом подщелачивании мочи воздействия АМФ и МАФ на организм более длительны, что связывается с реабсорбцией и длительным удерживание соединений в организме. Для лиц с «амфетаминовыми» психозами установлена корреляция между интенсивностью психоза и концентрацией основных полярных метаболитов в моче, в то время как корреляция с концентрацией АМФ в плазме отсутствует.
При употреблении (+)–АМФ выведение характеризуется следующими величинами (% дозы): ■ АМФ – 30 ■ п–ОН–АМФ, свободный и конъюгированный – 3 ■ п–ОН–норэфедрин, свободный и конъюгированный – 5 ■ фенилацетон – 3 ■ бензойная кислота, свободная и конъюгированная – 20.
После введения МАФ 90% дозы выводится с мочой в течение 4 дней, за 24 ч при нормальных условиях выводится (% дозы): ■ МАФ – 22–44 ■ АМФ – 4–7 (до 20) ■ п–ОН–МАФ – 4–15 ■ п–ОН–АМФ – 1 64 ■ п–ОН–норэфедрин – 1–2 ■ норэфедрин – 2 ■ гиппуровая кислота – 5 ■ фенилацетон – 1.
В условиях метаболизма, продуцирующего мочу с кислыми значениями рН, за 24 ч выводится около 76% дозы в виде неизмененного МАФ и 7% дозы в виде метаболита АМФ. В метаболитически щелочной моче МАФ составляет лишь 2% дозы, а АМФ – менее 0,1 % дозы.
После орального приема в контролированных условиях дозы (+)–МАФ 30 мг/70 кг веса десятью наркоманами с длительным опытом использования МАФ содержание в пробах мочи, собранной в интервале до 12 ч, составило: МАФ – 20% и АМФ – 2% дозы. Максимальная концентрация МАФ 3000–3500 нг/мл приходится на время 4–6 ч. Длительность детектирования МАФ в моче – до 7 дней. В этих пробах концентрация метаболита АМФ в интервале 4–6 ч составляла 100–200 нг/мл. При разовом приеме рацемического МАФ ва период 0–24 ч концентрация неизмененного МАФ в моче составила 0,5–4 мкг/мл и через 80 ч после приема уменьшалась до 200 нг/мл. Метаболит АМФ появлялся в моче в интервале 7–24 ч и определялся до 60 ч при содержании 45,5–250 нг/мл. При метаболическом подщелачивании в результате приема 10 мг МАФ–гидрохлорида вместе с 7,2 г соды в период 24–48 ч в моче определено (нг/мл): МАФ – 3605, АМФ – 415, п–ОН–МАФ – 400, п–ОН–АМФ не обнаружен. При курении 22 мг S(+)–МАФ HCl содержание МАФ в моче за несколько первых часов экскреции 6–7 мкг/мл.
Вследствие стереоселективности метаболизма в случае приема рацемического (+,–)–МАФ преобладает выведение (–)–энантиомера МАФ и метаболита (+)–энантиомера АМФ. Отношение (–)/(+) изомеров для 4 проб мочи в среднем составило 63:97 для МАФ и 28:72 для метаболита АМФ. Контролирование использование ингалятора Викса, основным компонентом которого является (–)–МАФ, при условиях: повторные ингаляции в течение 6 ч через каждые 20 мин тремя добровольцами, – показали преобладающее наличие в моче в интервале 1–24 ч (–)–МАФ – с максимальным содержанием 1,5–6 мкг/мл в, интервале 7–24 ч (рН мочи 6–6,4) или 3 ч (рН мочи 5,0). Энантиомер (+)–МАФ либо не детектируется, либо определяется в незначительном количестве и отношение (+)/(–) для МАФ в среднем составляет 0,1 (от 0,00 до 0.12). При использовании рацемического МАФ в первые 16 ч с мочой экскретируется равное количество энантиомеров и для этого периода отношение (+)/(–)–МАФ приближается к 1. Пб данным разных авторов, отношение (+)/(–)–изомеров МАФ в моче в интервале до 24 ч изменяется от 0,6 до 0,97. Таким образом, появляйся возможность дифференцировать легальное терапевтическое использование лекарственного (–)–МАФ и нелегальное потребление рацемического МАФ.
При хроническом потреблении концентрации неизмененного МАФ в моче могут достигать высоких значений. Например, по данным одной из лабораторий, при рутинном анализе наркотических средств в биожидкостях интервал содержания МАФ определен как 0,6–60 мкг/мл. При анализе мочи наркоманов с симптомами метамфетаминового отравления, включая агрессивное и грубое поведение (n=7), концентрация в моче (мкг/мл) МАФ: 24–333, основного метаболита АМФ: 1–90. В табл. 1 приведены концентрации МАФ и его метаболитов: АМФ, конъюгированного и свободного пара–ОН–МАФ и норэфедрина, – в моче наркоманов после употребления неизвестных доз МАФ.
Таблица 1. Концентрации МАФ и метаболитов в моче наркоманов, мкг/ мл
| Субъект | МАФ | АМФ | п–ОН–МАФ конъюгат | п–ОН–МАФ свободный | Норэфедрин |
|---|---|---|---|---|---|
| 1 | 149 | 6,88 | 2,47 | 0,44 | 0,60 |
| 2 | 11,62 | 0,58 | 0,74 | 0,18 | 0,048 |
| 3 | 37,2 | 2,43 | 0,63 | 0,85 | 0,196 |
| 4 | 0,19 | 0,175 | 0,026 | 0,05 | 0,023 |
| 5 | 123,6 | 13,09 | 6,27 | 3,46 | 1,81 |
| 6 | не дет. | не дет. | не дет. | не дет. | не дет. |
| 7 | 5,51 | 1,28 | 0,31 | 0,26 | 0,127 |
Содержание амфетаминов в волосах, ногтях, слюне и поте
МАФ и АМФ присутствует в так называемых «нетрадиционных» объектах исследования: волосах, ногтях, слюне, поте людей, употреблявших амфетамины. МАФ можно обнаружить спустя несколько дней после прекращения регулярного употребления препаратов: в волосах – спустя 18 дней, в ногтях – 45 дней, слюне – 2 дня (данные для 25 наркоманов). Данные о количественном содержании приведены в табл. 2–4.Для определения содержания наркотических веществ в поте его собирают с помощью пластырей, содержащих сорбирующий материал (см. раздел «Опиаты»). После ингаляции МАФ (ингалятор викса, (–)–дезоксиэфедрин) 160 мг/день, при общей дозе за 7 дней 1,12 г в поте за 4–10–дневный период определено от 6,7 до 19 нг/мл АМФ (N=2).
Таблица 2. Содержание метамфетамина и амфетамина в волосах.
| Наркоман | МАФ, нг/мг | Метаболит АМФ, нг/мг |
|---|---|---|
| А | 27,4 | 2,2 |
| В | 7,1 | 0,7 |
| С | 2,1 | не детектируется |
| д | 17,7 | 2,0 |
Таблица 3. Распределение метамфетамина по длине волос наркомана. Секции по 20 мм, начиная от корня.
| № секции | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| МАФ, нг/мг | 28.5 | 20,8 | 7,4 | 0,8 | 0.7 | 0,8 |
Таблица 4. Содержание метамфетамина и амфетамина в волосах, ногтях, поте и слюне (25 наркоманов – потребителей метамфетамина)
| № | Волосы, нг/мг | Ногти, нг/мг | Пот, нг | Слюна, мкг | ||||
|---|---|---|---|---|---|---|---|---|
| МАФ | АМФ | МАФ | АМФ | МАФ | АМФ | МАФ | АМФ | |
| 1 | 3,8 | 0 | ||||||
| 2 | 13,9 | 0,9 | ||||||
| 3 | 2,5 | 0 | 59,0 | 7,0 | ||||
| 4 | 7.5 | 0.7 | 23,6 | 0.3 | 85,5 | 9,3 | 0 | 0 |
| 5 | 0 | 0 | 0 | 0 | 0 | 0 | ||
| 6 | 1,8 | 0 | 0 | 0 | 0 | 0 | ||
| 7 | 9,8 | 0,5 | 7,3 | 0 | 164 | 13 | 0 | 0 |
| 9 | 0 | 0 | 20 | 3,4 | 0 | 0 | ||
| 11 | 0,6 | 0 | 0,4 | 0 | 0 | 0 | 0 | 0 |
| 14 | 5,8 | 0 | 25,2 | 0 | 0 | 0 | ||
| 16 | 9,0 | 0 | 642 | 23,2 | 2,1 | 0 | ||
| 17 | 15,8 | 0 | 16,9 | 0 | 0 | 0 | ||
| 20 | 9,8 | 0 | 0,5 | 0 | ||||
| 24 | 17,6 | 1,2 | ||||||
| 25 | 0,3 | 0 | ||||||
Содержание метамфетамина и амфетамина в организме новорожденных
Если МАФ употребляют беременные или кормящие матери, то он проникает в организм плода или ребенка и оказывает на него губительное воздействие. В табл. 5 приведены данные о содержании МАФ и АМФ в органах новорожденных близнецов, умерших вскоре после рождения, чья мать за 5 ч до родов ввела внутривенно дозу МАФ.Меконий – первородный кал новорожденного (см. раздел «Опиаты») является объектом, имеющим определенные преимущества перед мочой или плазмой в отношении анализа наркотических средств и метаболитов. Присутствие МАФ и АМФ в меконии указывает на употребление амфетаминов матерями в период вынашивания или кормления.
Таблица 5. Концентрация метамфетамина и амфетамина в тканях организма плода и матери, мкг/мл или мг/кг
| Организм | Биоматериал | МАФ | АМФ |
|---|---|---|---|
| 1 близнец | почки | 6,34 | 0,97 |
| 1 близнец | печень | 9,20 | 0,18 |
| 1 близнец | мозг | 5,31 | 0,76 |
| 2 близнец | кровь | 6,3 | 0,28 |
| 2 близнец | почки | 7,38 | 0,95 |
| 2 близнец | печень | 11,0 | 1,43 |
| 2 близнец | мозг | 4,53 | 0,61 |
| мать | плацента | 8,66 | 1,18 |
Содержание амфетаминов в организме людей, погибших в результате передозировки
Содержание амфетаминов в крови и печени в фатальных случаях, связанных с передозировкой при употреблении, составляет в случае приеме амфетамина (n=3, неизвестная доза внутривенно): 0,5–7,0 мкг/мл (среднее значение 4,5 мкг/мл) в крови и 12–45 мкг/г (среднее 31 мкг/г) в печени. При передозировке метамфетамином содержание неизмененного МАФ в крови составило (N=157) 25–2030 (среднее 308) нг/мл, АМФ 10–100 (среднее 30) нг/мл, но может доходить до 3050 нг/мл МАФ и 320 нг/мл АМФ и выше. Содержание в печени (мкг/г): МАФ 0,11–11,6; АМФ 0–1,06 (N=11).Таблица 6. Метамфетамин и амфетамин в органах жертв передозировки, мкг/мл, мкг/г.
| Орган, биожидкость | Случай 1, N=I | Случай 2. N=I | ||
|---|---|---|---|---|
| МАФ | АМФ | МАФ | АМФ | |
| кровь | 0.68 | 0.03 | 5.6 | 0,35 |
| желчь | 21,7 | 0.58 | – | . |
| моча | 32,0 | 1,6 | 320 | 10 |
| желудок | 2,9 | 0,13 | 11.6 мг | 0.2 мг |
| печень | 2,2 | 0,1 | 175 | 13 |
| мозг | 2,7 | 0.25 | 102 | 0,8 |
В некоторых случаях, несмотря на высокие концентрации МАФ в крови и моче, метаболит АМФ не обнаруживается. Ниже приведено описание четырех таких случаев. ■ Смерть от употребления неизвестной дозы МАФ. Концентрация МАФ в крови 779 нг/мл. Из этого количества: d–МАФ 753, 1–МАФ 23 нг/мл. d–АМФ – не обнаружен. ■ Смерть от употребления неизвестной дозы МАФ. Концентрация МАФ в крови 175 нг/мл, в моче 1154 нг/мл. Из этого количества d–МАФ 911,1–МАФ 243 нг/мл. d–ДМФ – не обнаружен. ■ Убийство, связанное с употреблением МАФ. Концентрация МАФ в крови 20 нг/мл, в моче 2080 нг/мл. Из этого количества d–МАФ 2282,1–МАФ 616 нг/мл. d–АМФ – не обнаружен. ■ Живой наркоман. Концентрация МАФ в крови 104 нг/мл, в моче 5288 нг/мл. d–АМФ – не обнаружен в крови, а в моче 169 нг/мл.
Во всех случаях подтверждено употребление d–энантиомера МАФ, что выдает его нелегальное происхождение. Содержание метаболита d–АМФ обычно составляет 4–7% дозы, но, как показано выше, он может отсутствовать и в крови и в моче даже в присутствии больших количеств d–МАФ.
В табл. 7 приведено распределение МАФ в тканях организма человека, погибшего от передозировки инъекции героина и метамфетамина. Содержание АМФ в моче составило 0,1 % от уровня МАФ, в других образцах он детектирован в следовых количествах.
По данным, концентрация МАФ и АМФ в центральной системе крови выше, чем в периферической.
В тканях мозга и сердца (+)–АМФ содержится в большем количестве, чем его (–)–изомер. (+)–АМФ метаболизирует в мозге до пара–гидрокси–норэфедрина, который, возможно, несет ответственность за развитие психозов, выполняя функции нейротрансмиттера.
Таблица 7. Распределение МАФ в органах трупа при передозировке, нг/мл, нг/г.
| Орган | МАФ |
|---|---|
| Кровь левого желудочка сердца | 875 |
| Кровь правого желудочка сердца | 551 |
| Кровь правой бедренной вены | 1730 |
| Перикард | 750 |
| Спинномозговая жидкость | 610 |
| Моча | 9550 |
| Головной мозг | 2060 |
| Сердечная мышца | 2970 |
| Легкие, правая средняя доля | 1730 |
| Печень, внутренняя ткань правой доли | 8280 |
| Селезенка | 5280 |
| Правая почка | 6880 |
| Мышца правого бедра | 1450 |
| Содержимое желудка | 9760 |
Таблица 8. Содержание метамфетамина и амфетамина в организме наркокурьера, проглотившего упаковку «крэнка» (метамфетамин), мкг/мл, мкг/г.
| Орган, биожидкость | МАФ | АМФ |
|---|---|---|
| Кровь периферической системы | 53,7 | 0,43 |
| Кровь центральной системы | 65,7 | 0,70 |
| Моча | 375,6 | 5,06 |
| Желчь | 353,7 | 3,29 |
| Желудок | 514,3 | 3,46 |
| Печень | 90,9 | 0,88 |
| Стекловидное тело | 45,8 | 0,64 |
Амфетамин и метамфетамин как метаболиты лекарственных средств
Некоторые лекарственные соединения (см. рис. 3) в организме человека метаболизируют с образованием АМФ и/или МАФ (или замещенных), которые могут быть обнаружены в моче при анализе. Так, концентрация АМФ в моче после приема 30 мг аноретика «clobenzorex» в интервале 1–7 ч после приема составила 51–1365 нг/мл. Кроме АМФ определены п–ОН–АМФ и нор эфедрин.После приема терапевтической дозы «fenproporex» концентрация АМФ в моче 1200–2100 нг/мл в интервале 6–20 ч и около 5 нг/мл спустя 119 ч с момента приема.
После употребления в контролируемых условиях тремя добровольцами двух таблеток анальгетика, в состав которого входят 25 мг «famprafazone», 250 мг ацетаминофена, 75 мг изопропилантипирина и 30 мг кофеина, в моче за 1–72 часовой период определены метаболиты «famprafazone»: МАФ и АМФ в концентрации 0,2–5,0 и 0,2–0,7 мкг/мл, соответственно. Максимальные концентрации метаболитов в моче приходятся на период 9–12 ч, но даже спустя 24 ч они все еще достаточно высоки: 0,4–1,5 мкг/мл (МАФ) и 0,2–0,7 мкг/мл (АМФ).
После приема внутрь 50 мг бензфетамина (дидрекс), входящего в состав многих «диетических пилюль», метаболиты выводятся с мочой в концентрациях: МАФ 1,8–6,5% и АМФ 0,7–2,8% дозы (N=10). Содержание в моче сильно зависит от индивидуальных особенностей метаболизма, и при рН 5–6,35 в течение 3–45 ч составило: МАФ 139–965 нг/мл, АМФ 169–3776 нг/мл.
В результате приема неизвестной дозы лекарственного средства селегилин (Selegiline=Deprenyl=Eldepryl 1 таблетка весом 70 мг содержит 2,5 мг действующего начала: (–)–пропинил–метамфетамина) в моче определены только 1–изомеры МАФ 829–4690 и АМФ 342–1895 нг/мл (N=4). Соотношение АМФ/МАФ изменялось от 0,37 до 0,42, что существенно отличается от величин, полученных при использовании МАФ: например, при ингаляции (ингалятор викса) оно равно примерно 0,1.
Дифференцирование легального применения некоторых лекарственных средств, дающих АМФ и МАФ при метаболизме, от нелегального употребления МАФ можно провести по данным анализа (+) и (–)–изомеров МАФ в моче. Многие лекарственные средства, являясь «чистыми» (+) или (–)–энантиомерами, соответственно образуют «чистые» (+) или (–)–энантиомеры метаболитов. Нелегальные формы МАФ являются либо d–МАФ, либо рацематом МАФ, что позволяет отличить их от l–изомера МАФ метаболита l–лекарственных средств. Однако некоторые лекарственныесредства, например, furfenorex, дают в качестве метаболитов смесь d– и l–МАФ, что затрудняет дифференцирование с нелегальным употреблением МАФ по данным анализа мочи.
 Рис. 3. Лекарственные средства, метаболизирующие в организме человека до амфетамина (левая колонка) и метамфетамина (правая колонка).
Рис. 3. Лекарственные средства, метаболизирующие в организме человека до амфетамина (левая колонка) и метамфетамина (правая колонка).
Длительность определения амфетаминов в моче.
Неизмененный АМФ может быть определен в моче вплоть До 29 ч после орального приема разовой дозы 5 мг. Неизмененный МАФ детектируется в моче вплоть до 23 ч после разовой оральной дозы. Положительный анализ мочи на амфетамины в общем случае указывает на использование АМФ или МАФ в предыдущие 24–48 ч. При хроническом употреблении больших доз амфетаминов толерантными субъектами длительность их детектирования в моче может быть существенно более длительной: до 7 дней после последнего приема.Стабильность метамфетамина в моче.
Концентрация АМФ и МАФ в моче практически не меняется при сохранении проб замороженными при –20°С.в течение 12 мес. Образцы мочи (N=20) с начальной концентрацией МАФ в интервале 262–3102 (среднее 1589) нг/мл в конце срока хранения содержали 191–3565 (среднее 1554) нг/мл МАФ. Образцы (N=32)с начальной концентрацией АМФ 179–9179 (среднее 1554) нг/мл порке 12–месячного срока хранения содержав» 152–9784 (среднее 1532) нг/мл АМФ.Глава 3. Кокаин
Кокаин – это алкалоид, выделяемый из содержащих 1% кокаина листьев кустарника КОКИ (Erythroxylon coca), культивируемого в высокогорных районах Перу, Боливии, Эквадора и многих других стран, число которых неуклонно растет. Синтетический кокаин может быть получен из экгонина. Кокаин – сильнодействующий стимулятор ЦНС, сходный с амфетамином по действию изменять сознание, снимать усталость и стимулировать работу различных систем организма.Еще в древней цивилизации Инков жрецы использовали листья коки для вхождения в транс при религиозных действах, а позднее среди жителей высокогорных районов был распространен обычай жевать листья коки для улучшения самочувствия, снятия усталости и уменьшения чувства голода.
Впервые выделенный в 1860 г. кокаин получил широкое распространение в США к концу 1800–х годов, когда он прочно вошел в категорию доступных и безвредных стимуляторов. Кокаин применяли в медицине для местного обезболивания, он входил в состав многих лекарственных средств, напитков и тоников, включая Кока–колу. Однако в течение нескольких лет неуклонного распространения кокаина накапливались факты его негативного влияния на здоровье людей, и становилось все более очевидным его разрушительное действие: вызываемые кокаином психозы, смертные случаи от передозировок и развитие сильной наркотической зависимости. Начиная с 1914 г., Конгресс США принял серию указов, ограничивающих распространение кокаина и фактически ставящих его вне закона.
В период с 1930 по 1960 г. кокаин не привлекал к себе особенного общественного внимания. К началу 70–х годов в США он был трудно доступен, и использование ограничивалось в основном шоу–бизнесом, где распространился обычай нюхать кокаин в небольших дозах и где поэтому редко сталкивались с тяжелыми последствиями его употребления. Многие эксперты даже стали сомневаться в способности кокаина вызывать наркотическое пристрастие и требовали его легализации. В результате этих ошибочных представлений о кокаине как веществе, не Приносящем особый вред людям и обществу в целом, общественное мнение не противилось распространению нового средства. На этом фоне кокаин быстро вошел во все социальные группы общества, независимо от экономического и социального статуса.
Распространение кокаина приняло угрожающий характер и стало подлинным бедствием после появления в нелегальной коммерческой торговле («на улицах») в 1986–1990 гг. «Крэка»–кокаина для курения в форме основания. Число смертей от передозировки кокаина, а также связанных с его длительным употреблением, в том числе женщинами в период беременности и кормления, сильно возросло, и кокаин вместе с героином и амфетаминами рассматривается как особенно опасный наркотик.
В настоящее время кокаин включен в Список № 2 Конвенции ООН по наркотикам и в соответствующий Список № 2 Постоянного Комитета по контролю за наркотиками РФ, что означает возможность легального использования кокаина при определенных медицинских показаниях при международном и внутреннем контроле за производством, употреблением и распространением.
Формы кокаина в «уличной» торговле ■ кокаин–гидрохлорид ■ кокаин–основание – «крэк» ■ смесь кокаина и героина – «спидболл».
«Уличные» формы кокаина часто содержат примеси других веществ, например, различные сахара, а также более дешевые наркотические и лекарственные средства: стимуляторы (амфетамин, кофеин), местные анестетики (лидокаин, прокаин) и т.д. Содержание кокаина может быть менее 10%. Кокаин, произведенный из растения Коки, в отличие от синтетического кокаина, содержит примеси различных минорных алкалоидов (см. далее).
Листья коки (Erythroxylon coca, Е. Novgranatense). В некоторых регионах земного шара еще сохраняется обычай жевать листья коки. Из–за видовых различий кустарника Erythroxylon листья различаются по внешнему виду и размерам. Все они имеют более темную верхнюю сторону листа и более светлую нижнюю, часто серо–зеленого цвета. Характерным признаком листьев коки является наличие с нижней стороны листа двух линий, параллельных главному сосуду.
Помимо 0,5–1,5% кокаина, в листьях коки содержатся минорные алкалоиды: около 1% норкокаина, цис– и транс–циниамоилкокаин, тропакокаин, псевдококаин, гидроксикокаин, метиловый эфир экгонина и его 2'–пирролоил–, 2'–никотиноил–, 2'– и 3'–фураноил–производные, 3',4',5'–триметокси–замещенные кокаина, цис– и транс–циннамоилкоканна и тропакокаина и др.
Паста коки, basuco, bazooka. Паста Коки – дешевый продукт, получаемый на ранних стадиях производства кокаина при экстракции из листьев коки. Это беловатый, кремовый или бежевый, обычно сырой порошок, содержащий агрегаты, легко разрушающиеся при легком надавливании, и имеющий характерный запах. В состав пасты, помимо кокаина и других алкалоидов коки, входят вещества, добавляемые при экстракции, например, карбонат марганца. Содержание кокаина от 40 до 90%.
Кокаин. Coke. Snow. Хотя вариабельность форм нелегального кокаина менее широка по сравнению с героином, тем не менее трудно встретить две полностью идентичные нелегальные пробы кокаина. В большинстве случаев это белый или тонкий беловатый порошок, иногда влажный, имеющий характерный запах.
Редко встречаются образцы Кокаина, в состав которых, помимо порошка, входят большие, иногда бесцветные, довольно твердые кристаллы («rock cocaine»).
Кокаин, поступающий из производящей страны в международный оборот наркотиков, обычно представляет собой продукт высокого качества с содержанием кокаина–гидрохлорида 80–90%, и редко содержит примеси и добавки. Для внутренней нелегальной продажи кокаин разбавляется до содержания около 30% (12–75%) добавлением различных препаратов: пирацетама, кофеина, неконтролируемых синтетических местных анестетиков (лидокаин, прокаин, бензокаин), углеводов (маннитол, лактоза, глюкоза, крахмал). Внешний вид нелегальных образцов Кокаина при этом практически не меняется, поскольку добавляемые вещества представляют собой тонкие, сухие, белые порошки, похожие на Кокаин, Кроме указанных, в качестве добавок–разбавителей используют крахмал, борную кислоту, соду и др.
Крэк. crack. rock. До конца 70–x годов в нелегальной торговле в основном присутствовал кокаин в солевой форме (гидрохлорид, солянокислая соль кокаина, кокаин, НСl), применявшийся для вдыхания носом и инъекций и гораздо реже – для курения и орально. С 1979 г. преобладающее место принадлежит кокаин–основанию, продукту, называемому на сленге крэком из–за характерного потрескивания, издаваемого кристаллами при нагревании. Крэк почти исключительно используется для курения. Его получают из гидрохлорида при щелочной экстракции органическими растворителями (эфиром). Кокаин–основание выделяется в этой процедуре (называемой фрибэйзингом, от английского freebasing) в виде остатка от белого до коричневого цвета. После высушивания масса разламывается на маленькие кусочки, напоминающие во внешнему виду кристаллы или гранулы, и поступает в нелегальную коммерческую продажу. Крэк почти целиком (примерно на 90%) состоит из кокаина–основания и, как правило, более чистый, чем исходная соль кокаина, поскольку в процессе экстракции осуществляется и очистка от примесей. Температура плавления крэка 98°С. При более высокой температуре происходит испарение без значительного разложения, что позволяет использовать крэк для курения.
Спидболл. Это смесь крэка и героина, обладающая высоким наркотическим потенциалом. Он является очень опасной новой возможностью выбора наркотика среди наркоманов и несет угрозу развития пристрастия к героину у нового поколения.
Действие кокаина на организм
По характеру воздействия на различные системы организма кокаин является эффективным стимулятором и даже разовое, а тем более хроническое употребление вызывает в организме различные, нередко серьезные нарушения. Кокаин действует непосредственно на мозг, особенно на лимбическую систему, содержащие центры, ответственные за состояние инстинктивного наслаждения. Кокаин продуцирует эффект эйфории, блокируя реабсорбцию дофамина, и повторяющееся потребление кокаина может исчерпать запас дофамина, что становится причиной «ломки», ощущаемой к концу действия наркотика. Это также объясняет развитие физического пристрастия и толерантности к кокаину.Особенно катастрофично воздействие кокаина на сердечно–сосудистую систему, систему дыхания и ЦНС, проявляющееся в поведенческих отклонениях, тяжелой депрессии, параноидальных расстройствах, психозах (для которых введен термин «кокаиновый» психоз), галлюцинациях, мозговых инсультах и кровотечениях.
Действие кокаина на организм как стимулятора ■ эмоциональный подъем, эйфория ■ ощущение прилива энергии ■ усиление умственной активности ■ долгий период бодрствования ■ снижение потребности во сне ■ подавление аппетита ■ увеличение физической выносливости.
Физиологические проявления действия кокаина ■ учащение пульса, тахикардия ■ учащение ритма дыхания ■ сужение кровеносных сосудов ■ подъем давления ■ повышение температуры тела ■ потливость ■ расширение зрачков.
Признаки потребления кокаина. На первых порах факт употребления кокаина может ничем не проявляться. Однако по мере продолжения использования «наркотика проявляются очевидные признаки, подтверждающие это: потеря веса, неопрятный внешний вид, покраснения кожи из–за расчесывания кажущихся укусов так называемых «кокаиновых клопов», хронический насморк, частые респираторные инфекции. Находясь под воздействием кокаина, человек может оставаться бодрым несколько часов, а затем спать длительный период времени. Психологические признаки зависимости могут включать потерю интереса к дружескому общению, прежним увлечениям или любой другой активной деятельности, проблемы дома, в школе и на работе, финансовые проблемы. Развивающийся психоз может проявляться в совершении повторяющихся конвульсивных движений, подобных работе пальцев при печатании или игре с волосами. В случае острой передозировки характерны расширенные зрачки, тахикардия, потливость, гипертензия. Кокаин может вызывать слуховые галлюцинации (человек «слышит голоса») и тяжелую депрессию, а также резкую смену настроения. Часты проявления нетерпеливости и агрессивности, нервозности и чрезвычайного озлобления.
Симптомы привыкания. последствия применения. хронические эффекты. эффекты передозировки ■ проблемы со сном, бессонница ■ головная боль ■ снижение аппетита ■ тошнота ■ усталость ■ насморк, воспаления носовых путей, геморрагический нос, кровотечения, некроз носовой перегородки ■ расширенные зрачки ■ неразборчивая речь ■ покраснение кожи от расцарапывания кажущихся «укусов кокаиновых клопов» ■ повторяющаяся судорожная активность, конвульсивные движения пальцев рук (подобно печатанию на машинке или игре с волосами) ■ раздражительность, злость, агрессивное поведение ■ тремор, конвульсии, судороги, припадки ■ депрессия ■ психоз, паранойя ■ бред, ложные и иррациональные идеи ■ галлюцинации: обонятельные, слуховые, тактильные (ощущение присутствия «кокаиновых клопов» под кожей) ■ нарушения дыхания, легочные заболевания, остановка дыхания, отек легких ■ сердечно–сосудистые проблемы: аритмия, фибрилляция, инфаркт, остановка сердца ■ церебральный инфаркт, инсульт ■ склонность к самоубийству.
Последствия употребления кокаина женщинами во время вынашивания, родовой и последующий период: ■ риск спонтанного прерывания беременности (выше, чем для героина) ■ риск врожденных уродств и пороков развития ■ высокая смертность плода в период вынашивания, при родах и в послеродовом периоде ■ отклонения поведения новорожденных, связанные с нарушениями нервной системы.
Потенциальной проблемой для потребителей кокаина можно также считать СПИД и гепатит, так как при использовании одних шприцов очень велика опасность переноса инфекции. Инфицированные кокаинисты могут далее заразить партнеров, супругов и детей, способствуя распространению инфекции и делая ее неконтролируемой.
Действие кокаина на новорожденных
Доступность кокаина в уличной торговле поставило новую проблему – дети, рождающиеся с симптомами влияния кокаина. Беременным женщинам категорически запрещается его использование, так как даже одноразовое употребление кокаина во время беременности может привести к катастрофическим последствиям для плода. Прием кокаина на ранних сроках беременности может привести к нарушению вынашивания или даже к рождению мертвого ребенка. На более поздних сроках наркотик может вызвать преждевременные схватки или выкидыш. Иногда происходит раннее отделение плаценты, что ведет к серьезной опасности для жизни как младенца, так и матери.Дети рождаются с различными отклонениями, обусловленными употреблением кокаина в процессе их вынашивания. Многие их этих детей начинают жизнь с агонизирующего состояния отмены, которое может длиться до трех недель («кокаиновые младенцы»). Иногда они 80 страдают от сердечных приступов до и после родов. Дети, матери которых принимали кокаин, имеют высокий риск проявления «Синдрома Внезапной Детской Смерти». Наиболее часты отклонения функционирования легких, почек, печени, мозга, гениталий. Имеют место также проблемы с дыханием, трудности двигательных функций, церебральный паралич и физические уродства.
Признаки расстройства нервной системы, связанные с действием кокаина: оцепенелость, возбудимость, трудности при кормлении, сверхчувствительность к свету и звукам. «Кокаиновые младенцы» не осознают своего окружения и проявляют тип поведения, указывающий на неврологические и психологические отклонения. Однако глубина нарушений может не проявляться и не распознаваться вплоть до достижения ребенком школьного возраста.
Рождение детей со сформировавшимся пристрастием к кокаину вследствие его употребления матерями в процессе беременности – одна сторона проблемы. Вторая – дети, подвергающиеся воздействию наркотика уже после рождения при кормлении молоком матерями, имеющими пристрастие к кокаину. Эффекты такого воздействия все еще не изучены, по всей вероятности, младенцы, питающиеся молоком, содержащим кокаин, испытывают те же проблемы, что и кормящие их матери.
В странах, переживших сильное увлечение кокаином, в частности, в США, последствия этого увлечения проявляются в последующем поколении, а возможно и в следующих. В настоящее время на десять детей, рожденных в США, один рождается от матери, употреблявшей в течение беременности какой–либо из запрещенных средств.
Действие крэка
При курении или ингаляции через трубку пары кокаина попадают прямо в легкие, сильный эффект начинается практически мгновенно и длится всего лишь около десяти минут, по истечении которых для его поддержания требуется следящая доза. Передозировка возникает очень легко и Может привести к тяжелым последствиям и летальному исходу, не говоря уже о развитии зависимости. По субъективным оценкам людей, куривших КРЭК, пристрастие к кокаину сильнее по сравнению с героином, но для крэка еще «в 3–5 раз выше».Немедленный эффект приема крэка может выражаться в затруднении дыхания и эмфиземе. Обычными следствиями являются хроническая хрипота и болезни горла. Однако непосредственные эффекты ничего не значат в сравнении с опасностью катастрофических изменений, которые крэк вызывает в организме. Крэк воздействует на систему кровообращения, вызывая резкое сокращение кровеносных сосудов. Увеличение кровяного давления и сердечного ритма может привести к коронарному приступу, а интенсивная стимуляция мозга к конвульсиям.
Возникающее вначале чувство эйфории вскоре сменяется столь же сильной депрессией, для противодействия которой необходимо снова выкурить дозу препарата, чтобы вернуть состояние эйфории и хорошего самочувствия. Эти циклически повторяющиеся взлеты и падения приводят к привыканию и зависимости от наркотика.
Продолжающееся использование крэка может вызвать бессонницу, нервное возбуждение и тяжелую паранойю. «Крэковые наркоманы» становятся хроническими больными тяжелыми формами депрессии с тягой с самоубийству или убийству.
Последствия длительного употребления крэка
■ ЦНС – Находясь под воздействием крэка, человек становится гиперактивным, энергичным и раздражительным. ■ Легкие – Хрипота, бронхиты и другие респираторные проблемы. ■ Вес – Потеря интереса к еде и сну. Многие страдают катастрофической потерей веса. ■ Мозг – Изменяются биохимические процессы мозга. Привыкание развивается быстрее, чем в случае других наркотиков, включая героин. Крэк достигает мозга за секунды после начала курения и вызывает мощный эффект, за которым следует болезненный спад, ломка. Чтобы смягчить проявление синдрома отмены, наркоман жаждет получить или следующую дозу препарата, или обратиться к другому наркотику или алкоголю. ■ Глаза – Расширение зрачков вызывает повышенную светочувствительность. Наркоманы видят «снежинки» или «гало» вокруг предметов при попытке сфокусировать зрение. ■ Сердце – Пульс учащается, возникает аритмия. Может наступить остановка сердца.Действие спидболла на организм
Основания для популярности спидболла – смеси крэка и героина заключаются в самой природе их действия. Крэк, как известно, является стимулятором с коротким, от 8 до 10 мин, и чрезвычайно интенсивным эффектом. Затем наступает сильное нервное возбуждение и тяжелая депрессия. Героин, проявляя седативное действие, длящееся до четырех часов, противодействует вызываемой крэком тяжелой депрессии. Смесь героина и кокаина как в солевой форме для внутривенного введения, так и в форме для курения, усиливает действие каждого наркотика на психику и организм в целом. ■ ЦНС. Действие кокаиновой составляющей проявляется как действие стимулятора, вызывающего гиперактивность, раздражительность, агрессивность. Действие героиновой составляющей приводит к расслабляющему эффекту, человек успокаивается и становится миролюбивым. Настроение потребителя спидболла меняется быстро и непредсказуемо. ■ Дыхательная система. Постоянное использование спидболла для курения вызывает болезни горла, эмфизему, бронхиты, различные респираторные проблемы. ■ Вес. Наркоманы часто теряют интерес к еде и сну. Многие страдают катастрофической потерей веса. ■ Мозг. Изменяется биохимическое состояние мозга, очень быстро наступает привыкание.Зависимость и синдром отмены
Эффективность развития пристрастия к кокаину зависит от способа его потребления человеком. Высокий потенциал развития зависимости характерен для курения и внутривенного введения наркотика. При интраназальном способе введения зависимость возникает более постепенно. Физическая зависимость, относительно наличия которой до сих пор нет однозначного мнения, выражается в симптомах при отказе от потребления препарата (синдроме отмены).Продолжительность и сила проявления симптомов различны в зависимости от степени пристрастия, длительности употребления и т.п. Различные стадии, определяющиеся временем с момента последнего приема наркотика, характеризуются разными симптомами. Тяга к наркотику ослабевает в некоторый период (в интервале 1–10 нед с момента последнего приема), но затем вновь возникает в очень сильной степени.
Основные симптомы: ■ тревожность, беспокойство, раздражительность ■ усталость, упадок сил ■ бессонница ■ депрессия
Фармакокинетика кокаина
Клиническая доза кокаина – 1,5 мг/кг.Разовая «уличная» доза – 15–60 мг.
Для вдыхания через нос («дорожка» длиной 3–5 см) – 10–20 мг (может доходит до 50–100 мг).
Токсическая доза–орально 500 мг.
Летальная доза – 1,2 г, при индивидуальных отклонениях в организме может снижаться до 20 мг и менее.
Способы употребления кокаин гидрохлорид ■ интраназально: вдыхание или втягивание через нос (основной) ■ инъекции внутривенные и внутримышечные ■ курение (редко) ■ орально, подъязычно, вагинально, ректально (редко).
Паста коки ■ курение (в смеси с табаком или марихуаной).
Кокаин основание, крэк ■ Курение с применением специальных трубок, самодельных примитивных устройств или сигарет с добавками табака или марихуаны.
Спидболл ■ курение.
При интраназальном способе (втягивании через нос) порошок кокаина располагают в узкую полоску («дорожку») на гладкой поверхности и втягивают его через соломинку или узкую трубочку, свернутую из бумаги. Наиболее опасные формы использования – внутривенное введение и курение, часто приводящие к развитию привыкания и к передозировке, ведущей к смертельному исходу.
Фармакокинетические параметры
Время полувыведения (полужизнь) T½: кокаина 38–67 мин, бензоилэкгонина – 4–6 ч, метилэкгонина – 2,5–7,6 ч.Биодоступность кокаина при различных способах введения (%): ■ оральный – 20–40. ■ интраназальный – 20–40. ■ курение – 6–32. ■ внутривенный – 100.
Всасывание. При курении и внутривенном введении всасывание быстрое. Пик концентрации кокаина в плазме достигается быстро и через очень короткое время снижается. Длительность максимальных психотропных и физиологических эффектов также очень мала, по субъективным данным эйфорические эффекты ощущаются при курении не более 20 мин. Интраназальное и оральное введение дают сходные концентрационные профили в плазме: максимум достигается за время около 30–60 мин. Однако при интраназальном введении действие наступает быстрее, а его продолжительность доходит до 60–90 мин.
Оральный способ введения характеризуется медленным развитием эффектов и значительно более слабой их интенсивностью.
Распределение. Кокаин и метаболит норкокаин – липофильные соединения, легко преодолевают гематоэнцефалический (ГЭБ) и плацентарный барьер. В высоких концентрациях кокаин накапливается в жировых депо. Метаболиты бензоилэкгонин и экгонин, являясь высоко полярными, не преодолевают ГЭБ, по крайней мере, в фармакологически значимых концентрациях.
Концентрация кокаина в плазме: ■ терапевтическая – 50–300 нг/мл ■ токсическая – 900 нг/мл (однако приводятся случаи острой интоксикации при гораздо меньших концентрациях в крови: 200 нг/мл) ■ летальная – 1–20 мкг/мл (концентрацию около 9 мкг/мл связывают со смертью от передозировки кокаина в отсутствие других средств).
Метаболизм кокаина. Кокаин быстро метаболизирует в плазме и печени в процессах энзимного гидролиза (с участием холинэстеразы плазмы) с потерей бензоила до метилэкгонина, неэнзимного гидролиза с потерей сложноэфирной метиловой группы до бензоилэкгонина и N–деметилирования до норкокаина.
Основные метаболиты: ■ бензоилэкгонин (БЭ) ■ метиловый эфир экгонина или метилэкгонин (МЭ).
Минорные метаболиты: ■ экгонин (Э) ■ норкокаин (НК) ■ бензоилнорэкгонин (БНЭ).
Гидроксилированные продукты: ■ мета–гидроксикокаин (м–ОН–К) ■ пара–гидроксикокаин (п–ОН–К) ■ мета–гидрокси–бензоилэкгонин (м–ОН–БЭ) ■ пара–гидрокси–бензоилкокаин (п–ОН–БЭ) ■ N–гидроксиноркокаин.
Продукты расщепления кокаина при курении: ■ α–, β–, γ–, δ–карбометоксициклогептатриены ■ ангидроэкгонинметиловый эфир, метилэкгонидин (АЭМЭ).
В присутствии этилового спирта в организме: ■ кокаэтилен (КЭ) ■ норкокаэтилен (НКЭ) ■ этиловый эфир экгонина (ЭЭЭ).
Образование МЭ из кокаина идет под действием холинэстеразы, присутствующей в плазме крови, в печени и поджелудочной железе, но не найденной в моче человека. МЭ не накапливается в крови, а непрерывно выводится в мочу, где может быть обнаружен. БЭ образуется из кокаина в процессе химического гидролиза при физиологических значениях рН 7,4. МЭ превращается в экгонин по этому же механизму. В отличие от МЭ БЭ не образуется и не деградирует под действием холинэстеразы плазмы.
На степень энзимного превращения кокаина в МЭ влияют доза, способ введения, фенотип холинэстеразы, величина константы Михаэлиса и максимальная скорость гидролиза. Индивидуальные различия в активности холинэстеразы приводят к резкому отличию профилей кокаина и метаболитов. Скорость образования МЭ из кокаина достаточно высока, однако из–за спонтанного гидролиза МЭ в Э со скоростью, подобной скорости превращения кокаина в БЭ, МЭ не обнаруживается в плазме в значительных количествах. Норкокаин – активный метаболит, в действии на ЦНС и кардиоваскулярной активности подобен кокаину. Может метаболизировать в N–гидроксиноркокаин.
Внутривенное введение кокаина
Для внутривенного введения (ВВВ) используется раствор кокаина гидрохлорида в воде или физиологическом растворе. Начало действия через 0,5–2 мин. Для дозы 100 мг получены следующие значения (п – 3) : максимальная концентрация кокаина в плазме достигается через 5 мин и составляет в среднем 1390 нг/мл (интервал 1080–1820 нг/мл), через 5–6 ч концентрация снижается до примерно 50 нг/мл. Метаболит БЭ появляется в плазме через 5 мин, достигает через 60 мин максимального уровня 800 нг/мл и затем сохраняет это значение в течение 2–4 ч. В результате последующего медленного уменьшения концентрация БЭ в плазме через 24 ч после ВВВ составляет в среднем 100 нг/мл (интервал 90–160 мкг/мл).Курение
Для курения используется кокаин–основание (КРЭК).Начало действия – в течение 8–10 с.
Пик концентрации в плазме – через 5 мин (2–10 мин). Эффект очень сильный, но короткий.
Пик эффекта достигается через 6–8 мин.
Длительность эффекта – 10–20 мин.
При курении только 6,5% дозы поступает в легкие в виде паров, остальные 93,5% – в виде аэрозоля.
Фармакокинетика кокаина при курении и внутривенном введении носит сходный характер, за исключением уровня концентраций кокаина и бензоилэкгонина, который в 1,5–2 раза выше при ВВВ (табл. 1).
Интервал максимальных концентраций кокаина: при курении.
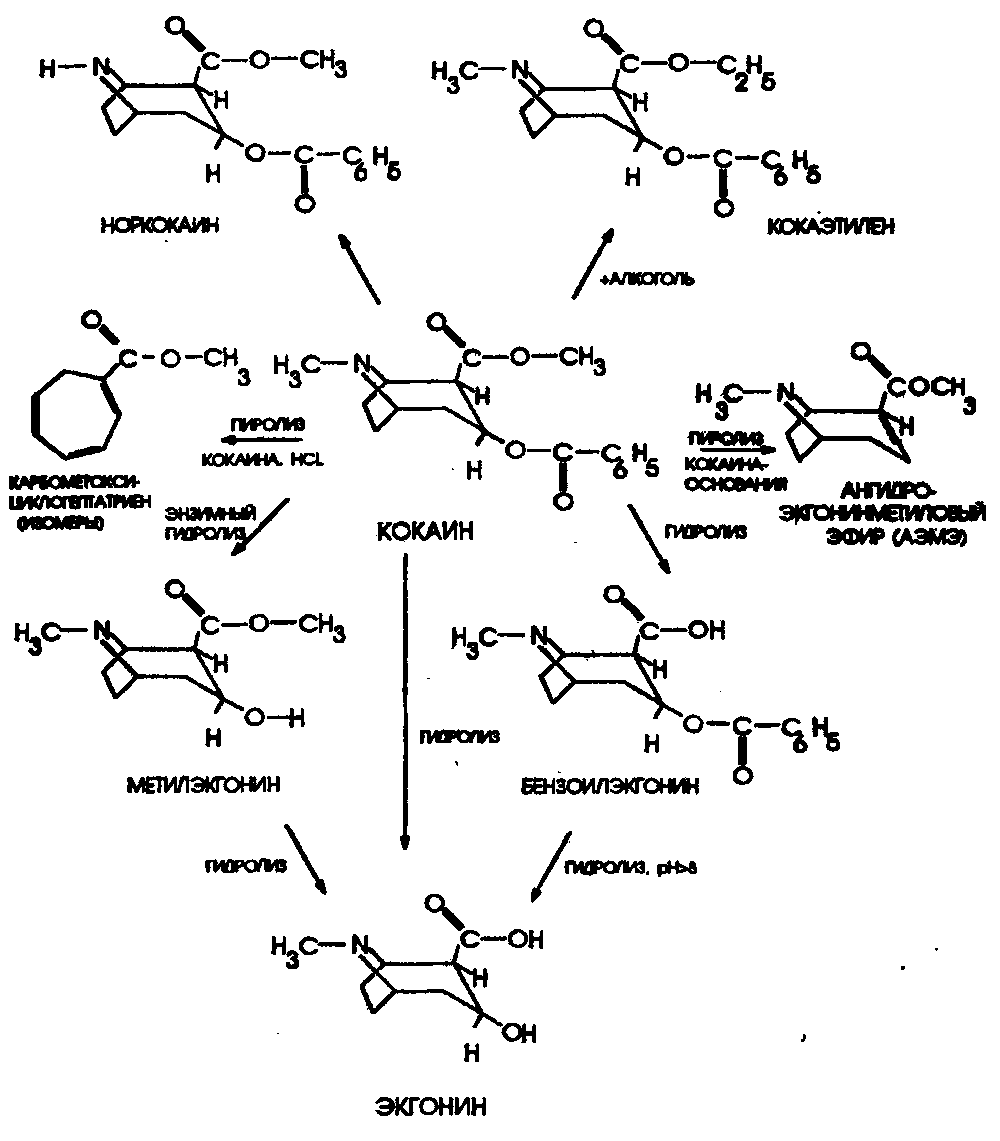 Рис. 1. Схема метаболизма кокаина в организме человека.
Рис. 1. Схема метаболизма кокаина в организме человека.
46–291 нг/мл, при ВВВ 122–442 нг/мл, спустя 2 ч после сеанса курения и через 4 ч после инъекции содержание кокаина в плазме уменьшается до менее 25 нг/мл.
Концентрация БЭ имеет максимальное значение в интервале 1–2 ч и 2–4 ч после курения и ВВВ, соответственно (среднее значение 2 ч для обоих вариантов). Максимальная концентрация при ВВВ 94–239 нг/мл примерно в 2–3 раза выше по сравнению с величинами, определяемыми при курении 31–119 нг/мл.
Таблица 1. Средние концентрации кокаина и метаболитов в плазме после курения и внутривенного введения кокаина. нг/мл. Курение – 40 мг кокаина–основания (п = 7), внутривенное введение – 44,8 мг кокаина–гидрохлорида (п = 7)
| Время, мин | Курение | Внутривенно | ||
|---|---|---|---|---|
| Кокаин | Бензоил–Экгонин | Кокаин | Бензоил–Экгонин | |
| 2 | 153 | 0 | 244 | 14 |
| 5 | 120 | менее 1 | 217 | 7 |
| 10 | 103 | И | 234 | 16 |
| 15 | 91 | 21 | 222 | 36 |
| 30 | 69 | 49 | 173 | 80 |
| 60 | 39 | 65 | 124 | 128 |
| 120 | 23 | 70 | 66 | 155 |
| 240 | 6 | 58 | 20 | 135 |
| 480 | 0 | 24 | 2 | 109 |
| 720 | 0 | 13 | менее 1 | 59 |
| 1440 | 0 | менее 1 | 0 | 11 |
Продукты пиролиза кокаина – основания и гидрохлорида
Ингаляционная эффективность курения вследствие пиролиза кокаина падает с увеличением температуры и составляет (для смеси кокаин–основание + бикарбонат натрия 1:20):при 170°С – 73%, при 220°С – 62%, при 270°С – 37%.
При пиролизе кокаина–гидрохлорида в результате элиминирования метиламина и бензойной кислоты с раскрытием пиррольного кольца образуются α–, β–, γ–, δ–изомеры карбометоксициклогептатриена.
В результате пиролиза кокаина–основания элиминируется бензойная кислота и образуется основной летучий продукт метилэкгонидин: ангидроэкгонин–метиловый эфир (АЭМЭ). Его образование начинается при 220" С, а в заметных количествах он накапливается при 255°С, выше 400°С около 89% кокаина превращается в АЭМЭ. АЭМЭ может служить маркером курения крэка (кокаина основания).
Другие продукты пиролиза: бензойная кислота, метилбензоат, N–метилбензамид, метил–4–(3–пиридиннл)–бутират.
В первые 2 ч средняя концентрация АЭМЭ (п = 9) при курении: 816 нг/мл (интервальные значения 51–2866 нг/мл), затем происходит быстрое уменьшение концентрации с периодом элиминирования T½ около 60 мин.
Таблица 2. Концентрация АЭМЭ в моче в интервале до 48 ч после употребления кокаина при разных способах введения, нг/мл. Курение – 100 мг кокаина основания при 250°С с применением специально сконструированной трубки. ВВВ – 0,6 мг/кг кокаина. Интраназально – 2 мг/кг кокаина в физиологическом растворе в виде аэрозоля. Указаны интервальные значения, средние величины (n=9) приведены в скобках.
| Вещество | Курение | ВВВ | ИН |
|---|---|---|---|
| АЭМЭ | 93–3740 (850) | 0–34 (7.7) | 0–60/42) |
| кокаин | 250–4250 (1580) | 740–7340 (3010) | 1320–13900(4140) |
| БЭ | 6450–46700(21500) | 25 400–107000(51400) | 40900–162000(94 500) |
| АЭМЭ/Кокаин | 0,03–1,08 (0,58) | 0–0,04(0,01) | 0–0,07 (0,02) |
Специальными опытами показано, что АЭМЭ после курения в плазме не детектируется, в то время как в слюне он присутствует в заметных количествах: 558–4374 нг/мл через 2 мин после начала курения (n=7).
Вместе с тем известно, что АЭМЭ может образоваться в инжекторе при газохроматографическом анализе кокаина, что требует тщательного контроля для исключения возможности его появления в процессе анализа.
Вдыхание через нос (интраназальное введение)
Используется кокаин в форме солянокислой соли (кокаин HCl).Начало действия – через 5–15 мин.
Пик концентрации в плазме – через 15–60 мин (в среднем 30 мин).
Пик эффекта – через 15–20 мин. Длительность эффекта – 1–1,5 ч После употребления дозы 1,5 мг/кг кокаина гидрохлорида интервал максимальных концентраций в плазме 120–474 нг/мл (n=7), спад концентрации происходит за время 3–5 ч.
БЭ появляется в плазме через 20 мин после употребления средства, достигает максимального содержания через 120 мин, которое остается постоянным в течение длительного времени. См. также таблицу 3.
Таблица 3. Время и величина максимальной концентрации кокаина и метаболитов в плазме после интраназального введения кокаина–гидрохлорида в зависимости от дозы среднее значение (п =525 проб)
| Вещество | Доза 48 мг | Доза 96 мг | ||
|---|---|---|---|---|
| Время, мин | нг/мл | Время, мин | нг/мл | |
| Кокаин | 45 | 81 | 45 | 201 |
| МЭ | 100 | 37,5 | 80 | 67 |
| БЭ | 170 | 262 | 170 | 531 |
Подкожное введение кокаина
Кокаин–гидрохлорид вводили подкожно (попеременно с кодеином) в течение нескольких дней пяти наркоманам с длительным опытом использования кокаина в клинических условиях. Дозы делились на «низкие» (далее: н.д.) по 75 мг/70 кг и «высокие» (далее: в.д.) по 150 мг/70 кг. Максимальная концентрация кокаина в плазме достигалась через 30 мин и составляла для н.д. 258–434 (среднее 363) нг/мл и для в.д. 406–1154 (среднее 706) нг/мл. Через 1–2 ч концентрация кокаина начинала снижаться и через 24 ч после введения составляла менее 10 нг/мл. Метаболиты БЭ и МЭ появлялись в плазме через 5–10 мин после введения и достигали максимума через 2–4 ч. Кроме этих основных метаболитов, в некоторых образцах плазмы найдены (в скобках приведены максимальные концентрации в нг/мл): бензоилнорэкгонин (23), норкокаин (7), мета–гидрокси–кокаин (6), пара–гидроксикокаин (5), мета–ОН–БЭ (16), пара–OH–БЭ (34), КЭ (14). В интервале 48 ч после введения элиминирование кокаина и метаболитов обычно заканчивалось.Выведение кокаина из организма
Время полувыведения после орального и интраназального приема кокаина составляет соответственно: 78 и 48 мин. В течение 2–3 дней с мочой выводится 90–95% принятой дозы кокаина, в основном, в виде метаболитов.| Неизмененный кокаин составляет | 1–9% дозы |
| Бензоилэкгонин | 35–60% дозы |
| Метилэкгонин | 32–49% дозы |
| Экгонин | 1–8% дозы |
| Норкокаин и гидроксилированные метаболиты | около 10% дозы |
При вдыхании через нос (ИН) кокаина–гидрохлорида 1,5 мг/кг, концентрация кокаина в моче С(К)=24 мкг/мл максимальна через 2 ч после введения и затем быстро уменьшается, С(БЭ)=75 мкг/мл в интервале 1–12 ч, затем медленно снижается и детектируется в течение 6 сут (радиоиммунным методом анализа).
Второй важный метаболит, выводимый с мочой, МЭ. В пробах мочи наркоманов («уличные» пробы, п = 13, дозы – неизвестны, способы введения: ВВ и ИН) концентрации МЭ 8,2–559,0 (среднее 151), кокаина 0–58,2 (среднее 16,2) мкг/мл.
Отношение С(МЭ)/С(К) изменяется от 2 до 110 при дозе кокаина 100 мг (среднее 21, п = 13.). Скорость мочевой экскреции в общем случае подчиняется закономерности: Кокаин > МЭ > БЭ. Обобщенные данные разных авторов по кинетике выведения метаболитов приведены в табл. 4.
В табл. 5 приведены концентрации основных и минорных метаболитов, в том числе редко определяемых гидроксилированных метаболитов в моче хроников–наркоманов (18 женщин и 17 мужчин), которые свидетельствовали о приеме кокаина в течение 10 дневного периода перед анализом. Интервальные значения отражают вариабельность концентраций. Приведены средние значения отдельно для женщин и мужчин.
Таблица 4. Концентрация основных метаболитов кокаина в моче, мкг/мл. Интраназальное или внутривенное введение 100 мг кокаина–гидрохлорида.
| Время, ч | Кокаин | БЭ | МЭ |
|---|---|---|---|
| 0,5 | 9,6 | 19,1 | – |
| 1 | 9,3 | 43,5 | – |
| 3 | 4,0 | 52,5 | – |
| 4 | 6,6 | 32 | 32,4 |
| 5 | 2,4 | 34,4 | – |
| 6 | 0,7 | 39,8 | – |
| 10 | 0,48 | 35,2 | – |
| 12 | 0,20 | 20,5 | 10,4 |
| 18 | н.д. | 14,8 | – |
| 20 | н.д. | 18,5 | 5,4 |
| 36 | Н.Д. | 2,2 | 0,2 |
| 60 | Н.д. | 0,45 | – |
Таблица 5. Концентрации метаболитов кокаина в моче.
| Вещество | Концентрация, нг/мл | ||
|---|---|---|---|
| Диапазон N=35 | Среднее N=18, жен. | Среднее N=17, муж. | |
| бензоилэкгонин | 50 000–1 200 000 | 292 954 | 251 917 |
| метилэкгонин | 400–500 000 | 106 230 | 79 422 |
| кокаин | 0–100 000 | 26 575 | 8 504 |
| бензоилнорэкгонин | 200–50 000 | 13 387 | 8 743 |
| норкокаин | 0–6 071 | 1 107 | 339 |
| кокаэтилен | 0–4 924 | 763 | 28 |
| норкокаэтилен | 0–735 | 81 | 9 |
| этилэкгонин | 0–11 780 | 1 695 | 367 |
| мета–ОН–кокаин | 60–50 000 | 1552 | 736 |
| пара–ОН–кокаин | 56–2263 | 567 | 300 |
| мета–ОН–БЭ | 271–7054 | 2429 | 1773 |
| пара–ОН–БЭ | 558–43 070 | 12 129 | 8 705 |
| АЭМЭ | 0–4244 | 219 | 310 |
Метаболит экгонин – новый маркер употребления кокаина
МЭ легко подвергается гидролитическому превращению в экгонин (Э) и часто не детектируется в крови. При подщелачивании гидролиз МЭ может проходить и в моче. БЭ устойчив к гидролизу в интервале рН 5–8. Содержание Э в моче часто превышает содержание БЭ, что рекомендуется использовать при анализе, особенно если БЭ обнаруживают в очень малом количестве, ниже 100 нг/мл. Э накапливается в моче в период, когда уровень БЭ спадает. Из исследованных проб мочи наркоманов (121 проба) с содержанием БЭ от 11 до 123 нг/мл, в 96% проб концентрация Э превышала 10 нг/мл, в 95% – 50 нг/мл (диапазон 50–1769 нг/мл), в 84% – 100 нг/мл (112–1769 нг/мл). В среднем концентрация Э превышала концентрацию БЭ в 5 раз.Э является конечным продуктом процесса химического гидролиза кокаина, МЭ и БЭ in vivo и in vitro. В гидролизованной моче с раздельно введенными добавками кокаина, БЭ и МЭ по 50 мкг/мл каждого соединения найден Э в концентрации 48,5 нг/мл (0,097% превращения), 135 нг/мл (0,27%) и 560 нг/мл (1,12%) соответственно. Таким образом Э может быть определен в моче людей, употреблявших кокаин, после процедуры химического гидролиза. В моче с добавленными гидрохлоридами кокаина, БЭ и МЭ по 100 мкг каждого соединения после проведения щелочного гидролиза и ионообменного изолирования Э эффективность определения суммы введенных веществ составила 90,4%.
Метаболит кокаина и этанола – кокаэтилен
Кокаэтилен – активный, токсичный продукт, образующийся при совместном употреблении кокаина и этанола. T½=148 мин. Концентрация КЭ часто близка, а иногда превышает концентрацию кокаина в крови, печени, мозге, моче. В пяти случаях смерти от передозировки кокаина при совместном употреблении алкоголя содержание кокаина в крови изменялось от 0,03 до 1,4, а КЭ – от 0,03 до 0,53 мкг/мл (табл.6). Предполагается аддитивность токсического действия кокаина и этилена на организм человека.Кокаэтилен также может образоваться при длительном хранении кокаина в спиртовом растворе, а также в печени трупа при совместной кокаиновой и алкогольной интоксикации.
Таблица 6. Содержание кокаина, этанола и кокаэтилена в организме при смертных случаях, связанных с употреблением кокаина, мг/л или мг/кг
| Вещества | Психоз, суицид | Остановкадыхания | ||
|---|---|---|---|---|
| кровь (сердце) | мозг | кровь (сердце) | мозг | |
| этанол | 0,02 г/дл | – | 0,01 г/дл | – |
| кокаин | 1,4 | 2,2 | 0,040 | 0,37 |
| кокаэтилен | 0,18 | 0,44 | 0,21 | 0,15 |
| (БЭ) | (+) | (+) | ||
Гидролитические превращения кокаина и метаболитов
Кокаин, бензоилэкгонин и метилэкгонин в плазме претерпевают следующие превращения: ■ В процессе ферментативного гидролиза под действием холинэстеразы плазмы кокаин теряет бензоильную группу с образованием метаболита МЭ. БЭ к действию фермента инертен и холинэстераза не участвует в процессе образования или деградации БЭ. Кокаин → (холинэстераза) → метилэкгонин. ■ В процессе химического (спонтанного) гидролиза при физиологических значениях рН кокаин и МЭ теряют сложноэфирную метильную группу с образованием соответственно БЭ и Э. Кокаин и МЭ быстро удаляются из крови с близкими величинами скорости. Кокаин → (химический гидролиз, рН 7,4) бензоилэкгонин метилэкгонин → (химический гидролиз, рН 7,4) → экгонин.Таким образом, в общем случае при физиологических значениях рН МЭ не аккумулируется в крови, в отличие от БЭ, который накапливается. Эти соотношения, однако, вследствие индивидуальных особенностей организма могут нарушаться, поскольку скорость гидролиза сильно зависит от величины рН.
При хранении образцов крови, как и в трупном материале, рН по различным причинам (например, из–за анаэробного метаболизма) падает до 5,5–6,0, что приводит к замедлению (вплоть до полной остановки) химического гидролиза, в результате чего образование БЭ из кокаина и Э из МЭ подавляется. Скорость же энзимного гидролиза в этом случае хотя и может снижаться по сравнению со значениями, характерными для живого организма, но незначительно. В результате энзимный гидролиз протекает, когда химический замедлился или остановился. Таким образом, соотношение описанных процессов изменяется в пользу энзимного гидролиза, и в крови концентрация кокаина уменьшается, МЭ увеличивается, а БЭ остается неизменной. При хранении образцов крови и в трупном материале происходит аккумулирование МЭ при непрерывном расходовании кокаина.
Кокаин претерпевает спонтанный гидролиз в моче, плазме, крови живых лиц и водных щелочных растворах. Его метаболиты БЭ и МЭ при щелочных значениях рН в моче гидролизуются в Э. Около 40% кокаина теряется при рН мочи 8, а при более высоких значениях рН – более 50% БЭ, но в интервале рН 5–8 БЭ устойчив (или гидролизуется незначительно). Количество МЭ в моче при щелочных значениях рН может уменьшаться вплоть до величин, ниже пределов детектирования.
Содержание кокаина в слюне и кожных выделениях
Слюна является биологической матрицей, имеющей некоторые преимущества перед другими традиционными биожидкостями (кровь или моча) как объект исследования для обнаружения наркотиков из–за быстроты и неинвазивности процесса отбора пробы. После ВВ 44,8 мг кокаина пик его концентрации в слюне изменяется в интервале 428–1927 нг/мл (N=7), в то время как после курения эти величины значительно выше – в интервале 15 852–504 880 нг/мл (N=7). Кроме того, в значительных количествах обнаруживается АЭМЭ: максимальная концентрация 558–4374 нг/мл (N=7) достигается через 2 мин после курения. Присутствие АЭМЭ в слюне может служить признаком курения кокаина.Пот – как объект исследования представляет еще одну возможность для быстрого и неизвазивного отбора пробы. В настоящее время для этой цели используют пластыри, содержащие адсорбирующий материал для поглощения выделяемого пота и легко крепящиеся к коже липкой пленкой. Размер пластырей, производимых разными фирмами–изготовителями, различен, как и площадь коллектора – адсорбирующего слоя, например, 2·3 дюйма (51·76 мм). Адсорбент обладает большой емкостью и насыщается в течение нескольких дней, однако уже за 24 ч сорбируется достаточное для определения количество растворенного в поте наркотика или метаболита. После интраназального введения 50 или 126 мг кокаина (в эксперименте участвовали 15 человек) пот был собран в течение от 1 ч до 8 дней пластырями с размером коллектора 14 см2 с различных участков тела (торс, бицепсы, спина). Кокаин появлялся в поте через интервал времени от 1 ч до 2 дней при концентрации от 2 до 100 нг/мл. Максимальная концентрация кокаина в поте достигалась на третий день и составляла в среднем (N =15) около 60 нг/мл. Через 8 дней интервал концентрации кокаина от 6 до 100 нг/мл. Содержание метаболита БЭ составило 0–10% от содержание родительского соединения.
Кожный жир и ороговевшие частички кожи людей (верхний слой эпидермиса), длительно (в течение 40 нед) употреблявших кокаин, также содержат наркотик в небольших количествах. В кожном покрове и кожных выделениях кокаин появляется позже, чем в плазме. Если после подкожного введения 75–150 мг кокаина в плазме пик кокаина достигается через 30 мин после введения, то в кожном жире максимальная концентрация приходится на 1–2 ч и составляет для кокаина 1–11,4; БЭ 0,2–5; МЭ 0,4–5 нг/мг. В кожном жире кокаин может быть определен в течение 24–48 ч. В роговом веществе кожи кокаин появляется спустя сутки после введения в количестве 0–3 нг/мг й определяется в течение 6–15 дней в зависимости от дозы. БЭ и МЭ присутствуют в незначительных количествах: 0,1–2 нг/мг.
Содержание кокаина в волосах
Интервальное содержание кокаина в волосах живых наркоманов: 0,037–129,68 нг/мг. Диапазон концентраций кокаина и метаболитов, (нг/мг): кокаин – 6,4–19,2 (N=10); БЭ – 0,3–2,5 (N=10); МЭ – 0–1,9 (N=4); норкокаин – 0,5–0,7 (N=4); кокаэтилен – 0–2,6 (N=6). Эти величины имеют сильные индивидуальные вариации. Например, для 2 «умеренных» (прием кокаина 1–2 раза в неделю) и 4 «тяжелых» (прием кокаина более 3 раз в неделю) наркоманов определено в волосах: кокаин во всех пробах в интервале от 0,16 до 5,7 нг/мг, БЭ только в одной пробе – 1,1 нг/мг. При курении крэка содержание АЭМЭ от 0,2 до 2,4 нг/мг.В случае острого отравления кокаином хронического наркомана с летальным исходом (клиническое наблюдение) распределение кокаина по сегментам волос (по 2 см от корня) характеризуется значениями, представленными ниже.
| Сегмент волос | Кокаин, нг/мг | Примечание |
|---|---|---|
| 1 | 53,7 | потребление кокаина в течение длительного времени до момента острого отравления |
| 2 | 60,2 | то же |
| 3 | 98 | момент острого отравления, содержание в крови: кокаин – 2,3, БЭ – 4,5 мкг/мл |
| 4 | 25,6 | медленное выведение или распределение кокаина по структуре волос |
| 5 | 6,3 | момент смерти, кокаин в моче и крови отсутствует |
Таблица 7. Распределение кокаина по длине волос в процессе роста. 0,6 мг/кг d5–кокаина, N=1, сегмент 2 см (от корня).
| Отбор волос | Содержание d5–кокаина нг | d5–кокаина общее содержание | ||||
|---|---|---|---|---|---|---|
| месяц | сегмент 1 | сегмент 2 | сегмент 3 | сегмент 4 | сегмент 5 | нг |
| 0,26 | 1,20 | 2,82 | . | – | – | 4,02 |
| 1.17 | 1,26 | 0,54 | 0,38 | 0,22 | – | 2,40 |
| 2,20 | 0,83 | 0,38 | 0,25 | 0,19 | 0,24 | 1,89 |
| 3,13 | 0,11 | 0,23 | 0,34 | – | – | 0,08 |
Эти выводы таковы: ■ пороговая доза кокаина–гидрохлорида для последующего детектирования в волосах: 25–35 мг. ■ длительность определения в волосах после одно разовой дозы кокаина–гидрохлорида: 2–6 мес. ■ содержание кокаина в волосах не зависит от способа введения (при внутривенном и интраназальном способах). ■ содержание в волосах: • кокаин – 0,1–5 нг/мг • БЭ – менее 1 нг/мг не во всех пробах • МЭ – ниже предела обнаружения и не во всех пробах. ■ максимальное содержание кокаина в волосах приходится на 1–2 мес после приема дозы кокаина (однако эта величина имеет сильные индивидуальные различия).
Содержание кокаина в организме новорожденных
Если матери в пред– и послеродовой период употребляли кокаин, то в организме младенцев (плазме, плаценте, моче, меконии) определяют кокаин, бензоилэкгонин и другие метаболиты, а также кокаэтилен. Наличие кокаина и метаболитов в плазме пуповины и моче новорожденного, собранной в период 2–77 ч после рождения, указывает на недавнее употребление матерью кокаина. Из 18 исследованных младенцев все содержали БЭ в плазме пуповины: от 74 до 3880 нг/мл и в моче: от 314 до 41 ООО нг/мл. Кокаин найден в плазме 9 детей: от 5 до 88 нг/мл и в моче 7 детей: от 7 до 205 нг/мл. Меконий (см. раздел «Опиаты») в последние годы становится альтернативой моче и крови в качестве биологического образца для определения содержания наркотических веществ в организме новорожденного. В меконии аккумулируются вещества, поступавшие в организм плода за срок вынашивания, и концентрация этих веществ превышает концентрацию в моче. Помимо основных метаболитов кокаина, в значительных количествах накапливаются гидроксилированные метаболиты: мета– и пара–гидроксибензоилэкгонин (м– и п–ОН–БЭ). В шести образцах мекония новорожденных, чьи матери подтвердили употребление кокаина в течение беременности, определено 13 соединений (табл. 8), из которых кокаин, кокаэтилен и АЭМЭ могут попадать в организм плода исключительно из организма матери, а остальные кроме того могут быть метаболизированы печенью плода.Таблица 8. Кокаин и метаболиты в меконии новорожденного, нг/г, N=6
| Соединение | Содержание | Среднее |
|---|---|---|
| Бензоилэкгонин | 52,7–6370 | 1550,9 |
| метилэкгонин | 76,5–5672,1 | 1516,8 |
| кокаин | 44,2–1294,3 | 523,1 |
| мета–гидроксибензоилэкгонин | 47,8–1061,1 | 296 |
| пара–гидроксибензоилэкгонин | 0–709,3 | 208,7 |
| бензоилнорэкгонин | 0–519,3 | 162 |
| АЭМЭ | 12,4 177,9 | 83,3 |
| мета–гидроксикокаин | 0–167,8 | 53,6 |
| норкокаин | 0–122,9 | 46,0 |
| этиловый эфир экгонина | 0–36,7 | 16,3 |
| кокаэтилен | 0–31,4 | 14 |
| пара–гидроксикокаин | 0–30,7 | 11,9 |
| норкокаэтилен | 0–28,6 | 11,2 |
Кокаин и метаболиты в организме людей, умерших в результате употребления кокаина
Определяемые при аутопсии концентрации кокаина и метаболитов в биожидкостях и тканях изменяются в широком диапазоне. Для 180 проб крови (из банка судебно–химических образцов) получены следующие значения (мкг/мл): кокаин – 0,001–5,0; БЭ – 0,004–2,0. Для других 7 случаев смерти, связанной с употреблением сверхдоз кокаина, содержание в крови (мкг/мл): кокаина от 0,01 до 2,97; БЭ от 0,94 до 7,42; норкокаина (НК) от 0,01 до 0,42. В крови трех жертв передозировки определены (мкг/мл): кокаин 0,068–0,086; БЭ 0,698–1,76; МЭ 0,043–0,244; Э 0,086–1,417. При исследовании мочи и крови людей, погибших от интоксикации неизвестными дозами кокаина, помимо самого кокаина и его метаболитов: бензоилэкгонина, метилэкгонина, норкокаина и норбензоилэкгонина (НБЭ), – в некоторых образцах определяют АЭМЭ и кокаэтилен, а также метаболиты кокаэтилена: норкокаэтилен (НКЭ) и этиловый эфир экгонина (ЭЭЭ).Интервальное содержание для 13 проб (нг/мл):
| • Кокаин | кровь 23–2088 | моча 391–199 225 |
| • БЭ | кровь 215–9195 | моча 962 – более 300 000 |
| • МЭ | кровь 220–7275 | моча 831–126 150 |
| • НК | кровь 23–264 (3 пробы) | I моча 350 (1 проба) |
| • НБЭ | кровь 28–267 (6 проб) | моча 78–35 980 (11 проб) |
Таблица 9. Содержание кокаина и метаболитов в органах, мкг/мл, мкг/г.
| Органы | Сверхдоза кокаина | Сверхдоза кокаина | |||
|---|---|---|---|---|---|
| кокаин | БЭ | НК | кокаин | БЭ | |
| кровь | 2,97 | 7,42 | 0 | 0,01 | 2,9 |
| печень | 3.2 | 6,18 | 0,01 | 0,04 | 2.3 |
| моча | 124,2 | 185 | 0,03 | – | – |
| почки | – | . | – | 0,12 | 2,9 |
| мозг | – | – | – | 10.40 | 1.0 |
Ранее (см. табл. 6) приводились данные по содержанию кокаина, этанола и кокаэтилена в организме умерших от совместной интоксикации кокаина и алкоголя.
Время обнаружения кокаина и метаболитов в пробах мочи
При контролируемом введении кокаина: 80 мг (в виде аэрозоля 2 мл 4% раствора ИН, хирургическая анестезия, п = 12), время обнаружения кокаина и БЭ в моче (5 мл) зависит от индивидуальных особенностей и составляет при пределе обнаружения 50 нг/мл: ■ 24 ч – определяется БЭ во всех 12 пробах (67–2459, среднее 727 нг/мл) ■ 48 ч – кокаин и БЭ определяются в 9 пробах (концентрация БЭ 93–387, среднее 187 нг/мл) ■ 72 ч – кокаин и БЭ определяются только в 3 пробах (концентрация БЭ 60–88, среднее 72 нг/мл).После ингаляции 1,5 мг/кг (6 пациентов) кокаина определяется в течение 8–12 ч, а БЭ 48–72 ч при использовании иммуноферментного метода анализа и 96–144 ч радиоиммунным методом.
В общем случае время определения в моче при пределе обнаружения ПрО=50 нг/мл: кокаина – 12–24 (не более 36) ч, метаболитов – 2–3 дня. При ПрО=15 нг/мл БЭ может детектироваться до 5–7 дней.
В первые 10–12 ч после приема кокаина для подтверждения факта его потребления (после положительного результата скрининга пробы мочи) рекомендуется анализировать МЭ, концентрация которого превышает или равна концентрации БЭ, а мочевая экскреция более медленная. Начиная с 10 ч, МЭ выводится быстрее, чем БЭ, а в интервале 40–60 ч определяется только БЭ. С уменьшением введенной дозы кокаина до 38 мг время детектирования МЭ уменьшается до менее 30 ч.
Ориентировочный расчет момента приема кокаина по результатам анализа мочи на содержание кокаина и метаболитов (для разового употребления кокаина).
Основываясь на количественном содержании кокаина и метаболитов в моче, в общем случае невозможно сделать какие–либо выводы относительно дозы принятого кокаина или времени последнего приема.Однако в случае однократного разового приема по относительным концентрациям кокаина, БЭ и МЭ в одной пробе мочи можно сделать ориентировочные заключения о длительности периода времени, прошедшего с момента принятия последней дозы кокаина. ■ Кокаин детектируется в первые несколько часов после последней дозы: обычно 1–6 ч. ■ Если кокаин обнаружен, а отношения концентраций МЭ/КОК или БЭ/КОК превышает 100, то доза принята более чем 10 ч назад. ■ Если отношение концентраций МЭ/КОК менее 100, то доза была принята менее 10 ч назад. Дополнительное доказательство этому – отношение концентраций МЭ/БЭ более 1. ■ Если значение концентраций МЭ и ВЭ приблизительно одинаковы (отношение концентраций МЭ/БЭ превышает 0,5) – Доза принята в интервале последних 20 ч. ■ Если отношение концентраций МЭ/БЭ менее 0,5 – с момента последнего приема прошло более 20 ч. ■ МЭ обычно не детектируется, если с момента приема последней дозы прошло более 48 ч. ■ Если МЭ детектируется, а отношения концентраций МЭ/БЭ ниже 0,1 – то последний прием был более 48 ч назад.
При повторных введениях кокаина в течение длительного периода (нескольких часов) количественные соотношения метаболитов в моче иные и представленные закономерности не соблюдаются.
Стабильность кокаина в биологических образцах
В крови трупа в результате различных причин рН крови может снижаться до 5,5–6,0, что замедляет или останавливает скорость химического гидролиза кокаина в БЭ и МЭ в Э. Скорость энзимного гидролиза после смерти или при хранении проб может снижаться по отношению к значениям, характерным для живого организма, но это снижение незначительно и энзимный гидролиз может протекать, в то время как химический замедлился или остановился. Эти изменения ведут к накоплению МЭ, уменьшению кокаина и сохранению БЭ на постоянном уровне в трупе или в хранящихся образцах. Для подавления энзимного гидролиза кокаина рекомендуется добавлять консерванты: 2% фторида натрия или органические фосфаты при рН 5 и хранить биологические образцы при температуре не выше 4°С. При этих условиях обеспечивается стабильность кокаина в течение 150 дней. Для сохранения проб мочи, содержащих кокаин и метаболиты, с целью подавления гидролитических превращений и искажения результатов анализа, рекомендуется хранить пробы в стеклянных несиланизированных сосудах в темноте в замороженном виде при – 15°С после установления рН 5,0 с помощью аскорбиновой кислоты. В этих условиях не происходит потерь кокаина до 110 дней хранения. При соблюдении тех же условий, с разницей в температуре хранения 4°С в отсутствие глубокого охлаждения постоянный уровень кокаина в пробе сохраняется в течение 4 нед. При хранении 8 проб мочи с исходным содержанием кокаина 232–18656 (среднее 5582) нг/мл в течение 12 мес при –20°С к концу срока концентрация изменилась до 154–15 601 (среднее 3547). Изменения составили от – 87 до +20%, в среднем отмечено уменьшение на 36%. Концентрация бензоилэкгонина при этом практически не изменилась: начальные значения 181–130 ООО (среднее 9 270), конечные 241–120 000 (среднее 8981) нг/мл.Глава 4. Марихуана
Cannabis sativa (каннабис) – повсеместно распространенная дикорастущая конопля, с давних пор, благодаря психоактивным свойствам, используемая для лечения, а также для достижения особого экстатического состояния как эйфоригенное и галлюциногенное средство.Еще в рукописных источниках XV века до IX. в Китайской фармакопее указывается на использование смолы каннабиса в качестве анестетика. В медицинских и культовых целях его применяли в Индии, затем в странах Среднего Востока и Северной Африки. Термин assassin принесен в Европу крестоносцами из арабских стран XI века: это вещество использовалось в сектах при совершении обрядов. В Европе и США каннабис становится популярным с XIX века как лекарственное и психоактивное средство. О нем пишут и изучают воздействие на организм человека. В США до 1942 г. препараты из конопли были разрешены для употребления в качестве лекарственных средств, входили в Фармакопею США и продавались в аптеках как средства широкого профиля.
Конец XIX и начало XX в. характеризуются ростом популярности марихуаны и значительным увеличением ее коммерческой продажи. Борьба на правительственном уровне ведется с 1930 г, когда Федеральные органы США по борьбе с распространением наркотиков добиваются принятия Закона, запрещающего не только выращивание конопли и коммерческую продажу, но и употребление изготавливаемых из нее препаратов. Многие штаты поддерживают этот закон. Однако, несмотря на заявления административных органов, научных институтов и организаций, накопивших достаточно фактов негативного медицинского и социального влияния наркотика, в обществе долгое время сохранялось устойчивое мнение о безопасности использования марихуаны и отсутствии привыкания. Марихуану выделяют в класс «мягких» наркотиков, в отличие от «тяжелых» (героина). В общественном сознании укрепляется мнение об использовании марихуаны как социально приемлемого факта. Игнорирование опасности для здоровья и отсутствие запрета на фактическую популяризацию курения марихуаны в кино– и видеопродукции привели к повсеместному распространению марихуаны среди американских подростков, включая учебные заведения различного ранга. Динамика употребления марихуаны в молодежной среде в США показывает пик, приходящийся на 1960–1970 гг. В последующие годы отношение общества к этой проблеме коренным образом изменилось, миф о ее безвредности рассеивается, и большинство исследователей утвердились во мнении, что марихуана, хотя и проявляет более низкую тенденцию к продуцированию психической и физической зависимости, все же может вызывать наркотическое пристрастие и оказывать 104 вредное воздействие на ментальные, эмоциональные и физические функции организма. В результате совместных усилий различных государственных и общественных организаций по борьбе с распространением марихуаны в период 1975–1993 гг. отмечено некоторое снижение ее употребления в среде студентов высших курсов. Вместе с тем она остается одним из наиболее часто употребляемых наркотиков молодежью США. Дискуссия о легализации препаратов из каннабиса с целью использования в медицине в качестве лекарственных средств и в качестве «мягкого» наркотика для наркоманов продолжается, несмотря на серьезность выдвигаемого аргумента о наличии опасности перехода к другим, «тяжелым» наркотикам, героину или кокаину.
До 1992 г. в США марихуана была помещена в Список № 2, что означало возможность ограниченного использования с медицинскими целями (в основном для больных СПИДом, онкологическими заболеваниями и глаукомой). Но с 1992 г. только основной психоактивный ингредиент марихуаны: тетрагидроканнабинол (ТГК), легально производимый в США, разрешен в некоторых странах (США и Германия) к использованию в медицине под контролем и в основном для лечения глаукомы и токсикоза раковых больных, прошедших курс химиотерапии: препараты Дронабиол (Маринол) и Набинол (Цезамет). В Нидерландах и Испании выращивание небольшого количества конопли и использование ее для собственных нужд не преследуется законом. В настоящее время каннабис, его препараты и все изомеры ТГК входят в Список № 1 Постоянного Комитета по наркотикам РФ, что запрещает использование с любыми, в том числе медицинскими целями.
Формы, используемые в нелегальной продаже
Марихуана – высушенная и измельченная верхняя часть растения с листьями и цветками, содержание в которых активных веществ наиболее высоко. Содержание психоактивных веществ в марихуане доходит до 13–15% (ранее эти величины были значительно ниже 0,5–11%).Гашиш (hash) – смола (смолка), производимая каннабисом (cannabis sativa) в определенный период вегетации, зеленого, темно–коричневого или черного цвета. Содержание основного психоактивного вещества (ТГК) обычно около 2%, но может достигать и 9–10%.
Гашишное масло – концентрированный темный жидкий и вязкий по консистенции экстракт растительного материала или смолы каннабиса с содержанием психоактивных веществ (ТГК) от 10 до 30–60%.
Биологическая активность этих средств при хранении в этаноле или в кунжутном масле сохраняется долгое время, но при хранении на свету или при доступе кислорода со временем уменьшается из–за деградации основного активного компонента.
Способы употребления ■ курение (вдыхание дыма) – для курения используют сигареты с марихуаной (500–750 мг при содержании активного компонента ТГК 1–4%) или обычные табачные сигареты с добавкой гашиша или небольшого количества гашишного масла. Иногда для курения используют особые стеклянные трубки. Гашишное масло добавляют и в обычные табачные сигареты и в сигареты с марихуаной или курят с применением небольших стеклянных трубок. Также распространено вдыхание паров масла, нагреваемого в пламени на алюминиевой фольге или на лезвии ножа. ■ оральное потребление (жевание, в виде заварки или как добавка к пище). ■ внутривенное введение применяют редко.
Производство и свойства продуктов каннабиса
I. Растительные продукты: марихуана
Вследствие широкого распространения каннабиса (Cannabis sativa L.) большинство стран мира в умеренных и тропических зонах нелегально выращивают и продают растительные продукты, производимые из каннабиса. Формы этих продуктов весьма разнообразны и меняются не только от региона к региону, но и в пределах различных местностей одного региона.Наибольшее количество психоактивных компонентов содержится в цветущих и плодоносящих верхушках растения каннабис. Эти части заготавливают и используют для производства высококачественных запрещенных продуктов, поступаемых в нелегальный оборот. Обычно их срывают с растения, оставляя нетронутой остальную его часть. Нижние листья («капуста»), центральный стебель и основные боковые побеги не используются. Второй способ предусматривает заготовку целого растения. Центральный стебель срезается над самыми нижними боковыми побегами с листьями.
Срезанные части или целое растение сушат на воздухе либо на земле, либо в плоских поддонах, либо подвешивая их цветками вниз. Если заготовляли растение целиком, то после высушивания цветущие верхушки, содержащие активные компоненты, отделяют от центрального и боковых стеблей. Далее высушенный растительный материал может поступать в нелегальный оборот без обработки (Центральная и Южная Африка, Юго–Западная и Юго–Восточная Азия) или, чаще, после придания ему соответствующей формы, в зависимости от способа обработки, принятого в данной местности. Материал прессуют, придавая ему форму блоков (характерно для регионов Западной Африки и Карибского бассейна), реже свертывают в виде кукурузного початки и заворачивают в грубое растительное волокно (Центральная и Южная Африка).
Для стран Юго–Восточной Азии характерен продукт высокого качества, изготавливаемый исключительно из цветущих и плодоносящих верхушек, которые обвязывают бечевкой вокруг бамбукового стержня, придавая им форму палочек. Эти палочки, известные на нелегальном рынке как «Палочки Будды», весят около 2 г и имеют в длину примерно 8 см. При транспортировке их связывают по 20 штук. Для Южно–Африканского региона характерен аналогичный высококачественный продукт значительно меньшего объема в виде небольших рулончиков, обернутых коричневой бумагой. В каждом рулончике содержится менее 0,5 г каннабиса. В некоторых образцах содержатся семена, что снижает качество продукта.
Продукт высокого качества, изготавливаемый из цветущих верхушек, не должен содержать семян, частей стебля и растительных волокон, т.е. тех частей каннабиса, которые бедны активными компонентами или не содержат их вовсе. Это достигается в операции просеивания высушенного растительного материала. Полученный тонко измельченный порошок (название на сленге «Kif») имеет высокое содержание смолы и легко прессуется в плитки. Это характерный продукт Северной Африки.
Другой высококачественный продукт носит название «Sinsemilla» (в переводе с испанского означает «без семян») и производится исключительно в Америке из растений, не производящих семян. Это достигается особым приемом культивирования каннабиса, заключающимся в том, что в определенный период вегетации, до созревания пыльцы, с плантации удаляются все мужские растения и остающиеся женские не производят семян. При таком способе культивирования значительно повышается уровень психоактивных компонентов (особенно ТГК) в смолосодержащих частях растения.
Растительные продукты, изготавливаемые из каннабиса, весьма разнообразны. Тем не менее выделяют несколько типов, отличных по внешнему виду (форме, цвету, физическому составу) и химическому составу и характерных для того или иного региона. 1. Каннабис умеренного климата. Культивируется в Европе, Северной Америке, Южных районах Южного полушария. Имеет ярко–зеленую листву, которая после сбора становится желтой или, реже, коричневой. Цветущие верхние части растений при сжимании в руках не выделяют клейких веществ смолы. В продуктах этого типа, особенно из Европы, содержится заметное количество листового материала. Химический состав. Содержание ТГК, КБД (каннабидиола) и ТГВ (тетрагидроканнабиварина) изменяется в широких пределах.
Таблица 1. Виды продуктов каннабиса.
| Тип | Регион | Свойства |
|---|---|---|
| 1. Марихуана: 0,5–5% ТГК | ||
| Каннабис умеренного климата | Европа, Сев. Америка | Растительный материал желтого или коричневого цвета. Содержит семена и листья. Качество невысокое. |
| Каннабис тропического климата | Северная Африка | Тонко измельченный травяной порошок светло–зеленого или желто–зеленого цвета. Встречается также в виде блоков или плиток. Семена и волокно отсутствуют. Качество очень высокое. |
| Тот же | Зап. Африка и Карибский бассейн | Растительный материал прессуется в блоки. Цвет зеленый или коричневый. Содержит семена, части стеблей, волокно. Качество невысокое. В последние годы встречаются более качественные образцы. |
| Тот же | Центральная Африка | Растительный материал в обычном виде или завернутый подобно початку. Цвет зеленый или коричневый. Содержит семена и волокнистые материалы. Качество невысокое. |
| Тот же | Южная Африка | Растительный материал в обычном виде, а также свернутый в виде початка или рулончика. Цвет: зеленый, желтый или коричневый. Содержит листья. Качество невысокое. |
| Тот же | Южная Америка | Продукт, произведенный из сорта «синсемилла», очень высокого качества. Встречается продукт, подобный продукту Карибского бассейна, иногда очень низкого качества. |
| Тот же | Индийский субконтинент | Три вида продукта: 1. Очень высокого качества. Состоит из цветущих верхушек коричневого цвета, липкий на ощупь. 2.Продукт более низкого качества от темно–зеленого до коричневого цвета.3.Продукт из зеленого листового материала без цветков с низким содержанием ТГК–Качество невысокое. |
| Тот же | Юго–вост. Азия | Растительный материал в обычном виде. «Палочки Будды». Качество очень высокое. |
| 2. Гашиш: 2–10% ТГК | ||
| Гашиш стран Средиземноморья | Сев. Африка | Тонкие пластины желто–коричневого цвета, обернутые целлюлозой. |
| Тот же | Вост. Средиземноморье | Пластины, завернутые в ткань или порошок красно–коричневого цвета. |
| Тот же | Сев.–вост. Средиземноморье | Порошок зелено–коричневого цвета или, редко, тонкие пластины в целлофане. |
| Гашиш Индийского субконтинента | Индийский субконтинент | Продукт, спрессованный в брикеты или прямоугольные пластины, снаружи черного цвета, внутри темно–зеленые. Редко в форме палочек, шариков или неправильной формы. |
| 3. Гашишное масло: 1–60% | ||
| Гашишное масло Средиземноморья | Страны Средиземноморья | Экстракт смолы. |
| Гашишное масло Индийского субконтитента | Индийский субконтинент | Экстракт смолы. |
| Гашишное масло Карибского бассейна | Карибский бассейн | Экстракт растительного материала. |
II. Смола каннабиса: гашиш
Производство смолы сосредоточено в двух основных регионах: Южное и Восточное Средиземноморье и регион Индийского субконтинента. Различие их внешних признаков и химического состава позволяет продукт каждого региона выделить в отдельный тип.Тип I. Гашиш стран Средиземноморья. Обработка растительного материала заключается в обмолачивании для отделения не выделяющих смолу частей, мало значимых с точки зрения содержания психоактивных компонентов. В этом процессе частицы смолы, листьев и семена отделяются от основной массы волокнистого материала. В результате дальнейшей обработки – просеивании удаляются семена и оставшиеся волокнистые частицы, и продукт приобретает вид тонко измельченного порошка, в котором растительные компоненты обнаруживаются только при микроскопическом исследовании. Далее материал прессуют в пластины, предварительно поместив в ткань (Восточное Средиземноморье) или обернув в целлюлозу (Северная Африка). В некоторых случаях продукт поступает в нелегальную торговлю просто в виде порошка (Северо–Восточное Средиземноморье). 1.1. Северная Африка. Продукт представляет собой желто–коричневые тонкие прямоугольные пластины, обернутые в целлофан. Редко маркируются, но иногда имеют отпечатки монет. Недавно появился продукт, похожий на смолу Индийского субконтинента. Он имеет форму блоков туалетного мыла, завернут в целлофан, с поверхности почти черный, а внутри гораздо темнее, чем обычные желто–коричневые брикеты. Некоторые образцы имеют отпечатки монет, но в основном маркировка отсутствует. Химический состав. Относительно ТГК содержание КБД низкое. Также очень низко содержание ТГВ. Каннабиноидные кислоты присутствуют в вариабельных количествах. 1.2. Восточное Средиземноморье. Это красно–коричневый спрессованный порошок, который для транспортировки помещается в тканевые мешочки, ранее исключительно из белой ткани иногда с чернильной печатью. В настоящее время мешочки могут быть из яркой ткани с или без печати. При разворачивании на смоле остается отпечаток тканевых волокон. Вес до 0,5 кг, иногда до 1 кг. Химический состав. Содержание КБД и кислот, главным образом, каннабидиоловой кислоты, больше, чем в других видах смолы, а ТГВ, напротив, очень низкое. 1.3. Северо–восточное Средиземноморье. Зеленовато–коричневый порошок или в редких случаях имеет вид небольших тонких пластин, завернутых в целлофан. Химический состав. КБД присутствует в гораздо меньшем количестве, чем ТГК. Содержание ТГВ низкое. Но высоко содержание каннабиноидных кислот.
Тип.2. Гашиш индийского субконтинента. Каннабис этого типа отличается высоким содержанием смолы, из–за чего цветущие верхушки растения наощупь липкие. Выделение смолы из растения основано на процессах растирания или трения, хотя это более трудоёмкий и длительный процесс, чем обмолачивание. При растирании цветков между ладонями смола остается на руках и может быть затем счищена тупым металлическим лезвием. Остающийся растительный материал используется затем как продукт второго сорта, например, для приготовления настоев. Собранная в достаточном количестве смола затем прессуется в плитки или скатывается в стержни, шарики или ей придается иная произвольная форма. Для извлечения смолы применяют и другие приемы, например, с помощью резиновых, кожаных и т.п. пластин. Второй способ состоит из последовательных операций сбора верхушек растения, высушивания, ручного размалывания в грубый порошок и просеивания. Образующийся тонкий порошок зеленого цвета хранится в кожаных сумках в течение 4–5 мес до жаркой погоды и затем выставляется на солнце для выплавления смолы. После выдерживания в течение нескольких дней порошок растирают деревянными скалками и выступающую на поверхности смолу собирают и прессуют в пластины. В некоторых местностях используют обработку собранного растительного материала кипящей водой, в процессе которой смола извлекается и после охлаждения выделяется в виде затвердевшего слоя на поверхности воды. Смола снимается и формуется в брикеты. Однако из–за наличия в смоле воды при хранении брикеты быстро становятся хрупкими и рассыпаются. Смола этого типа представлена в нелегальной продаже разнообразными видами продукта. Преобладающим является вид, производимый в Северо–Восточной части региона: завернутые в целлофан прямоугольные (иногда квадратные) пластины, черные на поверхности и темно–зеленые внутри. Часто на поверхности имеется рельефная маркировка. Толщина пластин различна: от 5 до 20 мм. Типичный вес 0,25, 0,5 и 1 кг, но может быть и выше. Свежий материал имеет характерный запах и обладает пластичностью, которая утрачивается по мере хранения: старые образцы смолы хрупкие и ломкие. Пластины из Северных районов Индийского субконтинента часто плохого качества: заплесневелые и легко крошатся. Другие виды продуктов из смолы этого типа включают: палочки, часто в связках по несколько штук, небольшие шарики диаметром 1 см или большие диаметром 8 см, а также кусочки неправильной формы. Все они имеют темно–коричневый или черный поверхностный слой и темно–зеленый или темно–коричневый внутренний. Химический состав очень изменчив. Содержание каннабиноидных кислот ниже, чем в смоле Средиземноморья. Содержание КБД сильно варьирует, оно может быть очень низкое и в некоторых видах КБД отсутствует. Содержание ТГВ также в основном низкое.
III. Жидкие продукты каннабиса: гашишное масло
Гашишное масло – это концентрированный экстракт растительного материала или смолы. Продукт наиболее удобен для транспортировки из–за возможности перевозки малых объемов и отсутствия запаха, поскольку масло расфасовывают в небольшие герметичные контейнеры или фармацевтические капсулы. Процесс получения масла подобен экстракции в аппарате Сокслета или в кофеварках. Основными производящими регионами являются Средиземноморье и Индийский субконтинент (из смолы) и Карибский бассейн (из травы каннабиса).Гашишное масло – темная вязкая жидкость с характерным запахом. При разбавлении органическими растворителями оно приобретает зеленое или коричневое окрашивание. Цвет зависит от исходного продукта (травы или смолы), зрелости исходного материала и растворителя. Масло нельзя разбавлять водой из–за возможности образования эмульсии. Иногда в продажу поступает неконцентрированный продукт зеленого или коричневого цвета с консистенцией и запахом использованного органического растворителя.
Химический состав гашишного масла качественно подобен составу растительных продуктов или смолы, производимой в данном регионе, однако не содержит каннабиноидных кислот. Количественное содержание компонентов в масле за счет концентрирования гораздо выше. Анализ состава гашишного масла позволяет в некоторой степени идентифицировать источник его производства.
Химический состав марихуаны
Марихуана – исходный продукт, получаемый из листьев и цветков верхних частей растения каннабис, содержащих микроскопические капсулы со смолой. После высушивания марихуана содержит более 400 компонентов. При курении в результате пиролитических превращений они трансформируются в 2000 химических веществ.Более 70 из 400 ингредиентов марихуаны составляют группу каннабиноидов, биологически активных веществ особого строения, встречающихся исключительно в растении каннабис (рис. 1). Основной компонент, ответственный за психоактивные свойства марихуаны, транс–дельта–9–тетрагидроканнабинол (ТГК). Но суммарный эффект действия марихуаны определяется всеми активными каннабиноидами. Дельта–8–ТГК, содержание которого гораздо ниже ТГК (по некоторым данным дельта–8–ТГК в свежесобранном материале вообще отсутствует ), имеет такую же активность, как и ТГК. Каннабинол (КБН) в десять раз менее активен, чем ТГК, каннабидиол (КБД) – не обладает психоактивными свойствами. Содержание ТГК как и других каннабиноидов (рис. 2) зависит от вида растения. В индийской разновидности конопли, помимо транс–дельта–9–ТГК, в заметных количествах присутствуют: аналог ТГК с пропиловой боковой цепью дельта–9–тетрагидроканнабиварин (ТГВ) и каннабидиол, в меньшем количестве – каннабидиварин, каннабихромин, цис–дельта–9–ТГК, каннабиварин и каннабинол.
 Рис. 1. Основные каннабиноиды. 1. дельта–9–тетрагидроканнабинол (ТГК) 2. дельта–8–ТГК 3. каннабинол 4. каннабидиол.
Рис. 1. Основные каннабиноиды. 1. дельта–9–тетрагидроканнабинол (ТГК) 2. дельта–8–ТГК 3. каннабинол 4. каннабидиол.
В следовых количествах – каннабигерол, каннабициклол и бутиловые аналоги ТГК, КБН и КБД. Подобно ТГК каннабинол и каннабидиол имеют в качестве заместителя в ароматическом ядре пятичленную углеводородную цепь. Пропиловые гомологи КБН и КБД: каннабиварин и каннабидиварин составляют от 0 до 20% от их суммарного содержания. На гомологи с бутиловым заместителем приходится менее 1% от суммы КБН и КБД. Кроме нейтральных каннабиноидов, присутствуют различные каннабиноловые кислоты, особенно в формах смолы и масла.
Помимо каннабиноидов, в состав марихуаны входит множество веществ других классов: терпены, стероиды, углеводы, фенолы, карбоновые кислоты, азотсодержащие соединения, алкалоиды и др.
По некоторым данным, дельта–8–ТГК в свежем растительном материале отсутствует, но изомеризация Д–9–ТГК в Д–8–ТГК проходит очень легко.
Действие каннабиноидов на клетки организма
Все каннабиноиды жирорастворимые вещества и накапливаются в тканях, богатых липидами: мозге, легких, половых органах, а также в клеточных мембранах. Проникая через стенки мембран в ядра клеток, каннабиноиды вызывают изменения в биохимических процессах и клеточном метаболизме, нарушая процессы синтеза ДНК, РНК и клеточных белков. В результате клеточная активность падает или останавливается, что имеет следствием подавление соответствующей функции организма. Рис. 2. Структура некоторых каннабиноидов. 1. Бутиловый аналог ТГК. 2. Тетрагидроканнабиварин. 3. Бутиловой аналог каннабинола. 4. Каннабиварин. 5. Бутиловый аналог каннабидиола. 6. Каннабидиварин. 7. Каннабихромин. 8. Каннабициклол.
Рис. 2. Структура некоторых каннабиноидов. 1. Бутиловый аналог ТГК. 2. Тетрагидроканнабиварин. 3. Бутиловой аналог каннабинола. 4. Каннабиварин. 5. Бутиловый аналог каннабидиола. 6. Каннабидиварин. 7. Каннабихромин. 8. Каннабициклол.
Обладая липофильными свойствами, после введения й организм каннабиноиды аккумулируются в жировой ткани. Высвобождение в систему кровообращения происходит медленно, в результате чего они могут обнаруживаться в организме в течение длительного периода времени даже после однократного употребления.
Эффекты, возникающие при употреблении марихуаны
Марихуана оказывает на организм стимулирующее и седативное воздействие, дополняемое при более высоких дозах галлюциногенными эффектами.Физиологические эффекты марихуаны ■ опухание слизистой глаз, воспаленные глаза ■ учащение пульса, усиление сердцебиения ■ повышение кровяного давления ■ нарушение двигательной функции ■ расслабленность ■ колебания температуры тела ■ головная боль ■ головокружение ■ тошнота ■ ощущение голода.
Поведенческие эффекты марихуаны ■ релаксация ■ снижение психомоторной активности ■ ухудшение концентрации внимания, нарушение способности правильно оценивать расстояние ■ снижение способности к вождению автомобиля и другой деятельности, требующей внимания ■ быстрая речь, безудержная болтливость.
Эмоциональные эффекты ■ эйфория, чувство благополучия ■ беззаботное состояние ■ чередование с состоянием тревоги и беспокойства.
Нервно–психические эффекты ■ ухудшение краткосрочной памяти, понимания, способности выполнения какой–либо задачи ■ изменение восприятия времени и пространства ■ повышенная тактильная чувствительность ■ обострение зрительного и слухового восприятия, обоняния ■ снижение болевого барьера ■ изменения в сфере сексуальных эмоций ■ галлюцинации ■ потеря осознания себя как личности, деперсонализация ■ психоз (при высоких дозах).
Токсические проявления высоких доз ■ сведение мышц ■ беспокойство ■ подозрительность ■ бред ■ паранойя ■ паническое состояние ■ нарушение мозгового кровообращения ■ затруднения с речью ■ возвратные галлюцинации (иногда после 6 месяцев воздержания)
Последствия длительного употребления марихуаны для различных систем организма
■ Мозг – Марихуана влияет на мыслительные способности, способность к пониманию, абстрактному мышлению, обучению и на ближнюю память. В зависимости от силы средства и восприимчивости потребителя она может вызвать состояние паники, беспокойство и токсические психозы. Долговременное потребление может привести к структурным и функциональным изменениям. ■ Легкие – Курение марихуаны вызывает все вредные эффекты, свойственные табакокурению: бронхиты, фарингиты, синуситы, рак легких. Марихуана в большей степени, чем табак, способствует развитию заболеваний верхних дыхательных путей и отеки. ■ Сердце – Использование марихуаны вызывает усиленное сердцебиение, учащение пульса и повышение кровяного давления. Курение марихуаны особенно опасно для людей, страдающих сердечными недугами. ■ Система репродуцирования (мужчины) – Курение снижает содержание тестостерона, основного мужского гормона. Упорное и продолжительное применение может изменить гормональный фон настолько, что нарушается развитие половой функции подростков.. В тяжелых случаях наблюдается уменьшение числа сперматозоидов и их подвижности, и увеличение числа анормальных клеток в сперме. ■ Система репродуцирования (женщины) – Каннабиноиды накапливаются в женских репродуктивных органах. Изменения мозговой деятельности может привести к нарушениям овуляции и уменьшению плодовитости. Каннабиноиды могут оказывать токсическое действие на развитие плода, вызывая отклонения при вынашивании, тяжелое протекание родов и раннюю смерть младенцев. Так называемый, «Фетальный синдром марихуаны», характеризующийся снижением веса рожденных детей и отклонениями развития, наблюдается в 5 раз чаще, чем «Фетальный алкогольный синдром». Вместе с молоком матери каннабиноиды переходят в детский организм при кормлении. ■ Двигательные функции – Курение марихуаны может оказывать влияние на умственные и физические реакции, нарушать координацию и увеличивать время реакции. Нарушается ответная реакция человека на световые и звуковые сигналы, ухудшается способность к выполнению последовательных операций и степень восприятия. Появляется сильная потребность двигаться, ходить, разговаривать, характерны неестественные позы в состоянии покоя ■ Другие системы организма – хроническая усталость, головные боли, тошнота.Социальные последствия длительного употребления: ■ социальная самоизоляция. ■ переход к более «тяжелым» наркотикам. ■ связь с преступностью.
Толерантность и зависимость
Противоречивость имеющихся у специалистов данных ведет к тому, что до сих пор ведется дискуссия о толерантности и зависимости как неизбежных следствиях употребления марихуаны. Принято, что толерантность развивается ко многим эффектам марихуаны и наиболее вероятна при длительном употреблении больших доз.Физическая зависимость – относительно слабая и развивается не всегда, поэтому синдром отмены также не выраженный. Психическая зависимость – сильная при хроническом употреблении.
Синдром отмены
Длительность синдрома отмены – от нескольких часов до 4–5 дней. ■ тошнота ■ диарея ■ потеря аппетита, потеря веса ■ озноб и потливость ■ тремор ■ нестерпимые боли ■ бессонница ■ раздражительность ■ тревожное состояние ■ депрессия ■ затемненное сознаниеФармакокинетические свойства
Минимальная доза ТГК 5 мг, эффективная оральная доза 50–200 мкг/кг веса, эффективная доза при курении 25–50 мкг/кг. Токсичная доза 0,035 мг/кг (сильно зависит от толерантности). Продаваемые «на улицах» сигареты содержат обычно 300–750 мг марихуаны с долей ТГК от 0,5 до 11 % (иногда до 13–15%, в редких случаях – выше). Обычная суточная доза: 2 сигареты в день (около 40 мг ТГК). В процессе курения значительная доля ТГК подвергается термической деструкции. При глубоком вдыхании и длительной задержке в легких (20–30 с) до 50% ТГК попадает в систему кровообращения, в среднем биодоступность при курении определяется интервалом 10–23%. Связывание ТГК с липопротеинами около 97%.Всасывание
При курении и внутривенном введении концентрационные профили ТГК в плазме подобны, но в случае курения концентрация вдвое меньше, хотя эта величина сильно зависит от умения курильщика (продолжительности затяжки, объема ингаляции, задержки вдоха после ингаляции). ТГК поступает в систему кровообращения за нескольких минут, достигая максимума концентрации в плазме в течение 5–30 мин. Последующее уменьшение до 1–3 нг/мл происходит за 3–5 ч. Кинетика выведения из плазмы описывается согласно модели двухфазного элиминирования: «быстрое» – в течение примерно 40 мин, «медленное» – до 24 ч. Интервал концентрации в крови 226 лиц, потребителей марихуаны, составляет 0–113 нг/мл при среднем значении 15,4 нг/мл. Максимум психологического эффекта (high) соответствует максимальной концентрации в крови. T½ ТГК в плазме для «быстрой» и «медленной» фазы 3–4,5 мин и около 20 ч соответственно.Распределение
Обладая липофильными свойствами, после поступления в организм ТГК быстро покидает кровяное русло, распределяясь в тканях, богатых липидами: жировых отложениях, мозге, легких, половых органах, клеточных мембранах. Объем распределения 10 л/кг. Детектируемые количества ТГК в жировых отложениях организма, взятых методом биопсии у хронических курильщиков марихуаны, обнаруживаются спустя более четырех недель после сеанса курения и составляют 0,4–8 нг/г. Количество ТГК в жире зависит от дозы, частоты приема и индивидуальных особенностях организма.Изучение распределения ТГК в органах (смерть, связанная с потреблением марихуаны) показало содержание ТГК в жировых отложениях 657 нг/г, что от 6 до 355 раз превышает содержание в крови, моче и других тканях организма.
Аккумулированный ТГК медленно возвращается в систему кровообращения и может быть определен высокочувствительными методами в крови в течение нескольких часов после выкуривания 1 сигареты или инъекции одной разовой дозы.
При регулярном курении 2 сигарет в неделю в течение 6 мес следовые количества ТГК могут быть обнаружены спустя несколько недель после прекращения курения.
Метаболизм
Поскольку высвобождение ТГК из мест депонирования в кровяное русло, где подвергается биотрансформации, происходит медленно, то лимитирующей стадией метаболизма является процесс перераспределения ТГК из тканей в кровь. Есть указания на различие метаболизма в легких, где проходит начальная стадия биотрансформации ТГК при курении, и в печени.Пути биотрансформации ТГК в организме человека: ■ гидроксилирование аллильной и алифатической групп. ■ окисление до кислот, альдегидов, кетонов. ■ конъюгирование с глюкуроновой кислотой или насыщенными кислотами. ■ эпоксидирование двойной связи. ■ восстановление терпеновой двойной связи.
В организме человека основной путь метаболизма ТГК – быстрое окисление углерода аллильной группы энзимной системой печеночного цитохрома Р450 до первичного психоактивного короткоживущего 11–гидрокси–дельта–9–тетрагидроканнабинола (11–ОН–ТГК), который далее под действием алкогольдегидрогеназы окисляется в конечный биологически неактивный продукт: 11–нор–дельта–9–тетрагидроканнабинол–9–карбоновую кислоту (ТГК–СООН). Начальный продукт биотрансформации 11–ОН–ТГК обладает равной с ТГК активностью или превышает ее. Пиковая концентрация 11–ОН–ТГК в плазме гораздо ниже, чем исходного ТГК. В моче 11–ОН–ТГК обычно не обнаруживают.

 Рис. 3. Структура ТГК–СООН и метаболитов.
Рис. 3. Структура ТГК–СООН и метаболитов.
Продукты метаболизма: монозамещенные гидрокси– и карбоксипроизводные, диолы, триолы, гидроксикислоты, гидроксикетоны, замещенные гексагидроканнабинолы. Идентифицировано более 75 мочевых метаболитов (см. рис. 3).
Основные метаболиты ТГК: ■ ТГК–СООН ■ 11–ОН–ТГК.
Минорные метаболиты ТГК: ■ 8β–ОН–ТГК ■ 8α–ОН–ТГК ■ 8β,11–ди–ОН–ТГК ■ 8α,11–ди–ОН–ТГК.
Биологической активностью обладают 11–ОН–ТГК и 83–ОН–ТГК.
Следовые метаболиты ТГК: ■ моно– и дикарбоксипроизводные (в том числе бокового пентилового заместителя с укорачиванием длины углеродной цепи) ■ продукты гидроксилирования боковой пентиловой цепи (4“–ОН–ТГК–СООН).
Конъюгаты: гидроксилированные и карбоксилированные метаболиты далее на 75–80% конъюгируются в соответствующие глюкурониды и сульфаты.
В крови ТГК–СООН присутствует в значительной степени в неконъюгированной виде. Уже спустя 30 мин после курения ее концентрация в плазме превышает концентрацию неизмененного ТГК. Интервал концентрации ТГК–СООН в крови для 226 хронических курильщиков марихуаны 0–292 (среднее 35,2) нг/мл (как приводилось ранее, для ТГК интервал от 0 до 113 (среднее 15,4) нг/мл).
После разового сеанса курения обычной дозы марихуаны содержание ТГК–СООН в плазме в интервале 1–5 ч превышает содержание ТГК в 1,3–3,4 раза, что предлагается использовать в качестве теста на относительно недавнее курение марихуаны.
Таблица 2. Содержание ТГК и метаболитов в биожидкостях после курения, нг/мл (две сигареты с суммарным содержанием ТГК 150 мкг/кг, приведены средние значения для 10 лиц).
| Время, мин | Плазма | Время, ч | Моча | |||
|---|---|---|---|---|---|---|
| ТГК | 11–ОН–ТГК | ТГК–СООН | ТГК–СООН | 8β,11–ди–ОН–ТГК | ||
| 5 | 80 | 5,9 | 7,0 | 0–4 | 17.1 | 56,2 |
| 10 | 83,9 | 20,8 | 11,9 | 4–6 | 31,4 | 16,3 |
| 20 | 52,1 | 20,2 | 18,2 | 6–12 | 24,2 | 4,7 |
| 30 | 38,9 | 18,5 | 31,4 | 12–18 | 16,0 | 2,6 |
| 50 | 27,6 | 12,7 | 35,6 | 18–22 | 6,0 | 0.7 |
| 65 | 16,6 | 9,5 | 24,4 | |||
| 2 час | 9,7 | 6.6 | 15,1 | |||
| 3 час | 4,9 | 3.3 | 12,5 | |||
| 4 час | 2,9 | 2,2 | 7,1 | |||
| 5 час | 1.1 | 0.7 | 3,6 | |||
| 22 час | не детектир. | 0,3 | 0.9 | |||
Таблица 3. Содержание ТГК и метаболита в крови хронических курильщиков марихуаны, курение 10 сигарет в неделю в течение 5 лет, приведены средние значения для 226 проб.
| Время с момента курения, часы | ТГК, нг/мл | ТГК–СООН, нг/мл |
|---|---|---|
| 0–2 | 31,6 | 45,2 |
| &4 | 23,8 | 44,7 |
| 5–6 ' | 27,6 | 51.2 |
| 7 и более | 7,5 | 19,9 |
Кинетика выхода ТГК из системы кровообращения практически одинакова для ингаляционного и инъекционного способов введения. Концентрация в крови короткоживущего метаболита 11–ОН–ТГК после ВВ 5 мг ТГК: 0,6–2,3 нг/мл (N=4), после курения 2 сигарет с общей дозой ТГК 20 мг: 0,3–20,8 нг/мл (N=10).
Таблица 4. Содержание ТГК и метаболита в крови после внутривенного введения 5 мг ТГК, нг/мл, среднее для N=4.
| Время, мин | ТГК | 11–ОН–ТГК |
|---|---|---|
| 10 | 70 | 0,9 |
| 20 | 60 | 1,5 |
| 30 | 25 | 2,2 |
| 40 | 10,3 | 2,3 |
| 60 | 10 | 1,6 |
| 90 | 8 | 0,8 |
| 1440 = 24 ч | 4 | 0,6 |
После курения марихуаны в крови обнаруживаются небольшие количества каннабинола, превышающие количества, найденные при внутривенном введении. По–видимому, в этом случае КБН образовался в результате термической ароматизации ТГК в процессе курения.
Выведение
Продукты мочевой экскреции ТГК практически полностью конъюгированы, поскольку они представляют собой гидрокси– и карбоксипроизводные ТГК.Основной метаболит: ■ ТГК–СООН–глюкуронид (ТГК–СООН–диглюкуронид). в меньшем количестве выделяются ■ ТГК–СООН свободный. ■ 11–ОН–ТГК–глюкуронид и 11–ОН–ТГК свободный ■ 8–β–ОН–ТГК ■ 8β11–ди–ОН–ТГК–глюкуронид и 8β11–ди–ОН–ТГК свободный. ■ ТГК–глюкуронид и ТГК–свободный. ■ большое количество не идентифицированных метаболитов кислого характера: гидрокси– и карбоксипроизводные, в том числе бокового алкильного заместителя, в следовых количествах: ■ каннабинол (КБН). ■ каннабидиол (КБД).
Концентрация метаболитов в моче меняется в широких пределах и зависит от дозы ТГК, частоты и периодичности потребления, времени отбора пробы мочи по отношению к последнему приему марихуаны, скорости высвобождения аккумулированных каннабиноидов из жировой ткани, количества жидкости, принятой до момента отбора пробы мочи и других факторов.
Содержание неизмененного ТГК в продуктах выведения мочой составляет всего менее 1 % дозы. При приеме 30 мг ТГК за 6 ч экскретируется в мочу 0,005% дозы неизмененного ТГК (среднее для четырех образцов). 15–20% дозы выводится в виде кислых метаболитов. Остальное количество аккумулируется в организме и медленно экскретируется в течение следующих нескольких дней. За 5 дней выводится 80–90% введенной дозы, из них только 20% с мочой и 65% с каловыми массами. При курении за 72 ч выводится в виде метаболитов 50% дозы, остальные 50% распределяются в организме и в течение нескольких дней выводятся с мочой (25%) и с калом (65%).
Основной продукт выведения – неактивный метаболит ТГК–кислота в виде моноглюкуронида и, возможно, диглюкуронида, хотя, по некоторым данным, фенольная группа ТГК–СООН конъюгированию не подвергается. ТГК–СООН присутствует также в молоке кормящих матерей, организме новорожденных, волосах и слюне потребителей препаратов, содержащих ТГК. Интервал общей концентрации ТГК–СООН в моче (среднее значение для более 200 проб мочи курильщиков марихуаны): от 5 до 580 нг/мл.
80,11–ди–ОН–ТГК выделяется в мочу в интервале меньшем 24 ч после момента курения и может служить маркером недавнего потребления марихуаны. Максимум концентрации приходится на период 0–4 ч, затем снижается до 10–20 нг/мл в интервале 4–6 ч.
Из кислых метаболитов в моче в частности идентифицированы: 4“,5“–биснор–ТГК–9,3“–ди–СООН и 4“–ОН–ТГК–СООН.
Присутствие следовых количеств КБН в моче объясняется его образованием из ТГК при курении в результате термического превращения. Кроме того, КБН может переходить в мочу как компонент каннабиса. В стандартных растворах ТГК содержание КБН может доходить до 0,3%. Второй важный компонент, входящий в состав растения, не обладающий психической активностью КБД широко метаболизируется, образуя многочисленные гидрокси– и карбоксипроизводные КБД и давая вклад в метаболизм, приписываемый ТГК.
При клиническом изучении выведения ТГК–СООН с мочой после курения шестью субъектами сигарет с содержанием ТГК 1,75 и 3,55% (15,8 и 33,8 мг ТГК) было показано, что максимум концентрации ТГК–СООН составляет в среднем 89,8 нг/мл при 7,7 час для малой дозы и 153,4 нг/мл при 13,9 ч для высокой дозы. За 7 дней с мочой выделилось в среднем 93,9 мкг (интервал 34,6–171,6 мкг) и 197,4 мкг (107,5–305 мкг), что соответствует примерно 0,54% введенной дозы для обоих вариантов. Время детектирования для метода с пределом обнаружения 15 нг/мл (ГХ/МС) – 33,7 ч и 88,6 ч после выкуривания одной сигареты, содержащей 15,8 и 33,8 мг ТГК, соответственно.
В табл. 5, 6 и 7 приведены данные по кинетике выведения ТГК и метаболитов 11–ОН–ТГК, ТГК–СООН и 8β,11–ди–ОН–ТГК после курения одной или нескольких сигарет с различным содержанием ТГК.
Таблица 5. Концентрация ТГК и метаболитов в моче после курения марихуаны, нг/мл. Курение 1 сигареты (753 мг) с 3,58% ТГК (26,9 мг ТГК), среднее значение для 8 образцов мочи, взятой в интервале от 5 мин до 8 час.
| Мин | Час | ТГК | 11–ОН–ТГК | ТГК–СООН |
|---|---|---|---|---|
| 5 | 1,5 | 13 | 60 | |
| 60 | 1 | 10 | 38 | 20 |
| 120 | 2 | 21 | 70 | 75 |
| 180 | 3 | 6,5 | 78 | 110 |
| 240 | 4 | 4 | 55 | 180 |
| 300 | 5 | 2,5 | 42 | 120 |
| 360 | 6 | 2 | 32 | 120 |
| 420 | 7 | 0 | 24 | 58 |
| 480 | 8 | 0 | 13 | 58 |
Таблица 6. Концентрация ТГК–СООН в моче после курения марихуаны, нг/мл. Каждая сигарета содержит 2,6% ТГК
| дни | час | 1 сиг. | 2 сиг. | 4 сиг. |
|---|---|---|---|---|
| 0 | 0 | 2,2 | 3,1 | 2,1 |
| 0,5 | 12 | 238 | 324 | 489 |
| 1 | 24 | 187 | 188 | 352 |
| 1,5 | 36 | 81 | 213 | 164 |
| 2 | 48 | 35 | 121 | 60 |
| 2,5–4,5 | 60–108 | около 20 | 69–30 | 187–24 |
| 5–6 | 120–144 | около 12 | 24–9 | 17–53 |
| 6,5–13,5 | 156–324 | 3–5 | 15–5 | 7–19 |
Особенности фармакокинетики при оральном способе введения препаратов ТГК
При оральном способе введения ТГК–содержащих препаратов фармакокинетика и профиль метаболизма в крови в течение первых часов заметно отличаются от установленных для курения или внутривенного введения.Всасывание гораздо более медленное и максимальный уровень ТГК в плазме достигается лишь через 1,5–3 ч после введения. Уровень концентрации ТГК в плазме ниже, а метаболитов ТГК–СООН и 11–ОН–ТГК значительно выше соответствующих величин для курения или ВВ. При этом содержание 11–ОН–ТГК превышает содержание ТГК.
Таблица 7. Зависимость мочевой экскреции метаболитов ТГК от способа введения, нг/мл. Суммарная радиоактивность определена после курения 1 сигареты, содержащей 19 мг меченого С–14–ТГК или орального введения 20 мг меченого С–14–ТГК, 1 и 2 – случайное, 3 и 4 – хроническое потребление.
| Время, час | Субъект 1 | Субъект 2 | Субъект 3 | Субъект 4 | ||||
|---|---|---|---|---|---|---|---|---|
| кур | ор | кур | ор | кур | ор | кур | ор | |
| 0–8 | 74 | 1443 | 607 | 2874 | 318 | 1348 | 464 | 24 |
| 8–12 | . | 591 | 315 | 1811 | 179 | 640 | 92 | 1723 |
| 12–24 | 84 | 454 | 93 | 303 | 169 | 69 | 117 | 360 |
| 24–48 | 22 | 209 | 59 | 281 | 31 | 38 | 33 | 90 |
| 48–72 | 20 | 81 | 36 | 139 | 23 | 21 | 20 | 60 |
| 72–96 | 10 | 42 | 17 | 175 | – | – | – | 24 |
| 96–120 | – | 19 | – | 112 | – | 11 | – | 14 |
Для мочевой экскреции эта разница менее заметна, но тем не менее концентрация ТГК–СООН (или суммы метаболитов) выше в случае орального потребления эквивалентной дозы ТГК. В табл. 7 приведены данные о выведении суммы метаболитов (определено по суммарной радиоактивности), полученные при курении и введении внутрь ТГК меченого изотопом С–14 [Неопределенное по данным таблицы 7 значение T½ мочевой экскреции суммы метаболитов составило 18,2 ч.
Пассивное курение
Ситуация с пассивным потреблением марихуаны (так называемое «пассивное курение») может возникнуть, когда некурящий находится в непроветриваемом замкнутом пространстве (автомашина или небольшая комната) одновременно с одним или несколькими курящими и длительность сеанса курения составляет по меньшей мере один час .За 8 ч «пассивного курения» некурящий получает ингаляционную дозу около 15 мкг ТГК. При этом в моче детектируются ТГК и ТГК–СООН, с концентрацией ТГК–СООН 4,4 нг/мл.
Различие случайного и хронического потребления
Большие запасы ТГК в тканях организма хронических потребителей марихуаны и других ТГК–содержащих продуктов ведут к непрерывному выходу ТГК в систему циркуляции крови и метаболизму. Поэтому в течение длительного времени после прекращения употребления этих продуктов ТГК–СООН выводится в мочу.Случайное потребление (менее двух раз в неделю). Пробы мочи “положительны” в течение 1–3 дней при пороге значимости результата иммунных методов скрининга (cut–off, ПЗР)50 нг/мл и в течение 2–6 дней при ПЗР 20 нг/мл, как и при подтверждении по метаболиту ТГК–СООН методами с пределом обнаружения ПРО 10–15 нг/мл.
При выкуривании одной сигареты марихуаны с. 1.75 или 3,55% ТГК пробы мочи при иммунном скрининге дают положительны^ результат в течение от 0,5–1,5 дней до 1–6 дней в зависимости от дозы и ПЗР (данные получены для 6 лиц) (11).
При внутривенном введении 5 мг ТГК положительная реакция мочи сохраняется в течение 2–12 дней (ПЗР = 20 нг/мл). После орального приема умеренной дозы 20 мг ТГК метаболит ТГК–СООН и другие могут детектироваться в моче до 12 дней.
Хроническое курение. При хроническом потреблении ТГК аккумулируется в тканях, богатых липидами, быстрее, чем выводится. Для этих случаев свойственно более длительное время получения положительной иммунной реакции мочи: до 25–40 дней при ПЗР=20 нг/мл. При регулярном курении даже не чаще 2–3 раз в неделю моча дает положительный результат возможен более месяца после курения : для хроника со стажем курения марихуаны 10 лет – 77 дней (ПЗР–20 нг/мл). Определение ТГК–СООН возможно в течение 17–22 дней (ПрО 10–15 нг/мл). Эта ситуация сохраняется даже в случае приостановки или полного прекращения курения. По этой причине трудно провести различие между хроническим курением с перерывом на несколько недель и курением нехроническим.
Содержание ТГК и метаболитов в слюне
Слюна по некоторым критериям является лучшей биологической матрицей для судебно–химического анализа при доказательстве факта недавнего потребления ТГК–содержащих продуктов. Отбор слюны осуществляется просто и быстро, исключается возможность инвазии. Концентрации активных веществ в слюне после приема обычных доз ТГК 5–20 мг достигают 1000 нг/мл, т.е. значительно превосходят величины, получаемые при анализе крови, и, кроме того, коррелируют с динамикой психотропных эффектов в отличие от данных, полученных при анализе мочи, пота или волос. Через 3–4 ч концентрация ТГК в слюне уменьшается примерно до 50 нг/мл. Контролированный прием ТГК, КБН и КБД по 5 мг в этиловом спирте орально показал, что через 1 ч содержание в слюне (4,5 мл) составляет 135,1; 178,3 и 157,7 нг/мл, соответственно. Через 3 ч концентрация каннабиноидов падает до 20–35 нг/мл, а через 4 ч – ни один из них не детектируется. Неидентифицированный метаболит появляется также в пределах 1–3 час после приема смеси.Содержание ТГК в волосах
Для доказательства факта употребления продуктов каннабиса по анализу волос более правильно проводить определение метаболита ТГК–СООН, чем самого ТГК, из–за возможности загрязнения волос, вследствие «пассивного курения». Из 30 проб волос людей, погибших в результате приема сверхдозы героина, 17 проб содержали большое количество ТГК (определен только качественно по приведенным выше основаниям) и метаболит ТГК–СООН в диапазоне 0,02–0,39 нг/мг (среднее 0,12 нг/мг). Однако содержание ТГК–СООН в волосах может на порядок превышать приведенные величины и доходить до 4–5 нг/мг. Вместе с тем метаболиты ТГК–СООН и 11–ОН–ТГК не были определены в волосах 8 курильщиков марихуаны, несмотря на присутствие ТГК. Основные компоненты, вводимые в организм человека при курении марихуаны, это ТГК, КБН и КБД. В волосах 30 хронических курильщиков обнаружены ТГК в 5 случаях, КБД – в 23 случаях и КБН – в 22 случаях. Количественные данные приведены в табл. 8.Содержание ТГК и метаболитов в организме новорожденных
При употреблении матерями ТГК–содержащих продуктов в процессе вынашивания и кормления ребенка в его организме определяют ТГК и метаболиты. Меконий как объект исследования для определения наркотиков, попадающих в организм плода из материнского организма, имеет преимущества перед традиционными объектами: мочой и кровью (см. соответствующий раздел в главе опиаты). В меконии, помимо основного метаболита ТГК–СООН, также присутствуют 11–ОН–ТГК и 8(3,11–ди–ОН–ТГК. Неизмененный ТГК, как и 8а–ОН–ТГК и 8Р–ОН–ТГК в образцах мекония в основном отсутствуют. В табл. 9 приведены концентрации ТГК и метаболитов в меконии новорожденных, чьи матери заявили об употреблении марихуаны во время беременности. В некоторых пробах (11 и 12, табл.9), в которых метаболит ТГК–СООН не детектирован, два других метаболита: 11–ОН–ТГК и 8,11–ди–ОН–ТГК присутствуют в значительных количествах.Таблица 8. Содержание ТГК, каннанинола (КБН) и каннабидиола (КБД) в волосах курильщиков марихуаны. Приведены средние значения для 30 образцов.
| Каннабиноид | Интервал, нг/мг | Среднее, нг/мг |
|---|---|---|
| ТГК | 0,1–0,29 | 0,15 |
| КБН | 0,01–1,07 | 0,17 |
| КБД | 0,03–3 | 0,44 |
Таблица 9. Концентрация метаболитов ТГК в меконии, нг/г. Все образцы подвергались ферментативному гидролизу
| Образец | ТГК–СООН | 8,11–ди–ОН–ТГК | 11–ОН–ТГК | ТГК | 8–ОН–ТГК |
|---|---|---|---|---|---|
| 1 | 259 | 17,7 | 25 | 0 | 16,7 |
| 2 | 5,6 | 0 | 13 | 0 | 0 |
| 3 | 4,6 | 4,9 | 40 | 0 | 0 |
| 4 | 25,2 | 2,8 | 17 | 4 | 0 |
| 5 | 97,5 | 17,7 | 74 | 3 | 0 |
| 6 | 60,6 | 14,9 | 44 | 0 | 0 |
| 7 | 102,9 | 18,8 | 81 | 0 | 0 |
| 8 | 9,1 | 4,7 | 259 | 0 | 0 |
| 9 | 2,7 | 0 | 75 | 0 | 0 |
| 10 | 9,8 | 5,3 | 204 | 0 | 0 |
| 11 | 0 | 32,2 | 929 | 0 | 0 |
| 12 | 0 | 68,6 | 144 | 0 | 0 |
Содержание ТГК и метаболитов в организме после употребления в пищу конопляного масла
Масло семян конопли содержит ТГК (а также другие активные каннабиноиды) от 7 до 150 мкг в 1 мл. По субъективным оценкам действие масла после употребления его в качестве пищи проявляется в виде специфических психотропных эффектов, подобных эффектам ТГК. При употреблении 40–135 мл масла в течение 1–2 дней уже через 1 ч в крови определяется ТГК в средней (N=13) концентрации 6 нг/мл. Концентрация метаболита ТГК–СООН в моче от 5 до 68 нг/ мл, но может быть и выше (431 нг/мл ) при употреблении масла с высоким содержанием ТГК. При этом время детектирования ТГК–СООН в моче может достигать 3–6 дней.Стабильность ТГК и ТГК–СООН
ТГК и ТГК–СООН разлагаются при хранении под действием кислорода воздуха, света и при нагревании. Основной продукт разложения ТГК и других каннабиноидов при длительном хранении – каннабинол (КБН). Установлено, что даже в стандартных препаратах ТГК часто присутствует примесь КБН, содержание которого может доходить до 0,3%. В крови при комнатной температуре в течение 6 мес содержание ТГК может уменьшаться на 90%, метаболита 11–ОН–ТГК на 44%. Содержание ТГК–СООН в моче значительно уменьшается при стоянии в комнатных условиях в течение недели и примерно на 45% за полгода хранения при тех же условиях. Стабильность стандартных растворов и образцов биожидкостей обеспечивается при хранении в условиях глубокого охлаждения при температуре – 20°С: интервал концентрации ТГК для 48 проб мочи от 7 до 776 (среднее 127) нг/мл не изменился за 12 мес хранения и составил 7–774 (среднее 132) нг/мл.Содержание ТГК и метаболитов в органах
В табл. 10 приведены величины концентраций ТГК и ТГК–СООН в организме людей, смерть которых в той или иной степени была связана с употреблением марихуаны. Можно отметить высокие уровни ТГК в жировой ткани, легких, мышечной ткани и мозге.Таблица 10. Распределение ТГК и ТГК–СООН в тканях трупа. Смертельные случаи, связанные с потреблением марихуаны
| Биожидкость | ТГК, нг/мл или нг/г | ТГК–СООН, нг/мл или нг/г |
|---|---|---|
| кровь | 1,85 | 15,5 |
| моча | – | 57.6 |
| печень | 1,85 | |
| почки | 7,42 | |
| селезенка | 6,37 | |
| легкие | но | |
| мышцы | 16,2 | |
| мозг | 9,78 | |
| жир | 657 |
Заключения по результатам аналитического исследования биожидкости
На основании полученных при анализе мочи данных в общем случае нет возможности установить, когда имел место «сеанс» приема ТГК–содержащих продуктов.Можно лишь сделать некоторые ориентировочные выводы относительно времени и интенсивности их употребления. ■ Положительная проба мочи поданным иммунного анализа указывает на потребление марихуаны (или продуктов ее переработки) в течение периода от 1 ч вплоть до нескольких недель от момента отбора пробы. Возможны следующие варианты. • Если общая концентрация каннабиноидов в моче менее 50 нг/мл (по Данным иммунного анализа), то, возможно, это связано с употреблением дозы ранее чем период 36 ч, или быть следствием долговременной экскреции, свойственной хроническим потребителям. • Если при последовательных еженедельных анализах первая проба была положительной, а вторая и третья отрицательные, то это может быть вызвано случайным или разовым потреблением средства. • Если пробы положительны в течение 3 или более недель, но концентрация постепенно уменьшается и в течение длительного времени (не менее двух недель) пробы остаются отрицательными, то это может быть результатом прекращения использования марихуаны хроническим потребителем. • Если пробы положительны в течение нескольких недель без тенденции к уменьшению концентрации, то можно сделать вывод о хроническом потреблении марихуаны. ■ Индикатор недавнего использования марихуаны – обнаруженный в моче метаболит 80,11–ди–ОН–дельта–9–ТГК, который появляется в первые несколько часов после приема. ■ Разовая единственная положительная проба мочи не означает, что субъект, принимавший марихуану, находился в момент отбора пробы под ее воздействием. Положительная проба мочи означает лишь то, что субъект принимал марихуану в недавнем прошлом, причем это могут быть часы, дни или недели назад, в зависимости от способа использования и др.
Длительность обнаружения каннабиноидов
Чувствительные методы анализа: иммунные и ГХ/МС позволяют детектировать метаболиты каннабиноидов в моче в течение дней и недель после момента их использования. Продолжительность времени, в течение которого образцы мочи дают положительный отклик при анализе на каннабиноиды, зависит от многих факторов: дозы, способа и частоты использования, метаболизма, времени отбора пробы мочи, количества жидкости, принятой перед отбором, и, в значительной степени, от длительности периода употребления марихуаны (см. ранее). Из–за липофильного характера и быстрого метаболизма содержание ТГК в моче чрезвычайно мало (нанограммовые уровни), а интервал определения составляет 5–6 ч, в плазме – до 72 ч. Выведение метаболитов охватывает больший Период и длится несколько дней и более.В общем случае при употреблении марихуаны 2 раза в неделю метаболит ТГК–СООН может быть обнаружен в моче в течение 1–3 дней при пороговом уровне детектирования 100 нг/мл. При хроническом потреблении этот срок может продлеваться до недели или даже дольше.
Использование иммунных методов с пороговым уровнем 20 нг/ мл позволяет продлить эти сроки до 3–6 дней, а в случае хронического потребления до 25–40 дней (11). Следует отметить значительные вариации результатов анализа при ежедневном отборе проб, вплоть до чередования положительного и отрицательного отклика.
Глава 5. Галлюциногены
Галлюциногены вызывают нарушения в восприятии реального мира, особенно световых сигналов, запаха, вкуса, а также искажения в оценке пространства (направления, расстояния) и времени. Под влиянием галлюциногенов может происходить визуализация цвета и звука, по субъективным отзывам можно «слышать цвет» и «видеть звуки». Большие дозы вызывают визуальные галлюцинации и видения.Общей чертой галлюциногенов является их способность изменять настроение и характер мышления. Они вызывают состояние возбуждения ЦНС, приводящее к сдвигу сознания, обычно к эйфории, но иногда к сильной депрессии или агрессивному состоянию. Самым опасным следствием применения галлюциногенов является нарушение способности логически рассуждать, что ведет к неадекватным решениям и несчастным случаям. Находящиеся под воздействием галлюциногенов люди должны быть под постоянным наблюдением, чтобы не спровоцировать критическую ситуацию, когда они могут причинить вред себе или окружающим. Острое состояние: беспокойство, возбуждение, бессонница, – обычно длится, пока не прекратится действие средства. Иногда депрессия и «деперсонализация» столь велики, что приводят к самоубийству.
В течение долгого времени после выведения из организма могут ощущаться «возвратные вспышки» (flashbacks) – небольшие повторения психоделических эффектов, таких как интенсификация цветового восприятия, наблюдение передвижения фиксированных объектов, путаница в идентификации объектов.
Наиболее известные галлюциногены: ЛСД, мескалин, псилоцибин и псилоцин грибов, фенциклидин (РСР), метоксипроизводные амфетамина.
Классификация по способу воздействия
Серотонергические галлюциногены – ЛСД, мескалин, псилоцибин/псилоцин. Их эффекты объясняются влиянием на обмен серотонина в мозге.Диссоциативные анестетики – РСР и его аналоги, в том числе применяемый в медицине анестетик кетамин, которые действуют преимущественно на глутаминергические рецепторы.
Классификация по химической структуре
По химической структуре можно выделить несколько групп галлюциногенов.Галлюциногены: ЛСД, ДМТ, ДЭТ, псилоцин, псилоцибин, буфотенин, гармалин, – относятся к группе индолов, т.е. к производным 2,3–бензопиррола (рис.1). Индолами являются многие фармакологически активные соединения, например, триптофан – важнейшая аминокислота, триптамин, серотонин (5–гидрокситриптамин), многие природные алкалоиды.
 Рис. I. Структура галлюциногенов–аналогов серотонина.
Рис. I. Структура галлюциногенов–аналогов серотонина.
Среди контролируемых веществ индолами являются: ■ лизергиновая кислота ■ амид лизергиновой кислоты ■ диэтиламид лизергиновой кислоты (ЛСД) ■ N.N–диметилтриптамин (ДМТ) ■ N.N–диэтилтриптамин (ДЭТ) ■ N,N–диметил–5–гидрокситриптамин (Буфотенин, Bufotenine, «уличные» названия Love Stone,Chan Su) ■ N,N–диметил–4–гидрокситриптамин (псилоцин) ■ N,N–диметил–4–гидрокситриптамин–фосфат (псилоцибин) ■ этриптамин.
Первые три соединения являются алкалоидами эргота. Изомер псилоцина буфотенин (см. рис. l)(Love Stone, Black Stone, Stud 100, Hart Rock, Chinese Love Stone) в последнее время получил распространение в США в сфере запрещенного оборота, а также как составной компонент китайского медицинского средства Chan Su. Это слабый галлюциноген с очень сильным побочным депрессивным действием на сердечно–сосудистую систему. Псилоцин и его дефосфорилированный аналог псилоцибин – орально активные галлюциногены, выделяемые из некоторых видов грибов: Psilocybe, Panaeolina, Panaeolus, Copelandia, Conocybe, Gymnopilus, Stropharia, Pluteus, распространенных по всему миру.
Основной вид галлюциногенных грибов в Скандинавских странах и северных регионах европейской части РФ – Psilocybe semilanceata содержит (в расчете на сухие грибы) до 2% основного активного ингредиента псилоцибина, следовые количества псилоцина и до 0,3% деметилированного производного псилоцибина: бейоцистина (baeocystin).
В странах средней и северной Европы также распространены галлюциногенные грибы Panaeolus subbalteatus.
Чистый псилоцибин синтезируют в подпольных лабораториях и употребляют внутрь в количестве 6–10 мг. Грибы используют свежими или высушенными: 5–10 г, в зависимости от вида, а также в виде настоев или отваров, содержащих 10–20(6–12) мг активного вещества (250 мкг/кг). Известны также случаи внутривенного введения псилоцибина. Начальные эффекты проявляются в интервале от нескольких минут до часа. Пик действия от 0,5 до 3 ч. Продолжительность галлюциногенного действия 4–6 ч. Около 11 % дозы выделяется в виде неизмененного соединения, остальная часть как метаболиты и конъюгаты.
Эффекты, развивающиеся при употреблении грибов–галлюциногенов ■ эйфория ■ расслабленное состояние ■ галлюцинации ■ расширение зрачков ■ замедление сокращения сердца ■ нарушения координации.
Эффекты передозировки ■ двоение в глазах ■ тахикардия ■ гипертензия ■ повышение температуры ■ тошнота и рвота.
Вторую группу составляет фенциклидин (1–(1–Фенилциклогексил)–пиперидин, РСР) и родственные соединения, которые по химической структуре являются производными циклогексил–пиперидина. В эту группу входит медицинский препарат анестетик – кетамин, также обладающий галлюциногенными свойствами.
К третьей группе можно отнести метоксипроизводные амфетамина. Эта группа также называется группой мескалина, по названию триметоксифенилэтиламина, родоначальника метоксиамфетаминовых галлюциногенов, природного соединения, добываемого из мексиканского кактуса и употребляемого в виде высушенных на солнце кусочков растения: «мескалиновых подушечек». Наиболее известные соединения этой группы: 2,5–диметоксиамфетамин (ДМА), 3,4,5–триметоксиамфетамин (ТМА), 4–метил–2,5–диметоксиамфетамин (ДОМ, STP), 4–этил–2,5–диметоксиамфетамин (ДОЕТ), 4–бром–2,5–диметоксиамфетамин (ДОБ), 4–бром–2,5–диметокси–фенилэтиламин (2–CD, Nexus), 4–хлор–2,5–диметоксиамфетамин (ДОХ).
Сравнительная активность различных галлюциногенов по отношению к мескалину: мескалин – 1, ЛСД – 3000, ДОЭТ – 100, ДОМ – 80, ТМА – 2–20, ДМА – 6–8.
Как правило, галлюциногены принимают орально, но РСР и ДМТ обычно курят.
Первичным источником появления этих запрещенных средств являются подпольные лаборатории.
Галлюциногены вызывают сильную психологическую зависимость, кроме того, их интенсивное использование ведет к постепенному поражению мозга. Даже относительно безопасные с точки зрения токсикологии соединения представляют большую проблему для личности и общества своим асоциальным и суицидальным проявлением. Наиболее распространенными наркотиками–галлюциногенами в настоящее время являются ЛСД и РСР, к которым в северных регионах РФ добавляются препараты, приготовленные из галлюциногенных грибов.
В табл. 1 приведены различные галлюциногены природного происхождения и их ботанические источники. Многие из галлюциногенов имеют синтетические аналоги, производимые подпольными лабораториями.
Таблица 1. Галлюциногены природного происхождения и их ботанические источники
| Наркотик | Ботанический источник | Распространение |
|---|---|---|
| ЛСД | Грибы спорыньи, в настоящее время используется синтетический препарат | Происходит из Европы |
| Ибогаин | Растение Ибога, Tabernanthe Iboga | Африка |
| Псилоцибин | Грибы семейства Psilocybe, Conocybe, Panaeolus, Stropharia и др. | По всему миру |
| ДМТ | Дерево Virola calophylla и другие виды | Южная Америка |
| Миристицин | Мускатный орех, Meristrica fragrans | Восточная Индия |
| Мескалин | Кактус пейот Lophophora Williamsii | Мексика и юго–запад США |
| Гармалин, гармин | Виноград Banisteriopsis inebrians | Южная Америка |
| Эргин, изоэргин | Семена вьюнка Rivea coryniboza, Ipomoea violacea | По всему миру |
Глава 6. ЛСД
ЛСД – чрезвычайно сильный галлюциноген, который был особенно популярен в 1960–х годах и вновь обретает популярность сейчас. Его получают из лизергиновой кислоты вещества в свою очередь, добываемого из спорыньи (ergot fungus), поражающей зерновые культуры.Впервые ЛСД был синтезирован в 1938 г. и в течение многих лет из–за чрезвычайно высокой эффективности его применяли при изучении механизма ментальных расстройств.
Галлюциногенные свойства синтетического ЛСД были открыты случайно швейцарским химиком Альбертом Хоффманом 8 1943 г. при изучении производных эргота. Среди 25 соединений, изученных Хоффманом, только d–диэтиламид лизергиновой кислоты обладал галлюциногенной активностью.
В 1947 г. после систематического изучения клинических эффектов ЛСД в Психиатрической клинике Цюрихского Университета лекарственное средство Delysid (фирма Sandoz), представляющее собой ЛСД в виде тартрата, было выпущено на фармацевтический рынок. Последующие годы характеризуются повсеместным распространением ЛСД в США и Европе в качестве лекарственного средства в психиатрии, вслед за которым последовал спад интереса и полное прекращение клинического использования в начале 70–х годов.
Начало употребления ЛСД в качестве наркотика приходится на шестидесятые годы и уже к 1966 г. около 4 млн американцев пробовали этот препарат. Общественное мнение вначале было терпимо к ЛСД и позволило возникнуть культу поклонников ЛСД во главе с бывшим психиатром Гарварда, уволенным за «эксперименты» с грибами и наркотиками, доктором Тимоти Лири. В культуре движения «хиппи» ЛСД играло ключевую роль. Однако по мере знакомства с последствиями употребления ЛСД общественное мнение и контролирующие организации стали решительно бороться за его запрещение, и в 1966 г. США объявили производство, распространение и употребление ЛСД вне закона. В РФ ЛСД, как и другие производные лизергиновой кислоты, запрещены.
Семидесятые годы характеризовались спадом употребления ЛСД, но никогда оно не прекращалось полностью. Более того, в последние годы наметился некоторый рост числа наркоманов, принимающих ЛСД. В течение более 20 лет ЛСД не имеет никакого легального применения, и весь препарат, появляющийся в нелегальной торговле, синтезируется в подпольных лабораториях.
Химические названия ЛСД: lysergide, лизергид, диэтиламид d–лизергиновой кислоты, N.N–диэтил–d–лизергамид.
По химической структуре ЛСД аналог серотонина (см. ранее). Известно, что ЛСД является сильным антагонистом 5–НТ2–рецепторов, однако полностью механизм его действия еще не изучен.
В молекуле лизергиновой кислоты имеются два хиральных центра у атомов С–5 и С–8, таким образом возможно образование 4 стереоизомеров. Из них единственным активным соединением является d–ЛСД, в молекуле которого содержится экваториальная С–амидная группа. Изомер, содержащий С–8–амидную группу в аксиальном положении, под названием ИЗО–ЛСД – неактивен (рис. 1).
Синтез ЛСД в подпольных лабораториях осуществляют обычно, исходя из лизергиновой кислоты или алкалоидов эргота. Лизергиновую кислоту получают из эргометрина или эрготамин–тартрата.
Все эти методы дают «сырой» продукт, содержащий большие количества неактивного ИЗО–ЛСД и другие побочные продукты, для удаления которых сырой продукт подвергают очистке различными способами. Как правило, запрещенные формы ЛСД, продаваемые «на улице», содержат значительные количества ИЗО–ЛСД.
ИЗО–ЛСД может образоваться непосредственно из ЛСД в реакции эпимеризации при атоме С–8 в щелочной среде, а также « процессе щелочной экстракции ЛСД в качестве артефакта при Диализе. При нагревании раствора ЛСД в щелочной среде эпимеризации подвергается около 10%, в то время как при кислых рН – менее пяти.
ЛСД обладает ограниченной устойчивостью к нагреванию, ультрафиолетовому освещению, присутствию кислот. При рН менее 4 ЛСД нестабилен. За четыре недели стояния при температуре 45°С теряется около 45% вещества. Проблемы при анализе создает способность ЛСД легко сорбироваться на стенках стеклянной посуды в процессе пробоподготовки.
Вследствие неустойчивости ЛСД–основания, вещество переводят в форму солей, обычно виннокислой соли (тартрата).
Чистый ЛСД бесцветен и не имеет запаха.
Виды запрещенных форм ЛСД
Когда ЛСД впервые появился в нелегальной продаже в 60–ё годы, он применялся обычно в виде разнообразных субстратов, получаемых при добавлении капли раствора ЛСД к различным сорбирующим материалам. Наиболее часто применяемые носители: кубики сахара, марки или кусочки фильтровальной бумаги в другом виде, или фармакологически инертные порошки, которыми затем наполняются пустые желатиновые капсулы. В качестве другой распространенной формы ЛСД существуют так называемые пирамидки («window panes» или «pyramids»), для получения которых ЛСД вводится в желатиновую матрицу и затвердевший желатин режется на маленькие кусочки.В 70–е годы таблетированные формы ЛСД разных размеров, формы и окраски были Наиболее распространенными. Содержание ЛСД в таблетках менялось в очень широком интервале (от.20 до 500 микрограмм) из–за трудности получения гомогенного порошка для таблетирования. В настоящее время число их типов значительно уменьшилось, что обусловлено лимитированным числом подпольных лабораторий, способных производить наиболее однородный продукт. Один ие типов, превалирующих в настоящее время на нелегальном рынке и называемый микродот («microdot»), представляет собой круглые таблетки, примерно 1,6 мм в диаметре, характеризующиеся однородной дозировкой 50–100 микрограмм ЛСД.
80–е годы характеризуются повсеместным распространением импрегнированных бумажных форм. В отличие от ранее принятого способа их приготовления (также все еще встречающегося в некоторых странах), когда некоторое количество раствора ЛСД капельным способом наносилось на бумагу, новый способ приготовления бумажных дозированных форм состоит в погружении листов подготовленной бумаги в раствор ЛСД, что гарантирует получение наиболее однородного продукта. Обычно эти листы перфорируются на квадраты 0,25–1 см2, содержащие типичную дозу 30–50 микрограмм ЛСД. На поверхность листов наносятся разнообразные рисунки от абстрактных картинок до анимационных фигурок. Бумажки с капельным нанесением, однако, до сих пор часто распространяются в некоторых странах.

 Рис. 1. Структура ЛСД и изо–ЛСД.
Рис. 1. Структура ЛСД и изо–ЛСД.
В общем случае в настоящее время преобладающими типами дозированных форм ЛСД являются бумажные формы (марки), маленькие таблетки, подобные «микродоту», и желатиновые формы. Содержание активного компонента в них обычно 50–100 микрограмм ЛСД. Тем не менее могут также появляться различные другие формы, вследствие простоты их изготовления способом нанесения раствора ЛСД на какой–либо субстрат.
«Уличные» названия ЛСД:
| acid | кислота |
| blotter acid | кислота на фильтре (марка) |
| microdot | микродот |
| white lighthing | белое сияние |
Действие ЛСД на организм человека
Начало галлюциногенного действия ЛСД спустя 30–90 мин после приема, длительность – от 2 до 12 ч.В течение этого времени может нарушаться способность рассуждать, меняется визуальное восприятие, возникают галлюцинации.
Физиологические симптомы приема ЛСД: ■ расширенные зрачки ■ увеличение температуры тела ■ высокое кровяное давление ■ потеря чувства направления, расстояния и времени ■ потение ■ тошнота ■ тремор.
Вместе с тем могут проявляться и другие эффекты.
Психические проявления: ■ паническое состояние ■ паранойя ■ возбуждение ■ потеря контроля ■ путанное сознание ■ психозы.
Последствия употребления ЛСД: ■ хромосомные нарушения ■ рождение детей с различными наследственными заболеваниями ■ провоцирование актов насилия ■ помешательство ■ суицид.
Социальные последствия употребления ЛСД представляют собой основную проблему, связанную с его распространением. Вызываемые ЛСД психологические и психические нарушения ведут не только к асоциальному поведению, но и провоцируют действия и поступки, ведущие к причинению вреда непосредственно для личности и даже к смерти.
Таблица 1. Концентрация ЛСД в крови и моче лиц, употреблявших ЛСД, нг/мл. РИА – радиоиммунный метод, КЭ – капиллярный электрофорез
| Субъект | РИА | КЭ | ||
|---|---|---|---|---|
| кровь | моча | кровь | моча | |
| 1 | 0,25 | – | 0,2 | – |
| 2 | 0,07 | 0,59 | – | 0,75 |
| 3 | 0,54 | – | 0,74 | . |
| 4 | – | 0,67 | 0,51 | 0,45 |
Фармакокинетика
Минимальная эффективная доза ЛСД 10–25 мкг. Доза 10 мкг уже вызывает эйфорию, 50–200 мкг – галлюцинации и другие изменения восприятия. Обычная употребляемая разовая доза 30–50 (20–80) мкг.При повторных употреблениях развивается толерантность.
ЛСД быстро всасывается и распределяется по организму, легко преодолевая гематоэнцефалический барьер и достигая мозга. Время «полужизни» в плазме T½= 3,6(2,9–5,14) ч. Длительность действия 8–12 ч. Уровни ЛСД в плазме и моче в течение нескольких часов после приема разовой дозы – менее нанограмма/мл (табл.1). Максимальная концентрация в плазме после приема орально 1 мкг/ кг ЛСД достигается через 1 ч и в интервале до 3 ч составляет 1,7–1,85 нг/мл. Затем концентрация резко снижается: через 6 ч до 1,1 нг/мл, через 24 ч до 0,2 нг/мл. Пик концентрации в плазме после употребления дозы 2 мкг/кг устанавливается в пределах одного часа и составляет 4–6 нг/мл.
Метаболизм
ЛСД быстро метаболизируется и выводится. Менее 1 % дозы обнаруживается в моче в виде неизмененного соединения. Метаболизм ЛСД в организме человека полностью не изучен, основные сведения получены из экспериментов с животными или из экспериментов in vitro с микросома ми печени человека. Помимо известных основных метаболитов образуется много не идентифицированных.Основные метаболиты ■ 2–оксо–ЛСД. ■ 2–оксо–3–гидрокси–ЛСД (ОГ–ЛСД). ■ N–деметил–ЛСД (нор–ЛСД) ■ этиламид лизергиновой кислоты (ЛАЭ) ■ 13– и 14–гидрокси–ЛСД.
13– и 14–Гидроксилированные производные далее конъюгируются и выводятся в виде глюкуронидов.
Количественное содержание метаболитов в плазме и моче находится на субнанограммовых уровнях. Время «полужизни» в плазме T½ нор–ЛСД составляет 10 ч.
Биотрансформация ЛСД под действием микросомальной фракции печени in vitro приводит к образованию большого числа метаболитов, основным из которых является ЛАЭ. Характерно, что энзимы печени вызывают эпимеризацию метаболитов, имеющих структуру ЛСД.
 Рис. 2. Метаболизм ЛСД в организме человека.
Рис. 2. Метаболизм ЛСД в организме человека.
Обнаружены: ■ неизмененным ЛСД. ■ изо–ЛСД. ■ нор–ЛСД. ■ изо–нор–ЛСД. ■ 2–оксо–ЛСД. ■ ЛАЭ. ■ изо–ЛАЭ. ■ гидрокси–производные ЛСД (моно– и три–ОН–ЛСД) в виде глюкуронидов.
Основной продукт превращения ЛСД in vitro: ЛАЭ и его эпимер: изо–ЛАЭ. В моче со сроком хранения около года» давшей положительную реакцию при иммунном анализе на присутствие ЛСД, обнаружены те же метаболиты, за исключением триоксилированных производных и 2–ОКСО–ЛСД. Последний термически неустойчив и детектируется только в течение небольшого периода времени после отбора мочи. При метаболизме ЛСД в организме человека (в отличие от опытов in vitro) ЛАЭ образуется в незначительной Степени, а основными продуктами является ИЗО–ЛСД и нор–ЛСД вместе с эпимером. Значительное количество ИЗО–ЛСД в моче, возможно связано с его присутствием в нелегально изготовленном препарате ЛСД или эпимеризацией этого препарата при хранении. Специальными исследованиями было показано, что при метаболизме не происходит окисления N–этильных групп с образованием N–этил–N–(2–гидро–ксиэтиламида) лизергиновой кислоты. Удаление в процессе биотрансформации одной или обеих N–этильных групп ведет к образованию соединений с пониженной активностью в отношении галлюциногенных и токсических свойств приблизительно до 1/8 и 1/3 активности ЛСД, соответственно.
Выведение
ЛСД быстро выводится из организма с мочой. Основными продуктами выведения являются неизмененный ЛСД, нор–ЛСД, ОГ–ЛСД и глюкурониды 15– и 14–ОН–ЛСД. Как указывалось ранее, многие метаболиты ЛСД присутствуют в очень малых концентрациях и не идентифицированы. Доля неизмененного ЛСД за 24 ч. выведения составляет 0,9–1% дозы, нор–ЛСД – порядка 1,2% дозы.Таблица 2. Выведение неизмененного ЛСД с мочой, нг/мл. Доза ЛСД 1 мкг/кг, орально.
| Время, ч | 2 | 4 | 6 | 8 | 10 | 12 | 22 |
|---|---|---|---|---|---|---|---|
| ЛСД, нг/мл | 0,75 | 0,42 | 0,57 | 0.72 | 0,33 | 0,15 | 0,15 |
Таблица 3. Результаты клинических и лабораторных исследований случаев интоксикации ЛСД, нг/мл. С – концентрация ЛСД, Св – сыворотка, М – моча, Т – время с момента введения.
| № | Доза ЛСД | Эффекты | Т, час | С (РИА), пг/мл | С (ВЭЖХ), нг/мл | ||
|---|---|---|---|---|---|---|---|
| Св | м | Св | м | ||||
| 1 | 6 табл. | возбуждение, делириум | 10 | 1 | –1 | 1,9 | 7,7 |
| 2 | 4 марки | галлюцинации | 2 | + | + | 1,8 | 1,4 |
| 3 | неизв. | паника | 10 | + | + | 1,5 | 3,8 |
| 4 | неизв. | паника, галлюцинации | 2 | + | 1,4 | 5,7 | |
| 5 | неизв. | нарушение восприятии | 8 | + | + | 1,3 | 0,2 |
| 6 | неизв. + кокаин | нарушение восприятия, возбуждение, паранойя | 7 | + | 1.0 | 6,3 | |
| 7 | 1–2 табл. | возбуждение, галлюцинации | 7 | + | 0,8 | 0,7 | |
| 8 | 3 дозы + алкоголь | возбуждение, делириум, агрессия | и | + | 0,6 | 2,4 | |
| 9 | 1 марка | возбуждение, эксцентричное поведение | 6 | + | 0,5 | 0,5 | |
| 10 | 1 доза | возбуждение, эксцентричное поведение | 8 | * | 0,6 | ||
| 11 | 1 марка | кататония | 7 | + | + | 1– | 21 |
| 12 | 1,5 марки | возбуждение, эксцентричное поведение | 8 | н | н.д. | н.д. | |
| 13 | ценз в. | галлюцинации, нарушение восприятия | – | + | л | н.д. | н.д. |
| 14 | неизв. | нарушение восприятия, паранойя | – | + | – | н.д. | н.д. |
| 15 | неизв. | возбуждение, нарушение восприятия, агрессия | * | * | ~ | н.д. | н.д. |
| 16 | неизв. | нарушение восприятия, эксцентричное поведение, делириум | 3 | ~ | н.д. | н.д. | |
| 17 | неизв. | возбуждение, галлюцинации | – | – | – | н.д. | н.д. |
| 18 | 4 пил. | делириум | 2 | – | – | н.д. | н.д. |
После приема I мкг/кг ЛСД концентрация неизмененного ЛСД в моче через 22 ч составила 0,15 нг/мл, а через 48 ч – всего 0,1 нг/ мл (табл. 2). По данным, полученным при изучении действия ЛСД на лабораторных животных (макаки–резус), 24–39% дозы выводится с мочой за 48 ч и 15–19% – с калом. При этом на каждый метаболит приходится не более 1–3% дозы. Интервал концентрации ЛСД в клинических пробах мочи (31 проба): 0,21–0,96 нг/мл. В 23 пробах присутствует ИЗО–ЛСД в количестве от 0,01 до 5,43 нг/мл. Содержание ЛСД в моче при приеме галлюциногенных доз 100 мкг 1–20 нг/мл в период до 24 ч после введения.
Из 49 проб мочи лиц, подозреваемых в употреблении ЛСД, концентрация (пиког/мл) ЛСД: 13–1494 (среднее 357), ОГ–ЛСД: 17–21 406 (среднее 3470). Отношение ОГ–ЛСД к ЛСД составляет в среднем 24 (0,03–136).
Сопоставление клинических и лабораторных данных для 18 случаев, связанных с употреблением ЛСД, показало, что в некоторых случаях с подтвержденной клиническими обследованиями и признаниями самих испытуемых интоксикацией ЛСД, анализы крови и мочи тем не менее не дают положительных результатов (табл. 3). Интервал концентраций ЛСД в сыворотке крови: 0,5–1,9 (среднее значение 1,2), в моче: 0,2–7,7 (среднее 2,9) нг/мл. Между содержанием ЛСД в биожидкостях и клиническими проявлениями интоксикации четкой корреляции установить не удалось.
Содержание ЛСД в волосах 2 человек из 17, употреблявших ЛСД, также очень мало и составляет всего 8–17 пикограмм/мг.
Из–за чрезвычайно низких концентраций ЛСД и метаболитов в моче их обнаружение возможно в интервале не более 72 ч после момента приема. Приводится интервал 30–48 ч для методов анализа с пределом обнаружения 0,1 нг/мл ЛСД и 0,25 нг/мл нор–ЛСД.
Глава 7. Фенциклидин, РСР
РСР вместе с кетамином составляют группу диссоциативных анестетических галлюциногенов, действие которых на организм человека определяется взаимодействием с глутаминергическими рецепторами.1–(1–Фенилциклогексил)–пиперидин (РСР, Фенциклидин) (CAS 77–10–1) был синтезирован как препарат для внутривенного наркоза во второй половине пятидесятых годов в США и под наименованием SERNYL внедрен в медицинскую практику. В отличие от опиатов он не дает угнетения сердечно–сосудистой деятельности или дыхания. Однако в процессе клинического применения были выявлены токсические побочные эффекты, включающие постоперационные галлюцинации, возбуждение, ментальные расстройства и депрессивные состояния, и, несмотря на хорошие терапевтические свойства, препарат был исключен из клинической практики. После непродолжительного применения в ветеринарии в 1960–е годы под названием SERNYLAN с 1979 г. производство лекарства было остановлено, РСР был изъят из обращения и запрещен для использования. Большая часть РСР, производимого в США (если не весь), поступает из подпольных лабораторий. В настоящее время он находится под международным контролем и включен в Список Постоянного Комитета по контролю наркотиков РФ как наркотическое средство.
РСР в нелегальной торговле: формы и способы употребления
В нелегальном обороте РСР существует с 1967 г. под различными «уличными» названиями: Peace pill, Angel dust, HOG, Killer weed, KJ, Embalming fluid, Rocker fuel, Sherms. Иногда он продается под видом других средств, например, как ЛСД, мескалин или кокаин.Чистый РСР – это белый кристаллический порошок, который легко растворим в воде. РСР, производимый в самодеятельных лабораториях, как правило, содержит примеси, придающие окраску от беловатой до коричневой и консистенцию от сыпучего порошка до вязкой массы. В нелегальную продажу РСР поступает в виде таблеток или капсул для орального приема или порошка для ингаляций через рот или нос. Жидкие формы для внутривенных инъекций встречаются реже. Их продают расфасованными в небольшие виалы или стеклянные флаконы небольших объемов.
Основной способ потребления РСР – курение (около 73%). Для этой цели обычно используют смеси РСР с растительным материалом: марихуаной, табаком, листьями мяты, петрушки и т.д.
Для орального введения или вдыхания также часто используются смеси РСР с другими наркотическими средствами: кокаином, опиатами, амфетамином, LSD и др. Зарегистрировано более 30 смесей, находящихся в нелегальном обороте, содержащих РСР.
К настоящему времени синтезировано большое количество структурных аналогов РСР, которые запрещены к употреблению, но встречаются в нелегальной продаже (табл. 1). Некоторые из них по фармакологической активности близки РСР (РСРу), другие – значительно превышают (РСЕ).
Таблица 1. Аналоги фенциклидина.

 PCP, TCP, PHP, РСЕ – запрещены, находятся под международным контролем, кетамин–анестетик, используется в клинической практике.
PCP, TCP, PHP, РСЕ – запрещены, находятся под международным контролем, кетамин–анестетик, используется в клинической практике.
Действие РСР на организм человека
Человек, находящийся под воздействием РСР, проявляет себя так же, как при приеме ЛСД: поведение, отрешенное от реальности, отчуждение от окружения. Доза 1–10 мг вызывает эйфорию и состояние, напоминающее алкогольную интоксикацию. Дозы 0,075–0,1 мг/кг внутривенно уже являются психоактивными, вызывающими отчужденность, негативизм, путаницу мыслей, апатию, сонливость и чувство опьянения. Более высокие дозы вызывают головокружение, анальгезию, необычные физические ощущения, расстройство сознания, при котором нарушаются способность концентрироваться и воспринимать, ослабевает память. Дозы выше 1 мг/кг приводит к анестезии с кататоническим эффектом и общей ригидности мышц.Обычные «уличные» дозы РСР 1–7 мг, действие наступает быстро и длится до 11 ч, дозы 5–15 мг вызывают токсические эффекты при курении и вдыхании, иногда продолжающиеся до 1–4 нед, дозы 25 мг и выше вызывают тяжелое отравление, кому и смерть.
Время проявления эффектов после введения: через 5–15 мин после курения, инъекций, вдыхания носом и через 1–2 ч после орального приема. Продолжительность действия – от 2 до 8 ч. В моче РСР обнаруживается в течение нескольких недель после однократного приема дозы.
При хроническом употреблении быстро развивается толерантность и привыкание. Синдром отмены длится несколько дней, сопровождаясь тяжелой депрессией и дезориентацией.
Симптомы употребления РСР ■ эйфория ■ расслабление, релаксация ■ отрешенность от окружения ■ ощущение легкости в теле ■ прилив физической силы ■ быстрые и непроизвольные движения глаз, нистагм ■ затуманенное зрение, двоение в глазах ■ нарушения слуха ■ потеря ориентации в пространстве и времени ■ онемение конечностей ■ фиксированный взгляд ■ заторможенность ■ оцепенение, мышечная ригидность ■ непрестанное хождение, повторяющиеся движения ■ повышение кровяного давления ■ тахикардия ■ усиленная потливость ■ гиперсаливация ■ лихорадка ■ рвота.
В случае приема высоких доз эти симптомы могут длиться до нескольких дней и даже недель. При интоксикации состояние характеризуется дезориентацией, отрешенностью, нарушениями восприятия пропорций тела, слуховыми и зрительными галлюцинациями. Развиваются тревожность, депрессия, паранойя, бред, психозы. Характерны резкие колебания настроения, агрессивность, анальгезия, членовредительство, проявления физической силы, выше обычной. Токсические психозы, похожие по признакам на шизофрению и сопровождаемые паранойей, грубым или эксцентричным поведением, вспышками ярости и т.п., могут длиться до нескольких дней.
В поведении отмечается психомоторное возбуждение, враждебность, нарушение в оценке окружающих обстоятельств и собственных возможностей. Смертные случаи после употребления РСР являются следствием ие только его токсичности, но и иррационального поведения, вызванного действием препарата.
Диагностические признаки употребления РСР
Для диагностики могут быть использованы три признака: ■ нистагм. ■ повышенное давление крови. ■ неустойчивый уровень сознания.При оценке наркотического действия сообщается, что в 50–80% случаев РСР вызывает состояние с тяжелыми эффектами, так называемые «плохие трипы, или плохие путешествия».
Фармакокинетика
Фармакокинетические свойства РСР изучены достаточно подробно. Терапевтические дозы РСР как анестетика – 0,25 мг/кг, но, как указано выше, при внутривенном введении 0,075–0,1 мг/кг уже проявляются психоактивные свойства. Начало действия при оральном или интраназальном приеме (втягивание носом) «уличной» дозы 1–3 мг наступает через 30–45 мин, при курении 1–2 мг и внутривенном введении (ВВ) – через 1–2 мин. Длительность эффектов 4–6 ч независимо от способа введения.РСР легко всасывается и распределяется по периферическим органам (главным образом, в тканях печени, легких, мозга и жировой ткани), лишь в очень малом количестве оставаясь в системе кровообращения, что отражено в большой величине объема распределения, составляющей 6,2 л/кг. Время T½ полужизни в плазме 7–16 ч, для токсических концентраций 1–4 дня. Максимальная концентрация в плазме устанавливается через 5–15 мин при курении и через 2 ч после орального приема. После внутривенного введения 5 мг/кг РСР максимальное содержание в плазме 1 мкг/мл приходится на 1,5 ч, затем концентрация РСР уменьшается: через 12 ч до 10 нг/мл, через 15 ч до 5 нг/мл, через 24 ч до 1 нг/мл. Область токсических концентраций в плазме определяется как 7–240 нг/мл, область летальных концентраций 1–5 мкг/мл.
Биодоступность РСР 50–90%. При курении из–за пиролитического расщепления до 1–фенил–циклогексена, ацетилпиперидина и пиперидина в организм вводится только около 30% исходной дозы РСР.
Метаболизм
Основные направления метаболизма РСР в организме человека – окислительное гидроксилирование циклогексанового и пиперидинового колец с образованием биологически активных соединений: ■ 1–(1–фенил–4–гидроксициклогексил)–пиперидин (4–ОН–цикло–РСР, I) ■ 1–(1–фенилциклогексил)–4–гидроксипиперидин (4–ОН–пип–РСР, II) ■ S–(N–(1–фенилциклогексил)амино)валериановая кислота (PC–кислота, III).Концентрация PC–кислоты в моче в ряде случаев превышает концентрацию родительского соединения, что послужило основанием для рекомендации выявлять потребление РСР по присутствию РС–кислоты в пробе.
3–ОН–цикло–РСР (IV) – продукт гидроксилирования циклогексанового кольца в положение 3 найден среди продуктов окисления РСР микросомами печени и плаценты организма человека (in vitro), а также является метаболитом организма животных (мышей, крыс, обезьян, кроликов и собак). Для метаболизма животных также характерно гидроксилирование в положение 3 пиперидинового цикла с образованием 3–ОН–пип–РСР.
В очень малых количествах (минорный метаболит) образуется 1–фенил–циклогексиламин (VIII) .
Дигидроксилированные (VI,VII) производные, являющиеся важными метаболитами крыс, мышей и других животных, в меньшей степени характерны для человека. Гидроксилированные метаболиты далее конъюгируются с образованием глюкуронидов и сульфатов.
Гидроксилированные в циклогексановое кольцо метаболиты РСР образуют стереоизомы: транс– и цис–4–ОН–цикло–РСР. Их содержание в биожидкостях может существенно различаться. По данным для мочи собаки транс– и цис–изомер составляют, соответственно, 12,9 и 2,9% введенной внутривенно дозы 100 мг РСР.
 Рис. 1. Метаболизм фенциклидина. I – цистранс–4–ОН–цикло–РСР, II–4–ОН–пип–РСР, III – PC–кислота, IV – цис,транс–3–ОН–цикло–РСР,V – 3,4–ди–ОН–цикло–РСР, VI – цис,транс–4–ОН–цикло, 4–ОН–пип–РСР, VII – цис,транс–3–ОН–цикло, 4–ОН–пип–РСР, VIII – фенилциклогексиламин.
Рис. 1. Метаболизм фенциклидина. I – цистранс–4–ОН–цикло–РСР, II–4–ОН–пип–РСР, III – PC–кислота, IV – цис,транс–3–ОН–цикло–РСР,V – 3,4–ди–ОН–цикло–РСР, VI – цис,транс–4–ОН–цикло, 4–ОН–пип–РСР, VII – цис,транс–3–ОН–цикло, 4–ОН–пип–РСР, VIII – фенилциклогексиламин.
Таблица 2. Содержание РСР и метаболитов в моче до и после гидролиза, мкг/мл.
| № | РСР | 4–ОН–цикло–РСР | 4–ОН–пип–РСР | |||
|---|---|---|---|---|---|---|
| до | после | до | после | до | после | |
| 1 | 6,3 | 5,94 | 0,02 | 0,48 | следы | 1,79 |
| 2 | 0,33 | 0.37 | 0 | 0,07 | 0 | 0,03 |
| 3 | 4,10 | 4,13 | 0 | 0 | 0 | 0,10 |
| 4 | – | 1,7 | . | 0,10 | . | 0,81 |
| 5 | 23,65 | 24 | 0,05 | 0,28 | 0 | 1,53 |
Интервал концентраций РСР и кислотного метаболита РС–кислоты в моче (по данным исследования 31 пробы) составляет 26–672 (среднее 147) и 9–999 (среднее 174) нг/мл, соответственно. Для 15 проб превышение концентрации РС–кислоты составляет от 1,2 до 12 раз. В пяти пробах, имевших очень низкое содержание РСР: 2–9,8 (среднее 6,4), концентрация метаболита PC–кислоты составила 5–29 (среднее 15,9) нг/мл.
Основное количество введенной дозы РСР выводится с мочой в виде конъюгированных метаболитов: 30–50% дозы (1 мг РСР внутривенно) выводится за 7 ч и 77% дозы – за 10 суток, при этом 73% в виде конъюгатов гидроксилированных метаболитов и только 10% (по другим данным до 30%) в виде исходного соединения. В большинстве (примерно 85%) случаев, связанных с потреблением РСР, его концентрация в биожидкостях очень мала – ниже 30 нг/мл, особенно Спустя 2–4 дня после потребления.
Выведение РСР увеличивается при метаболитическом подкислении мочи, но на выведение метаболитов это не влияет. Величины времен полувыведения T½ РСР, приводимые в различных источниках, изменяются в широком диапазоне от 8 до 55 ч, составляя в среднем 18 ч. Интервал обнаружения РСР в моче после приема разовой дозы может доходить до 7 дней, при хроническом употреблении до 20 дней.
Содержание РСР и метаболитов в волосах
В волосах наркоманов, употреблявших РСР, определены: РСР в концентрации 0,33–14 нг/мг, метаболит 4–ОН–пип–РСР – 0,02–0,12 нг/мг, транс–4–ОН–цикло–4–ОН–пип–РСР 0,09–0,45 нг/мг. Последний является основным метаболитом в волосах фенциклидиновых наркоманов.Таблица 3. Распределение РСР по длине волос.
| Пациент | Длина сегмента волос от корня, см | РСР, нг/10 мг |
|---|---|---|
| 3 | 0–1,5 | 14,7 |
| 3 | 1,5–3,0 | 15,4 |
| 3 | 30–4,5 | 12,8 |
| 5 | 0–1 | 42 |
| 5 | 1–3 | 38 |
| 5 | 3–6 | 25 |
| 5 | 6–9,5 | 15,5 |
| 5 | 9,5–134 | 12,0 |
| 5 | 13–18 | 12,0 |
| 5 | 18–23 | 12,0 |
Содержание РСР в волосах при различной частоте курения, нг/мг ■ случайное использование, 5 сигарет в течение 6 мес – 0,3 ■ слабое потребление в течение 4 мес или менее – 1,7 ■ умеренное потребление в течение 6–30 мес – 1,7–2,7 ■ хроническое потребление 10–12 сигарет в день в течение 3 лет – 2,8.
Содержание РСР в организме новорожденных
Биожидкости и ткани новорожденных, чьи матери употребляли фенциклидин при вынашивании и кормлении, могут содержать наркотик в значительных количествах. Так, описан случай, когда содержание РСР в моче и меконии (см. раздел “Опиаты”) новорожденного составило 150 нг/мл и 938 нг/г, соответственно, при этом концентрация РСР в моче матери была 287 нг/мл.Содержание РСР и метаболитов при интоксикации и смертных случаях
Концентрация РСР в биожидкостях при интоксикациях различной степени тяжести изменяется в широких пределах. При действии небольших доз содержание РСР в крови от 10 до 180 нг/мл (n=50), в моче от 28 до 670 нг/мл (n=31). При тяжелых отравлениях диапазон РСР 0,005–1 мкг/мл в крови и 0,4–18 мкг/мл в моче. В случае летального исхода от передозировки содержание РСР в крови 0,3–25 мкг/мл, в моче 0,4–48,6 мкг/мл, в ткани мозга 0,1–32 мкг/г, в ткани печени 0,9–80 мкг.Глава 8. Метилендиоксипроизводные амфетамина
Существует большая группа наркотических средств, которые синтезируются в условиях, приближенных к заводским, и выглядят подобно обычным лекарственным средствам как таблетки, капсулы или порошки. Эта группа включает большое количество соединений, например, аналоги фентанила и распространенные в настоящее время метилендиоксипроизводные амфетамина, среди которых огромной популярностью среди молодежи пользуется средство экстази (жидкий экстази – уличное название у–оксибутирата).Для противодействия государственному контролю наркотиков подпольные лаборатории выработали тактику производить соединения, еще законодательно не регулируемые, за счет некоторой химической модификации молекулярной структуры, сохраняющей или даже увеличивающей фармакологическую активность исходных соединений. Пользователи и уличные торговцы дают этим новым средствам привычные «уличные» названия, под которыми распространяются предшествующие контролируемые аналоги, или даже имена других наркотиков, уже завоевавших нелегальный рынок. Покупатели этих средств часто оказываются жертвами передозировок из–за отсутствия информации о возросшей активности препаратов, как это было с аналогами фентанила (см. далее).
Помимо основного активного компонента, наркотики, поступающие в нелегальную продажу, обычно содержат различные добавки других химических веществ. Состав компонентов в капсулах одного и того же вида меняется от случая к случаю, по–видимому, из–за перемены в составе сырья, доступного в данный момент подпольной лаборатории для производства. Это также может приводить к серьезным проблемам для пользователей.
Синтезированные в подпольных лабораториях синтетические средства оказываются весьма выгодными для наркобизнеса, но таят в себе огромную опасность непредсказуемости последствий для потребителя.
Метилендиоксипроизводные амфетамина. Группа «экстази»
Синтезированный в 1914 г. метилендиоксиметамфетамин (МДМА, известный под «уличным» названием «экстази») некоторое время использовался в психиатрии в качестве средства, снижающего беспокойство и придающего пациенту эмоциональную открытость. Отсутствие информации о тяжелых побочных эффектах и привыкании, свойственных другим подобным средствам, обусловило его популярность и отсутствие социального противодействия распространению в обществе. Долгое время считалось, что МДМА и родственные соединения безопасны для употребления в обществе близких друзей для отдыха, расслабления и снятия барьеров при общении.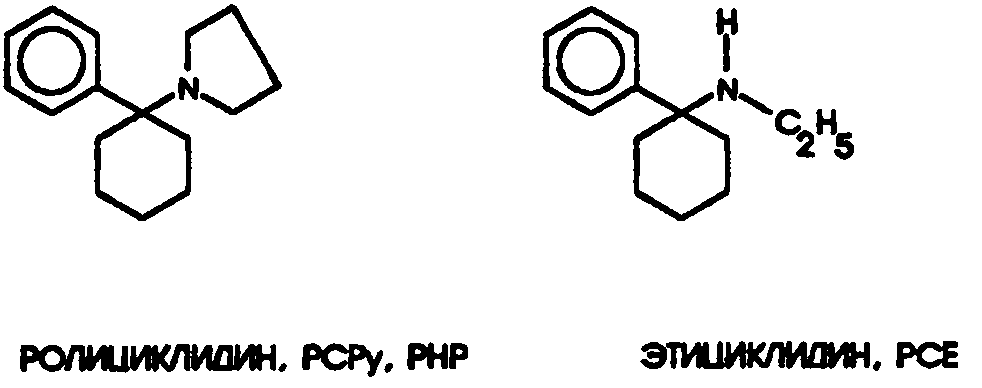 Однако по мере ознакомления с последствиями применения этих соединений отношение к ним стало меняться, и в официальном заключении ДЕА (Drug Enforcement Administration, Управление по борьбе с распространением наркотиков, США), посвященном соединениям этой группы, были высказаны соображения о ложности распространенного мнения о безопасности их использования для человека. Было установлено, что, подобно всем амфетаминам, МДМА опасно для людей с нарушениями системы кровообращения и с сердечными расстройствами, появились сообщения о вредных побочных эффектах, о психотических отклонениях и мозговых нарушениях среди лиц, употреблявших МДМА. В результате были приняты срочные правительственные акты, которые позволили ДЕА рассматривать нелегальное применение МДМА и родственных соединений как угрозу общественному здоровью и объявить их средствами, запрещенными к применению.
Однако по мере ознакомления с последствиями применения этих соединений отношение к ним стало меняться, и в официальном заключении ДЕА (Drug Enforcement Administration, Управление по борьбе с распространением наркотиков, США), посвященном соединениям этой группы, были высказаны соображения о ложности распространенного мнения о безопасности их использования для человека. Было установлено, что, подобно всем амфетаминам, МДМА опасно для людей с нарушениями системы кровообращения и с сердечными расстройствами, появились сообщения о вредных побочных эффектах, о психотических отклонениях и мозговых нарушениях среди лиц, употреблявших МДМА. В результате были приняты срочные правительственные акты, которые позволили ДЕА рассматривать нелегальное применение МДМА и родственных соединений как угрозу общественному здоровью и объявить их средствами, запрещенными к применению.
Амфетамин (АМФ), фенил–изопропила мин, структурно является родоначальником наркотических средств с различными свойствами. Модификация структуры АМФ, достигаемая введением в бензольное кольцо циклического 3,4–метилендиокси–заместителя (табл. 1) привела к появлению нового класса наркотических веществ, отличающихся как от родоначальника – стимулятора ЦНС амфетамина, так и от структурно близкихгаллюциногенов класса мескалина – метокси–производных амфетамина. Метилендиоксипроизводные амфетамина (МДОА) оказывают на человека столь специфическое воздействие, что их выделяют в особый класс энтактогенов. Основные представители этого класса в настоящее время: МДА, МДМА, МДЕА, БДБ и МБДБ. Все эти соединения запрещены для употребления и введены в Список 1 Конвенции ООН и Постоянного комитета по контролю наркотиков РФ. Тем не менее в некоторых странах МДМА легально применяют в психотерапии для облегчения лечения, а также назначают онкологическим больным в терминальной стадии.
МДОА получили широкое распространение в настоящее время во многих странах, включая РФ, из–за их способности вызывать легкую эйфорию й особое психическое состояние, проявляющееся в расширении и обострении эмоционального восприятия, возрастании силы эмоций и ощущений. Возникающее при этом чувство эмоциональной близости и повышенного доверия к окружающим, миролюбие и сочувствие, потребность в интеллектуальных и физических контактах, а также повышенная самооценка, исчезновение неловкости и застенчивости проявляются в возрастании коммуникабельности и общительности. Эти свойства обеспечивают особую привлекательность МДОА в среде молодежи, поклонников стиля рейв или техно, на вечеринках и дискотеках, собирающих огромные массы молодых людей й сопровождающихся громкой музыкой, световыми и звуковыми эффектами и продолжающихся всю ночь. Эмоциональные эффекты не сопровождаются стимулирующими и галлюциногенными проявлениями. Галлюциногенный эффект развивается при употреблении МДА в высоких дозах, в незначительной степени свойствен МДМА и не наблюдается для МБДБ. В этом смысле МБДБ является «чистым» энтактогеном.
Таблица 1. Метилендиокси–аналоги амфетамина.
 МДА – 3,4–метилендиоксиамфетамин (Love Drug).
МДМА – 3,4–метилендиоксиметамфетамин (Ecstasy. Adam, ХТС, ESSENCE).
МДЕА – N–этил–3.4–метилендиоксиамфетамин (Eve).
МДДМА – N,N–диметил–3,4–метилендиоксиамфетамин.
БДБ – 1–(3,4–метилендиоксифенил)–2–бутанамин.
МБДБ – N–метил–1–(3,4–метилендиоксифенил)–2–бутанамин.
N–OH–МДА–N–гидрокси–3,4–метилендиоксиамфетамин (FANTASY) (молярные массы приведены в скобках).
МДА – 3,4–метилендиоксиамфетамин (Love Drug).
МДМА – 3,4–метилендиоксиметамфетамин (Ecstasy. Adam, ХТС, ESSENCE).
МДЕА – N–этил–3.4–метилендиоксиамфетамин (Eve).
МДДМА – N,N–диметил–3,4–метилендиоксиамфетамин.
БДБ – 1–(3,4–метилендиоксифенил)–2–бутанамин.
МБДБ – N–метил–1–(3,4–метилендиоксифенил)–2–бутанамин.
N–OH–МДА–N–гидрокси–3,4–метилендиоксиамфетамин (FANTASY) (молярные массы приведены в скобках).
Побочные эффекты употребления МДОА: обильное потоотделение, непроизвольное заклинивание челюсти, прикусывание щек, затуманенное зрение, колебания кровяного давления.
При длительном употреблении МДОА развивается толерантность, а характер воздействия меняется в сторону усиления отрицательных эффектов. Наиболее серьезными последствиями являются необратимые процессы в мозге, а именно тяжелые нейротоксические нарушения серотонергической системы.
Токсические эффекты передозировки МДОА: ■ тахикардия ■ повышение кровяного давления ■ аритмия ■ расширение зрачков ■ потение ■ головокружение ■ беспокойство, возбуждение ■ бессонница ■ судороги ■ сведение челюстей ■ напряжение мышц.
Среди психических нарушений – глубокие длительные депрессии, панические состояния, параноидальные реакции.
Смерть наступает в результате осложнений сердечно–сосудистой системы, острой сердечной недостаточности и остановки сердца, отказа почек, а также гипертермии (до 40–42°С), чему способствует окружающая обстановка дискотек и вечеринок, обычно сопутствующая приему МДОА: большое скопление людей, повышенная температура помещения, длительная интенсивная физическая нагрузка, недостаточный прием жидкости, обезвоживание. При аутопсии установлены также значительные изменения печени, почек и мозга у лиц, употреблявших МДМА и МДЕА.
Прием МДОА часто является косвенной причиной смерти при дорожно–транспортных происшествиях, когда после спада основных эффектов развиваются сонливость, спутанность сознания, нарушение координаций и способности концентрироваться.
Известны также случаи суицидов, в той или иной степени связанных с употреблением МДМА.
Примеси в продуктах подпольного синтеза
Нелегальный синтез подпольными лабораториями осуществляется разными методами. В зависимости от выбора в препарате могут присутствовать примеси, указывающие на способ нелегального синтеза. Обычный набор примесей, включающий исходные, промежуточные и побочные продукты синтеза, приведен ниже. ■ сафрол ■ изосафрол ■ гликоль изосафрола ■ пиперонилацетон (3,4–метилендиоксифенил–2–пропанон) ■ N–формил–3,4–метилендиоксиметиламфетамин ■ N–формил–3,4–метилендиоксиметилметамфетамин ■ 1–(3,4–метилендиоксифенил)–2–бромпропан и другие.Формы и способы употребления
В нелегальную продажу МДОА поступают в виде солянокислых солей (гидрохлоридов) в форме таблеток, капсул или порошков. Наиболее распространенной формой являются таблетки с различными логотипами на поверхности. Основной способ употребления – оральный, но также применяется ингаляция через нос и внутривенное введение. В состав таблеток входят различные наполнители и добавки: крахмал, лактоза, сахароза, карбонат кальция, сода, кофеин, аспирин, парацетамол, хинин и др. Нередко одна таблетка содержит два–три соединения класса: например, МБМА и МДЕА или МДБД и МДЕА.Разовая доза в зависимости от типа соединения 50–100 (80–125) мг (для МДА – до 230 мг), при развитии толерантности количество может быть увеличено до 300–500 мг, однако доза выше 500 мг приводит к летальному исходу.
Фармакокинетика метилендиоксиамфетаминов
Фармакологический эффект проявляется через 30–45 мин после орального приема, достигает максимума через 1–1,5 ч и продолжается от 3 до 10 (4–6) ч. Последействие может продолжаться в течение нескольких дней. Период «полужизни» МДМА в плазме T½ =7,6 ч. После приема внутрь соединения быстро всасываются и через 15–30 мин могут быть обнаружены в плазме.Концентрация МДМА в крови, определяемая как «терапевтическая», составляет 0,1–4),35 мг/л, а летальные значения колеблются в пределах 0,9–2,0 мг/л для МДМА и 2–10 мг/л для МДА. Интервал концентрации в плазме для 7 случаев токсикологического анализа: МДМА 62–528 нг/мл, метаболита МДА 20–60 нг/мл.
После орального приема дозы МДМА 1,5 мг/кг двумя субъектами максимальная концентрация в плазме достигается через 2 ч и составляет около 330 нг/мл. Затем в интервале от 2 до 9 ч следует медленное уменьшение до 130–170 нг/мл. Спустя 9 ч после приема значительные количества МДМА присутствуют в плазме. Через 24 ч после приема разовой дозы 50 мг МДМА концентрация в плазме снижается до 5 нг/мл. В плазме обнаруживается единственный метаболит МДА, который появляется спустя 135 (субъект А) и 90 (субъект Б) мин после приема и достигает максимальной концентрации 15,3 (субъект А) и 10 (субъект Б) нг/мл через 380 и 150 мин, соответственно.
Всасывание из ЖКТ происходит быстро. Соединения легко преодолевают гематоэнцефалический барьер.
Метаболизм метилендиоксиамфетаминов
Биотрансформация МДОА (см. рис 1) протекает в основном как два перекрывающихся процесса.Первый – не затрагивает циклический заместитель и включает: ■ Дезалкилирование азота боковой цепи (метаболит 1). ■ Окислительное дезаминирование (метаболит V). ■ Гидроксилирование ароматического кольца (метаболит VI).
Второй идет с окислением метилендиоксизаместителя и образованием соответствующих 3,4–метокси– и/или гидроксизамещенных фенилалкиламинов (метаболиты II–IV). Аналогичный процесс идет и с участием метаболитов I (VII, VIII) и метаболитов V (IX, X). Гидроксилированные метаболиты далее конъюгируются с образованием глюкуронидов и сульфатов.
Основные метаболиты МДМА и МДЕА – 4–гидрокси–3–метоксипроизводные (III на схеме). Деалкилированный метаболит МДА образуется в меньшем количестве.
Основные метаболиты МДМА ■ 4–гидрокси–3–метоксиметамфетамин (ГММА, III) ■ 3,4–метилендиоксиамфетамин (МДА, I).
Минорные метаболиты МДМА ■ 3,4–дигидроксиметамфетамин (ГГМА, II) ■ 4–гидрокси–3–метоксиамфетамин (ГМА, VIII) ■ 3,4–дигидроксиамфетамин (ГГА, VII).
Основные метаболиты МДЕА ■ 4–гидрокси–3–метоксиэтиламфетамин (ГМЭА) ■ 3,4–метилендиоксиамфетамин (МДА).
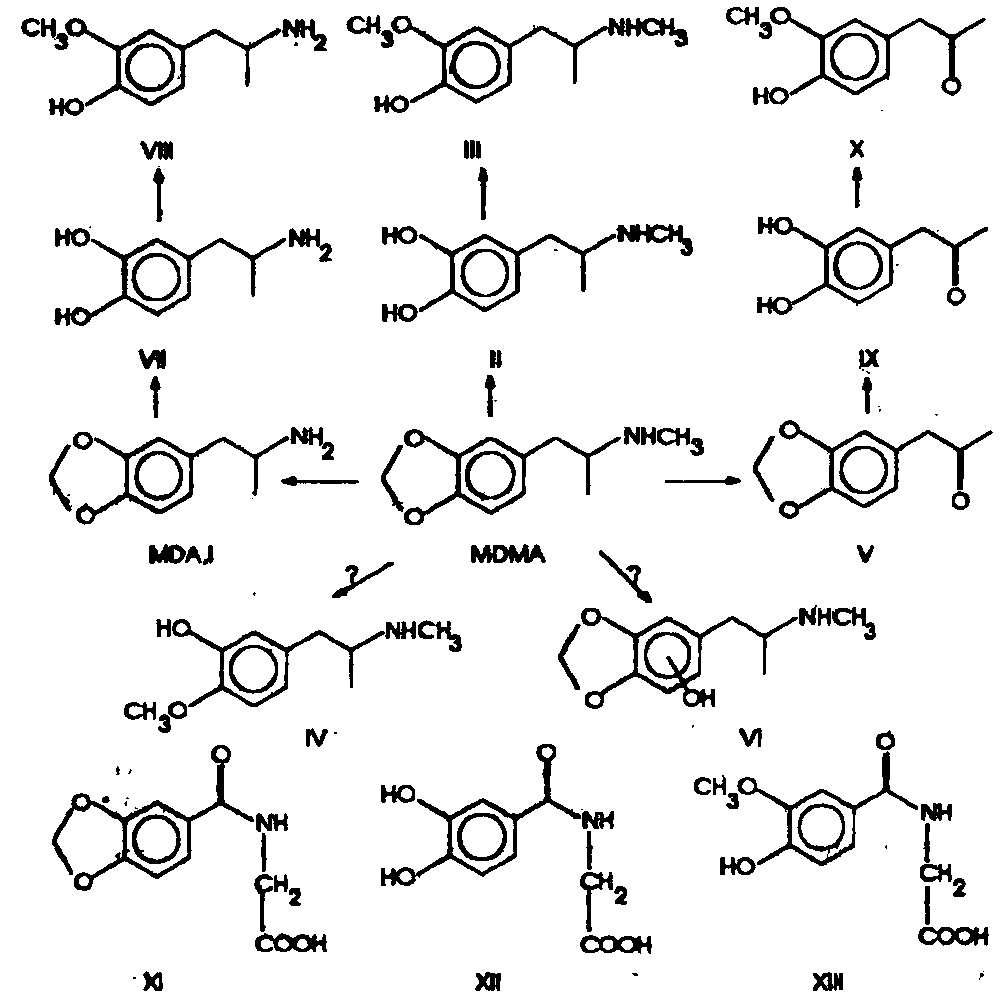 Рис. 1. Схема метаболических превращений МДМА:
I – метилендиоксиамфетамин (МДА), II – 3,4–дигидроксиметамфетамин, III – 4–гидрокси–3–метоксиметамфетамин, IV – 3–гидрокси–4–метоксиметамфетамин, V – 3,4–метилендиоксифенил–2–пропанон, VI – гидрокси–МДМА, VII – α–метилдофамин, VIII – 3–метокси–α–метилдофамин, IX – 3,4–дигидроксифенил–2–пропанон, X – 4–гидрокси–3–метоксифенил–2–пропанон, XI, XII, XIII – 3,4–замещённые гиппуровые кислоты. IV и VI – вероятные метаболиты.
Рис. 1. Схема метаболических превращений МДМА:
I – метилендиоксиамфетамин (МДА), II – 3,4–дигидроксиметамфетамин, III – 4–гидрокси–3–метоксиметамфетамин, IV – 3–гидрокси–4–метоксиметамфетамин, V – 3,4–метилендиоксифенил–2–пропанон, VI – гидрокси–МДМА, VII – α–метилдофамин, VIII – 3–метокси–α–метилдофамин, IX – 3,4–дигидроксифенил–2–пропанон, X – 4–гидрокси–3–метоксифенил–2–пропанон, XI, XII, XIII – 3,4–замещённые гиппуровые кислоты. IV и VI – вероятные метаболиты.
Минорные метаболиты МДЕА ■ 3,4–дигидроксиэтиламфетамин (ГГЭА) ■ 4–гидрокси–3–метоксиамфетамин (ГМА) ■ 3,4–дигидроксиамфетамин (ГГА).
Продукты окислительного дезаминирования: 4–гидрокси–3–метоксифенилацетон (ГМФА, X), 3,4–дигидроксифенилацетон (ГГФА, IX) и 3,4–метилендиоксифенил–2–пропанон (пиперонилацетон, V) образуются в следовых количествах.
МБДБ и БДБ претерпевают аналогичную биотрансформацию. Однако в отличие от пропиламинов (МДА, МДМА и МДЕА), которые образуют 3,4–замещенные бензойные кислоты, далее вступающие в реакцию конъюгации с глицином с образованием 3,4–замещенных гиппуровых кислот (XI–XIII), для бутанаминов (МБДБ и БДБ) подобное направление не установлено.
Выведение
Значительная часть принятого МДМА выводится в виде исходного соединения (65% дозы в 50 мг в течение 20 ч) и основного метаболита ГММА. На долю деалкилированного метаболита МДА приходится 7% дозы. Для дозы МДМА 1,5 мкг/кг концентрация в пробах мочи, собранной за время 16–21,5 ч, составляет, (мкг/мл): МДМА – 28,1, ГММА – 35,1, ГМА – 1,2, МДА – 2,3.Средний интервал концентраций неизмененного МБДБ в моче (10 образцов) при введении обычных разовых доз: 0,10–24 мкг/мл, МДЕА (8 образцов мочи, отобранных в период 1–7 ч) 1––23 мкг/мл. При неконтролируемом употреблении неизвестных доз (систематическое обследование служащих вооруженных сил США) интервал содержания в моче МДМА 0,38–96,2 (среднее значение 13,4), метаболита МДА – 0,15–8,6 (среднее 1,6) мкг/мл. После приема внутрь 100 мг МБДБ пик концентрации МБДБ в моче приходится на 4 ч, а в слюне – на 2 ч. Биожидкости дают положительный отклик при скрининге иммунными методами в течение 36 часов для мочи и 17 часов для слюны. Кроме исходного МБДБ, в значительно меньшем количестве присутствует метаболит БДБ.
В табл. 2 проиллюстрирована кинетика выведения с мочой Исходного соединения и метаболитов после орального приема 1,5 мг/кг МДМА в интервале 1,5–24 ч.
При употреблении разовой дозы МДА концентрация родительского соединения в моче 10 мкг/мл (в плазме 0,4). При хроническом потреблении концентрация МДА в моче значительно выше: 50–150 мкг/мл (в плазме 5–25.мкг/мл).
Основной метаболит выведения МДЕА – ГМЭА, концентрация деалкилированного метаболита МДА в моче значительно меньше (см. табл. 3).
По данным анализа 34 проб мочи живых лиц, употреблявших МДМА, отношение количества деметилированного метаболита МДА (диапазон 0,15–8,6 мкг/мл) к содержанию родительского соединения МДМА (диапазон 0,38–96,2 мкг/мл) не превышало 0,15. В случае потребления МДЕА количество деалкилированного метаболита МДА в моче в период 1–4 ч после Введения также не превышает 10–15% от количества исходного соединения. На основании этих количественных соотношений предложено проводить ориентировочное дифференцирование потребления МДА в смеси с аналогами (МДМА и/или МДЕА) от его образования в качестве метаболита. При более высоком содержании МДА по отношению к МДМА или МДЕА можно предполагать совместное употребление группы родственных соединений. Те же рекомендации высказываются относительно МБДБ и БДБ, поскольку последний, являясь деалкилированным метаболитом МБДБ, может также употребляться самостоятельно.
Таблица 2. Концентрация МДМА и метаболитов в моче, мкг/мл. МДМА 1,5 мг/кг (орально).
| Время отбора мочи, час | 1,5 | 3,5 | 5,5 | 7;5 | 10,4 | 22 | 24 |
|---|---|---|---|---|---|---|---|
| МДМА | 1,5 | 16 | 22 | 14 | 21,5 | 28 | 21,5 |
| НММА | 0 | 24 | 5 | 14 | 16 | ||
| НМА | 0 | 1,0 | 1,2 | 1,2 | |||
| МДА | 0 | 0,11 | 1,5 | 2.3 | 2,3 |
Таблица 3. Концентрация МДЕА и метаболитов в моче, мкг/мл. Доза МДЕА 140 мкг (n=1)
| Время, час | МДЕА | ГМЭА | МДА |
|---|---|---|---|
| 1 | 5,41 | 10,96 | 0,15 |
| 2 | 5,84 | 17,54 | 0,29 |
| 3 | 7,29 | 5,5 | 0,59 |
| 4 | 12,08 | 5,9 | 1,98 |
| 5 | 1,80 | 1,19 | 0,34 |
| 6 | 2,07 | 2,94 | 0,57 |
Время обнаружения метилендиоксиамфетаминов в моче
Исходное соединение и основные метаболиты могут быть обнаружены в биожидкости методами ПФИА и ГХ/МС спустя 1–2,5 сут после употребления. Так, после приема разовой дозы МДЕА 140 мг: исходное соединение и ГГЭА обнаруживаются в моче в течение 33–62 ч, МДА – 32–36 ч, основной метаболит ГМЭА – 7–8 дней, а ГМА, ГГА, ГМФА, ГГФА и пиперонилацетон в следовых количествах детектируются только первые несколько часов после приема. Таким образом, факт потребления МДЕА может быть установлен по длительному, до 7–8 дней, обнаружению в моче его основного метаболита ГМЭА. При употреблении 100 мг МБДБ моча дает положительный результат при иммунных анализах в течение 36 ч, а слюна – в течение 17 ч.Содержание в волосах
При систематическом употреблении МДОА могут детектироваться в волосах в широком диапазоне концентраций. В частности, найдено для волос головы, подмышечной впадины, паха и ног, соответственно: МДМА – 53,38; 16,17; 35,37 и 67,62 нг/мг, МДА – 7,96; 2,07; 4,19 и 12,50 нг/мг и АМФ – 10,16; 2,65; 6,35 и 15,60 нг/мг.Энантиомеры метилендиоксиамфетаминов
Поступающий в нелегальную торговлю МДМА представляет собой рацемическую смесь энантиомеров, которые различаются по фармакокинетическим свойствам. Выведение нейротоксичного S–(+)–МДМА, как и его метаболита S–(+)–МДА, примерно вдвое превышает выведение R–(–)–МДМА и R–(–)–МДА. В опытах с крысами было показано, что в различных участках мозга уровень (–)–МДМА выше, и, соответственно, уровень метаболита (–)–МДА ниже, чем для (+)–энантиомеров, что говорит о меньшей метаболитической активности (–)–МДМА в мозге крыс. Профили энантиомеров МДМА и метаболита МДА после введения 10 мг/кг рацемического МДМА, отражающие распределение в мозговую ткань и выведение в мочу, аналогичны.Смертные случаи, связанные с употреблением МДОА
Смерть непосредственно от употребления МДОА наступает, в основном по причине острой сердечной недостаточности и обезвоживания организма. При анализе биожидкостей и тканей в случаях смертей, связанных с систематическим употреблением МДА, МДМА, МДЕА и МБДБ, данные показывают широкий интервал концентраций исходных соединений и метаболитов, например, 0,9–2 мкг/мл МДМА и МДЕА в крови. В одном из описанных случаев гибели, связанной с приемом МДМА, приводятся величины концентраций: МДМА (мкг/мл) в крови 2,32, в моче 118,8 и в стекловидном теле 1,11, метаболита МДА (мкг/мл): в крови и стекловидном теле менее 0,25, в моче 3,86. При потреблении МДА «фатальные» концентрации МДА в крови 2,3–26, в моче 46–175 мкг/мл. Результаты анализа часто указывают на одновременное (или последовательное в течение небольшого интервала времени) введение смеси родственных соединений. В одном из таких примеров, например, концентрации МДА, МДМА и МДЕА в крови соответственно составили 0,25; 0,43 и 0,3 мг/л.Описано немало смертных случаев при автокатастрофах, связанных с употреблением МДМА, МДЕА и МБДБ. Для такого случая приводятся величины, характеризующие распределение МДЕА в тканях органов (мг/кг):
| печень | 4,51 |
| почки | 2,55 |
| сердце | 1,68 |
| легкие | 4,54 |
| селезенка | 3,33. |
Глава 9. Фентанил и его аналоги
Фентанил и его аналоги представляют класс синтетических наркотиков, многие из которых синтезированы в подпольных лабораториях с использованием обычных доступных реагентов и простого химического оборудования. Биологическое действие фентанилов подобно действию опиатов, однако некоторые фентанилы по эффективности в сотни раз превышают эффективность морфина.К настоящему времени синтезировано более сотни аналогов фентанила, которые различаются только по силе и продолжительности действия, из них более 12 циркулируют на нелегальном рынке наркотиков в различных странах. Высокая эффективность, низкие дозы, требующиеся для создания эффекта, множественность продуцируемых эффектов, возможность получения структурных аналогов делают детектирование аналогов фентанила, находящихся в нелегальной продаже, очень трудным. Несмотря на повсеместную борьбу с нелегальным производством, распространением и потреблением фентанилов, их чрезвычайно высокая эффективность и относительная легкость синтеза делают эти наркотики серьезной угрозой всему миру.
Фармацевтическое использование фентанила и аналогов
Фентанил (далее ФНТ), химическое название М–(1–фенэтил–4–пиперидил) пропионанилид – синтетический наркотический анальгетик высокой эффективности (в 100 раз сильнее морфина) и короткого действия был синтезирован впервые в конце пятидесятых фармацевтической компанией в Бельгии (Janssen). Под названием Sublimaze он введен в клиническую медицину как внутривенный анестетик для пре– и постоперативной медикации. Действие наступает через 1–2 мин и длится 30–60 мин.Вскоре после этого синтезированы два других аналога: альфентанил (далее АФТ), (alfentanil, Alfenta*) и суфентанил (далее СФТ), (Sufentanil, Sufenta*). Оба предназначены для обезболивания при хирургических операциях: АФТ как анальгетик ультракороткого действия (5–10 мин) и СФТ, вследствие исключительной эффективности анальгетического действия, – для использования в кардиохирургии (рис. 1, схема 1).
Среди других соединений этой группы следует выделить карфентанил – очень сильный анальгетик, используемый в ружейных капсулах для обездвиживания диких животных и лофентанил, отличающийся очень длительным действием, который эффективен в травматологии.
Фентанил. Фармацевтическое использование
При медицинском использовании в качестве анестетика для премедикации, первичной анестезии и постхирургического обезболивания ФНТ вводится внутривенно. Для этой цели он выпускается в ампулах по 2–20 мл с концентрацией 50 мкг/мл под наименованием Sublimaze и в комбинации с 2,5 мг/мл дроперидола под названием Innovar. Терапевтическая доза ФНТ 2–50 мкг/кг.Основная область применения ФНТ – кардиохирургия, где его используют в комбинации с окисью азота и мускульными релаксантами для уменьшения вызываемой опиатами ригидности и для обеспечения принудительной вентиляции.
ФНТ применяется также в виде пластыря для чрезкожного обезболивания (Duragesic) при хронических болях у пациентов, которым показано опиоидное обезболивание, обычно в дозах 25 мкг/ч/10 см2 поверхности. Кроме того, применяются более высокие дозы 50, 75 и 100 мкг/ч для пластырей размера 20, 30 и 40 см2, соответственно.
 Рис. 1. Структура фентанила и некоторых аналогов. 1 – фентанил (ФНТ). 2 – суфентанил (СФТ). 3 – альфентанил (АФТ). 4 – α метилфентанил (АМФ). 5 – 3–метилфентанил (3–МФ).
Рис. 1. Структура фентанила и некоторых аналогов. 1 – фентанил (ФНТ). 2 – суфентанил (СФТ). 3 – альфентанил (АФТ). 4 – α метилфентанил (АМФ). 5 – 3–метилфентанил (3–МФ).
Схема 1. Фармацевтические аналоги фентанила.
 В настоящее время используются также таблетки ФНТ на держателе (типа леденца) как средство для премедикации в педиатрии и для раковых пациентов.
В настоящее время используются также таблетки ФНТ на держателе (типа леденца) как средство для премедикации в педиатрии и для раковых пациентов.
Таблица 1. Сравнение фармакологической активности аналогов фентанила (данные из опытов с животными)
| Наркотик | ЕД50мг/кг ВВ | ЛД50мг/кг ВВ | ЛД50/ЕД50 | Относит. эффективность | Пик эффекта, мин |
|---|---|---|---|---|---|
| морфин | 3 | 200 | 67 | 1 | 4 |
| фентанил | 0,015 | 5 | 333 | 200 | 4 |
| альфентанил | 0,1 | 20 | 200 | 30 | 1 |
| суфентанил | 0,0015 | 3 | 2000 | 2000 | 8 |
| 3–метилфентанил * | 0,0005 | 1 | 2000 | 6000 | – |
Аналоги фентанила. Фармацевтическое использование
Все аналоги ФНТ относятся к опиоидам, так как связываются опиатными рецепторами, и их фармакологическое действие, в том числе и побочные эффекты, подобны опиатным, но различаются по силе и продолжительности действия (табл. 1).АФТ в дозах 8 мкг/кг вызывает анестезию длительностью 5–16 минут и пробуждение через 2–20 мин. По сравнению с ФНТ обезболивающее действие АФТ оценивается как 0,25, угнетение дыхания – 0,1, продолжительность короче на 2/3. Благодаря короткому действию (около 15 мин), АФТ часто используется при небольших хирургических операциях. В отличие от ФНТ, который аккумулируется в организме и при повторных приемах проявляется повторным эффектом угнетения дыхания, АФТ в тканях сохраняется ограниченно и может использоваться для аналгезии среднего или продолжительного действия без развития повторного эффекта угнетения дыхания.
СФТ, обладая анальгетической активностью, в 2000 раз превышающей активность морфина, применяется в кардиохирургии в дозах 10–30 мкг/кг. Схема 2. Запрещенные аналоги фентанила

Нелегальное использование фентанила
Начало нелегального использования ФНТ приходится на середину семидесятых годов, когда появились сведения об использовании фармацевтического ФНТ в качестве допинга на лошадиных скачках и о его применении врачами, медсестрами и фармацевтами в немедицинских целях. Сообщалось о смертных случаях от сверхдозы ФНТ после съедания пластыря с ФНТ. Известны случаи курения украденных или использованных пластырей или вдыхания через трубку счищенного с пластыря вещества при нагревании его на алюминиевой фольге.Запрещенные аналоги фентанила
Подпольно синтезированные аналоги фентанила впервые появились в 1979 г., когда было установлено, что причиной большого числа смертей в Калифорнии (США) от сверхдозы неизвестного наркотика, представленного распространителями «на улице» как героин, является аналог фентанила – α–метилфентанил (далее АМФ). Дальнейшее изучение показало, что АМФ в 2 раза сильнее самого ФНТ и в 200 раз сильнее морфина. Симптомы, обнаруженные при вскрытиях, были идентичны известным симптомам, сопутствующим смертям от передозировки героина. Сообщалось, что жертвы принимали наркотик, называемый либо China White, либо Synthetic Heroin. Причиной всех этих смертей явилась передозировка, поскольку жертвы не имели информации о значительном превышении эффективности АМФ по отношению к героину.В следующее десятилетие в нелегальной продаже появилось, по крайней мере еще 10 различных аналогов ФНТ, за чем последовало более 100 зарегистрированных смертей, непосредственно приписываемых их действию.
Пик нелегального использования фентанилов в США приходился на 1985 г., затем в течение нескольких последующих лет наблюдалось устойчивое снижение до осени 1988 г. когда подпольные лаборатории синтезировали и выбросили на нелегальный рынок 3–метилфентанил (3–МФ) – мощный и наиболее опасный аналог фентанила, в 6000 раз превышающий морфин и в 1000 раз героин по эффективности и вызвавший новую вспышку смертей среди опийных наркоманов. Минимальная летальная доза 3–МФ оценивается в 250 мкг. В настоящее время это наиболее распространенный аналог фентанила, представляющий смесь цис– и транс–изомеров в соотношении 80:20. ФНТ также синтезируют в подпольных лабораториях, и в этом случае он содержит примесь исходного продукта синтеза бензилфентанила. В препаратах 3–МФ присутствует некоторое количество ФНТ, побочного продукта синтеза.
Все запрещенные аналоги фентанила оказывают на организм качественно подобное фармакологическое действие опиатного типа и отличаются только по эффективности и продолжительности действия.
К настоящему времени в нелегальном обороте наркотиков могут находиться аналоги фентанила (схема 2): ■ 3–метил–фентанил ■ α–метилфентанил ■ ацетил–α–метилфентанил ■ бета–гидроксифентанил ■ тиофентанил ■ α–метилтиофентанил ■ пара–фторфентанил ■ бета–гидрокси–3–метилфентанил.
Все они являются запрещенными и включены в Список 1 Конвенции ООН и Постоянного комитета РФ по контролю наркотиков. Однако нельзя исключать появления новых соединений этого класса, несколько отличающихся по химической структуре, но сохраняющих наркотическую активность.
Формы и способы введения при нелегальном использовании фентанила и аналогов
Наиболее распространенный способ введения ФНТ – внутривенное введение, также, подобно героину, ФНТ курят и вдыхают носом. Имеются сведения о существовании двух форм препарата: для колющих наркотик («shooters») и для использующих интраназальный способ («snorters»). Запрещенные аналоги фентанилов обычно разбавляют очень большим количеством лактозы или крахмала и иногда смешивают с кокаином или героином. Так как «уличные» образцы содержат слишком малые количества активного средства, обычно менее 1%, они, как правило, не отличаются по цвету, запаху или вкусу. Окраска образцов ФНТ может изменяться от чисто белого («Persian White») до беловатого или светло–бежевого («China White», «Synthetic Heroin», «Fentanyl») и светло– и темно–коричневого («Mexican Brown»). Коричневый цвет придает лактоза, которая при нагревании подвергается карамелизации. Текстура образцов также изменяется от легкого и тонкого порошка до более грубого, рыхлого, похожего на сухое молоко. Иногда образцы ФНТ могут иметь медицинский или химический запах, но это не может рассматриваться как характеристическое свойство. Внешний вид образцов ФНТ не содержит никаких особых черт, что позволило бы визуально отличить его от героина. Идентифицировать фентанил и аналоги можно только при химическом анализе.Токсическое и наркотическое действие аналогов фентанила
Фентанилы продуцируют все эффекты и побочное действие классических наркотических анальгетиков. Среди известных в настоящее время средств они являются наиболее эффективными анальгетиками, способными приносить стойкое облегчение при болях при приеме низких доз.Инъекции 50–100 мкг фармацевтического ФНТ вызывают анальгезию и быструю потерю сознания. Развитие неполной амнезии, гипотензии или гипертензии происходит в меньшей степени, чем это известно для морфина, а продолжительность периода угнетения дыхания короче.
Побочные эффекты: ■ эйфория ■ угнетение дыхания ■ суженные в булавочную головку зрачки ■ увеличение мускульного тонуса ■ тошнота.
Среди эффектов, не свойственных опиатам, после употребления ФНТ иногда наблюдается уменьшение частоты пульса и падение кровяного давления у хирургических больных.
При регулярном приеме аналогов ФНТ, как и в случае с другими наркотическими анальгетиками, развивается толерантность и физиологическая зависимость. В экспериментах с животными подтверждено, что производные ФНТ имеют перекрестное замещение с морфином и подобно опиатам обладают наркотической активностью. Опийные наркоманы воспринимают ФНТ как заменитель героина со сходными эффектами.
Клинические проявления сверхдозы фентанила: ■ глубокое подавление дыхания ■ брадикардия ■ гипотензия ■ ригидность стенок грудной клетки ■ тошнота, рвота ■ конвульсии ■ кома.
Минимальная летальная доза ФНТ 2 мг.
Благодаря высокой липидной растворимости, независимо от способа введения аналоги фентанила быстро достигают мозга, что обеспечивает быстрое начало действия: первые эффекты развиваются в течение 90 с после внутривенного введения ФНТ, через 2 мин достигается состояние релаксации и эйфории. Пик эффекта подавления дыхания приходится на время 2–3 мин. В случае отсутствия толерантности в это время может произойти спонтанная остановка дыхания и даже смерть от передозировки.
Длительность фармакологического действия меняется в зависимости от используемого соединения. Эффекты опиатного типа сохраняются в течение 5 мин для альфентанила, 30–60 мин для ФНТ, около 4 ч для 3–метилфентанила.
Эффекты, наблюдаемые при аутопсии
Почти во всех случаях смертей, вызванных приемом сверхдозы фентанила, диагностируется отек легких и эмболия. Наблюдаются также старые следы уколов и места новых инъекций. Результаты вскрытия и обстоятельства, сопутствующие смерти от фентанила, подобны случаям «внезапной смерти», последовавшей за приемом героина. Непосредственной причиной смерти чаще всего является подавление дыхания, что вполне согласуется с известными фармакологическими свойствами фентанилов. Реже встречаются такие симптомы, как бронхопневмония или засасывание желудочного содержимого в легкие.Хотя большинство жертв фентанила, как правило, имеют длительный опыт его внутривенного использования, патология различных органов развивается в незначительной степени. Редки даже случаи хронического воспаления печени или цирроз.
Значительным фактором риска является прием алкоголя. В огромном числе случаев этанол сопутствует смертям от сверхдозы фентанилов и, кроме того, присутствует часто в количествах, вызывающих обычную алкогольную интоксикацию.
Фармакокинетика фентанила и аналогов
Практически все сведения о фармакокинетических свойствах аналогов ФНТ получены для фармацевтических препаратов (табл. 2). Фентанилы обычно вводят внутривенно или внутримышечно. Клинических данных об интраназальном, легочном (курение) и желудочно–кишечном всасывании очень мало.Фентанилы хорошо растворяются в липидах и поэтому легко и быстро преодолевают мембранный барьер и эффективно всасываются при любом способе введения. После внутривенного введения фентанилы быстро исчезают из кровяного русла и распределяются по системам организма, где связываются с периферическими тканями, протеинами плазмы и красными кровяными тельцами. Более 90% дозы ФНТ выводится из плазмы в течение 5 мин. Благодаря широкому распределению в периферические ткани ФНТ имеет большой кажущейся, объем распределения 60–300 л. Быстрое распределение в ткани является главной причиной короткой продолжительности действия и чрезвычайно низкой (субнанограммовые уровни) концентрации в крови и других биожидкостях. ФНТ примерно на 80% связан с белками плазмы и эритроцитами, отношение содержания в цельной крови к содержанию в плазме равно 1:1.
Таблица 2. Фармакокинетические параметры аналогов фентанила.
| Соединение | T½α, мин | T½β, мин | Клиренс, мл/мин | Объем распределения, л |
|---|---|---|---|---|
| фентанил | 13–28 | 90–360 | 150–575 | 60–300 |
| альфентанил | 16 | 100 | 178–560 | 40–70 |
| суфентанил | 17 | 150 | 730 | 150 |
Концентрации фентанилов в тканях и биожидкостях чрезвычайно низки, обычно на уровне низких значений нанограммового диапазона.
Хирургическая аналгезия, как и угнетение дыхания (основной побочный эффект, свойственный опиатам), связываются с концентрацией ФНТ в плазме 2–5 нг/мл. Для разных лиц эти величины меняются в широких пределах («межпациентная вариабельность»). В опытах с пациентами, определяющими собственную эффективную дозу послеоперационного обезболивания с помощью особого устройства для внутривенного введения, зарегистрирована эффективная концентрация ФНТ в плазме в интервале от 0,3 до 0,7 нг/мл.
После разовой внутривенной инъекции 200 мкг ФНТ максимальная концентрация в крови 3,1 нг/мл быстро уменьшается до 0,5 нг/ мл спустя 3 ч и через 7–12 ч составляет всего 0,1 нг/мл. При более высоких дозах 60 мкг/кг максимальная концентрация в плазме превышает 100 нг/мл, но уменьшается до 10 нг/мл спустя один час.
Концентрация ФНТ в плазме (842 пробы) лиц, употреблявших ФНТ с немедицинскими целями, изменяется в диапазоне 0,02–35,5 нг/ мл (среднее значение 1,2 нг/мл), но в некоторых пробах доходит почти до 4 мкг/мл.
Средняя концентрация ФНТ в крови 112 жертв передозировки, измеренная с помощью радиоиммунного анализа (РИА), высоко специфичного к фентанилам, составляет 3,0 нг/мл при диапазоне от 0,2 до более чем 50 нг/мл.
После ВМ инъекций начало действия через 7–8 мин с продолжительностью 1–2 ч.
В случае применения пластырей с ФНТ в течение 2 ч достигаются измеримые уровни ФНТ в плазме. Через 8–12 ч величины концентрации в сыворотке, плазме и крови подобны величинам, достигаемым при внутривенном введении тех же доз ФНТ.
«Леденцы» с дозой ФНТ 0,5–1 мг при оральном приеме через слизистую оболочку продуцируют эффективное обезболивание короткого действия с мягким седативным эффектом и незначительным угнетением дыхания.
Концентрация ФНТ в крови после орального приема через слизистую оболочку обычно менее 1 нг/мл. Относительно абсорбции ФНТ в желудочно–кишечном тракте информации мало. Сообщается, что после приема двумя лицами по 5 мг «леденцов» с ФНТ седативный эффект не наблюдался, но спустя 60–80 мин после приема возникало состояние сонливости, длившееся 15–20 мин. Также имеются сведения об отсутствии опиатных эффектов: седативного действия, аналгезии или угнетения дыхания после орального приема ФНТ (ампулы) по 500 мкг один или два раза в день, несколько дней в неделю в течение трех месяцев операционной медсестрой, принимавшей ФНТ как наркотик. По–видимому, высокий печеночный клиренс первой фазы метаболизма объясняет отсутствие опиатных эффектов после абсорбции ФНТ в ЖКТ.
В основном, процессы распределения, метаболизма и выведения фармацевтических аналогов фентанила сходны, хотя в количественном описании этих процессов наблюдаются значительные различия.
Хирургическая аналгезия связывается с содержанием АФТ в плазме в среднем 200–300 нг/мл. При внутривенном введении 90 мкг/кг АФТ концентрация в плазме быстро достигает максимальной величины 450 нг/мл, но уже через 1 ч падает до 70 и в интервале 6–8 ч до примерно 15 нг/мл.
Фармакокинетические параметры, приводимые в литературе для аналогов фентанила, изменяются в очень широких пределах. Хорошее согласие установлено для величин «полужизни» T½ начальной фазы, описывающей распределение ФНТ из плазмы в ткани: приблизительно 15 мин (короткая «полужизнь»). Меньшее согласие в величинах, характеризующих более поздние фазы элиминирования. Разброс значений может вызываться трудностями точного измерения чрезвычайно низких концентраций препаратов (от 10 нг/мл до менее 1 нг/мл) в крови и моче. Все же расхождение в значениях, приводимых различными исследователями, представляется слишком большим, чтобы приписывать это только различиям аналитической точности и воспроизводимости. Например, значения T½, приводимые для ФНТ, изменяются от 90 до 360 ч, величина объема распределения – от 60 до 381 л, клиренса – от 150 до,991 мг/мин. Для АФТ приводятся величины кажущегося объема распределения в диапазоне от 40 до 70 л. Возможно, что разброс величин фармакокинетических параметров отражает истинную биологическую вариабельность, а не различия аналитических методик.
Нелегальные аналоги фентанила запрещены для изучения на человеке, что объясняет отсутствие фармакокинетических данных. Из экспериментов с животными установлено, что АМФ имеет длительность действия 30 мин, а 3–МФ примерно 4 ч. Предполагается, что аналоги фентанила имеют сходный с ФНТ фармакокинетический профиль, характеризующийся быстрым распределением в ткани в пределах нескольких минут после приема, непрерывным перераспределением обратно в кровяной поток, широкой биотрансформацией и экскрецией в мочу в основном в виде различных гидроксилированных конъюгатов.
Биотрансформация
Все аналоги ФНТ быстро и широко метаболизируются по идентичному механизму, образуя около 10 более полярных метаболитов, которые фармакологически не активны.Основное направление (рис.2) – отщепление фенил–алкильного заместителя азота пиперидина: N–деалкилирование до норметаболитов. в меньшей степени идет гидролиз амидной группы до депропиониловых метаболитов. Менее значительные направления включают гидроксилирование пиперидинового кольца, фенильного кольца, или пропиониловой боковой цепи. Гидроксилированные метаболиты далее конъюгируются с образованием глюкуронидов.
Основной метаболит АФТ (рис. 3): нор–АФТ, продукт деалкилирования пиперидинового атома азота, в меньшем количестве образуются два продукта деалкилирования амидного атома азота, гидроксилированные метаболиты N–(4–гидроксифенил)–пропанамид (ГФПА) и N–(4–гидроксифенил)–ацетамид (ГФАА). Максимальное содержание нор–АФТ в плазме 9 нг/мл уменьшается до 5 нг/мл в интервале 1–4 ч и через 24 ч составляет 0,6 нг/мл (доза АФТ 90 мкг/ кг). При метаболизме 3–МФ, содержащего, как правило, примесь ФТН, образуются нор–3–МФ и нор–ФНТ.
Выведение
Фентанилы выводятся преимущественно в виде их фармакологически неактивных полярных метаболитов. Клиническое изучение показало, что около половины принятой дозы ФНТ выводится в первые 8 ч и около 70–80% обшей дозы элиминируется за 72 ч, при этом 92–98% в виде метаболитов. Менее 6–10% дозы элиминируется как неизмененное родительское вещество. Этот факт также обусловливает трудности детектирования ФНТ.Диапазон концентраций ФНТ в моче при медицинском и нелегальном употреблении не различается значительно и, как правило, не выходит за величину 100 нг/мл, однако в редких отдельных случаях концентрация неизмененного ФНТ может достигать больших значений: от 500 до 800 нг/мл. Так, интервал концентраций ФНТ в моче пациентов после анестезии 5–40 нг/мл за первые 6 ч после введения, но может доходить до более высоких значений: 87–485 нг/мл. Аномально высокое содержание ФНТ в моче около 500 нг/мл было определено после введения общей дозы 5 мг ФНТ в течение 5 ч (кардиохирургия). При немедицинском использовании ФНТ средняя концентрация в моче около 5,6 нг/мл (среднее для 28 случаев) при диапазоне от 0,14 до 35,5 нг/мл. Только в одной пробе из проанализированных 29 концентрация значительно превышала этот интервал и составила 531 нг/мл.

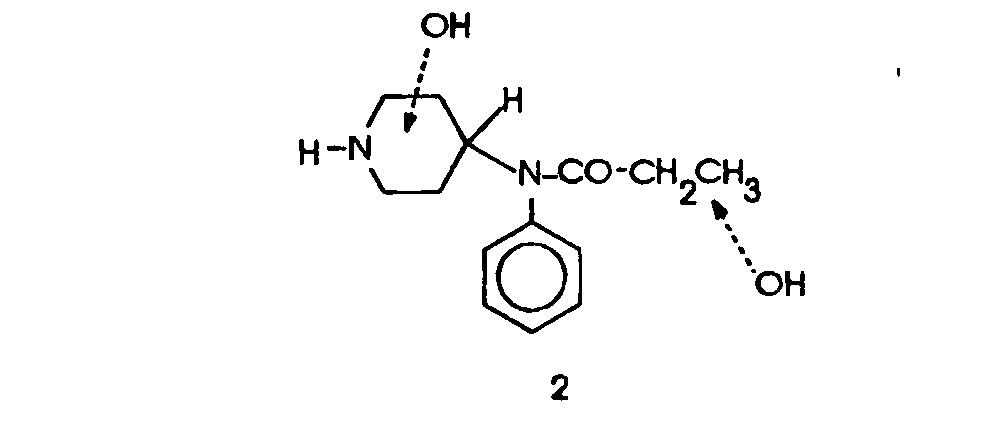
 Рис. 2. Метаболизм фентанила. 1 – фентанил и схема образования четырех гидроксилированных метаболитов. 2 – норфентанил и схема образования двух гидроксилированных метаболитов. 3 – депропионил–фентанил.
Рис. 2. Метаболизм фентанила. 1 – фентанил и схема образования четырех гидроксилированных метаболитов. 2 – норфентанил и схема образования двух гидроксилированных метаболитов. 3 – депропионил–фентанил.
 Рис. 3. Метаболизм алфентанила.
Рис. 3. Метаболизм алфентанила.
В исключительно редких случаях эта величина может доходить до 800 нг/мл. АФТ быстро выводится в течение 24 ч как неизмененное вещество (1% дозы), нор–АФТ (около 30% дозы), минорные ГФПА и ГФАА (см. выше). T½ элиминирования составляет 1–2 ч.
При анализе мочи субъекта, употреблявшего 3–МФ, определены: ФНТ – около 0,1 нг/мл, нор–ФНТ – 22 нг/мл, цис–нор–3–МФ 10 нг/мл и транс–нор–3–МФ – 7 нг/мл. Присутствие ФНТ и нор–ФНТ является следствием примеси ФНТ в «уличных» пробах 3–МФ.
Содержание фентанила в биожидкостях и тканях при передозировке фентанилом
Известно немало случаев смерти от ФНТ при самостоятельном приеме одного или в комбинации с другими средствами, среди которых морфин или кодеин встречаются редко, несмотря на то, что большинство жертв передозировки ФНТ обычно бывают опийными (героиновыми) наркоманами. Средние значения концентраций ФНТ в крови и моче для 112 фатальных случаев передозировки (внутривенное введение) 3,0 и 3,9 нг/мл соответственно. В других случаях смерти, непосредственно вызванной употреблением ФНТ, средняя концентрация в крови: 18 нг/мл при диапазоне 2,2–100 нг/мл, в моче: 6,3–92,7 нг/мл.При отравлении фармацевтическим препаратом Sublimaze (фентанил), введенном внутривенно, распределение по органам ФНТ характеризуется следующими значениями: кровь – 4,0 мкг/л, моча – 13 мкг/л, печень 9,7 мкг/кг, почки – 8,6 мкг/кг. В табл. 3 приведены обобщенные данные для распределения ФНТ в организме человека при смертельном исходе.
Описан случай отравления фармацевтическим ФНТ в комбинации с диазепамом врача–анестезиолога, наркомана, который был обнаружен в бессознательном сознании. Рядом был найден шприце жидкостью красного цвета. Результаты анализа приведены в табл. 4.
Таблица 3. Диапазон содержания фентанила при смертных случаях в результате передозировки, нг/мл или нг/г.
| Содержание | Кровь | Мозг | Печень | Почки | Моча |
|---|---|---|---|---|---|
| среднее | 8,3 | 20 | 37 | 18 | 28 |
| диапазон | 3,0–28 | 9,2–30 | 5,9–78 | 6,1–42 | 5,0–93 |
Таблица 4. Концентрация веществ в биожидкостях и органах при отравлении фентанилом в комбинации с диазепамом, мкг/л или мкг/кг. Н.о. = не обнаружен.
| Проба | Фентанил | ДЗП | Нор–ДЗП | Оксазепам |
|---|---|---|---|---|
| шприц | 2,8 | н.о. | н.о. | н.о. |
| сыворотка | 17,7 | обнаружен | . | – |
| кровь | 27.5 | 206,0 | 35,8 | 3800 |
| моча | 92,7 | 123,6 | 128,0 | 22800 |
| желчь | 58,2 | 492,7 | 147,2 | 4700 |
| печень | 77,5 | 271,4 | 164,7 | 9500 |
| почки | 41,5 | 139,0 | 141,5 | н.о. |
| мозг | 30,2 | 155,7 | 21,5 | 9300 |
| легкие | 83,4 | 72,8 | 119 | 6800 |
| ткань желудка | 31.6 | 855,5 | 52,5 | н.о. |
| содержимое желудка (450 г) | 7,4 мкг | 57,1 мкг | 25,0 мкг | н.о. |
При отравлении пластырем, содержащим ФНТ (3 пластыря с дозой 100 мкг/ч на теле), получены следующие значения содержания ФНТ: ■ кровь – 25 нг/мл ■ мозг – 54 нг/г ■ сердце – 94 нг/г ■ почки – 69 нг/г ■ печень – 104 нг/г.
При скрининговом исследовании биожидкостей или тканей обычные аналитические методы токсикологического анализа часто оказываются неэффективными для обнаружения запрещенных аналогов фентанила. В этих случаях результаты химико–токсикологического анализа могут вступать в противоречие с данными клинического обследования или данными аутопсии, указывающими на возможность употребления фентанилов. Для надежного детектирования этих соединений необходимо применять высокочувствительные и специфичные методики анализа.
Глава 10. Метадон
Метадон (6–диметиламино–4,4–дифенил–3–гептанон) является синтетическим опиоидом и, отличаясь от морфина по химической структуре, оказывает на организм человека во многом сходное действие. Изучение метадона началось с 1946 г., когда было установлено, что он является наркотическим анальгетиком. Некоторое время его использовали как замену морфина при сильных болях, причем в отличие от морфина метадон эффективен при оральном применении.Метадон имеет высокое сродство к мю–опиоидным рецепторам и с 1963 г. применяется для лечения больных с опиатной (героиновой) зависимостью. Чтобы предупредить развитие физической зависимости, дозировка при лечении должна поддерживаться на одном уровне или непрерывно уменьшаться. Лечение обычно проводят в течение продолжительного периода времени с одновременным назначением других терапевтических средств и сеансов психотерапии.
Вместе с тем, поскольку сам метадон является наркотическим средством, его применение для лечения не бесспорно и отвергается многими врачами–наркологами, считающими сомнительной пользу от его применения, а вред очевидным. Кроме того, метадон имеет значительный наркотический эффект, ведущий к злоупотреблениям, и его распределение должно тщательно контролироваться.
Торговые названия лекарственного средства: Амидон, Аданон, Фенадон, Долофин, Физептон, Гептадон, Amidone, Anadon, Phenadone, Dolophine, Physeptone, Heptadone
Оптические изомеры (энантиомеры) метадона
Лекарственное средство метадон является рацематом, т.е. смесью 1:1 двух оптических изомеров: ■ R–(–)–метадон, под названием «Левометадон» и ■ S–(+)–метадон.R–(–)–метадон (далее R–(–)–МТД) – фармакологически активен, S–(–1–)–метадон (далее S–(+)–МТД) – в 25–50 раз менее активен, таким образом активность метадона как лекарственного средства определяется активностью его Р–(–)–энантиомера.
Оптические изомеры метадона имеют различные фармакокинетические и фармакодинамические параметры, данные, имеющиеся в литературе, относятся в основном к рацемическому метадону.
Действие метадона на организм
При терапевтических дозах метадон проявляет аналгезирующее и седативное действие. Он воздействует на ЦНС, сердечно–сосудистую систему и гладкую мускулатуру. Эффект наступает спустя 20–30 мин после орального приема. Аналгезирующее действие проявляется через 4–6 ч. Побочные эффекты: головокружение, расслабление, тошнота, рвота, потение. При передозировке отмечается угнетение дыхания, подавление кровообращения, отек легких, миоглобинурия и острая почечная недостаточность. Симптомы хронического использования: расслабление, подавление дыхания, гипергликемия, повышение температуры и давления, брадикардия, запоры, спазмы желчных протоков и др. По мнению некоторых исследователей, эффекты синдрома отмены незначительны, однако в ряде случаев с ним связывают клинические эффекты, включающие генерализованные боли и бессонницу.Толерантность к метадону развивается медленно. Наркотический потенциал и длительность эйфорического эффекта сопоставима с известными для морфина.
Дозы, формы и способы введения
Метадон–гидрохлорид выпускается в форме для инъекций (10 мг/мл), в виде раствора и таблеток. Метадон вводят внутривенно, внутримышечно и подкожно и принимают внутрь (орально). Обычная оральная доза 5 или 10 мг в виде таблеток или 5 мг в 15 мл раствора. Для аналгезии 2,5–10 мг метадона вводят инъекционно каждые 3–4 ч. При детоксикационной терапии разовая оральная доза 15 мг, но в некоторых случаях может назначаться 30 мг и выше. Метадон, нелегально продаваемый «на улицах», обычно имеет свое происхождение из легального источника – больниц и клиник.Фармакокинетика и метаболизм
Всасывание. Спустя 10 мин после подкожного введения и 30 мин после орального приема метадон (далее МТД) детектируется в плазме. Пик концентрации в плазме после разового приема 15 мг достигается спустя 2–4 ч и составляет 70–85 нг/мл, затем концентрация быстро уменьшается (биэкспоненциальный). В первой фазе процесс элиминирования из плазмы характеризуется временем «полужизни» T½ = 14–15 (10–25) ч, во второй фазе – около 55 ч. При продолжительной терапии T½ увеличивается до 13–55 ч. (среднее 30). В случае хронического употребления концентрация МТД 6 плазме уменьшается экспоненциально: среднее значение T½= 22 ч.Фармакокинетические параметры сильно меняются в зависимости от индивидуальных особенностей субъектов. Это было продемонстрировано в опытах с участием 12 человек, проходивших лечение МТД в условиях стационара. Сильно менялось отношение дозы к концентрации в плазме, полужизнь в плазме T½ от 7 до 21 ч, содержание МТД в суточной моче от 23 до 52% общей принятой дозы.
Интервал содержания в плазме: 30 – менее 2000 нг/мл. При оральном приеме дозы от 0,46 до 0,58 мг/кг шестью пациентами концентрация в плазме: 140–220 нг/мл, при дозе от 0,85 до 1,33 мг/кг – 340–580 нг/мл, при дозе от 20 до 200 мг в течение 24 ч – от 59 до 1675 нг/мл. При ежедневной дозе 40 мг средняя дневная концентрация в плазме 182 нг/мл, а при дозе 80 мг – 420 нг/мл (см. также табл. 1).
Таблица 1. Концентрация метадона и метаболитов в плазме и моче наркоманов, нг/мл.
| Соединение | Плазма (п–22) | Моча (п–5) |
|---|---|---|
| Метадон | 33–358 | 126–3873 |
| ЭДДП | менее 10–24 | 3600–12910 |
| ЭМДР | менее 10 | менее 10–33 |
Таблица 2. Концентрация оптических изомеров метадона и метаболита в биожидкостях, мкг/мл.
| № | Доза, мг | Моча | Сыворотка | ||||
|---|---|---|---|---|---|---|---|
| R–(–)–(МТД) | S–(+)–(МТД) | ЭДДП | R–(–)–(МТД) | S (+)–(МТД) | ЭДДП | ||
| 1 | 90 | 2,48 | 1,35 | 19,4 | |||
| 2 | 85 | 3,52 | 1,65 | 2,71 | |||
| 3 | 85 | 6,36 | 2,86 | 18,1 | |||
| 4 | 60 | 2,33 | 1,49 | 10,3 | |||
| 5 | 45 | 1,16 | 0,45 | 7,3 | |||
| 6 | 50 | 0,014 | 0,041 | 0,021 | |||
| 7 | 50 | 0,011 | 0,025 | 0,017 | |||
| 8 | 60 | 0,015 | 0,057 | 0,031 | |||
Около 85% МТД связывается с белками плазмы (в основном с альбуминами и в меньшей степени с глобулинами).
Концентрация R–(–)–МТД и S–(+)–МТД в плазме при введении рацемического МТД различается в зависимости от индивидуальных особенностей организма и, возможно, дозы (табл. 2). Так, для пациента, получавшего в течение 3 дней разделенную дозу в сумме по 25–27,5 мг МТД в день, отношение концентраций изомеров R–(–)–МТД/S–(+)–МТД в среднем составило 0,8 (N–3). Для второго пациента, получавшего ежедневно в течение 6 дней разделенную дозу в сумме 10–20 мг МТД, R–(–)–МТД/S–(+)–МТД – 1,21 (N=6). Концентрация энантиомеров в первом случае: 15,3–21,7 нг/мл, во втором: 5,8–25,9.
 Рис. 1. Метаболизм метадона в организме человека. 1 – метадон, 2 – промежуточный продукт деметилирования метадона, 3 – 2–этилиден–1,5–диметил–3,3–дифенилпирролидин (ЭДДП), 4 – 2–этил–5–метил–3,3–дифенил–1–пирролин (ЭМДП), 5 – пара–гидрокси–ЭДДП, 6 – пара–гидрокси–ЭМДП, 7 – метадол (промежуточный продукт), 8 – норметадол, 9 – 4–диметиламино–2,2–дифенил–валериановая кислота, 10 – промежуточный продукт деметилирования метаболита (9), 11 – 1,5–диметил–3,3–дифенилпирролидин–2–он, 12 – пара–гидроксиметадон, 13 – N–оксид метадона.
Рис. 1. Метаболизм метадона в организме человека. 1 – метадон, 2 – промежуточный продукт деметилирования метадона, 3 – 2–этилиден–1,5–диметил–3,3–дифенилпирролидин (ЭДДП), 4 – 2–этил–5–метил–3,3–дифенил–1–пирролин (ЭМДП), 5 – пара–гидрокси–ЭДДП, 6 – пара–гидрокси–ЭМДП, 7 – метадол (промежуточный продукт), 8 – норметадол, 9 – 4–диметиламино–2,2–дифенил–валериановая кислота, 10 – промежуточный продукт деметилирования метаболита (9), 11 – 1,5–диметил–3,3–дифенилпирролидин–2–он, 12 – пара–гидроксиметадон, 13 – N–оксид метадона.
Распределение. МТД быстро выходит из системы кровообращения и локализуется в тканях: печени, легких, почках, селезенке. Небольшая часть достигает мозга. Объем распределения 5 л/ кг.
Метаболизм МТД проходит главным образом в печени. Основные направления биотрансформации (см. рис. 1): отщепление метильной группы от азота (2) с последующей спонтанной циклизацией до основного метаболита ЭДДП (3) и второго метаболита ЭМДП (4). Другие процессы метаболизма дают еще по крайней мере 9 метаболитов. Наиболее важные из них: гидроксилирование МТД и обоих метаболитов в пара–положение фенильного кольца (5, 6, 12), окисление МТД до метадола (7) с последующим N–деметилированием (8), N–оксидирование (13). Окислительное дезалкилирование МТД ведет к образованию кислотного метаболита (9), который далее подвергается циклизации в кетопроизводное пирролидина (11). Все основные метаболиты фармакологически неактивны.
Метаболиты метадона: ■ 2–этилиден–1,5–диметил–3,3–дифенилпирролидин (ЭДДП). ■ 2–этил–5–метил–3.3–дифенил–1–пирролин (ЭМДП). ■ пара–гидрокси–метадон. ■ пара–гидрокси–ЭДДП ■ пара–гидрокси–ЭМДП ■ Норметадон. ■ N–оксид метадона. ■ 4–диметил амино–2,2–дифенил–валериановая кислота. ■ 1,5–диметил–3,3–дифенил–пирролидин–2–ОН.
Основной метаболит метадона – ЭДДП образует два оптических изомера: R–(–)–(ЭДДП) и S–(+)–ЭДДП.
Выведение
Через 24 ч с мочой выводится 20–60% дозы, в виде нативного МТД – около 33% дозы, ЭДДП – 43%, ЭМДП – 5–10% дозы. При хроническом приеме содержание ЭДДП в суточной моче вдвое превышает содержание нативного соединения. Неконъюгированные соединения составляют около 75% выведенной дозы. Мочевая экскреция увеличивается в кислой среде. С каловыми массами выводится до 30% дозы, это количество уменьшается с увеличением дозы. В табл. 1 приведены концентрации МТД и метаболитов в плазме и моче людей, принимавших МТД.Фармакокинетика оптических изомеров R–(–)–МТД и S–(+)–МТД различна, т.е. стереоселективна. Разница в значениях концентраций изомеров в биожидкостях значительна, при этом отмечается преобладание R–(–)–МТД (табл. 3). Особенно это характерно для мочи: в 100% из 40 исследованных случаев, в меньшей степени – для плазмы и сыворотки крови: в 20–50% случаев. В волосах содержание R–(–)–МТД превышает содержание S–(+)–МТД в 90% случаев.
Концентрация рацемического МТД в суточной моче пяти пациентов, проходивших лечение от опийной зависимости, после орального приема разовой дозы 45–90 мг МТД лежит в интервале 1,61–9,22 мкг/мл. Количество R–(–)–(МТД) превышает количество S–(+)–(МТД) в 1,5–2,5 раза, а количество основного метаболита ЭДДП выше неизмененного МТД (сумма обоих энантиомеров) в 2–5 раз (табл. 2).
Метадон и метаболиты в волосах
Содержание МТД и метаболитов в волосах двух пациентов, проходивших лечение от героиновой наркомании дозами 60 и 80 мг/день в течение 6 мес, составило (нг/мг волос): МТД 10,1–21, ЭДДП 0,5–2,6, ЭМДП – не детектируется. Эти величины согласуются с данными, полученными при анализе 18 образцов волос наркоманов: МТД не выше 15 нг/мг, ЭДДП найден в 13 образцах в следовых количествах, ЭМДП определен только в 1 образце из 18 также в следовых количествах. При определении содержания оптических изомеров ЭДДП в волосах девяти наркоманов с героиновой зависимостью, проходивших лечение МТД в рамках детоксикационной программы, найдено, что хотя количества R – и S–ЭДДП различаются, четкого преобладания какого–либо изомера нет: в трех случаях из девяти выше содержание R–изомера, в пяти – S–изомера. Диапазон концентраций R–ЭДДП 0,42–1,73 нг/мг, S–ЭДДП – 0,40–2,10 нг/ мг, R–МТД 2,58–10,22 нг/мг и S–МТД 1,89–9,53 нг/мг.Таблица 3. Концентрация оптических изомеров в биожидкостях и волосах при приеме рацемического метадона, нг/мл, нг/мг
| Биоматериал | n | R–(–)–МТД | S–(+)ШТД | R/S |
|---|---|---|---|---|
| моча | 40 | 6–16783 | 4–6291 | 1.45–4,89 |
| плазма | 6 | – | – | 0,71–2 |
| сыворотка | 5 | 42–254 | 54–228 | 0,5 1.1 |
| волосы | 9 | 2,58–10,22 | 1,89–9,53 | 0,98–2,30 |
Метадон и метаболиты в меконии
В моче и меконии (см. главу опиаты) 16 новорожденных, чьи матери приобрели зависимость от метадона, детектированы МТД и метаболит ЭДДП. В меконии концентрация ЭДДП в среднем превышает концентрацию МТД в 9,6 раза, при этом в 8 образцах присутствует только метаболит.Токсичность
Минимальная летальная доза для случайного потребителя 50 мг, для наркоманов до 200 мг или более. Для не наркоманов токсические реакции проявляются при концентрации в плазме 1–2 мкг/мл. Концентрация МТД в плазме выше 2 мкг/мл может быть смертельной.В табл. 4 и 5 приведены величины, отражающие распределение МТД в тканях и биожидкостях организма в случаях со смертельным исходом, приписываемым действию МТД.
Таблица 4. Содержание метадона и метаболита в биожидкостях и органах в смертных случаях, приписываемых действию метадона. Мкг/мл, мкг/г (Ср. – среднее значение, п – число случаев).
| Ткань, биожидкость | Метадон | n | ЭДДП | n | ||
|---|---|---|---|---|---|---|
| Интервал | Ср. | Интервал | Ср. | |||
| кровь | 0–3 | 1,2 | 21 | 0–0,4 | 0,1 | 10 |
| моча | 0,52–76,2 | 21 | 22 | 0,4–46,2 | 11 | 17 |
| желчь | 1,1–75 | 13 | 18 | 0,2–315 | 41 | 18 |
| мозг | 0,23–2,2 | 0,9 | 7 | – | ||
| почки | 0,51–18,3 | 3,5 | 19 | 0,5–3,1 | 1г2 | 14 |
| печень | 0,05–49,5 | 6 | 23 | 0,02–2,7 | 0,6 | 16 |
| легкие | 1,6–110 | 16 | 17 | 0,01–0,98 | 0,2 | 10 |
| селезенка | 1,6–20,9 | 5,3 | 7 | 0–0,98 | 7 | |
Таблица 5. Содержание метадона в печени и моче в трех смертных случаях, приписываемых действию сверхдозы метадона
| Случай | Содержание в печени С(метадон) мкг/г | Содержание в моче С(метадон) мкг/мл |
|---|---|---|
| 1 | 1,9 | 13 |
| 2 | 1,3 | 11 |
| 3 | 0,7 | 4 |
Глава 11. Опиоидный анальгетик трамадол
Трамадол (ТРМ), химическое название: 2–(е)–[(диметиламино)–метил)–1–(е)–(3–метоксифенил)–циклогексан–1–(а)–ол, представляет собой синтетический опиоид со свойствами агониста–антагониста, анальгетик центрального действия средней силы, подобно кодеину, пентазоцину или пропоксифену. Он широко и эффективно применятся для обезболивания в терапии и хирургии, в частности при коронарных, онкологических или ортопедических болях.Лекарственное средство представляет собой гидрохлорид ТРМ и выпускается под разными названиями: Маброн (Кипр), Мендесик и Традол (Индия), Синтрадон (Югославия), Протрадон (Чехия) и др., но самым распространенным в РФ является трамал.
На ранних стадиях изучения ТРМ, когда был установлен опиоидный механизм анальгетического действия (ТРМ обладает селективностью к мю–опиоидным рецепторам), его относили к наркотическим анальгетикам. Однако дальнейшие исследования и опыт применения в клинической практике показали низкий уровень побочных эффектов опиатного типа, к которым относятся, прежде всего, ослабление функции дыхания, проявление эйфории, развитие лекарственной зависимости и толерантности, при приеме терапевтических (100 мг) и даже трехкратных терапевтических (300 мг) доз ТРМ по сравнению с эквивалентными по анальгетическому действию дозами морфина. Побочные эффекты, типичные в случае приема опиоидов, такие как тошнота, головокружение, рвота, расслабленность, сухость рта встречаются при длительном употреблении ТРМ, однако не превышают 5% из общего числа зарегистрированных около 13 тысяч случаев. Еще более редки проявления угнетения дыхания, задержка мочи, запоры.
Развитие толерантности и лекарственной зависимости при длительном приеме терапевтических доз ТРМ является исключительным и не было отмечено при использовании ТРМ в течение трех месяцев (225–258 мг ежедневно), как и выраженного синдрома отмены. Специальными экспериментами с участием двенадцати бывших наркоманов и шести опийно–зависимых наркоманов, проходящих курс лечения метадоном, было показано, что ТРМ не продуцирует морфиноподобный эффект, имеет низкую наркотическую активность и не может служить заменой морфина при опийной наркомании для лиц с низкими или умеренными уровнями опиатной зависимости, по крайней мере до доз 300 мг. В отношении ингибирования мю–опиоидного связывания ТРМ в 10 раз менее эффективен, чем кодеин, в 1000 раз, чем метадон, и в 6000 раз, чем морфин. Для продуцирования морфиноподобных эффектов у толерантных субъектов требуются более высокие дозы.
По принятой в настоящее время классификации ТРМ не является наркотиком и отнесен к сильнодействующим средствам. При назначении ТРМ вводятся ограничения на некоторые виды деятельности, связанные с необходимостью проявлять быструю реакцию, а также рекомендуется избегать длительных периодов приема.
Тем не менее существуют указания на немедицинское использование ТРМ лицами с опиатной (героиновой) зависимостью в дозах, значительно превышающих терапевтические. В этом случае наблюдается большое количество побочных эффектов, в том числе развитие пристрастия к препарату. Это диктует необходимость исследования влияния высоких доз ТРМ и прямого сравнения с прототипическими опиоидными средствами.
Стереоизомерия трамадола
По химической структуре ТРМ является производным циклогексанола и может существовать в виде двух стереоизомеров, отличающихся взаимным расположением заместителей. Стереоизомеры: 2–(е)–[ (диметиламино) метил]–1–(е)–(3–метоксифенил)–циклогексан–1–(а)–ол и 2–(а)–[(диметиламино)метил)–1–(е1)–(3–метоксифенил)–циклогексан–1–(а)–ол (CAS 27203–92–5 и 152538–36–8, соответственно) имеют различную анальгетическую активность. Конфигурация, отображенная на рис. 1, относится к более активному стереоизомеру, что объясняется соответствием этой структуры пространственной структуре морфина. В лекарственных препаратах содержание менее активного стереоизомера обычно не превышает 1–2%. В свою очередь, каждый из стереоизомеров представляет собой рацемическую (1:1) смесь двух оптических изомеров: (–)– и (+)–энантиомеров.Анальгетическое действие ТРМ осуществляется посредством двух одновременно протекающих в организме механизмов обезболивания: опиоидного (через влияние на опиоидные рецепторы) и неопиоидного (через влияние на моноаминергическую систему). Это было подтверждено влиянием на обезболивающий эффект ТРМ специфических антагонистов (налоксона и йохимбина – антагониста α2–адреноцепторов).
 Рис. 1. Конфигурация Трамадола в лекарственном средстве трамал: 2–(е)–[(диметиламино)метил]–1–(е)–(3–метоксифенил)–циклогексан–1–(а)–ол (CAS 27203–92–5).
Рис. 1. Конфигурация Трамадола в лекарственном средстве трамал: 2–(е)–[(диметиламино)метил]–1–(е)–(3–метоксифенил)–циклогексан–1–(а)–ол (CAS 27203–92–5).
Дальнейшее изучение показало, что реализация того или иного механизма обезболивания осуществляется разными оптическими изомерами. Это же объясняет кажущееся несоответствие низкого уровня свойственных опиоидам побочных эффектов (угнетение жизненноважных функций, развитие лекарственной зависимости) эффективности анальгетического действия ТРМ. Данные, полученные в экспериментах in vitro и in vivo, показали, что (+) – и (–)–энантиомеры ТРМ имеют различный фармакологический профиль и по разному реализуют анальгетический эффект. (+)–Энантиомер активнее примерно в 10 раз и обладает большим сродством к опиоидным мю–рецепторам, в то время как (–)–энантиомер в основном действует как неопиоидный анальгетик. Синергизм действия энантиомеров, установленный в отношении анальгетической активности, в отношении побочных эффектов не проявляется, в результате чего обезболивающий эффект рацемического ТРМ выше, чем каждого энантиомера, а уровень побочных эффектов ниже.
Фармакокинетика трамадола
Аналгезирующее действие при оральном приеме терапевтической дозы 50–150 мг ТРМ наступает через 30–60 мин, при внутривенном введении через 15–30 мин и сохраняется в течение 5–6 ч. Диапазон концентрации ТРМ в плазме составляет при этом от 10 до 1500 нг/мл. Максимальная суточная доза 400 мг. Биодоступность – 68%.Таблица 1. Средняя концентрация трамадола в плазме, мкг/л.
| Время, час | Разовая доза 100 мг орально (А) | Повторная доза 4 р 100 мг в день орально (Б) |
|---|---|---|
| 10 мин | 15 | 320 |
| 20 мин | 160 | 430 |
| 30 мин | 240 | 475 |
| 1 | 255 | 490 |
| 1,5 | 260 | 490 |
| 2 | 265 | 500 |
| 3 | 235 | 490 |
| 4 | 215 | 480 |
| 6 | 150 | 365 |
| 8 | 120 | 300 |
| 12 | 70 | 200 |
| 24 | 15 | 75 |
| 30 | 5 | 35 |
| 36 | 2 | 25 |
| 48 | 0,5 | 5 |
Таблица 2. Концентрация трамадола в плазме после внутривенного введения, нг/мл.
| Время, мин/час | А, доза 32,8 мг | В, доза 100 мг |
|---|---|---|
| 1 мин | – | 1149 |
| 3 мин | 2075 | 1011 |
| 5 мин | 484 | 941 |
| 10 мин | 236 | 635 |
| 15 мин | 173 | 582 |
| 30 мин | 138 | 579 |
| 1 час | 101 | 490 |
| 1,5 час | 89,9 | 447 |
| 2 час | 84,2 | 394 |
| 4 час | 61 | 284 |
| 8 час | 45 | 185 |
| 12 час | 34 | 122 |
| 24 час | не детектируется | 41 |
Кинетика выведения описывается двухкамерной моделью с временем «полужизни» в плазме T½= 5,1 ч для самого ТРМ и около 9 ч для активного метаболита (O–деметилированного ТРМ).
Измерение убыли ТРМ в плазме двух добровольцев (см. табл.2) после внутривенного введения разовой дозы 32,8 и 100 мг в интервале от 1 мин до 30 ч показало наличие двух фаз распределения ТРМ. Первая в интервале от 1 до 30 мин характеризуется временем «полужизни» T½ около 30 мин и соответствует резкому снижению содержания ТРМ в системе крови. Для второй, более длительной фазы, с медленной убылью концентрации ТРМ – T½ около 6 ч. Концентрация ТРМ в плазме (доза 100 мг, внутривенно) достигает максимального значения 1149 нг/мл через 1 мин и уменьшается до 41 нг/мл через 24 ч.
 Рис. 2. Схема биотрансформации трамадола:
I – 1–(3–метоксифенил)–2–(метиламинометил)–циклогексан–1–ол (N–МТБ).
II – 1–(3–гидроксифенил)–2–(диметиламинометил)–циклогексан–1–ол (O–МТБХ).
III – 1–(3–гидроксифенил)–2–(метиламинометил)–циклогексан–1–ол (N,O–МТБ).
IV – 1–(3–метоксифенил )–2–(аминометил)–циклогексан–1–ол (N,N–МТБ).
V–1–(3–гидроксифенил)–2–(аминометил)–циклогексан–1–ол (N,N,O–МТБ).
VI – 1–(3–метоксифенил)–2–(диметиламииометил)–гидроксициклогексан–1–ол (ОН–ТРМ).
ПТР – продукт термического разложения трамадола: ангидротрамадол.
Рис. 2. Схема биотрансформации трамадола:
I – 1–(3–метоксифенил)–2–(метиламинометил)–циклогексан–1–ол (N–МТБ).
II – 1–(3–гидроксифенил)–2–(диметиламинометил)–циклогексан–1–ол (O–МТБХ).
III – 1–(3–гидроксифенил)–2–(метиламинометил)–циклогексан–1–ол (N,O–МТБ).
IV – 1–(3–метоксифенил )–2–(аминометил)–циклогексан–1–ол (N,N–МТБ).
V–1–(3–гидроксифенил)–2–(аминометил)–циклогексан–1–ол (N,N,O–МТБ).
VI – 1–(3–метоксифенил)–2–(диметиламииометил)–гидроксициклогексан–1–ол (ОН–ТРМ).
ПТР – продукт термического разложения трамадола: ангидротрамадол.
Метаболизм трамадола
ТРМ интенсивно метаболизируется в организме и образует несколько метаболитов в результате последовательного отщепления метильной группы от атомов О и N и присоединения гидроксильного радикала к циклогексановому фрагменту (рис.2).Основные метаболиты: ■ 1–(3–гидроксифенил)–2–(диметиламинометил)–циклогексан–1–ол (O–МТБ). ■ 1–(3–метоксифенил)–2–(метиламинометил)–циклогексан–1–ол (N–МТБ). ■ 1–(3–гидроксифенил)–2–(метиламинометил)–циклогексан–1–ол (N.O–МТБ). в меньшем количестве образуются: ■ 1–(3–метоксифенил)–2–(аминометил)–циклогексан–1–ол (N.N–МТБ). ■ 1–(3–гидроксифенил)–2–(аминометил)–циклогексан–1–ол (N,N,0–МТБ). ■ 1–(3–метоксифенил)–2–(диметиламинометил)–гидроксициклогексан–1–ол (ОН–ТРМ).
Метаболиты, содержащие гидроксильную группу, далее конъюгируются (вторая фаза метаболизма).
Кроме указанных, обнаружен метаболит, имеющий, по–видимому, структуру эпоксида циклогексанового фрагмента молекулы ТРМ. Это соединение в небольших количествах также может присутствовать в стандартных растворах ТРМ.
Наиболее важным является продукт O–деметилирования ТРМ – метаболит O–ТРМ. Он активен фармакологически, отличается большим сродством к опиатным рецепторам, чем сам ТРМ, и превышает его по анальгетической активности в 2–4 раза, подобно тому, как продукт O–деметилирования кодеина, метаболит, морфин, также превышает родительское соединение по активности.
Для метаболитических процессов характерна стереоселективность, что было доказано при изучении раздельного метаболизма рацемического ТРМ и его энантиомеров in vitro с использованием микросомальной фракции печени человека. Установлено, что деметилирование метокси– и аминогрупп молекулы ТРМ (O–деметилирование и N–деметилирование) осуществляется по разным механизмам и описывается различными фармакокинетическими моделями. O–деметилирование (+)– и (–)–ТРМ микросомами печени человека описывается однокамерной моделью, причем скорость реакции образования O–МТБ из (–)–энантиомера ТРМ выше в 2 раза, чем из (+)–энантиомера. N–МТБ предпочтительнее образуется из (+)–ТРМ и процесс описывается двухкамерной моделью. На основании изучения влияния специфических ингибиторов цитохрома (хинидина и пропафенона) сделан вывод об ответственности цитохрома Р–450IID6 за процесс O–деметилирования. Предполагается, что полиморфизм Р–450 может быть причиной индивидуальных различий в скорости образования более сильного, чем ТРМ, анальгетика: О–деметилированного метаболита, аналогично влиянию полиморфизма Р–450 на деметилирование кодеина с образованием более сильного анальгетика морфина.
Выведение
Более 90% введенной в организм дозы ТРМ экскретируется почками, при этом в виде неизмененного ТРМ – около 30%. Опыты с меченым С–14 ТРМ показали, что после ферментативного гидролиза в моче обнаруживается 82–89% метки С–14. Распределение радиоактивной метки по метаболитам, изолированным из мочи, собранной за 72 часовой период после приема 1,25 мг/кг ТРМ, содержащего меченый изотоп углерода С–14, отражает выход метаболитов в процентном отношений к дозе: ■ неизмененный ТРМ – 25,1 % ■ О–МТБ – 10,4%; ■ О–МТБ–конъюгат – 15,5%. ■ N–МТБ – 2,4%; ■ N.N, О–МТБ – 0,1%; ■ N,N,О–конъюгат – 0,8%; ■ N, О–МТБ – 12,8%; ■ N.O–МТБ–конъюгат – 15,1%.По результатам анализа мочи после орального приема разовой дозы 100 мг ТРМ пятью добровольцами установлено для четырех участников эксперимента, что за 30 ч в мочу выделяется (в процентах от дозы); 54–69,16% ТРМ, 25,09–43,74% О–МТБ и 1,12–5,68% N–МТБ. Для пятого участника количество N–МТБ превышало количество О–МТБ, что связано, по–видимому, с проявлением индивидуальных особенностей биотрансформации ТРМ в организме человека, выражающихся в различии преимущественного направления деметилирования. Количественные различия метаболитов могут быть значительными. Так, для двух человек, принявших внутрь практически равные дозы ТРМ (1,25 и 1,06 мг/кг), содержание в моче за 72 часовой период составило соответственно (в % метки С–14): О–МТБ – 10,4 и 4,9, N–МТБ – 2,4 и 31,4, N.O–МТБ – 12,8 и 6,0, N.N–МТБ – 0 и 0,8.
Соотношения (+)– и (–)–энантиомеров метаболитов, выводимых с мочой после приема 100 мг трамала (n=5), сильно отличаются для О–МТБ и N–МТБ. Количество (+)–N–MTB превышает количество (–)–N–MTB, причем со временем это различие увеличивается: отношение (+)–/(–)–N–MTB составляет 2,4–2,6 и 5,4–6,6 в интервале 0–1 час и 14–24 ч, соответственно. Для О–МТБ эта тенденция менее выражена: 1,1–1,5 и 1,7–2,3 в тех же временных интервалах.
Токсичность трамадола
У пациентов с серьезными нарушениями функций почек и печени время полувыведения ТРМ увеличивается в 2–3 раза, поэтому в этих случаях рекомендуется увеличивать интервал между приемами, чтобы избежать накапливания в организме ТРМ и его О–деметилированного метаболита до токсических концентраций.Прием трамадола в дозах, значительно превышающих терапевтические, опиатными наркоманами нередко приводит к острым отравлениям или к фатальному исходу. Для исследованных 12 проб крови людей, чья смерть в той или иной степени была связана с употреблением трамадола, в 4 проб крови при нефатальной интоксикации, интервал концентрации составил (мг/л): ТРМ – от 0,09 до 22,59; О–ТРМ – от 0,02 до 1,84; N–МТБ – от 0,01 до 2,08. Часто смерть наступает при передозировке в результате приема нескольких различных веществ. Описан случай смертельного самоотравления трамалом в результате наступившего отека легких. В крови определен ТРМ в концентрации 13 мг/л и метаболит О–МТБ (концентрация не приведена), а также метаболит флунитразепама – 7–аминофлунитразепам.
Последние комментарии
5 часов 21 минут назад
5 часов 22 минут назад
12 часов 5 минут назад
12 часов 13 минут назад
18 часов 25 минут назад
18 часов 29 минут назад